Cu-MOF-199/铜硫化合物的制备及其电催化还原CO2性能
章 寅,侯昱竹,俞峥松,王 雨,王映雪,董玉林,刘 鹏,段俊新,李 曦
武汉理工大学化学化工与生命科学学院,湖北武汉430070
0 引 言
随着化石燃料消耗的与日俱增,温室效应和能源危机逐渐成为全人类共同面临的问题[1]。如果能将大气中的CO2富集,将其还原用于制备小分子燃料或高附加值化学品,则不仅可以降低大气中CO2的浓度,还能缓解当前能源紧缺的危机,实现“碳中和”[2]。传统的CO2热化学还原需要在高温高压下进行,这无疑增加了成本,而电化学还原可以在室温下进行,具有更广阔的前景[3,4]。为了减少电化学还原CO2的电能损耗,需要借助催化剂以降低整个过程中的能垒。廉价易得的铜基催化剂对CO2的电化学还原表现出较高的催化活性,其中,铜硫化物因具有较高的甲酸选择性而受到青睐[5,6]。
以金属有机框架(metal-organic frameworks,MOFs)为前驱体,衍生得到的金属硫化物可以继承MOFs 多孔的结构优点,具有较高的比表面积。此外,将金属有机框架部分硫化可以诱导其界面电荷再分布,促进甲酸中间体OCHO*的吸附,从而提升对甲酸的选择性[7]。
本研究以MOFs 材料Cu-MOF-199 为前驱体,以硫代乙酰胺为硫源,采用溶液浸渍法在低温下部分硫化Cu-MOF-199,制备了Cu-MOF-199/铜硫化合物(CuxS)复合材料Cu-MOF/CuxS。因为Cu-MOF-199 多孔结构的部分保留以及CuxS 的加入,Cu-MOF/CuxS 催化活性较Cu-MOF-199 有明显提升,同时对甲酸表现出高选择性。
1 实验部分
1.1 试剂及仪器
试剂:Cu(NO3)2·3H2O、1,3,5-均苯三甲酸(1,3,5-Benzenetricarboxylic acid, H3BTC)、硫代乙酰胺(thioacetamide, TAA)、碳酸氢钾、乙醇和N,N-二甲基甲酰胺(N,N-Dimethylformamide, DMF)购自国药集团化学试剂有限公司,Nafion 溶液、分析标准品甲醇和甲酸均购于阿拉丁生化科技股份有限公司,铜箔(copper foil, CF)购于昆山钦发电子科技有限公司;实验用水为去离子水。
仪器:CHI660E 型电化学工作站(上海辰华仪器有限公司)、全自动比表面及孔隙度分析仪(ASAP2460,Micromeritics 公 司)、RU-200B/D/MAX-Rb 型 转 靶X 射 线 衍 射 仪(XRD,Rigaku 公司)、JEM-7500F 型场发射扫描电镜(SEM,Zeiss 公司)、NMR 500 MHz 型磁共振仪(NMR,Bruker 公司)、iS5 型傅里叶变换红外光谱仪(FT-IR,Thermo公司)。
1.2 Cu-MOF/CuxS-n制备
Cu-MOF-199 参照文献[8]方法合成。将2.4 g Cu(NO3)2·3H2O 和1.2 g H3BTC 溶 入60 mL 水、乙醇、DMF(体积比为1∶1∶1)的混合溶剂中,90 ℃条件下处理20 h,冷却,抽滤,洗涤并干燥,得到粉末状Cu-MOF-199。
Cu-MOF-199 的硫化参考文献[9]方法。在20 mL 乙醇中加入0.3 g TAA 和0.2 g Cu-MOF-199,在35 ℃硫化一段时间,冷却,抽滤,洗涤并干燥,得到粉末状Cu-MOF/CuxS-n,其中CuxS 表示CuS 和Cu2S 的混合物,n代表硫化时间(n=1、3、5、7 h)。
在2 mL 去离子水中加入20 mg Cu-MOF/CuxS-n和15 μL Nafion 溶液,超声10 min,得 到10 mg/mL 的Cu-MOF/CuxS-n分 散 液。
1.3 Cu-MOF/CuxS-n/CF 电极制备及电化学测试
将1 cm×2 cm 的CF 用金相砂纸打磨以除去表面氧化物,随后分别在1 mol/L H2SO4、乙醇和水中超 声 洗 涤10 min。将320 μL Cu-MOF/CuxS-n分散液滴在CF 一端的1 cm×1 cm 部分,于35 ℃干燥,得到Cu-MOF/CuxS-n/CF 电极。
电化学测试在H 型电解池中进行,采用三电极体系,Cu-MOF/CuxS-n/CF 为工作电极,铂柱为对电极,饱和甘汞电极为参比电极,0.5 mol/L KHCO3为电解液,测试前向体系中通入30 min CO2。
2 结果与讨论
2.1 材料表征
2.1.1 Cu-MOF-199
图1 为Cu-MOF-199 的FT-IR、XRD 和SEM图。FT-IR 图(图1(a))给出了Cu-MOF-199 的官能团信息,1 373、1 447、1 645 cm-1处吸收峰分别归属为羧基中C—O 伸缩振动、O—H 弯曲振动和C=O 伸缩振动,730 cm-1处吸收峰则归属为Cu—O 的伸缩振动,与文献[10~12]中Cu-MOF-199 的FT-IR 图相吻合。XRD 图(图1(b))中6.6°、9.4°、11.5°、13.4°、14.5°、14.9°、18.9°、20.1°、25.8°和29.1°处的衍射峰分别对应Cu-MOF-199 的(200)、(220)、(222)、(400)、(331)、(420)、(440)、(600)、(731)、(751)晶面[13]。SEM 图(图1(c))表明合成的Cu-MOF-199 呈正八面体形貌,粒径约15 μm,具有孔道结构,为典型的Cu-MOF-199 形貌[14]。上述表征结果表明,具有孔道结构的Cu-MOF-199 成功合成。
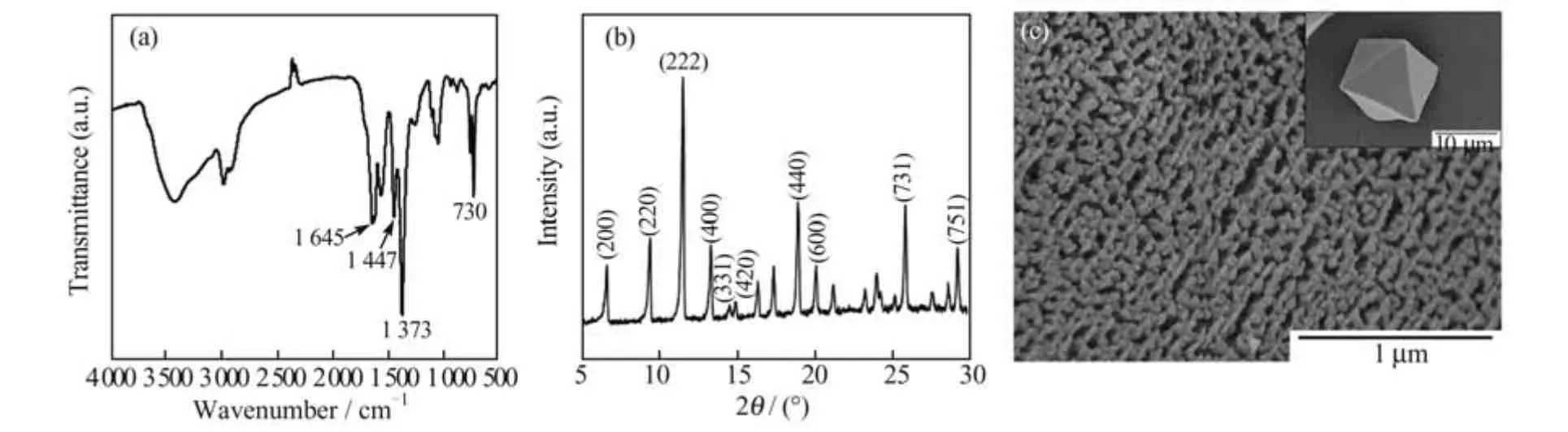
图1 Cu-MOF-199 的FT-IR 图(a)、XRD 图(b)和SEM 图(c)Fig.1 FT-IR spectrum (a), XRD spectrum (b)and SEM image (c)of Cu-MOF-199
2.1.2 Cu-MOF/CuxS-n
以Cu-MOF/CuxS-5 为例,给出Cu-MOF-199部分硫化产物的XRD 图,如图2 所示。29.3°、31.9°和47.9°处的衍射峰分别对应CuS 的(102)、(103)和(110)晶面[9],37.5°和46.0°处的衍射峰分别对应Cu2S 的(102)和(110)晶面[15],说明制备的复合材料为铜的硫化物。同时,在5°~30°区间还观察到Cu-MOF-199 的衍射峰。因此,Cu-MOF/CuxS-5 应为Cu-MOF-199 和铜硫化合物的复合物。
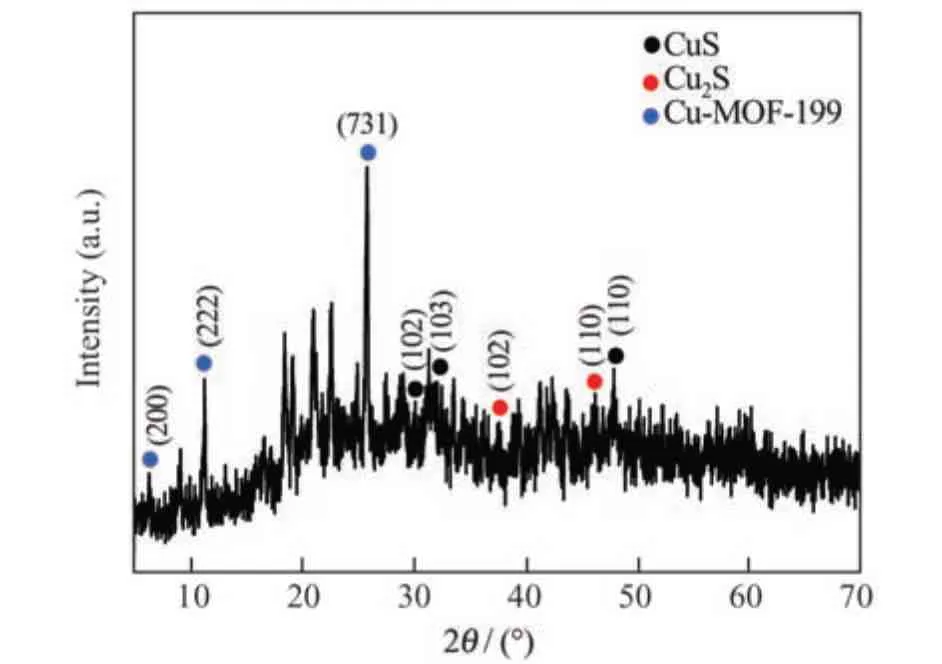
图2 Cu-MOF/CuxS-5 的XRD 图Fig.2 XRD spectrum of Cu-MOF/CuxS-5
图3 为Cu-MOF/CuxS-n的SEM 图。从SEM图可以看到,硫化1 h 后,Cu-MOF-199 八面体出现轻微碎裂,表面的孔道结构出现塌陷;硫化3 h 后,八面体结构开始瓦解,出现纳米片状物质;硫化5 h后,八面体结构进一步瓦解,纳米片逐渐形成纳米花状;硫化7 h 后,八面体结构完全瓦解,呈现纳米花状形貌。
图4(a)为Cu-MOF-199 及Cu-MOF/CuxS-n的N2吸/脱附等温曲线。Cu-MOF-199 表现为第Ⅰ类等温线,在低压区有较高的吸附量,表明材料中含有大量微孔;同时,在高压区出现H4 型回滞环,表明材料中有介孔存在,主要是由粒子堆积而产生[16]。与Cu-MOF-199 相 比,Cu-MOF/CuxS-n在低压区的吸附量大幅下降,说明微孔减少,但在高压区同样存在H4 型回滞环,表明Cu-MOF 或CuxS粒子堆积成介孔。其中,Cu-MOF/CuxS-7 在低压的吸附接近于零,高压的回滞环也比其他Cu-MOF/CuxS 样品的回滞环小,表明孔结构基本被破坏。图4(b)为由根据BJH 模型得到的孔径分布曲线。Cu-MOF-199 的孔径主要为1~2 nm 的微孔和22 nm 左右的介孔,而Cu-MOF/CuxS-1、Cu-MOF/CuxS-3 和Cu-MOF/CuxS-5 的孔径主要分布在17、19 和29 nm 左 右,Cu-MOF/CuxS-7 几 乎 没 有 直 径小于100 nm 的孔。此外,随着硫化时间的增加,孔体积逐渐从0.163 cm3/g 减小至0.059 cm3/g。根据N2吸/脱附等温曲线,由BET 模型计算得到Cu-MOF-199、Cu-MOF/CuxS-1、Cu-MOF/CuxS-3、Cu-MOF/CuxS-5、Cu-MOF/CuxS-7 的比表面积分别为741.9、186.2、106.1、19.5、1.9 m2/g。随着硫化时间的增加,比表面积减少,说明硫化过程中Cu-MOF-199 的孔道结构逐步被破坏。这与SEM 结果(图3)一致。另外,可以看到孔体积随硫化时间增加而减小的幅度远不及比表面积随硫化时间增加而减小的幅度,表明Cu-MOF-199 的比表面积主要为微孔的贡献,然而微孔不利于传质和活性位点的暴露。相比之下,Cu-MOF/CuxS-n的比表面积虽然远小于Cu-MOF-199,但其内部以介孔为主,更有利于活性位点接触反应物[17]。

图3 Cu-MOF/CuxS-n的SEM 图Fig.3 SEM images of Cu-MOF/CuxS-n
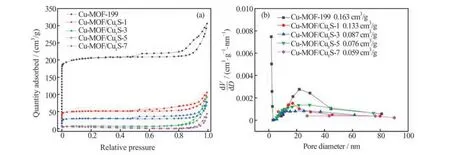
图4 Cu-MOF-199 及Cu-MOF/CuxS-n的N2吸/脱附等温曲线(a)和孔径分布曲线(b)Fig.4 N2adsorption-desorption isotherms (a)and pore size distribution (b)of Cu-MOF-199 and Cu-MOF/CuxS-n
2.2 Cu-MOF/CuxS-n的电催化性能
考察了Cu-MOF/CuxS-n的电催化性能,结果如图5(a)~(f)所示。图5(a)为Cu-MOF/CuxS-n/CF 电极的线性扫描伏安(linear sweep voltammetry, LSV)曲 线。与Cu-MOF-199/CF 相 比,Cu-MOF/CuxS-n/CF 的 电 流 密 度J(mA/cm2)明 显 增加,表明CuxS 的加入有利于催化活性的提升;随着硫化时间从1 h 增加到5 h,电流密度逐步增加,而当硫化时间达到7 h 时,电流密度有所下降,说明引入过多的CuxS 不利于催化活性的进一步提升。从SEM(图3)和N2吸/脱附实验结果(图4)可知,随着硫化时间的增加,虽然CuxS 的量愈来愈多,但材料的框架结构逐步被破坏,当硫化时间达到7 h 时,框架结构完全消失,CuxS 堆积团聚,不利于活性位点与反应物接触,导致催化性能下降。这说明催化性能与CuxS 的量和有效电化学活性面积有关。图5(b)是由循环伏安(cyclic voltammetry, CV)法得到的电流密度与扫速的关系图,其斜率代表双电层电容(Cdl),Cdl与电化学活性面积成正比[18]。随着硫化时间(1~5 h)的增加,材料中CuxS 的量愈来愈多,有效电化学活性面积增大,Cdl随之增大。其中,Cu-MOF/CuxS-5/CF 的Cdl最 高(9.30 mF/cm2),是Cu-MOF-199/CF 的(Cdl=0.78 mF/cm2)11.9 倍。但Cu-MOF/CuxS-7/CF 的Cdl(5.35 mF/cm2)反而有所下降,这与MOF 框架坍塌有关。图5(c)为Cu-MOF/CuxS-5/CF 的Nyquist 图。 Cu-MOF/CuxS-5/CF 在高频区的半圆半径远小于CF 和Cu-MOF-199/CF,表明其电荷转移阻抗(Rct)最小,电荷传输能力远高于CF 和Cu-MOF-199[19]。可见,CuxS 的掺入可以有效提升催化剂的电荷传输能力。

图5 所制备电极在CO2饱和的0.5 mol/L KHCO3溶液中的LSV 曲线(a)、电流密度与扫速的关系图(b)和Cu-MOF/CuxS-5/CF 的Nyquist 图(c)、-1.1 V(vs.RHE)下的I-t曲线(d)、参与电催化前后LSV 曲线(e)和法拉第效率(f)Fig.5 LSV curves (a)and relationships between current densities and scanning rates (b)of as-prepared electrodes in 0.5 mol/L KHCO3solution saturated with CO2;Nyquist plots (c),I-tcurve under -1.1 V (vs.RHE)(d), LSV curves before and after electrocatalysis (e)and Faraday efficiency (f)of Cu-MOF/CuxS-5/CF
电催化剂的稳定性通过测试电流-时间(I-t)曲线表征。图5(d)是Cu-MOF/CuxS-5/CF 在-1.1 V(vs. RHE)下的I-t曲线,可以看到,在长达10 h 的测试过程中,电流未发生明显衰减。图5(e)为Cu-MOF/CuxS-5/CF 在电催化前后的LSV 曲线,可以看到两条曲线几乎重合,说明Cu-MOF/CuxS-5/CF 具有良好的电化学稳定性。
在不同电势下还原6 h 后,采用磁共振氢谱对液相产物进行分析定量。图5(f)为Cu-MOF/CuxS-5/CF 电极上CO2的还原液相产物的法拉第效率(Faraday efficiency,FE)随电势的分布。可以看出,在-0.4 V~-1.2 V(vs. RHE)范围内,液相产物主要是甲酸(HCOOH);在-0.7 V(vs. RHE)时法拉第效率最高,达到了81.6%,具有较高的甲酸选择性。
3 结 语
本工作以Cu-MOF-199 为前驱体,用简便的溶液浸渍法将其部分硫化,得到Cu-MOF/CuxS 复合材料。电催化活性物质CuxS 的引入可以显著提升材料的电荷传输能力,Cu-MOF/CuxS 复合材料的电催化活性得到明显提升。同时考察了硫化时间对复合材料结构和电催化还原CO2性能的影响。结果表明,随着硫化时间的增加,活性物质CuxS 也会增多,但MOF 的框架会逐渐瓦解,导致有效电化学活性面积先增大后减小。在硫化时间不超过5 h时,活性物质的增多起主导作用,有效电化学活性面积随硫化时间增加而增大;当硫化时间达到7 h时,Cu-MOF-199 的结构几乎完全被破坏,CuxS 堆集,不利于活性位点暴露,导致有效电化学活性面积减小,催化活性降低。因此,硫化时间为5 h 时制备的Cu-MOF/CuxS-5 复合材料具有最佳的催化活性。此外,Cu-MOF/CuxS-5 还具有良好的选择性和稳定性,在-0.7 V(vs. RHE)的低电势下甲酸的法拉第效率可达81.6%,且在10 h 的催化过程中电流无明显衰减。本研究提供了一种以MOF 作为多孔模板制备金属硫化物的思路,对于设计兼具高活性、高选择性的CO2还原电催化剂有一定的启示。

