多指标综合评分法优化金蕾颗粒水提醇沉工艺
曲馨,薄双琴,柳娜,寇亮,陈晖,景明
甘肃中医药大学药学院,甘肃 兰州 730000
胆囊炎通常是病原微生物感染和化学损伤引发的一系列胆系感染、胆汁刺激(胆红素和类脂质等代谢失调)、胰液反流进入胆管等所致。胆囊炎大多与胆石症合并发病,且具有反复发作的特点。金蕾复方是甘肃省名中医张银川主任中医师的临床经验方,由湿生扁蕾、金钱草组成,临床用于胆囊炎具有良好疗效。藏药湿生扁蕾和金钱草具有清热、祛湿、利胆功效,主治肝胆湿热所致胁痛、口苦,急性胆囊炎、胆管炎等。课题组前期药理研究表明,金蕾复方具有一定的镇痛、抗炎、保肝、护肝作用,半数致死量(LD)>120 g/kg(成人剂量的12倍),未发现明显毒副作用。该方临床用药以汤剂为主,现遵循传统水煎工艺,制成颗粒剂。湿生扁蕾的黄酮类成分具有抗菌、抗氧化等作用,其代表成分为当药黄素、木犀草素;金钱草的黄酮类成分能够有效抑制并促进结石排出,结合2020年版《中华人民共和国药典》金钱草含量测定指标及初期试验,确定山柰酚为指标成分。故本研究以当药黄素、木犀草素、山柰酚及干浸膏得率为考察指标,采用L(3)正交试验,熵权法进行多指标综合加权评分优选水提工艺,采用单因素试验结合大生产耗能、经济因素优选醇沉工艺,为后续制剂成型奠定基础。
1 仪器与试药
ST-501流水式中药粉碎机(浙江省瑞安市赛特机电有限公司),XPE105型分析天平(梅特勒-托利多仪器上海有限公司),HGZF-9203型电热恒温鼓风干燥箱(上海跃进医疗器械有限公司),SHZ-D(Ⅲ)循环水式多用真空泵(合肥予华仪器有限公司),EV351旋转蒸发仪(北京莱伯泰科仪器股份有限公司),SB5200D超声波清洗器(宁波新芝生物科技股份有限公司),1260高效液相色谱仪(美国安捷伦科技公司)。
湿生扁蕾采自甘肃省定西市漳县大草滩(2020年8月),经甘肃中医药大学附属医院杨锡仓主任药师鉴定为龙胆科扁蕾属一年生草本植物湿生扁蕾(Munro)Ma.的干燥全草;金钱草购自甘肃省兰州市黄河中药材市场,经甘肃中医药大学附属医院杨锡仓主任药师鉴定为报春花科珍珠菜属植物过路黄Hance.的干燥全草。对照品木犀草素(批号B20888,HPLC纯度≥98%)、当药黄素(批号B20281,HPLC纯度≥98%)、山柰酚(批号B21126,HPLC纯度≥98%),上海源叶生物科技有限公司;其他试剂均为色谱纯。
2 方法与结果
2.1 指标成分含量测定
2.1.1 色谱条件
采用Agilent SB-C18色谱柱(150 mm×4.6 mm,5 μm),流动相为0.10%磷酸水溶液(A)-甲醇(B),梯度洗脱(0~10 min,70%~60%A;10~17 min,60%~50%A;17~40 min,50%~30%A;40~50 min,30%A),流速1.0 mL/min,检测波长360 nm,柱温30 ℃,进样量5 μL。
2.1.2 混合对照品溶液制备
精密称定当药黄素、木犀草素、山柰酚对照品适量,以甲醇溶解并定容,得到浓度分别为0.10、0.21、0.03 mg/mL的混合对照品溶液,用0.22 μm微孔滤膜过滤,取续滤液,即得。
2.1.3 供试品溶液制备
精密移取一定浓度水提浓缩液25 mL,置蒸发皿中,水浴蒸干,分次用少量甲醇溶解,移入25 mL容量瓶中,加甲醇定容至刻度,称定质量,超声(频率40 kHz,功率900 W,时间40 min)溶解,放冷,用甲醇补足减失的质量,0.22 μm微孔滤膜过滤,取续滤液,即得。
2.1.4 阴性对照溶液制备
分别称取缺湿生扁蕾、金钱草处方药物各10 g,分别加入12倍量水回流提取3次,每次0.5 h,合并滤液,浓缩后分别按“2.1.3”项下方法制备缺湿生扁蕾、金钱草的阴性对照溶液。
2.1.5 专属性试验
精密吸取上述混合对照品溶液、供试品溶液、湿生扁蕾阴性对照溶液、金钱草阴性对照溶液各10 μL,按“2.1.1”项下色谱条件进样测定,色谱图见图1。结果阴性对照无干扰,表明方法专属性良好。
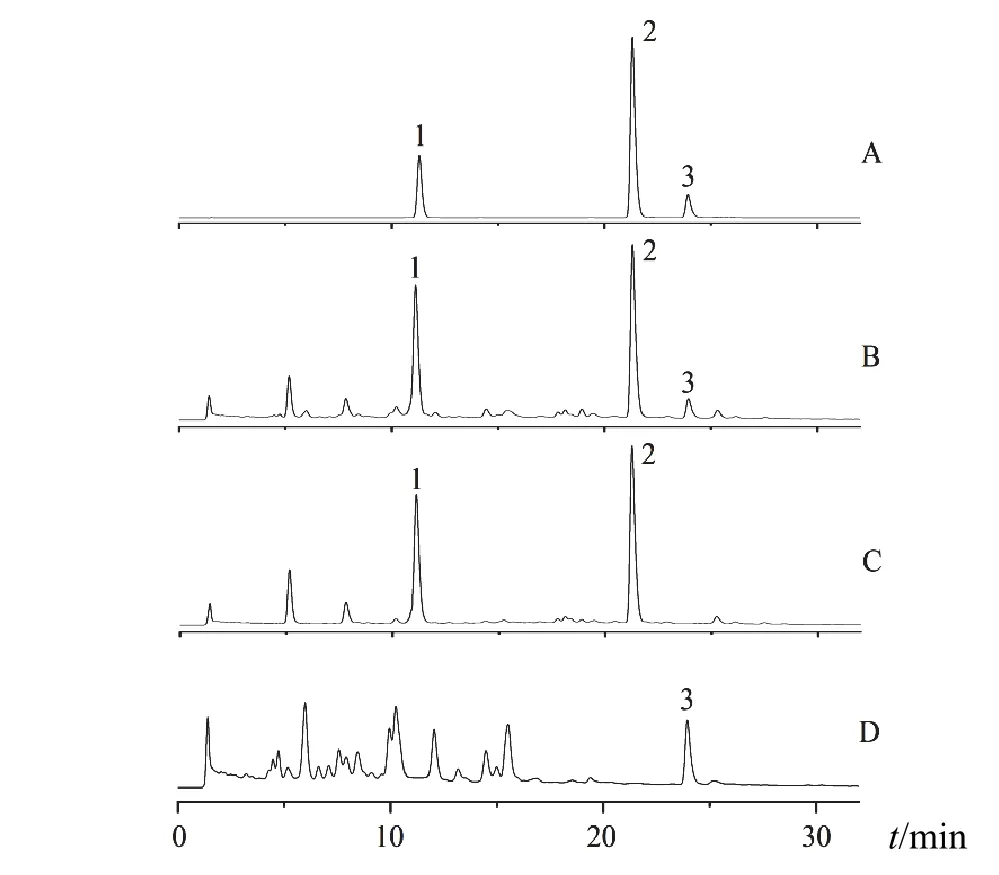
图1 金蕾颗粒水提液中当药黄素、木犀草素、山柰酚HPLC图
2.1.6 线性关系考察
分别配制系列浓度的当药黄素、木犀草素、山柰酚对照品溶液,精密吸取5 μL,按“2.1.1”项下色谱条件进样测定,以对照品浓度为横坐标,峰面积为纵坐标,进行线性回归,结果见表1。3种指标成分在各自浓度范围内线性关系良好。
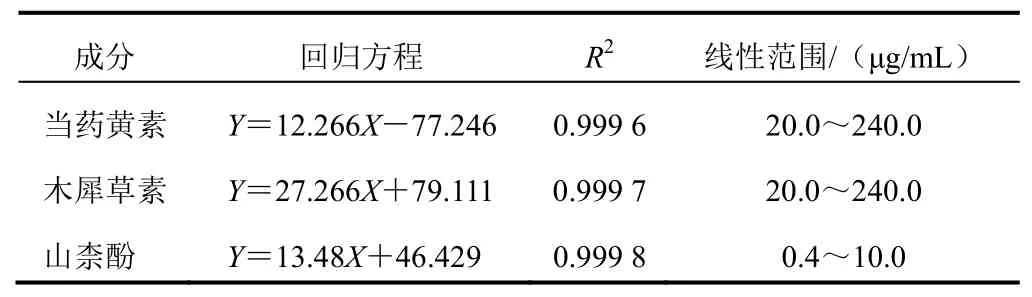
表1 3种指标成分线性关系考察结果
2.1.7 精密度试验
精密吸取“2.1.2”项下混合对照品溶液5 μL,按“2.1.1”项下色谱条件连续进样6次,测定并计算峰面积RSD,结果当药黄素、木犀草素、山柰酚峰面积RSD分别为0.83%、0.67%、0.98%。表明仪器精密度良好。
2.1.8 稳定性试验
取供试品溶液,室温放置,分别于0、4、6、8、12、24 h精密吸取5 μL进样测定,结果当药黄素、木犀草素、山柰酚峰面积RSD分别为0.97%、1.69%、0.88%,表明供试品溶液中上述3种成分于室温放置24 h内稳定。
2.1.9 重复性试验
平行制备6份供试品溶液,按“2.1.1”项下色谱条件进样测定,记录峰面积,计算当药黄素、木犀草素、山柰酚含量RSD分别为1.24%、2.38%、1.64%,表明方法重复性良好。
2.1.10 加样回收率试验
分别精密吸取已测定含量的供试品溶液6份,按1∶1比例添加当药黄素、木犀草素、山柰酚对照品适量,按“2.1.1”项下色谱条件进样测定,计算各成分平均加样回收率。结果当药黄素、木犀草素、山柰酚的平均加样回收率分别为98.28%、99.53%、98.49%,表明方法准确性良好。
2.1.11 样品测定
精密吸取正交试验水提浓缩液样品,按“2.1.3”项下方法制备供试品溶液,平行2份,进样测定,每份样品重复测定2次,根据线性回归方程,计算样品中当药黄素、木犀草素、山柰酚含量平均值。
医疗设备是医院影像科管理的重点,如CT影像设备、超声影像设备、腹腔镜等医疗设备等,随着现代医疗卫生条件的进步,这些医疗设备的精密程度以及造价也不断提高,因此,加强对设备的管理与维护,延长设备的使用寿命,是保证临床治疗效果,控制医院运行成本的关键。随着现代信息技术的不断发展,其在医院影像科医疗设备管理中的运用也得到了普及,因此,如何打造系统、完善的信息管理模式,推动影像科医疗设备的管理与维护是当前医院管理工作的重要内容。
2.2 干膏得率测定
参照2020年版《中华人民共和国药典》(四部)通则2201出膏率测定方法。精密吸取已知原药材浓度的水提浓缩液5.0 mL于恒重蒸发皿中,水浴蒸干,105 ℃干燥3 h,干燥器中冷却30 min,迅速精密称定质量,计算干膏得率。干膏得率(%)=(M1-M2)÷CV×100%。式中,M1为恒重蒸发皿加干膏质量,M2为恒重蒸发皿质量,C为水提浓缩液含原药材浓度,V为取样体积。
2.3 提取工艺优化
2.3.1 吸水量考察
按处方量称取湿生扁蕾、金钱草共30 g,置于干燥带塞广口瓶中,加入200 mL蒸馏水,浸泡至全部透心,称定湿重,计算得平均吸水量约为原药材的2.9倍,即在提取过程中第2、3次加水量比第1次少3倍量原药材。吸水率(%)=(原药材湿重-原药材干重)×100%÷原药材干重。
2.3.2 正交试验设计
基于传统水煎工艺,选择水作为提取溶剂,由于处方药物均为全草入药,质地较轻,故选择加水量(A)为原药材的12、14、16倍,提取时间(B)选择0.5、1.0、1.5 h,提取次数(C)选择常规的1、2、3次。为确定最佳水提工艺条件,拟定L(3)正交表进行试验,以当药黄素、木犀草素、山柰酚的提取量及干膏得率为评价指标,采用熵权法对评价指标进行权重系数分配,计算综合评分,确定最优水提工艺,因素水平见表2。
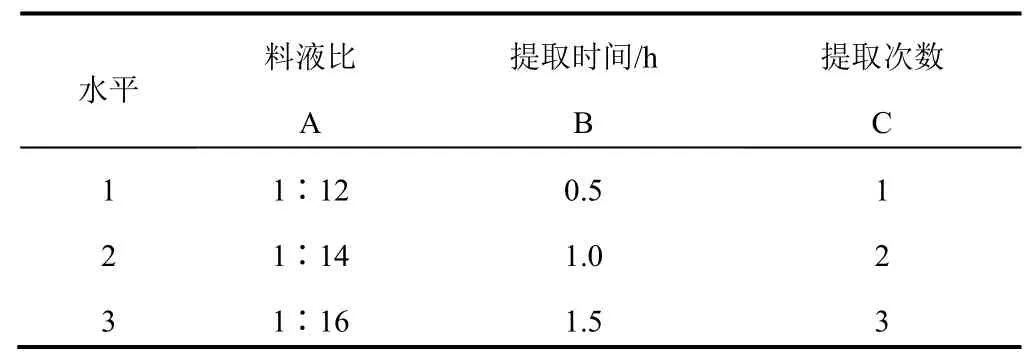
表2 金蕾颗粒提取工艺正交试验因素水平
2.3.3 正交试验数据处理
信息熵是衡量系统不确定性的无序程度的度量,也可用于在多指标系统中确定各指标权重。评价指标取值变异程度越大,数据越无序,提供信息量越多,该指标就越重要,反之则越不重要。
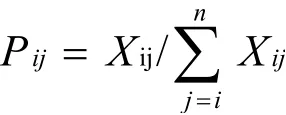
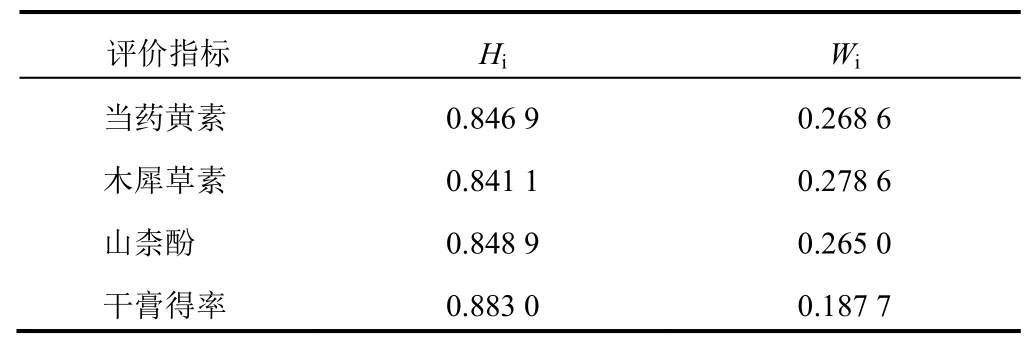
表3 金蕾颗粒提取工艺评价指标权重计算
根据各指标权重计算评价指标综合评分,对正交试验数据进行综合分析。综合评分=(当药黄素提取量/当药黄素最大提取量)×0.268 6×100+(木犀草素提取量/木犀草素最大提取量)×0.278 6×100+(山柰酚提取量/山柰酚最大提取量)×0.265 0×100+(干膏得率/最大干膏得率)×0.187 7×100。正交试验结果见表4。ABC、ABC、ABC综合评分分别为85.27、87.24、97.55,直观分析表明C因素(提取次数)对提取结果的影响最大。利用方差分析对最优提取工艺进行确定,结果见表5。
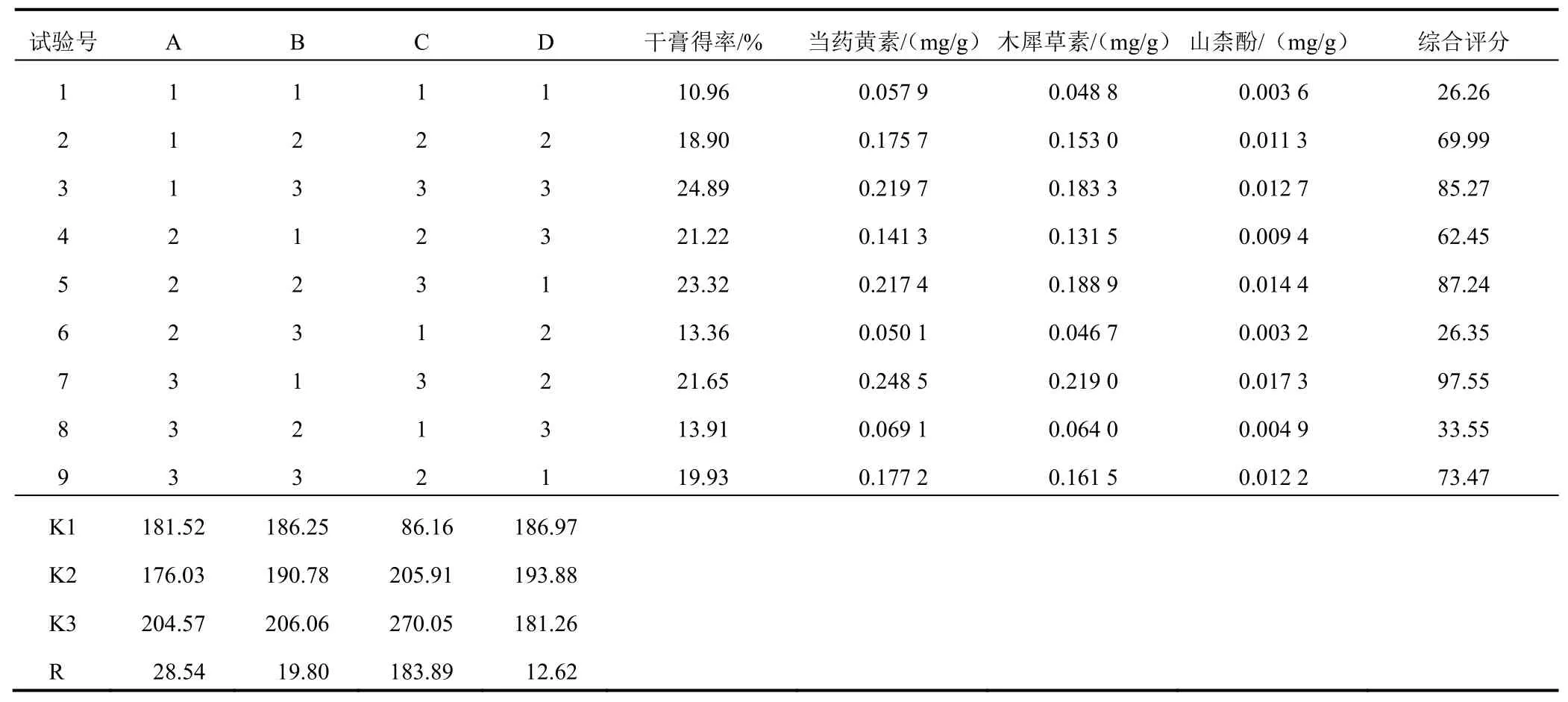
表4 金蕾颗粒提取工艺正交试验结果
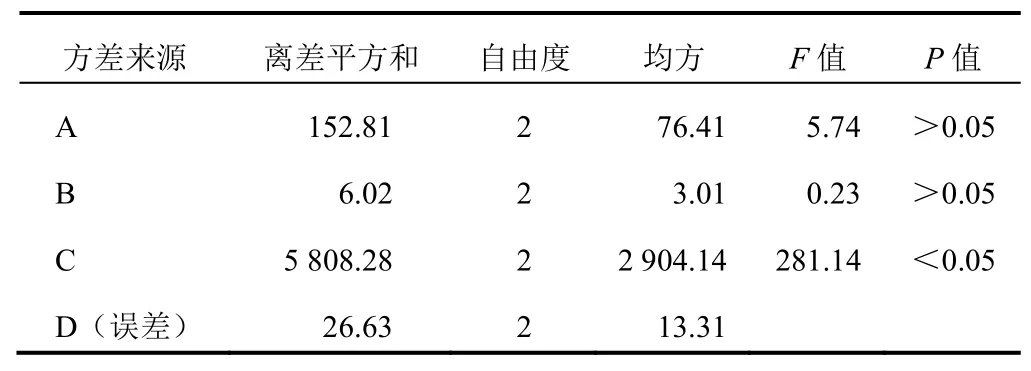
表5 金蕾颗粒提取工艺正交试验结果方差分析
由正交试验直观分析可知,各因素对金蕾颗粒水提工艺的影响为C>A>B,各因素不同水平的影响为:A>A>A,B>B>B,C>C>C。方差分析发现,C因素三水平间差异有统计学意义(<0.05),根据LSD两两比较方差分析并结合生产实际确定最优水平组合为ABC,即加12倍量水提取3次,每次0.5 h。
2.3.4 水提工艺验证
按处方量称取湿生扁蕾、金钱草共30 g,平行3批,按最佳水提工艺ABC进行提取,计算干膏得率和指标成分提取量,结果见表6。表明该工艺稳定可行,符合大生产要求。
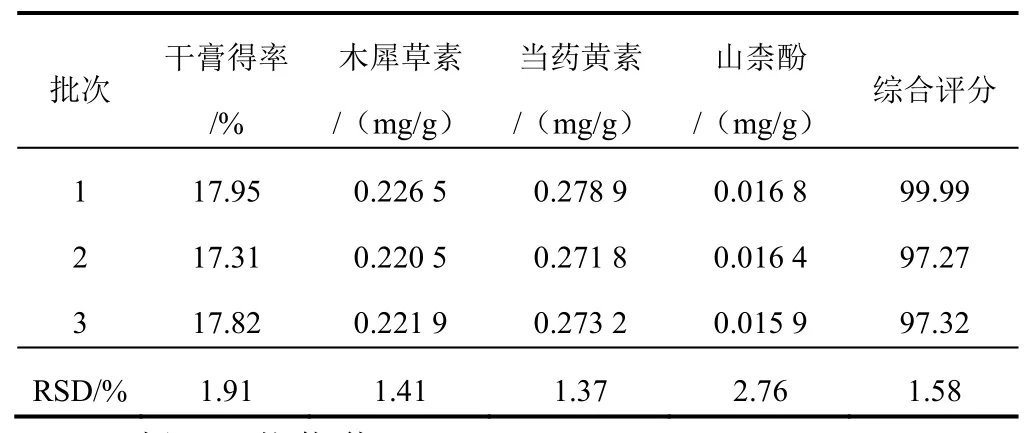
表6 金蕾颗粒提取工艺验证试验
2.4 醇沉工艺优化
水提后醇沉除杂可提高药物治疗效果、减少服用量,适用于工业化大生产。本研究选取对醇沉影响较大的醇沉终点乙醇浓度、药液相对密度、静置温度为考察因素,以当药黄素、木犀草素、山柰酚的转移率及干膏得率为指标,采用单因素试验确定最佳醇沉工艺。指标成分转移率(%)=醇沉前指标成分含量÷醇沉后指标成分含量×100%。
2.4.1 单因素试验
2.4.1.1 药液密度
按最佳水提工艺提取得水提液,分为3等份,分别浓缩至相对密度为1.00~1.02、1.03~1.05、1.06~1.08(25 ℃),精密量取30 mL浓缩液,在搅拌速度为900 r/min条件下匀速滴入95%乙醇至乙醇浓度为70%,室温静置24 h,取上清液减压旋蒸至无醇味,按上述方法测定当药黄素、木犀草素、山柰酚转移率及干膏得率,结果见表7。随着药液相对密度增加,干膏得率逐渐减小,指标成分转移率在药液相对密度为1.00~1.02、1.03~1.05时较高但相差不大,考虑工业大生产乙醇用量,选择药液密度为1.03~1.05。
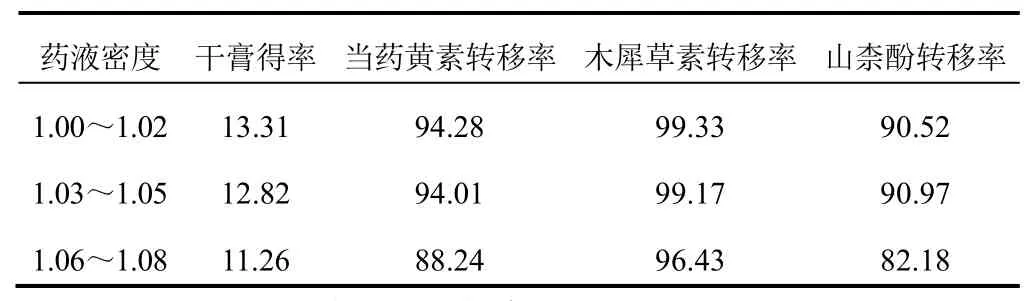
表7 不同醇沉药液密度的干膏得率及指标成分转移率比较(%)
2.4.1.2 醇沉终点乙醇浓度
精密量取30 mL相对密度为1.00(25 ℃)的水提浓缩液3等份,在搅拌速度为900 r/min条件下匀速滴入95%乙醇,使终点乙醇浓度分别达60%、70%、80%后密封,室温静置24 h,取上清液,减压旋蒸至无醇味,按上述方法测定当药黄素、木犀草素、山柰酚转移率及干膏得率,结果见表8。随着醇沉终点乙醇浓度增加,干膏得率逐渐减小,各指标成分的转移率在乙醇浓度为70%、80%时较高但相差不大,考虑后续成型的服用剂量及制剂成本,选择醇沉终点乙醇浓度为70%。
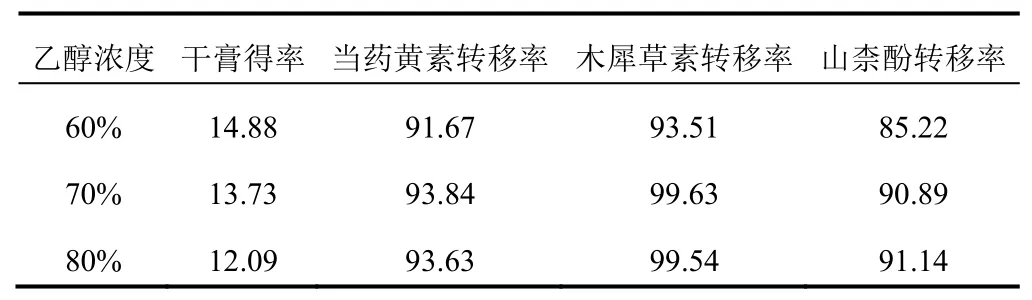
表8 不同醇沉终点乙醇浓度的干膏得率及指标成分转移率比较(%)
2.4.1.3 静置温度
按“2.4.1.1”“2.4.1.2”项下优选条件进行醇沉后,分别于室温、10 ℃、4 ℃环境静置24 h,测定当药黄素、木犀草素、山柰酚的转移率及干膏得率,结果见表9。不同静置温度的指标成分转移率均无明显变化。随着静置温度降低,颗粒沉降速度加快,醇沉上清液澄明度更好(表明药液质量更好),干膏得率逐渐减小,考虑药液质量及耗能因素,确定醇沉静置温度为10 ℃。
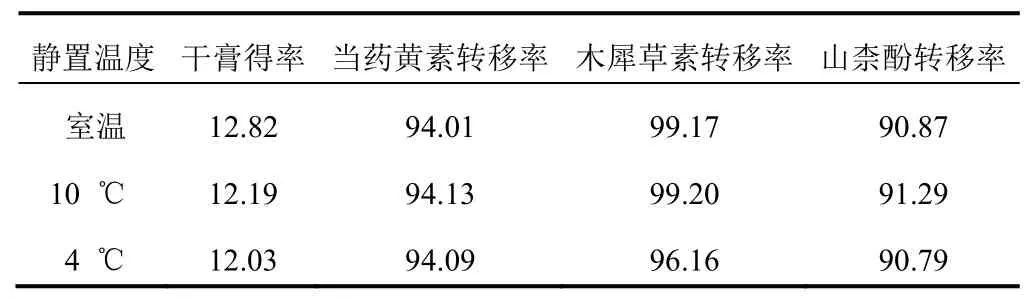
表9 不同醇沉静置温度的干膏得率及指标成分转移率比较(%)
2.4.2 醇沉工艺验证
对优选的醇沉工艺进行3批验证,按处方量称取90 g药物饮片,按最佳水提工艺提取,浓缩至醇沉前药液密度为1.03~1.05,在900 r/min转速下匀速滴入95%乙醇至乙醇浓度为70%,密封,10 ℃静置24 h,取上清液减压旋蒸至无醇味,定容至一定体积,测定干膏得率及各指标成分的转移率,结果见表10。表明该醇沉工艺稳定、可靠,符合大生产要求。
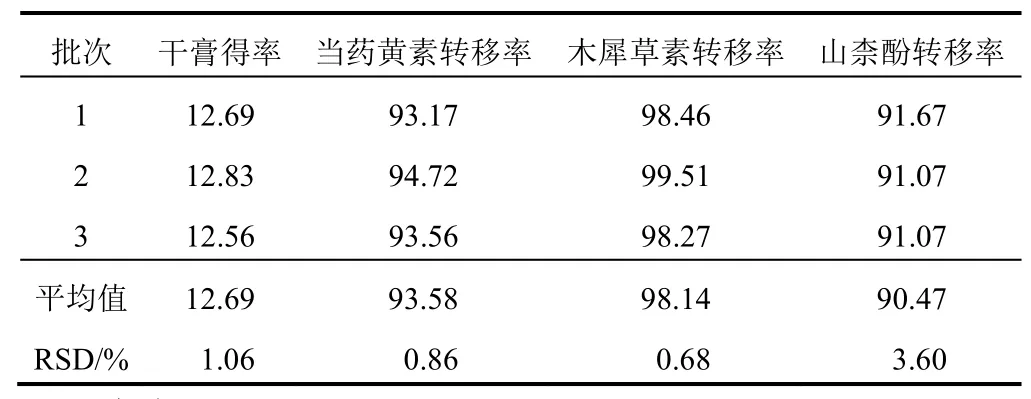
表10 金蕾颗粒醇沉工艺验证试验(%)
3 讨论
将金蕾复方改为颗粒剂,既可保留汤剂吸收迅速、起效快的优点,同时解决携带、贮存、服用不便的缺点。中药复方所含成分复杂,药理作用具有多层次、多靶点的特点,为避免破坏复方的整体性,采用传统的水提工艺。中药水提液中一般含有淀粉、蛋白质等无效组分,为提高单位有效组分含量、增加药液稳定性、减小后续颗粒剂的服用剂量,本试验在水提工艺基础上进行醇沉。在醇沉过程中,醇沉前药液密度过大会出现包合现象,造成有效成分转移率下降,密度过小则乙醇用量大,增加制药成本;醇沉终点乙醇密度过大会导致有效成分转移率降低,过小则杂质去除量减小,后续所得制剂无法显著减小服用剂量;醇沉后静置温度可影响颗粒沉降速度,进而影响醇沉上清液澄明度,故考察醇沉静置温度,可在保证最低耗能的前提下,提高药液质量和制药效率。因此,醇沉工艺选择醇沉前药液密度、醇沉终点乙醇浓度、静置温度为考察因素具有一定的实际意义。根据课题组前期药理研究,金蕾复方中黄酮类和■酮类成分为治疗胆囊炎的主要药效成分,在预试验中湿生扁蕾中■酮类成分以水为提取溶剂的条件下提取量极小,未达到最低定量要求,因此以当药黄素、当药醇苷、山柰酚为指标成分;干膏得率对后续颗粒剂成型、服用剂量有一定影响,因此将干膏得率纳入考察指标具有实际意义。
综上,本研究在中医理论指导下结合生产实际,对金蕾复方水提醇沉工艺进行优化,更接近大生产实际情况,但指标成分的确定仅依赖于目前相关药材的药理学研究,尚不全面,有待进一步完善。

