高效液相色谱-质谱联用法同时测定盐酸二甲双胍肠溶片中6种亚硝胺类基因毒性杂质
徐艳梅,李挥,张素平,乔晓宁,苗会娟,盖成,王茉莉,高燕霞
(河北省药品医疗器械检验研究院,石家庄 050200)
基因毒性杂质的毒性是近年来人用药物注册技术要求国际协调会(ICH)、美国食品药品监督管理局(FDA)、欧洲药品管理局(EMA)等国外药监部门密切关注的问题。基因毒性杂质可以直接或间接地损害DNA,从而导致基因突变或癌症,对人体具有潜在的危害[1]。自从缬沙坦检出N-亚硝胺类基因毒性杂质后,国内外持续对N-亚硝胺类基因毒性杂质高度关注。虽然基因毒性杂质的检测已经开展了很多年,但却集中在食品[2-7]、水[8-12]、烟草[13-14]等领域。随着对药品中基因毒性杂质的控制越来越严格,检测药品中N-亚硝胺类基因毒性杂质的研究方法逐渐增多[15-18]。
盐酸二甲双胍是目前国内外应用较为广泛的降糖药,其价格便宜、疗效好、不良反应少,是治疗单纯经饮食和运动不能良好控制的2型糖尿病的一线降糖药物。然而,2020年6月份,FDA发文表示,在一些二甲双胍制剂中,N-亚硝胺类基因毒性杂质含量超出限度,并建议一部分企业自愿召回[19]。目前,国内有高效液相色谱-质谱法用于测定盐酸二甲双胍片及二甲双胍格列本脲胶囊[20]中N-亚硝基二甲胺(NDMA)的报道,刘博等[21]使用液相色谱-质谱联用技术测定了盐酸二甲双胍缓释片中7种亚硝胺类基因毒性杂质。气相色谱-质谱法也被文松松等[22]用于盐酸二甲双胍缓释片及二甲双胍格列苯脲片等多种剂型中NDMA的测定。然而目前我国并没有对于盐酸二甲双胍肠溶片中N-亚硝胺类基因毒性杂质的测定。鉴于液相-色谱质谱联用技术灵敏性较高可完成微量基因毒性杂质的测定,为确保药品应用的安全,笔者参考以往实验方法[21-24],建立了高效液相色谱-质谱联用法同时测定盐酸二甲双胍肠溶片中6种基因毒性杂质的方法,并进行了方法学验证。
1 实验部分
1.1 主要仪器与试剂
高效液相色谱-质谱联用系统:高效液相色谱仪配备LC-30AD二元泵、CTO-20AC柱温箱、SIL-30AC自动进样器、SPD-20A紫外检测器,日本岛津公司;Triple Quad 6500型质谱仪,美国AB SCIEX公司。
电子天平:XS105型,感量为0.01 mg,瑞士梅特勒托利多有限公司。
盐酸二甲双胍肠溶片:批号分别为72105111、72105112、72105113,市购。
甲醇、甲酸:色谱纯,赛默飞世尔科技中国有限公司。
实验用水为超纯水。
6种基因毒性杂质对照品信息列于表1。

表1 6种基因毒性杂质对照品信息
1.2 溶液的制备
供试品溶液:取盐酸二甲双胍肠溶片20片,研细,精密称取500 mg,置于10 mL容量瓶中,加入适量甲醇溶液振摇使其溶解,用水定容至标线,摇匀,即得。
对照品储备溶液:分别称取对照品各25 mg,精密称定,分别置于25 mL容量瓶中,加甲醇溶液适量使其溶解,并稀释至标线,摇匀,制成各化合物质量浓度均为1 mg/mL的对照品储备溶液。
NDEA、NDMA、NMBA、NDBA、NDIPA、NEIPA混合对照品溶液:分别精密量取6种物质的对照品储备液适量置于同一容量瓶中,用甲醇溶液稀释至标线,摇匀,制成各物质质量浓度均为0.1 μg/mL的混合对照品溶液。分析前用甲醇稀释成系列浓度。
1.3 仪器工作条件
1.3.1 色谱
色 谱 柱:ACE C18-HL柱(150 mm×4.6 mm,5 μm,广州菲罗门科学仪器有限公司);柱温:40 ℃;流动相:A相为0.1%甲酸水,B相为甲醇;洗脱模式:梯度洗脱,洗脱程序列于表2;流量:0.6 mL/min;进样体积:5 μL。
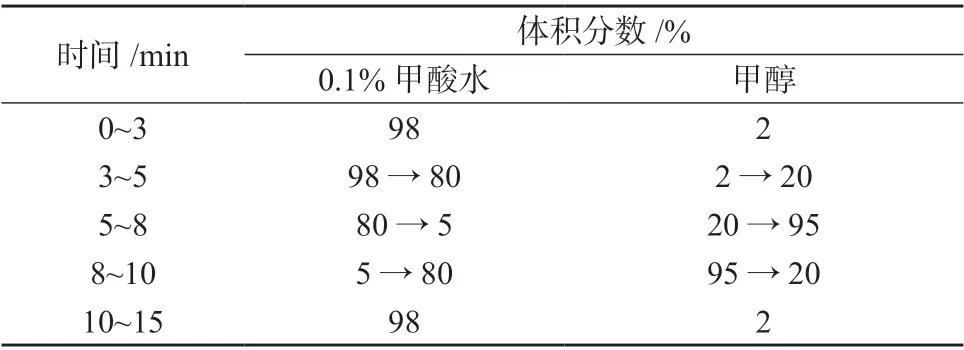
表2 洗脱程序
1.3.2 质谱条件
离子源为大气压化学电离源(APCI源);正离子模式检测;扫描模式为多反应监测模式(MRM);离子源温度:350 ℃;脱溶剂气流量:35 mL/min;NC电 流:3 μA;气帘气(CUR):206.8 kPa;雾化气(GS1):241.3 kPa。其它实验参数列于表3。
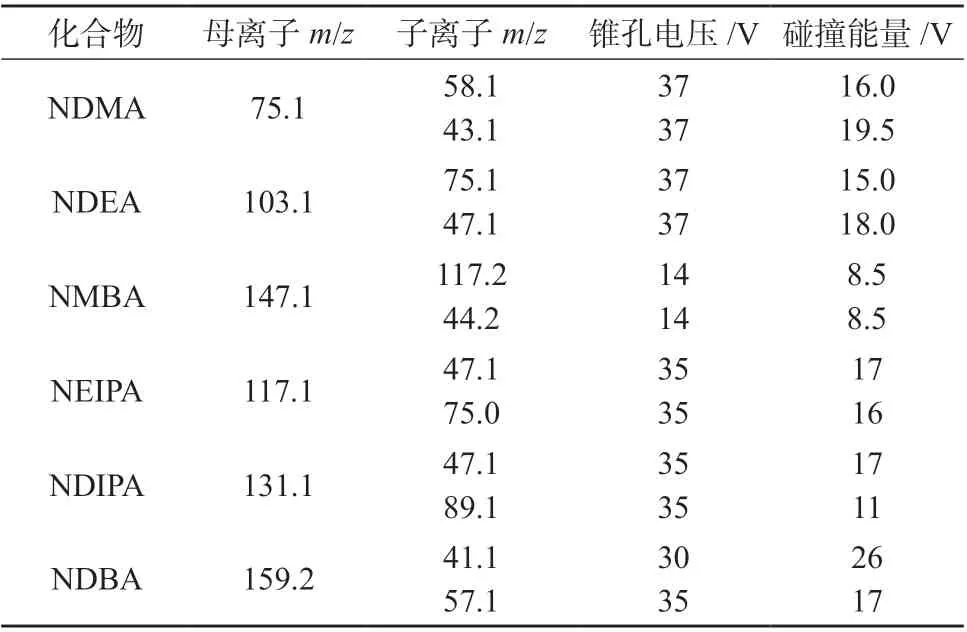
表3 质谱条件
2 结果与讨论
2.1 方法学考察
通过改变流量、柱温、流动相B的初始比例对1.3中方法的耐用性进行了考察[23-24]。结果表明,对流量、柱温、流动相B的初始比例进行微调后,各物质色谱峰峰面积基本一致,即6种N-亚硝胺类基因毒性杂质的测定量基本一致,说明该方法中的色谱条件耐用性良好。
2.2 溶剂的选择
分别选取水、甲醇及50%甲醇作为溶剂进行了考察。盐酸二甲双胍肠溶片中含有辅料羟丙甲纤维素,其溶于水及大多数极性溶剂,然而羟丙甲纤维素在水中会溶胀成澄清或微浊胶体溶液,严重影响盐酸二甲双胍的溶解性,故应避免使用水及水溶液作为溶剂,因此选择甲醇作为溶剂。
2.3 专属性考察
取混合对照品溶液、供试品溶液和溶剂,分别按1.3项下色谱条件进样分析,记录色谱图,溶剂、供试品溶液和混合对照品溶液色谱图分别见图1、图2、图3。

图1 溶剂色谱图
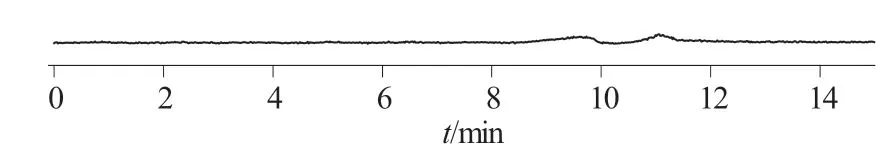
图2 供试品溶液色谱图
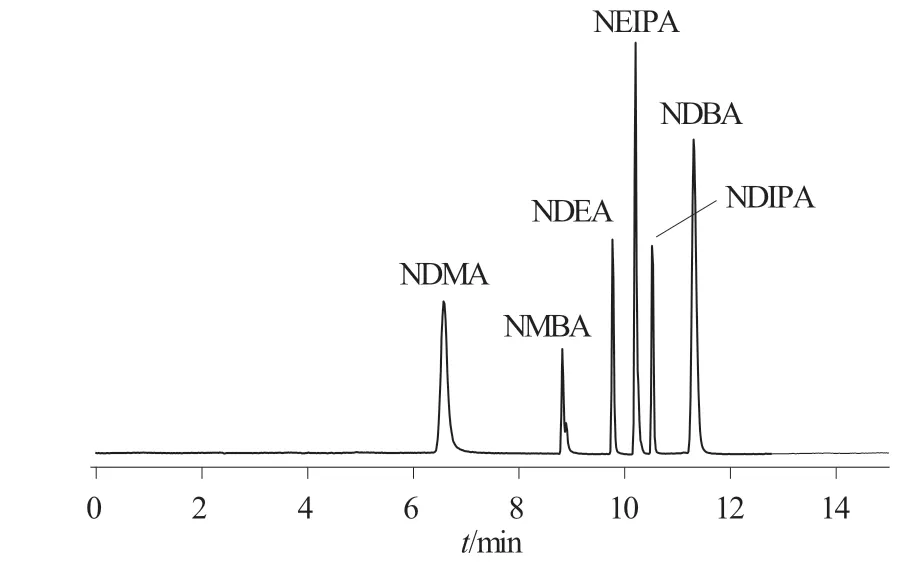
图3 混合对照品溶液色谱图
测定结果表明,溶剂不干扰测定,NDEA、NDMA、NMBA、NDBA、NDIPA、NEIPA在该色谱条件下分离度良好。
2.4 线性关系、检定限与定量限
分别精密量取1.2中混合对照品溶液0.1、0.2、0.5、1.0、5、10 mL置于10 mL容量瓶中,加甲醇稀释至标线,制成各物质质量浓度分别为1、2、5、10、50、100 ng/mL的系列混合标准工作溶液。按1.3色谱条件进样分析,记录色谱图,以NDEA、NDMA、NMBA、NDBA、NDIPA、NEIPA的质量浓度为横坐标(x),以色谱峰峰面积为纵坐标(x),绘制标准曲线,计算得到线性回归方程与相关系数,结果列于表4。
取混合对照品溶液逐步稀释成不同浓度,按1.3色谱条件进样分析,连续测定6次,记录色谱图,以信噪比S/N=3和S/N=10分别作为检测限(LOD)和定量限(LOQ),结果见表4。
由表4可知,6种化合物在各自范围内线性关系良好,相关系数均不小于0.999 5,方法灵敏度高。检测限和定量限分别为0.033 7~0.0338 9 ng/mL和0.100 76~0.102 68 ng/mL。

表4 6种化合物的线性方程、相关系数、线性范围、LOD、LOQ
2.5 仪器精密度与重复性试验
精密量取1.2中混合对照品溶液,按1.3项下色谱条件进样分析,重复进样6次,记录色谱图,计算各化合物色谱峰峰面积的相对标准偏差,考察本方法的仪器精密度,结果列于表5。

表5 仪器精密度实验结果
由表5可知,6种N-亚硝胺类化合物测定结果的相对标准偏差为0.8~3.5%,表明仪器的精密度良好。
2.6 加样回收试验
精密称取空白供试品约100 mg,共9份,置于10 mL容量瓶中,加入甲醇溶解,再分别精密加入混合对照品溶液0.2、0.5、1.0 mL各3份,加甲醇定容至标线,摇匀。按1.3的色谱条件进样分析,记录色谱图,计算加标回收率,结果列于表6。由表6可知,6种N-亚硝胺类平均回收率为97.83%~103.33%,测定结果的相对标准偏差为1.19%~4.45%,表明本法的回收率良好。

表6 加样回收率试验结果
2.7 稳定性试验
按1.2方法制备混合对照品溶液和供试品溶液,于室温放置0、1、2、3、6、10 h后按1.3项下色谱条件进样分析,记录色谱图,计算各物质含量的相对标准偏差,考察其稳定性,结果见表7。
由表7可知,6种N-亚硝胺类对照品含量测定结果的相对标准偏差为0.3%~1.8%,表明对照品溶液与供试品溶液在10 h内稳定性良好。

表7 不同时间下6种N-亚硝胺类物质色谱峰面积
3 结语
建立了高效液相色谱-质谱联用法适用于盐酸二甲双胍肠溶片中6种亚硝胺类基因毒性杂质的同时检测,且检测结果准确,操作简便、灵敏,可用于监控盐酸二甲双胍肠溶片中基因毒性杂质的水平,为其质量控制提供参考,同时能够更好的确保药品的安全性,具有实际的应用价值。

