高性能钛硅分子筛可控合成及其催化丙烯气相环氧化研究进展
林栋,冯翔,刘熠斌,陈小博,杨朝合
(中国石油大学(华东) 重质油国家重点实验室,山东青岛 266580)
钛硅分子筛的发现被认为是分子筛催化领域的里程碑之一,已经成功应用于烯烃绿色环氧化领域,高性能钛硅分子筛结构的有效调控成为当前烯烃环氧化技术发展的关键之一。环氧丙烷(PO)作为全球产量最大的50 种化学品之一,广泛应用于汽车、建筑、化妆品以及食品等日常生活中的诸多领域,以钛硅分子筛作为催化剂生产环氧丙烷由于其绿色环保优势得到广泛关注。
然而遗憾的是,我国近60%的环氧丙烷生产仍然采用以有毒氯气为原料的氯醇法,带来极为严重的环境和安全问题。除氯醇法外,目前工业化技术还有共氧化法和HPPO法,二者克服了氯醇法污染严重的问题,但经济性受制于其联产品,并存在高浓度双氧水溶液储运困难的问题。相比于上述环氧丙烷的工业生产工艺,使用H和O直接氧化丙烯制环氧丙烷的新工艺凭借绿色环保、操作流程简单、设备投资和操作成本低、经济利润高的独特优势受到学术界和工业界的共同关注。
本文系统总结了高活性钛硅分子筛的合成策略,同时基于丙烯临氢气相环氧化反应简要综述相关双活性位点的反应机理,总结高效金属位点的负载策略,并分析了目前丙烯环氧化所遇到的挑战及发展方向,以期为高性能环氧化催化剂的合成提供指导。
1 高效含钛载体的构筑与工业应用
烯烃环氧化需要高性能的钛硅分子筛来催化烯烃和过氧化物中间体反应生成相应的环氧化合物,因此精准设计高效的分子筛结构成为烯烃环氧化性能调控的关键。其中,钛硅分子筛的结构调控不仅包括在原子尺度上合成不同结构的含钛分子筛以及相应具有不同硅钛比的载体,还包括含钛载体的表界面疏水性以及颗粒的传质性能。
1.1 不同结构的含钛载体
分子筛载体结构的不同,导致分子筛骨架中插入的钛原子的环氧化性能呈现出显著的差异。Cheng 等成功合成含有0.67nm 微孔的Ti-YNU-1和含有2nm 介孔的Si/Ti-MCM-36,并采用沉积沉淀法负载金纳米颗粒,如图1(a)所示。结果显示,Ti-YNU-1中Ti的配位环境主要为孤立的四配位骨架钛(T),而Si/Ti-MCM-36中则主要为四配位骨架钛(T)和八配位骨架钛(O)的混合配位形式。Ti-YNU-1 中孤立的四配位骨架钛能够促使生成的金纳米颗粒更小,而Si/Ti-MCM-36 在较高Ti含量时可以锚定更多金物种,从而促使生成的金纳米颗粒更大。
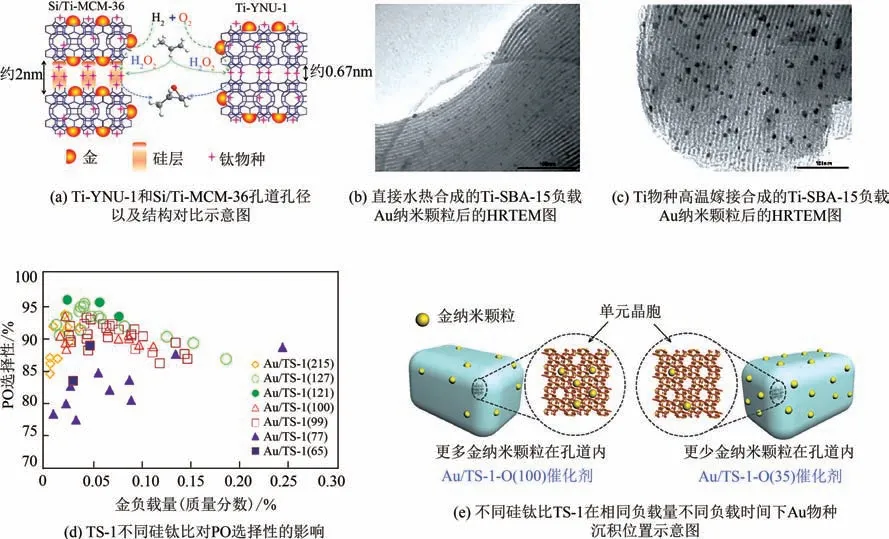
图1 具有不同结构的含钛分子筛
不同载体结构的分子筛可以通过改变骨架钛物种的配位环境来改善金纳米颗粒的分散度,从而改善烯烃环氧化反应性能。Nijhuis等通过水热原位合成和高温嫁接钛酸异丙酯到纯硅SBA-15上成功合成Ti-SBA-15,大量的实验表征证明在SBA-15骨架中成功插入Ti原子并没有引起SBA-15骨架结构的坍塌。环氧化实验考评表明,通过Ti 物种嫁接合成的Ti-SBA-15比直接水热合成的Ti-SBA-15具有更高的烯烃环氧化活性。这是由于相比于直接水热合成的Ti-SBA-15,通过Ti 物种嫁接合成的Ti-SBA-15具有更高的钛含量,并且金纳米颗粒的分散性更好,如图1(b)和(c)所示。Ti物种的嫁接不仅可以应用到具有晶体结构的分子筛上,同时还可以应用在无定形的二氧化硅上。Nijhuis等以钛酸四乙酯为钛源通过高温嫁接法将Ti 原子嫁接到无定形二氧化硅上(Ti-SiO)。通过沉积沉淀法负载金纳米颗粒,可以在Ti-SiO的钛位点周围得到高度分散的金纳米颗粒,这种特定的无定形二氧化硅(Ti-SiO)有效提高了Au-Ti 界面位的含量,进而提高活性过氧化物中间体的利用率,从而提高烯烃环氧化的活性。
华东理工大学周兴贵团队通过采用堵孔TS-2 作为载体来锚定金纳米颗粒,丙烯环氧化反应结果表明,Au/堵孔TS-2催化剂拥有较长的反应诱导期,稳定的丙烯环氧化反应性能和较高的环氧丙烷生成速率。优异的环氧化性能主要归结于Au-Ti-Ti三中心活性位点,其中堵孔TS-2载体所特有的Ti位点会显著抑制丙烯环氧化过程中焦炭的产生,从而有效提高丙烯环氧化稳定性。Haruta等合成Ti-MCM-41 和Ti-MCM-48 载体并通过沉积沉淀法来负载Au 纳米颗粒催化丙烯环氧化。气相色谱和质谱联用的结果表明,相比于单纯具有一维孔道结构的Ti-MCM-41,Ti-MCM-48 所具有的三维孔道结构,能更有效耐受环氧丙烷(PO)衍生低聚物以及尺寸更大的有机物所带来的孔道堵塞,从而进一步改善了丙烯环氧化的性能。Wu等通过硼酸辅助法采用哌啶做模板剂成功合成Ti-MWW分子筛,并采用沉积沉淀法负载Au 纳米颗粒合成Au/Ti-MWW 催化剂。然而,相比于传统Au/TS-1,该催化剂具有更低的产物选择性。红外光谱和硅核磁表明由于Ti-MWW 所具有的二维平面结构,表面暴露的大量硅羟基促使生成的PO 等产物无法及时脱附,造成了产物选择性的降低。此外,高分辨电镜(HRTEM)结果表明二维的平面促使表面Au 纳米颗粒尺寸变大,从而进一步降低了反应的选择性。Oyama 等通过负载金纳米颗粒于介孔Ti-TUD(约13nm)分子筛上来催化丙烯环氧化。相比于Au/TS-1,Au/Ti-TUD 催化剂的丙烯转化率较低(0.9%),即使在添加Ba 助剂之后,丙烯的转化率也只有1.4%,并且环氧丙烷的生成速率为25.3g/(h·kg)。本文作者团队开发了一种简单高效且具有普适性的无须添加剂的绿色合成路线,可以用于一系列钛硅分子筛(MFI、MEL 和BEA)的合成,如图2(a)所示。相比于传统钛硅分子筛合成方法[如图2(b)],通过采用紫外光辐射原位产生的羟基自由基来逆向解聚钛低聚物为钛单体[如图2(c)],并且加速硅前体水解为硅单体,从而在快速合成的条件下依然可以实现硅钛前体水解速率的匹配[如图2(d)],进而避免非骨架钛物种的生成。相比于传统合成方法,该方法更加高效(前体溶胶制备时间缩短为原来的1/8)、更加简便(直接将所有原料进行混合而不需要复杂且缓慢的滴加方式)、更加环保(不需要添加表面活性剂和异丙醇),这为钛硅分子筛的工业化生产提供了新的高效绿色合成思路。以该方法合成的TS-1 在负载金纳米颗粒后展现出优异的丙烯气相环氧化反应性能[320g/(h·kg)]。
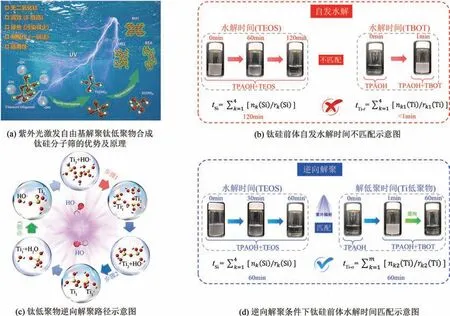
图2 紫外辐射辅助合成钛硅分子筛
对于钛硅分子筛而言,硅钛比成为TS-1 被广泛研究的内容之一。Delgass等在这方面进行了深入研究,发现在沉积沉淀法中,室温下控制金前体溶液pH 为7.3 左右时,随着载体中钛含量的增加,金物种的负载效率逐渐升高。丙烯环氧化反应结果表明,最佳硅钛比为100左右,而不是之前文献中所报道的30~100。如图1(d)所示,随着钛含量逐渐提升,TS-1硅钛比降低,丙烯环氧化选择性降低,丙醛选择性逐渐提高。这是由于钛含量的提升会促进非骨架钛物种的形成,丙烯环氧化产物的分布会明显受到Ti—O—Ti 键的影响,并且会加速过氧化氢中间体的分解,从而降低环氧化速率。载体的硅钛比会影响沉积沉淀过程中金物种的负载量。研究发现,在沉积沉淀法过程中,金物种会选择性地沉积到分子筛上的钛物种周围。因此,随着载体硅钛比的上升,在相同pH 下硅钛比为35 的TS-1 相较硅钛比为100 的TS-1 在达到相同Au 负载量时需要更短的老化时间,分别为6h和10h。氮气吸脱附实验表明,在室温条件下更长的老化时间会促进更多的Au前体进入分子筛孔道中[如图1(e)],促使Au纳米颗粒分散更均匀。但是过多的Au 纳米颗粒进入TS-1 微孔孔道中,则会导致催化剂更迅速地失活。
具有二维结构的含钛分子筛(如Ti-MWW)能够从物理结构上极大地改善烯烃反应物的空间位阻与内扩散,但是由于二维平面结构表面大量的骨架硅原子无法配位,从而造成载体含有大量的硅羟基,不利于反应产物的脱附。此外,尽管具有2~50nm介孔含钛分子筛(如Ti-SBA-15、Ti-MCM-41、Ti-MCM-48、Ti-TUD等)相比于传统具有<2nm微孔的含钛分子筛(如TS-1 和TS-2 等)具有更大的孔径,更有利于反应物分子的扩散,但是催化剂表征和烯烃环氧化反应的结果表明,微孔分子筛的限域效应能够有效减小Au纳米颗粒的尺寸,改善Au纳米颗粒的空间分布,提高活性位的数目,从而有效提高丙烯临氢气相环氧化的活性。因此微孔与介孔之间存在一个最优的比例,从而在强化丙烯环氧化活性的同时强化丙烯环氧化的稳定性。
1.2 含钛载体的表面疏水性
提高含钛载体的表面疏水性可以减弱硅羟基和环氧化产物的氢键相互作用,促进环氧化产物在催化剂表面的脱附,进而抑制环氧化产物的进一步开环,提高环氧化产物的选择性。目前来说,提高含钛载体表面疏水性主要是通过载体硅烷化的方法,此外氟化铵处理和构造核壳结构也是提高分子筛表面疏水性的一种方法。
含钛载体表面硅烷化是目前催化剂提高表面疏水性最常用的方法。Haruta等通过气相甲氧基三甲基硅烷处理三维介孔钛硅分子筛来修饰钛硅分子筛表面,提高该三维介孔钛硅分子筛的表面疏水性,有效改善了产物的脱附,提高了烯烃环氧化反应收率。此外,通过加强环氧化产物的脱附过程减少了催化剂的积炭量,提高了催化剂的环氧化稳定性。此外,Haruta等通过气相甲氧基三甲基硅烷处理来促使钛硅分子筛载体硅烷化并在混合气中添加三甲胺来控制催化剂的失活。如图3(a)所示,丙烯环氧化反应表明,负载金纳米颗粒的甲硅烷基化钛硅分子筛在含三甲胺的混合气体中处理后,环氧丙烷收率得到了提高,并且环氧化的失活速率被明显抑制。这是由于三甲胺在混合气体(氢气、氧气、氩气和三甲胺)处理过程中保护了硅烷化学键免受水分的破坏性影响。除采用传统的硅烷化来提高载体表面疏水性外,本文作者团队通过构造以纯硅S-1 分子筛为核、TS-1 分子筛为壳的核壳结构分子筛(TS-1/S-1)来改善分子筛载体的疏水性和传质性能,如图3(b)所示。负载金纳米颗粒之后的Au/TS-1/S-1具有优越的丙烯环氧化稳定性和活性。催化剂的积炭质量分数由传统催化剂的4.9%显著降低到0.99%,并且完全抑制了芳香碳在催化剂上的生成。该催化剂优越的性能除了归结于这种特殊的核壳结构所引起的反应物和产物扩散路径的缩短,更重要的是合成过程中的重结晶作用可能促使Si—OH变成Si—O—Ti,从而显著提升载体的疏水性[如图3(c)和(d)],促进环氧化产物的脱附。
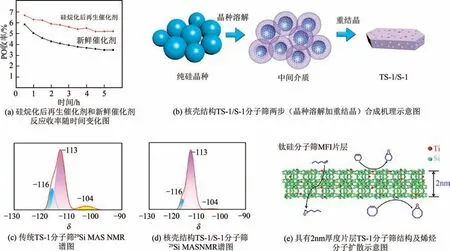
图3 含钛载体表面疏水性
此外,Ryoo等提出采用氟化铵处理片层钛硅分子筛减少片层钛硅分子筛表面大量暴露的硅羟基,从而提高载体表面疏水性,如图3(e)所示。不同于硅烷化方法在钛硅分子筛表面嫁接硅烷分子基团,氟化铵处理主要通过促进相邻硅羟基缩合形成全新的Si—O—Si 化学键来提高载体表面疏水性,载体表面发生的相关缩合反应如式(1)。
(SiO)Si—OH+(SiO)Si—OH===== HO+(SiO)Si—O—Si(SiO)(1)
和硅烷化法不同的是,氟化铵处理不需要在表面引入新的硅烷分子基团,主要通过相邻硅羟基缩合来提高表面疏水性。因此,氟化铵处理能够有效降低催化剂与反应物分子的空间位阻,提高反应物分子与催化剂活性位点的接触概率,进而改善烯烃环氧化的反应性能。经过氟化铵处理的疏水性片层钛硅分子筛能够提高环氧化反应的转化率接近一倍。该方法为疏水性分子筛的制备提供了一种全新且高效的方法,在有效提高载体表面疏水性的同时,降低了载体表面反应物分子的空间位阻。
1.3 含钛载体的传质性能
提高钛硅分子筛载体的传质性能不仅可以有效增大反应物分子和活性位点的接触概率,提高烯烃环氧化活性;而且可以加速环氧化产物在分子筛孔道内的扩散,减少产物的开环和聚合反应,抑制催化剂载体的生焦与失活,从而有效提高催化剂的环氧化稳定性。改善含钛载体的传质性能通常采用两种方法:合成介孔含钛分子筛和构造微介复合多级孔道钛硅分子筛。
Nakamura 等通过合成Ti-MCM-41(六方介孔结构)和Ti-MCM-48(立方介孔结构)载体来负载金纳米颗粒,如图4(a)和(b)所示。气相色谱-质谱联用(GC-MS)结果表明,相比于Ti-MCM-41 一维的介孔孔道结构,Ti-MCM-48 所具有的独特的三维介孔孔道结构能够有效抵抗大分子有机物质以及环氧化合物的低聚物所造成的孔道堵塞,从而有效改善Au/Ti-MCM-48的烯烃环氧化性能。但与微介复合的钛硅分子筛相比,其烯烃环氧化性能仍然有较大的差距。因此,近年来微介复合多级孔道钛硅分子筛的合成成为改善载体传质性能的热点之一。
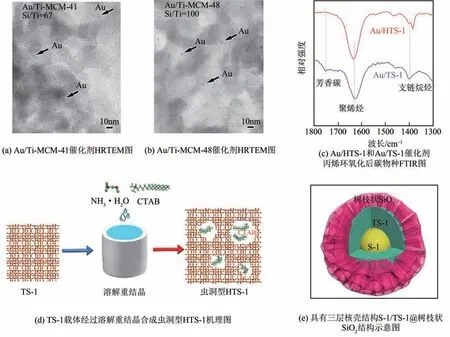
图4 含钛载体的传质性能
本文作者团队采用两步重结晶法成功合成具有45nm左右虫洞孔结构的TS-1分子筛(HTS-1),其中使用十六烷基三甲基溴化铵(CTAB)作为介孔模板剂,如图4(d)所示。负载金纳米颗粒的虫洞钛硅分子筛(Au/HTS-1)在无添加助剂的情况下展现出优越的丙烯环氧化活性、产物选择性和环氧化稳定性。氮气物理吸脱附测试结果表明环氧化反应过程中焦炭多在虫洞型介孔中生成,HTS-1载体相对于传统TS-1载体体现出更高的容碳能力。Au/HTS-1催化剂稳定的环氧化性能不仅归结于HTS-1优越的传质性能,而且HTS-1 通过重结晶作用促进Si—OH物种变成Si—O—Ti物种,提高载体疏水性,从而改善烯烃环氧化稳定性。如图4(c)所示,傅里叶红外谱图(FTIR)表明相对于传统TS-1 载体,HTS-1载体能够显著抑制芳香碳的产生,进而提高催化剂的稳定性。这种高稳定高活性的Au/HTS-1催化剂为烯烃环氧化提供了一种具有工业化前景的催化剂。此外,本文作者团队通过合成三层核壳结构S-1/TS-1@dendritic-SiO[如图4(e)]来减小环氧化活性层(TS-1)厚度,进而有效改善载体传质性能。氨气程序升温脱附谱图(NH-TPD)表明,最外层树枝状二氧化硅(dendritic-SiO)在避免遮盖环氧化活性位点(四配位骨架钛)的同时选择性地覆盖了载体表面的酸性位,从而有效抑制了环氧化产物的开环和聚合,提高产物选择性至93.9%。本文作者团队提出的构建多层核壳结构钛硅分子筛策略为强化载体传质性能提供了一种全新的方法。
1.4 TS-1钛硅分子筛工业化进展
基于目前相关文献的报道,钛硅分子筛的合成方法主要包括同晶取代法和水热合成法。同晶取代法又称为二次合成法,该方法主要包括气相同晶取代(TiCl为钛源)和液相同晶取代[(NH)TiF为钛源]两种方法。Kraushaar 等首次采用气相同晶取代法,以TiCl为钛源成功合成出Ti-ZSM-5。该方法首先将硅铝比(Si/Al)为50 的ZSM-5 在80℃的条件下用1mol/L 的盐酸脱去分子筛骨架上的Al 原子,从而形成硅羟基巢。然后通入TiCl气体将Ti原子插入酸处理形成的晶格空位中,形成骨架钛物种,进而合成含钛的ZSM-5。许章林等在液相体系中以(NH)TiF为钛源成功合成钛掺杂的ZSM-5。尽管同晶取代法可以有效降低操作的难度,但是由于其反应机理仍然存疑,且制备工艺中难以控制TS-1 的骨架钛含量,因此工业合成中很少涉及同晶取代法。
水热合成法产品质量稳定,目前在实验室合成和工业生产中均得到了广泛的应用。20 世纪80年代,意大利EniChem 公司在工业上成功合成出TS-1 钛硅分子筛并将该催化剂应用于氨气、双氧水和酮类物质一步反应生成肟。合成方法中首先需要将钛源和硅源进行混合,之后的晶化反应在130~200℃的溶液中进行,得到的固体物质在550℃的空气中焙烧后即为最终的产物。德国赢创(Degussa)公司和德国伍德(Uhde)公司合作开发的过氧化氢制环氧丙烷(HPPO)工艺中以钛硅分子筛为催化剂,合成方法为水热合成法,首先将钛源(四乙基原钛酸盐)和硅源(四乙基原硅酸盐)预先在低温下进行混合,然后不断向溶液中滴加模板剂(四烷基氢氧化铵)水溶液。其中,四丙基氢氧化铵用来制备TS-1,四丁基氢氧化铵用来制备TS-2,而四乙基氢氧化铵用来制备Ti-β。随后将得到的合成溶胶进一步晶化。产物经过离心干燥和焙烧即可得到相应的钛硅分子筛。
在我国钛硅分子筛领域,中国石油化工股份有限公司在钛硅分子筛专利申请保护方面居于领先。中国石油化工股份有限公司石油化工科学研究院(简称石科院)的林民团队成功开发出了单晶空心钛硅分子筛(HTS),并且成功将HTS-1 催化剂应用到环己酮肟化的工业生产中,打破了国外的技术垄断和控制。实际反应摩尔转化率大于99.5%,反应选择性大于99%。其HTS 的工业合成方法为水热合成法。首先将模板剂(TPAOH)、蒸馏水(HO)和硅源(TEOS)按照一定比例混合后将硅源适度水解,然后将含有钛源(TBOT)的异丙醇(IPA)加入上述溶液中。经过适当的低温成胶之后,将上述澄清透明的溶液加入晶化釜中高温晶化一段时间后冷却。冷却之后,分离出固体钛硅分子筛干燥焙烧后即可得到原粉。然后将该原粉与助剂混合均匀后,在晶化釜中通过分子筛的重排反应获得单晶空心钛硅分子筛(HTS)。之后,石科院以HTS 催化剂为活性组元,将其改性和成型后得到HPO-1 催化剂。HPO-1 催化剂成功应用到催化丙烯与双氧水合成环氧丙烷的工业放大实验中,双氧水转化率达到96%~99%,环氧丙烷选择性达到96%~98%。综上所述,钛硅分子筛的工业化合成方法中仍然以水热合成法为主,然而更简便且不含非骨架钛的高效合成方法仍然需要更进一步地探索。
2 丙烯临氢气相环氧化机理
以双氧水为氧化剂的绿色环氧化体系由于双氧水副产物仅为水,并且环氧化选择性高,引起了广泛的关注。其中双氧水的来源包括直接运输的成品双氧水和通过氢气氧气原位合成的双氧水。采用直接运输的成品双氧水来氧化丙烯,氧化效率较高,相关的工业开发技术不断涌现。其中,以双氧水为氧化剂,TS-1 分子筛为催化剂氧化丙烯生成环氧丙烷的HPPO 法已经实现了工业化。如果能进一步降低双氧水的成本,同时改善双氧水易爆炸和运输过程中易分解的难题,将有望继续提高HPPO技术的市场占有率。近年来,为了解决双氧水的运输和成本难题,采用氢气和氧气原位合成双氧水来氧化丙烯的技术吸引了工业界和学术界广泛的关注。该方法原料清洁廉价,成本较低,有利于工业的放大;其次,采用固定床反应,整体操作流程简单,产物容易进行分离;并且产物环氧丙烷的选择性高,可以减少分离成本。但是目前仍然处于实验室的研究阶段,反应稳定性的提升和氢效的提高仍然需要更进一步的研究与开发。
丙烯临氢气相环氧化作为钛硅分子筛重要的应用场景之一,其相关的机理研究对钛硅分子筛的应用有着重要的影响。尽管在液相环氧化反应中,钛硅分子筛中孤立的四配位骨架钛已经被广泛认为是丙烯和双氧水发生环氧化反应的活性位点,但是在丙烯临氢气相环氧化生成环氧丙烷的反应中,环氧化反应的具体活性位点及反应机制仍然存在争议。
自Haruta 等于1988 年首次发现Au/TiO可以催化氢气、氧气和丙烯反应生成环氧丙烷以来,这种具有高选择性、易操作性、分离简单、原子经济性等优点的丙烯环氧化技术受到了广泛的关注。该技术最大的特点是同时需要两种不同的活性位(载体的钛活性位和负载的金属活性位)来分别用于促进丙烯发生环氧化反应和活化氧气和氢气生成过氧化物,而其中关于丙烯环氧化的具体反应机理一直存在分歧。
Nijhuis等结合催化反应数据和原位红外光谱数据分析认为丙烯临氢气相环氧化的反应中间体为双配位丙氧基物种,如图5(a)所示。基于Nijhuis等的研究,负载于载体上的金纳米颗粒不仅可以促进氢气和氧气之间生成双氧水,从而进一步促进丙烯和双氧水发生环氧化反应;同时也可以促进反应中的丙烯和钛物种进行反应,进而在表面生成双配位丙氧基物种,该物种类似于环氧丙烷吸附在二氧化钛上形成的物种。金纳米颗粒进一步催化了吸附的双配位丙氧基物种生成相关的碳酸盐或者羧酸盐,这可能是催化剂失活的原因。而在氢气和氧气存在的条件下,该双配位丙氧基物种会从催化剂表面脱附,因而他们认为双配位丙氧基物种是丙烯临氢气相环氧化反应的中间体。
随后,Oyama 等采用原位紫外光谱(ultraviolet-visible diffuse reflectance spectroscopy)和原位X 射线吸收近边结构谱图(Ti K-edge X-ray absorption near-edge structure)精确测定丙烯临氢气相环氧化的真实反应中间体为Ti—OOH。根据实验结果,如图5(b)所示,他们认为H和O在零价金活性位上被活化并生成HO,之后HO转移到Ti—OH 上生成HO 和Ti—OOH。随后CH吸附在Ti位点上并与Ti—OOH 反应生成环氧丙烷和Ti—OH,最后生成的环氧丙烷和HO 从Ti位点上脱附,从而完成整个Au—Ti 双活性位点的反应循环。
Delgass等以Au/TS-1为催化剂,采用反应动力学实验来揭示丙烯临氢气相环氧化反应的反应机理,实验结果和之前设定的Au-Ti双位点同步机理相一致。如图5(c)所示,在Au(S)位点表面通过氧气和氢气反应生成的H—Au—OOH 和Au—Ti 界面位点(S)上吸附的CH反应生成CHO(环氧丙烷)-S和HO-S。并且认为环氧化反应是决速步骤,否定了丙烯环氧化传统上认为的顺序机理(即在Au 位点上生成的HO通过迁移到Ti 位点,并与Ti 位点上吸附的CH发生环氧化反应生成环氧丙烷)。该机理确立了Au-Ti 界面位点为丙烯发生环氧化反应的真正活性位点的观点。
Copéret等采用固体O核磁共振(solid-stateO nuclear magnetic resonance signature)和密度泛函理论(density functional theory)过渡态计算表明,在丙烯液相环氧化过程中,在双核钛位点上形成的氧转移过渡态能够促使环氧化反应以更低能量的反应路径进行,如图5(d)所示。在该反应机理中,反应物HO首先和邻位的双核钛位点反应生成TS1-(OOH),随后在该位点上吸附丙烯并反应生成环氧丙烷,脱附环氧丙烷后的位点再和HO反应后重新生成TS1-(OOH),从而建立一个完整的双核钛位点循环。该反应机理证明了双核钛位点在丙烯环氧化反应中的重要性,但是并未否认传统四配位单核骨架钛位点在反应中的重要性。该文中提出的在双核钛位点上发生的环氧化机理为认识丙烯气相直接环氧化机理提供了一个全新的视角。
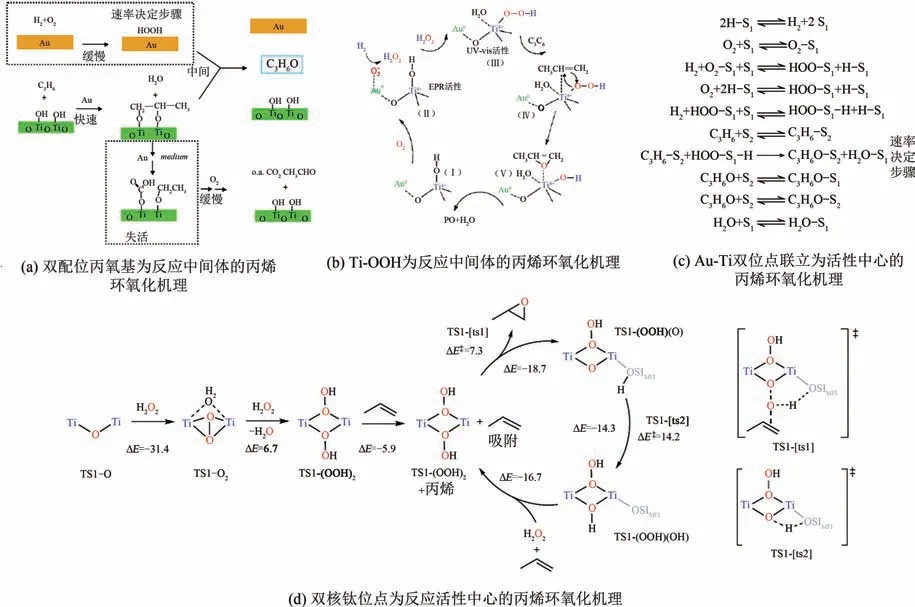
图5 不同类型的丙烯环氧化机理
随着原位表征技术与理论计算的进步,丙烯环氧化反应机理得到不断发展与更迭。因此,更加精确的丙烯环氧化机理的揭示需要不断发展和创新的表征技术和计算手段,这就给原位表征技术(原位红外、原位同步辐射、原位高倍透射电镜等)的创新和理论计算的迭代发展(密度泛函理论与机器学习相结合、无轨道密度泛函理论、从头算分子动力学等)提出了巨大的挑战。尽管丙烯气相临氢环氧化反应机理不尽相同,但是所有机理均肯定了双位点的重要性。丙烯临氢气相环氧化中,载体的钛位点或者负载的金属和钛位的界面位点主要用于催化丙烯和过氧化物反应生成环氧丙烷,而金属位点主要用于活化氢气和氧气并生成过氧化物。因此,理性设计与精准构筑载体的钛位点和负载的金属位点将会极大地推动丙烯临氢气相环氧化技术的发展。
3 高效金属位点的调控
丙烯临氢气相环氧化不仅需要高效的载体钛位点来催化丙烯和过氧化物中间体生成环氧丙烷,而且需要负载高效金属位点来有效活化氧气和氢气并原位生成过氧化物。高效的金属位点包含Au、Ag、Pt、Pd、Ni等,其中金纳米颗粒由于其高效的反应活性在众多金属位点中应用最为广泛。因此,关于金纳米颗粒的物化性质(空间分布、电子结构和粒径效应等)的调控已经开展了大量的研究工作。
由于贵金属所具有的独特的电子性质,通常采用Au、Ag、Pt、Pd 等贵金属来高效催化氢气和氧气反应生成过氧化物。1988年,Haruta等首次发现当金颗粒尺寸由微米级降低到纳米级时,金颗粒由催化惰性转为催化活性,从而能够有效催化氢气和氧气原位合成过氧化物,开辟了丙烯临氢气相环氧化的新纪元,随后金纳米颗粒的研究受到了广泛的关注。
除了金纳米颗粒外,其他贵金属也被尝试应用于丙烯临氢气相环氧化。Schüth等采用沉积沉淀法在TiO载体上负载2%(质量分数)的Ag纳米颗粒制备高活性丙烯环氧化催化剂。尽管纳米级Ag展现出与纳米级Au 相似的催化性质与失活行为,但是Ag/TiO催化剂的活性只有传统Au纳米颗粒催化剂活性的三分之一。Goddard等认为Ag纳米金属颗粒在催化烯烃环氧化时不同于Ag 基催化剂被广泛应用的乙烯环氧化体系[如图6(a)],丙烯末端的-H 极易与氧气分子接触,从而加速丙烯的完全氧化从而生成二氧化碳和水,进而降低丙烯环氧化选择性。因此,Nijhuis 等认为实现纳米级Ag在丙烯环氧化上的应用,需要创造孤立的Ag 活性位点用于氧气吸附,进而提高丙烯环氧化选择性。此外,Baiker 等在反应温度为43℃、反应压力为5×10Pa 和临氢反应条件下,使用Pt-Pd/TS-1 催化剂催化丙烯环氧化。反应初始阶段,环氧丙烷转化率为3.5%,环氧丙烷选择性高达99%;随着反应的进行,Pt-Pd/TS-1催化剂快速失活,反应的主要产物变为甲酸甲酯。如图6(b)所示,Pt-Pd 基催化剂主要副产物与传统临氢气相环氧化反应不同,除了包含传统机理会生成的丙烯醛、丙酮和丙烯酸外,还会产生一系列醇类化合物。
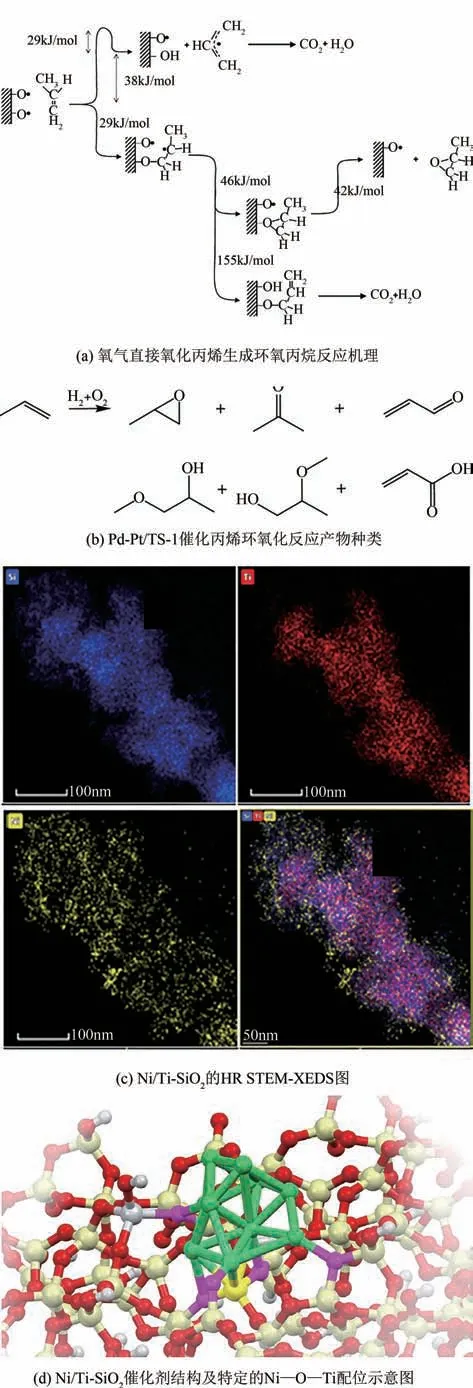
图6 不同金属位点催化丙烯环氧化
除了贵金属之外,镍基催化剂也被用于丙烯临氢气相环氧化中。Murcia 等采用沉积沉淀法在Ti-SiO上负载Ni 纳米颗粒合成Ni/Ti-SiO催化剂,如图6(c)所示。在200℃反应条件下,负载量0.5%(质量分数)的镍基催化剂的丙烯环氧化转化率为6.3%,环氧丙烷选择性达到85.5%。由于钛的电负性比硅低,因此孤立钛原子周围的氧原子具有更高的电子密度,这可能会促进其在初始浸渍阶段中与反应介质中阳离子态镍物种的相互作用。Ni原子和Ti 原子间更近的空间距离强化了二者的相互作用,从而生成了更多的Ni—O—Ti化学键[如图6(d)],进而促进临氢气相丙烯环氧化反应。
在丙烯临氢气相环氧化反应中,尽管不同种类的金属催化位点(如Au、Pd、Pt、Ag、Ni 等)已经被用于高效催化氢气和氧气反应生成过氧化物,但是由于金纳米颗粒优越的催化活性,关于金属催化位点的研究大多集中于金基催化剂。金纳米颗粒独特的电子性质(价态效应和助剂调控)、尺寸效应和空间分布成为高效Au 基催化剂可控制备研究的热点。
3.1 Au活性位的电子性质
金纳米颗粒独特的电子性质不仅受到自身d轨道得失电子所造成的价态变化的影响,同时也受到助剂金属(Ag、Pd等)对Au纳米颗粒传递电子的影响。Au纳米颗粒表面Au原子得到电子后,具有更多电子的Au原子将会有利于氧气的吸附与活化,从而促进氢气的吸附并在表面反应生成过氧化物。
通过调变Au物种自身价态,可以有效改变Au物种的d 轨道电子分布和电子性质。Oyama 等采用氰化钠处理负载于TS-1 载体上的Au 纳米颗粒,成功得到价态为+1 价的氰化金物种。采用X 射线光电子能谱(X-ray photoelectron spectroscopy,XPS)和原位X射线吸收近吸收边结构光谱(X-ray absorption near-edge structure,XANES)来精确表征金物种的价态与配位形式,如图7(a)所示。如图7(b)所示,反应结果表明,纳米尺度的+1价氰化金物种有利于丙烯加氢生成丙烷,而大尺度+1 价氰化金物种则不利于所有反应;纳米尺度零价金颗粒促进丙烯环氧化生成环氧丙烷,而大尺度零价金物种则有助于丙烯加氢生成丙烷。
本文作者团队通过调变预处理气氛来调变负载于TS-1 载体上+1 价金前体的动态演变方向,从而得到含有不同价态分布的金物种(Au、Au、Au)。实验结果表明,零价金物种是丙烯环氧化的活性位,而一价金则为丙烯加氢的活性位。如图7(c)所示,DFT计算表明氧气在吸附到金物种之后,零价金物种能够转移更多的电子给氧气,从而有效活化氧气,进而有利于接下来的反应(氧气和氢气反应生成过氧化物)。此外,提出了一种通过调变处理气氛来调控载体上零价金活性位数量的策略[如图7(d)],通过氢气和反应气的接力处理,将载体表面Au质量分数提升近100%,从而达到目前文献中报道的无助剂最高丙烯环氧化活性约220g/(h·kg)。
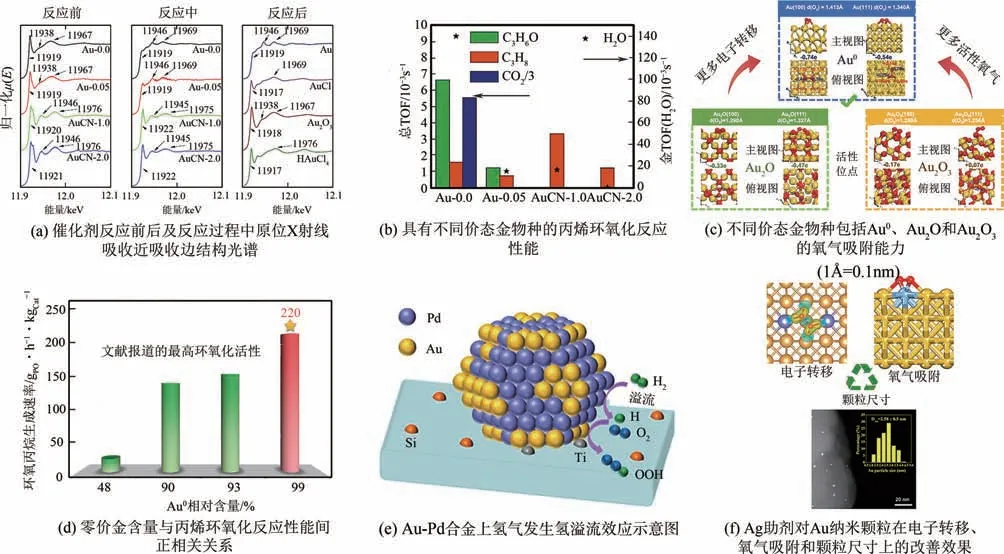
图7 Au基催化剂电子性质的调变
除了改变金纳米颗粒自身价态来调变金物种的电子数目外,通过添加金属助剂可以向金纳米颗粒转移更多的电子,从而提高金纳米颗粒吸附以及活化氧气的能力。马卫华等通过乙醇还原法成功在TS-1 载体上负载Au-Pd 合金,Au-Pd/TS-1 催化剂比Au/TS-1 和Pd/TS-1 催化剂显示出更好的丙烯环氧化性能。根据反应实验数据、程序升温还原谱图(H-TPR)和原位散射反射傅里叶变换红外光谱(-DRIFT)表征结果,揭示了Au-Pd 合金通过氢溢流效应[如图7(e)]显著降低了反应的活化能,进而有效提高了丙烯环氧化活性。此外,周兴贵团队通过沉积沉淀法成功在堵孔TS-1 上合成Au-Ag 合金,其中Au-Ag/TS-1-B 催化剂显示出优越的丙烯环氧化活性[174~233g/(h·g)]和稳定性。实验表征与理论计算表明[如图7(f)],Ag 助剂不仅可以有效减小Au 纳米颗粒的尺寸,提高反应活性位Corner位的数目;同时可以向Au原子转移电子,有效提高Au原子的电子含量,提高氧气吸附能力,促进表面Ti—OOH 物质的生成,提高丙烯环氧化活性。
3.2 Au活性位的尺寸效应
1988年Haruta等首次发现纳米级金颗粒能够有效催化氢气、氧气和丙烯反应生成环氧丙烷之前,金颗粒一直被认为是催化惰性的。这是由于制备方法上的不足导致合成的金纳米颗粒的尺寸基本上为微米级。Haruta等首次采用沉积沉淀法成功合成并负载纳米级金颗粒,成功打开了金催化的大门。
尽管围绕金纳米颗粒的尺寸效应开展了大量的研究,但是关于丙烯临氢气相氧化生成环氧丙烷的有效活性尺寸仍然处于争议当中。Qi等通过改变Au负载量来调变Au纳米颗粒的尺寸,反应结果表明[如图8(a)],当金纳米颗粒尺寸大于5nm 时,无论载体是否含有碱金属,反应倾向于丙烯加氢生成丙烷;而当Au 纳米颗粒小于2nm 且载体不含有碱金属时,无论Au 纳米颗粒沉积在Ti 位点还是Si位点附近,主反应为丙烯和氢气反应生成丙烷;当Au 纳米颗粒处于2~5nm 时,Au 纳米颗粒催化丙烯、氢气和氧气发生环氧化反应生成环氧丙烷。Huang 等通过碱处理TS-1 来改变催化剂表面粗糙度,进而强化对Au 纳米颗粒的锚定作用,如图8(b)所示。采用研磨法将乙酰丙酮金负载于TS-1载体上,通过高角环形暗场扫描透射电镜(HAADFSTEM)分析表明,经过碱处理后的载体能促使金纳米颗粒尺寸小于2nm;而未经过碱处理的TS-1则有利于金纳米颗粒生长到2nm以上。反应结果显示,小于2nm的金纳米颗粒负载于碱处理后的TS-1的环氧丙烷生成速率高达137g/(h·kg),而大于2nm 的金纳米颗粒负载于未经过碱处理后的TS-1的环氧丙烷生成速率仅为11g/(h·kg)。值得注意的是,在研究过程中,需要尽量控制单一变量的劣势,例如碱处理过后的载体会形成大量的介孔,有效改善载体的传质效应,进而提升催化剂活性。因此,金纳米颗粒的尺寸效应的研究需要更完备的实验设计以及更深入的理论探索。
随着合成技术的创新和表征技术的发展,丙烯气相环氧化关于尺寸效应的研究开始关注于金纳米颗粒的活性位本质,即金纳米颗粒的空间结构位点,并且小尺寸金团簇是丙烯环氧化反应的主要活性中心开始被逐渐认可。Delgass等通过将TS-1催化剂外表面包裹一层纯硅壳层后负载金纳米颗粒,成功合成Au/S-1/TS-1催化剂,该催化剂中的Au纳米颗粒被包裹于分子筛孔道内部,如图8(c)所示。在相同TS-1催化剂的质量下,该催化剂展现出更优异的丙烯环氧化活性,从而证明位于孔道内部的金纳米团簇为丙烯临氢气相环氧化的主要活性位点。此外,Ma 等也通过合成纯硅包裹的TS-1 并负载金纳米颗粒证明了小于1nm的金纳米团簇为丙烯临氢气相环氧化的主要活性位点,如图8(d)所示。
周兴贵团队通过沉积沉淀法将Au 纳米颗粒负载于堵孔TS-1 上,良好的反应稳定性(>30h)确保了对催化活性的精准分析。此外,无孔的TS-1促使Au 纳米颗粒沉积于载体外表面,进而确保所有的Au 纳米颗粒均可以接触到反应物分子,并且均可以被高倍透射电镜所观察到,有利于揭示不同尺寸Au 纳米颗粒的本征催化活性。通过调变沉积沉淀时间来有效改变Au 物种的负载量,进而在2.6~5.1nm范围内调控Au纳米颗粒的平均尺寸。如图8(e)所示,根据高倍透射电镜(HRTEM)所观察到的Au纳米颗粒形貌,搭建了Au纳米颗粒截断八面体物理模型。依据Au纳米颗粒截断八面体模型,如图8(f)所示,拟合不同活性位(corner site、edge site、surface site and perimeter site) 在 不 同 尺 寸(2.6~5.1nm)下的活性变化规律,结果发现Corner位点是丙烯临氢气相环氧化的Au 纳米颗粒的主要活性位点。
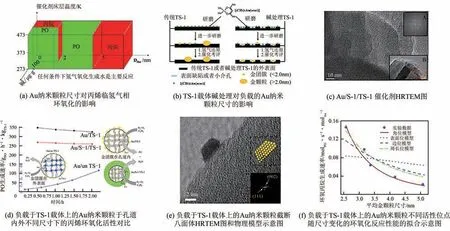
图8 Au纳米颗粒的尺寸效应
3.3 Au活性位的空间分布
丙烯临氢气相环氧化催化剂较差的稳定性和较低的活性极大地抑制了环氧化反应的工业应用前景,精准调控Au 纳米颗粒的空间分布,不仅可以提高Au 纳米颗粒分散度,增加环氧化活性位点,有效提高环氧化反应的活性;而且可以加速产物的扩散,抑制环氧化产物低聚,减少催化剂结焦量,进而改善孔道堵塞的影响和减少表面活性位覆盖的情形。因此,精准调控Au 纳米颗粒在含钛载体上的空间分布成为Au基催化剂的研究方向之一。
调变金纳米颗粒负载于孔道外表面可以加速产物脱附,抑制催化剂堵孔效应,提高丙烯环氧化稳定性。周兴贵团队在丙烯环氧化失活机理以及精准调控Au纳米颗粒在TS-1分子筛孔道内外的空间分布上作了大量深入的研究。以负载Au 纳米颗粒的开孔TS-1 为研究对象,提出/(为碳物种占据的体积;为氮气探针分子无法接触到的体积)作为催化剂堵孔程度的描述符。如图9(d)所示,随着反应的进行,/逐渐减小,表明碳物种导致的分子筛孔道内部无法利用的空间逐渐增加,揭示了丙烯环氧化失活的主要原因是催化剂孔道逐渐被堵塞导致反应位点无法与反应物相互接触。基于该失活机理,提出负载Au纳米颗粒于TS-1载体外表面来抑制催化剂失活的策略,如图9(c)所示。以堵孔TS-1为载体可以有效将Au纳米颗粒负载于分子筛孔道外部,如图9(e)所示,该催化剂在展示优越稳定性(30h)的同时也展示出优越的活性[125g/(h·kg)]。此外,周兴贵团队通过调变沉积沉淀法中的加料顺序来调变TS-1 载体孔道内外的Au 纳米颗粒的比例[如图9(f)],从而提出一种高稳定性的Au/TS-1催化剂的制备方法。
本文作者团队通过调变Au 前体的水解程度来增加孔道内Au 物种的空间落位比例,进而提高Corner活性位的数目,有效改善丙烯临氢气相环氧化的反应活性。如图9(a)所示,通过原位紫外可见光光谱(-UV-vis)建立了Au 前体的水解程度与吸收光谱峰位置的关系,定性判断不同水解温度下Au前体的水解程度。Au前体沉积沉淀过程中不同的水解温度有效提高了孔道内Au 纳米颗粒的比例,从而显著提高了丙烯环氧化的活性[约205g/(h·kg)]。但是,如图9(b)所示,孔道内过量的Au 团簇反而会堵塞催化剂孔道,抑制反应物与Au 团簇的接触,降低反应活性。因此,本文作者团队提出“孔道内有效金团簇量”的概念来突出在孔道内适量负载Au 团簇的重要性。Li 等通过晶种诱导无溶剂法并辅助生物提取法成功将Au 纳米颗粒封装于TS-1 孔道中,该催化剂展示出优越的丙烯临氢气相环氧化活性[约205g/(h·kg)]。这种封装的结构缩短了Au 位点和Ti 位点的空间距离,并且促使钛位点失去电子,进而从几何结构和电子结构优化Au-Ti界面的催化活性,提高了环氧丙烷生成速率。因此,提高TS-1 孔道内的金纳米颗粒数目可以有效改善金纳米颗粒的粒径分布,提高反应活性位数目,进而有效改善丙烯气相临氢环氧化活性,但孔道内过多金纳米颗粒则会加速催化剂失活;同时,提高分子筛孔道外金纳米颗粒数目可以有效抑制产物环氧丙烷在孔道内的分解和结焦,从而减少TS-1 微孔孔道堵塞情况,进而提高反应稳定性,但是孔道外过多金纳米颗粒则会降低反应活性。所以,协调孔道内外的金纳米颗粒的数目将会在改善丙烯临氢气相环氧化活性的同时优化反应的稳定性。
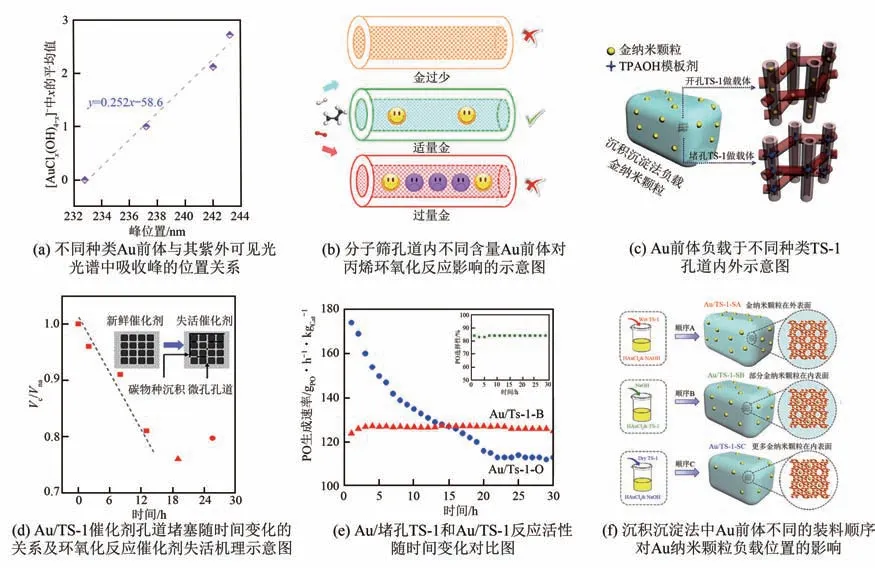
图9 Au纳米颗粒空间分布的调控
4 结语
钛硅分子筛的发现被认为是分子筛催化领域的里程碑之一,其已经成功应用于烯烃环氧化、环己酮氨氧化、苯酚羟基化等领域。本文总结高效钛硅分子筛合成策略,分别包括调节载体结构类型、硅钛原子比、表面疏水性、颗粒传质性能,并概括TS-1 钛硅分子筛工业化进展。同时总结以负载金属的TS-1 为催化剂的丙烯气相环氧化反应机理,尽管学术界关于丙烯临氢气相环氧化同时需要两个活性位点(载体钛位点和金属活性位点)的论点已经基本达成共识,但是关于环氧化反应过程中的具体机理仍然存在争议。原位条件下的表征(如-FTIR 和-EXAFS)和密度泛函理论的计算将会为具体反应机理提供更加确切的证据,同时也给实验表征提出了挑战。
构建高效的Au-Ti活性位点是丙烯临氢气相环氧化反应的关键。因此,关注高效载体钛位点合成的同时,也应关注高活性金属位点的负载。目前在不同的金属位点上(Au、Ag、Pt、Pd、Ni)均已取得一定的突破,采用非贵金属替代Au 纳米颗粒将会是未来丙烯临氢气相环氧化催化剂工业化进展的关键,但是目前使用最为广泛的金属位点仍然为Au纳米颗粒。改善Au纳米颗粒活化氧气和氢气分子并催化二者原位反应生成过氧化物的能力主要通过三个方面进行调控:电子性质、尺寸效应以及空间分布。其中,Au 纳米颗粒独特的电子性质可以通过Au 纳米颗粒自身的价态效应以及外加助剂的供电子效应进行调控。同时兼顾Au 纳米颗粒的电子性质、尺寸效应和空间分布的调控将会极大地改善金属位点的反应性能。尽管Au-Ti双活性位点各自的调控已经取得了一系列的突破,但是如何更加高效协同高活性的Ti 和Au 位点仍然是丙烯临氢气相环氧化催化剂制备的难点,合理高效地引入助剂可能是强化金属和载体协同效应的有力方法。此外,改善环氧化反应的长周期稳定性和氢效,开发相关反应器设计和过程优化,是加速丙烯临氢气相环氧化反应工业化进程的关键。

