黄芪皂苷改善膝关节骨性关节炎大鼠模型炎症及其机制研究
郑宇翔 刘德国 徐天波 汤霄朕 范亮全 侯振海 郑隆宝
骨性关节炎(osteoarthritis,OA)是最常见的关节疾病之一,其临床特征是关节痛、夜间疼痛、功能障碍和活动受限[1-2]。OA发病机制尚未明确,机械损伤、代谢障碍及炎症反应等均会引发OA,疾病发展可导致持续疼痛甚至残疾[3-5]。在OA的疾病进程中,软骨细胞和滑膜细胞会过度产生可溶性炎症介质,因此抗感染疗法可能为治疗该病提供潜在可能[6]。胰升糖素样肽1(glucagon-like peptide-1,GLP-1)是肠内分泌 L 细胞产生的肠降血糖素激素,通过与胰高血糖素受体的靶向结合激活腺苷酸环化酶诱导环状单磷酸腺苷(cyclic adenosine 3',5'-monophosphate,cAMP)的产生,进而激活蛋白激酶A(protein kinase A,PKA),PKA激活cAMP反应元件结合蛋白(cAMP responsive element-binding protein,CREB),从而调节与炎症相关基因的表达[7-9]。研究表明,CREB激动剂可以减少炎症介质的释放,调节磷酸肌醇3-激酶/蛋白激酶B信号传导,从而保护软骨细胞免受内质网应激的影响,抑制细胞凋亡和炎症[10]。黄芪皂苷可以通过CREB的激活抑制神经炎的发展,从而有效减轻坐骨神经慢性压迫性损伤大鼠模型的痛温觉过敏[11]。有关黄芪皂苷是否可在OA中发挥抗炎作用的研究较少。鉴于此,本研究初步探讨黄芪皂苷对OA的治疗作用及其潜在分子机制。
1 材料和方法
1.1 实验动物 成年雄性Wistar大鼠90只,体重200~250 g,购自北京维通利华实验动物技术有限公司。饲养于SPF级动物实验房,在(26±2)℃的环境温度下饲养,光暗周期为12 h。大鼠自由饮食饮水。本实验操作符合实验动物3R原则。
1.2 主要试剂 GLP-1激动剂购自美国Novo Nordisk公司;单碘乙酸盐(monoiodoacetate,MIA)购自美国Sigma-Aldrich 公司;兔抗 CREB、磷酸化 CREB(p-CREB)、PKA、磷酸化 PKA(p-PKA)、TNF-α、IL-1β 和 IL-6 抗体均购自英国Abcam公司;兔抗甘油醛-3-磷酸脱氢酶(glyceraldehyde 3-phosphate dehydrogenase,GAPDH)及辣根过氧化物酶(horseradishperoxidase,HRP)偶联的山羊抗兔IgG均购自美国Proteintech公司;A/G琼脂糖蛋白珠购自美国Santa Cruz Biotechnology公司;免疫组化试剂盒购自美国Boster Biological Technology公司;黄芪皂苷购自上海源叶生物公司;Fusion-FX7系统购自法国Collégien公司;Image-Pro Plus 6.0软件购自美国Media Cybernetics公司。
1.3 膝OA大鼠模型的建立及药物干预
1.3.1 膝OA大鼠模型的建立 取60只Wistar大鼠,按照随机数字表法分为对照组、OA-1组、OA-5组、OA-10组、OA-20组和OA-28组,每组10只。所有大鼠均使用50 mg/kg戊巴比妥钠腹膜内麻醉。对照组关节腔内单次注射40 μl 0.9%氯化钠注射液;OA-1组、OA-5组、OA-10组、OA-20组和OA-28组大鼠关节腔内单次注射4 mg MIA(溶于40 μl 0.9%氯化钠注射液中),并在注射后第1、5、10、20和28天分别处死。检测对照组、OA-1组、OA-5组、OA-10组、OA-20组和OA-28组大鼠模型软骨组织中CREB的表达。MIA的注射操作步骤:麻醉大鼠后将其仰卧位固定在手术台上,后腿右膝处剃毛并消毒,将4 mg MIA溶解于40 μl 0.9%氯化钠注射液中,并通过髌下韧带注射到右膝关节腔中,出针后用无菌纱布包扎放入笼中[12]。
1.3.2 药物干预 取另外30只Wistar大鼠按照1.3.1的方法制备OA动物模型,并按照随机数字表法分为OA组、OA+0.9%氯化钠注射液组(下称OA+生理盐水组)和OA+黄芪皂苷组,每组10只。OA+黄芪皂苷组大鼠皮下注射0.5 ml/(kg·d)黄芪皂苷[13](黄芪皂苷浓度:0.1 g/ml);OA+生理盐水组大鼠每天皮下注射0.5 ml 0.9%氯化钠注射液;OA组大鼠不予任何药物处理。OA+黄芪皂苷组和OA+生理盐水组大鼠持续注射28 d后,无不良反应发生。所有大鼠均使用50 mg/kg戊巴比妥钠腹膜内麻醉后脱颈处死。获得大鼠左膝关节标本,并迅速去除膝关节周围的肌肉。沿关节囊的股骨边缘横切去除股骨软骨。此外,沿骨表面切开股骨和胫腓骨,纵向切开关节囊,并分离滑膜组织。然后将软骨标本保存在液氮中备用。
1.4 PKA/CREB信号通路相关蛋白(PKA、p-PKA、CREB、p-CREB)、炎症相关蛋白(TNF-α、IL-6 和 IL-1β)表达水平检测 采用Western blot法。用含焦磷酸钠和蛋白酶抑制剂的放射免疫沉淀分析(RIPA)裂解液提取软骨组织的总蛋白。采用双辛可宁酸(BCA)试剂对蛋白质浓度进行定量。使用10%十二烷基硫酸钠-聚丙烯酰胺凝胶电泳(SDS-PAGE)分离收获的蛋白质或免疫沉淀物,然后将其转移到聚偏二氟乙烯(PVDF)膜上,置于封闭缓冲液中室温孵育2 h后,将PVDF膜用TBST缓冲液洗涤3次,5 min/次,随后与山羊抗兔一抗(1∶1 000)稀释液于4℃孵育过夜。用TBST洗涤3次(5 min/次)后,将膜与HRP偶联的山羊抗兔IgG(1∶3 000)抗体孵育1 h。然后将膜用TBST洗涤3次,5 min/次,并通过增强化学发光(ECL)进行显影。使用Fusion-FX7系统通过光密度扫描对印迹的吸光度进行定量,计算各基因与GAPDH的相对表达水平。
1.5 CREB表达水平检测 采用免疫组化染色法。将一部分软骨组织用于制备石蜡切片。3% H2O2封闭10 min,5%牛血清白蛋白(BSA)封闭 30 min后,将切片脱蜡并重新水化。然后,将切片与兔抗CREB(1∶50)在4℃孵育过夜,与山羊抗兔二抗室温孵育30 min。将切片在PBS中洗涤,并置于3,3-二氨基联苯胺(DAB)溶液中孵育3 min。使用苏木精复染细胞核。使用光学显微镜捕获图像并通过Image-Pro Plus 6.0软件进行分析,并使用吸光度积分值测量CREB的表达水平。每个标本至少使用3个切片测量CREB的表达水平。
1.6 统计学处理 采用SPSS 22.0统计软件。计量资料以表示,组间比较采用单因素方差分析,两两比较采用Tukey检验。P<0.05为差异有统计学意义。
2 结果
2.1 OA大鼠膝关节软骨组织中CREB表达水平比较 与对照组比较,OA-1组、OA-5组、OA-10组、OA-20组和OA-28组大鼠膝关节软骨组织中CREB表达水平均降低(均P<0.05);免疫组化染色显示,与对照组比较,OA-28组大鼠膝关节软骨组织中CREB水平下调(P<0.05),并且均值最低,见图1。

图1 OA大鼠膝关节软骨组织中CREB的表达比较(a:各组大鼠膝关节软骨组织中CREB表达的电泳图;b:各组大鼠膝关节软骨组织中CREB蛋白表达定量柱状图,与对照组比较,*P<0.05;c:免疫组化染色所见;d:各组免疫组化染色蛋白表达定量柱状图,与对照组比较,*P<0.05)
2.2 各组大鼠膝关节软骨组织中PKA/CREB信号通路相关蛋白表达水平比较 与对照组比较,OA-1组、OA-5组、OA-10组、OA-20组和OA-28组大鼠膝关节软骨组织中PKA、p-PKA、CREB和p-CREB蛋白表达水平均降低(均P<0.05),见图2。

图2 各组大鼠膝关节软骨组织中PKA/CREB信号通路相关蛋白表达水平比较(a:各组大鼠膝关节软骨组织中PKA、p-PKA、CREB和p-CREB蛋白表达的电泳图;b:各组大鼠膝关节软骨组织中PKA、p-PKA、CREB和p-CREB蛋白表达定量柱状图,与对照组比较,*P<0.05)
2.3 各组大鼠膝关节软骨组织中炎症相关蛋白表达水平比较 与对照组比较,OA-1组、OA-5组、OA-10组、OA-20组和OA-28组大鼠膝关节软骨组织中TNF-6、IL-6和IL-1β蛋白表达水平均增加(均P<0.05),见图3。

图3 各组大鼠膝关节软骨组织中炎症相关蛋白表达水平比较(a:各组大鼠膝关节软骨组织中TNF-α、IL-6和IL-1β蛋白表达的电泳图;b:各组大鼠膝关节软骨组织中TNF-α、IL-6和IL-1β蛋白表达定量柱状图,与对照组比较,*P<0.05)
2.4 黄芪皂苷对OA大鼠膝关节软骨组织中CREB蛋白表达的影响 OA组和OA+生理盐水组大鼠膝关节软骨组织中CREB蛋白表达水平比较差异无统计学意义(P>0.05)。与OA+生理盐水组比较,OA+黄芪皂苷组大鼠膝关节软骨组织中CREB蛋白表达水平增加(P<0.05),见图4a-b。免疫组化染色定量分析结果与Western blot分析结果相一致,见图4c-d。

图4 黄芪皂苷对OA大鼠膝关节软骨组织中CREB蛋白表达的影响(a:3组大鼠膝关节软骨组织中CREB蛋白表达的电泳图;b:3组大鼠膝关节软骨组织中CREB蛋白表达定量柱状图,与OA+生理盐水组比较,*P<0.05;c:免疫组化染色所见;d:3组免疫组化染色蛋白表达定量柱状图,与OA+生理盐水组比较,*P<0.05)
2.5 黄芪皂苷对OA大鼠膝关节软骨组织中PKA/CREB信号通路的调控 OA组和OA+生理盐水组大鼠膝关节软骨组织中PKA、p-PKA、CREB、p-CREB蛋白表达水平比较差异均无统计学意义(均P>0.05);与OA+生理盐水组比较,OA+黄芪皂苷组大鼠膝关节软骨组织中PKA、p-PKA、CREB、p-CREB蛋白表达水平均增加(均 P<0.05),见图 5。

图5 黄芪皂苷对OA大鼠膝关节软骨组织中PKA/CREB信号通路的调控(3组大鼠膝关节软骨组织中PKA、p-PKA、CREB、p-CREB蛋白表达的电泳图;b:3组大鼠膝关节软骨组织中PKA、p-PKA、CREB、p-CREB蛋白表达定量柱状图,与OA+生理盐水组比较,*P<0.05)
2.6 黄芪皂苷对OA大鼠膝关节软骨组织炎症的影响 OA组和OA+生理盐水组大鼠膝关节软骨组织中TNF-α、IL-6和IL-1β蛋白表达水平比较差异均无统计学意义(均P>0.05);与OA+生理盐水组比较,OA+黄芪皂苷组大鼠膝关节软骨组织中TNF-α、IL-6和IL-1β蛋白表达水平均降低(均P<0.05),见图6。
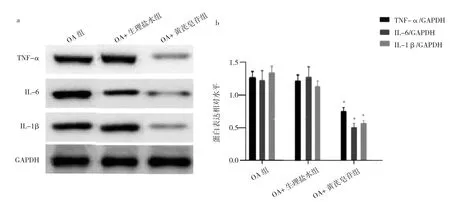
图6 黄芪皂苷对OA大鼠膝关节软骨组织炎症的影响(3组大鼠膝关节软骨组织中TNF-α、IL-6和IL-1β蛋白表达的电泳图;b:3组大鼠膝关节软骨组织中TNF-α、IL-6和IL-1β蛋白表达定量柱状图,与OA+生理盐水组比较,*P<0.05)
3 讨论
OA多见于中老年人,可以导致关节部位骨赘形成,髌下脂肪垫消失,从而损伤膝关节功能,严重时导致关节畸形,甚至致残,严重影响我国中老年人群的健康[14]。目前,OA的临床治疗仍以西医保守治疗为主,抗炎镇痛及关节活性物质药物使用虽然具有一定疗效,但往往肝肾毒性较大,同时会刺激患者消化道[15]。中药以其安全有效以及价格低廉等优势被越来越多的研究者关注,黄芪皂苷是中药材黄芪根茎的有效成分之一,具有免疫调节、保护心血管、抗炎、抗纤维化、抗病毒及抗肿瘤作用[16]。目前有关黄芪皂苷对OA是否具有治疗作用及其潜在机制鲜见报道。
研究表明,炎症在OA的发展中起着重要作用[17]。研究发现类风湿关节炎的早期和终末期滑膜组织中TNF-α、IL-6和IL-1β等细胞因子表达水平明显变化[18-19]。本研究结果表明,OA大鼠模型软骨组织中这些细胞因子的水平明显增加,表明软骨炎症可能与OA的发生和发展密切相关。因此,在OA的早期阶段阻断炎症途径,抑制过度的炎症反应可延缓或阻碍疾病的进展,为抗关节炎的药物开发提供理论的基础。
炎症由多种上游和下游分子介导。研究发现PKA/CREB信号通路相关蛋白具有抗炎功能,可作为炎症相关疾病治疗靶标[20-21]。CREB与组蛋白乙酰基转移酶家族的成员CREB结合蛋白结合,并催化组蛋白乙酰化,从而将染色质从闭合状态转换为开放状态,促进RNA聚合酶Ⅱ和基础转录因子与开放DNA的结合,进而启动包括炎症细胞因子在内的基因转录,例如IL-10和双重特异性磷酸酶1(dual specificity phosphatase 1,DUSP1)[22-23]。IL-10可以将产生高水平促炎细胞因子和低水平抗炎细胞因子的M1“炎症”表型的巨噬细胞转化为产生低水平促炎细胞因子和高水平的抗炎分子的M2b“调节”表型;糖皮质激素诱导的DUSP1可以通过p38 MAPK和c-Jun N末端激酶(JNKs)的去磷酸化和失活抑制MyD88信号通路的激活,从而参与炎症反应[24-25]。近年来研究证实,PKA/CREB信号通路与炎症的发生密切相关,第二信使cAMP可以通过PKA调节 CREB的磷酸化,p-CREB抑制CRE转录因子的活性,进而抑制炎症因子表达,抑制炎症的发生。活化的PKA/CREB信号通路还能通过调节神经保护相关蛋白的表达,在抑制神经炎症的同时发挥神经保护作用[26-29]。本研究结果表明,与对照组比较,MIA诱导的OA大鼠膝关节软骨组织中CREB表达较低,且炎症相关蛋白的上调伴随着PKA/CREB信号通路的下调,提示PKA/CREB信号通路相关蛋白在OA的发展中具有潜在的重要作用。
综上所述,在MIA诱导的OA大鼠模型中,CREB蛋白表达水平明显降低,同时伴随着PKA/CREB信号通路相关蛋白的下调和炎症相关蛋白TNF-α、IL-6和IL-1β的上调,黄芪皂苷可以通过激活PKA/CREB信号通路,抑制炎症相关蛋白的表达,进而发挥抗炎活性。

