海洋酸化与陆源DON对米氏凯伦藻和东海原甲藻生长的影响❋
张艳红, 贺云凤, 李克强, 张现盛, 杨 锐, 逄 凯, 梁生康, 王修林
(中国海洋大学海洋化学理论与工程技术教育部重点实验室, 山东 青岛 266100)
受全球CO2浓度升高影响,海水pH降低引起的海洋酸化愈来愈受到关注[1-2]。根据政府间气候变化专门委员会(Intergovernmental Panel on Climate Change)的预测,到2100年pCO2将达到约800~1 000 ppmv,海洋表面pH值将降至7.8~7.7[3]。海洋酸化直接影响着海洋生态系统的结构与健康,甚至改变海洋生态系统[4-5]。研究表明,海洋酸化会对海洋生态系产生不利影响,如钙化生物,深海珊瑚、浅水底栖无脊椎动物和海胆等可能是最为直接的受害者[5-8]。而且,海洋酸化与全球气候变暖、紫外辐射增强和富营养化等的协同作用可能会对海洋浮游植物的生长产生潜在的影响[9]。
随着社会经济的高速发展,近岸海域的富营养化引起的有害藻华已成为世界性问题[10]。自1998年以来,几乎每年的3-9月在东海长江口临近海域爆发米氏凯伦藻(Kareniamikimotoi)、中肋骨条藻(Skeletonemacostatum)以及东海原甲藻(Prorocentrumdonghaiense)等有害赤潮[11](东海海洋公报)。近年来,米氏凯伦藻和东海原甲藻赤潮经常在中国福建沿海地区大规模爆发,引起鱼类大量死亡,对海洋环境和渔业养殖造成巨大破坏[12-13]。研究表明,降雨导致的低盐度和高营养盐会使米氏凯伦藻细胞密度增加[14-15],东海原甲藻和米氏凯伦藻具有垂直迁移的能力[16],使它们能够更有利获得光能和营养盐从而成为优势藻种[17-18]。在河口和近海生态系统中,赤潮的种类,规模和持续时间与氮的含量和形态有密切关系[19]。高强度人类活动导致大量的含氮污染物排放入海,致使DON逐渐成为近岸海域氮的主要形态[20]。调查结果显示,DON在海水中总溶解态氮(TDN)中有相当高的占比,如大亚湾,胶州湾,珠江口,东海浅陆架区,北黄海和厦门湾等近海区域,DON约为TDN的30%~90%[21-24]。研究表明,DON不仅可以做某些浮游植物的氮源,而且对浮游植物的竞争与演替也起着一定的作用[25],DON含量的增加可能会诱发有毒有害赤潮发生[26]。例如,美国东海岸的两个海湾爆发的抑食金球藻褐潮与DOM有关[27];长江口及其领近海域爆发的东海原甲藻赤潮、米氏凯伦藻赤潮等赤藻的爆发可能是DOM在赤潮爆发过程中的供氮作用[28];美国缅因州西部海湾的亚历山大藻赤潮可能是由于高DON浓度引起的[29]。
DON是浮游植物生长的一种重要氮库[30],某些浮游植物能够直接吸收利用DON[31]。例如,米氏凯伦藻和东海原甲藻可以直接吸收利用尿素[32-33]。但是由于DON的来源和结构组成复杂,人类活动产生的DON会对米氏凯伦藻和东海原甲藻的生长产生什么影响,相关的认识还十分有限,限制了对这两种甲藻,特别是有毒米氏凯伦藻藻华的防治。因此,有必要研究人为源DON对两种甲藻生长和竞争的影响。
活性氧(ROS)在浮游植物的毒理和生理途径中起着关键的作用[34]。ROS通常以代谢副产物的形式出现[34],在正常的生理活动中,ROS的产生与消除之间存在动态平衡[35]。在浮游植物中,过氧化氢酶(CAT)和超氧化物歧化酶(SOD)等抗氧化生物酶在消除ROS中起关键作用[36]。研究表明,当生物体受到外部胁迫时产生大量的ROS同时会提高SOD和CAT酶活性以清除体内产生的自由基来保护细胞免受氧化损伤[37]。酸化环境会导致浮游植物细胞内外的酸碱失衡,进而激活抗氧化系统[38]。利用藻类细胞酶活性的变化反映藻类中氧化应激的发生[39],可以用来表征酸化等环境条件对浮游植物生长的影响。
东海原甲藻和米氏凯伦藻广泛分布于中国沿海水域,在初春和夏季,长江口和东海沿岸经常爆发东海原甲藻和米氏凯伦藻赤潮,或者两种藻演替发生。人为源DON和pCO2升高对东海和长江口附近的两种甲藻赤潮发生的影响的了解还十分有限。为此,本文以人为来源的DON为氮源,通过一次性培养实验,结合抗氧化生物酶活性,研究pCO2升高和DON加富对米氏凯伦藻和东海原甲藻的生长和竞争的影响,为控制和缓解赤潮提供科学依据。
1 材料与方法
1.1 样品的采集
本文于2018年4月初采集海泊河污水处理厂(36°6′0″N, 120°19′12″E)水样作为城镇生活源DON,水样中DON和溶解无机氮(DIN)含量分别为2 124和515 μmol·L-1。随后将所取水样分别通过1 μm的混合膜和0.22 μm的醋酸纤维膜(用0.5 mol/L的盐酸浸泡24 h并用Milli-Q水洗至中性)去除颗粒物和细菌。将收集到的滤液用1 000 Da膜(OmegaTM; PALL)的超滤系统(MinimateTM; Pall Corporation, Port Washington, NY, USA)进行浓缩(浓缩比为1∶10)以减少DIN在TDN中的占比,得到的浓缩液中DON和DIN含量分别为4 341和347 μmol·L-1。培养实验所用陈化海水取自胶州湾近海海域(36°5′42″N, 120°15′41″E),在实验室放置半年后海水中DON和DIN分别为9.7和1.5 μmol·L-1。
1.2 培养实验
培养实验所用米氏凯伦藻接种于中国科学院海洋研究所海洋生态与环境科学重点实验室藻种室,东海原甲藻接种于中国海洋大学海洋化学理论与工程技术教育部重点实验室藻种室,藻种保存于f/2培养液并置于光照培养箱中(光照强度191 μmol·m-2·s-1,光暗比为12 h∶12 h,温度为(20±1) ℃)。将培养实验所用陈化海水用0.45 μm的醋酸纤维膜过滤除去颗粒物,再将过滤海水在121 ℃下高温高压灭菌20 min以除去海水中的细菌。将3.5 L灭菌海水加入到5 L锥形瓶中,然后用锡纸(实验前450 ℃下灼烧4 h)密封(即不发生水交换)。通过连续鼓入(控制气体体积流量约5 mL·min-1,蠕动泵最大转速26.6 r·min-1)称重配置空气(99.999%的高纯气体,物质的量比CO2∶N2∶O2=1∶2 055∶500,pCO2为380 ppmv代表当前的pCO2水平)和称重配置二氧化碳加富气体(物质的量比CO2∶N2∶O2=1∶950∶250,pCO2为800 ppmv代表预测2100年的pCO2水平)[40],分别对应于海水pH值8.10和7.81。在所有的碳酸盐体系达到平衡后(pCO2: 380 ppmv对应的总碱度(TA)和无机碳(DIC)分别为1 980和2 087 μmol·L-1,pCO2: 800 ppmv对应的TA和DIC分别为2 145和2 193 μmol·L-1)加入藻种,分别将100 mL东海原甲藻和100 mL米氏凯伦藻分别加入相应培养体系,在混合培养体系分别加入50 mL东海原甲藻和50 mL米氏凯伦藻藻种(藻个数比为1∶1)。加入36 mL海泊河污水处理场浓缩样作为实验组,将与海泊河浓缩样所含等量DIN(NO3-N和NH4-N;国药集团化学试剂有限公司)添加的培养体系作为对照组。此外,本文添加了PO4-P(KH2PO4;国药集团化学试剂有限公司),维生素和微量元素(上海光语生物技术有限公司)(见表1)。东海原甲藻培养实验周期为10天,取样频次为1天/次。米氏凯伦藻单独培养实验和两种藻共培养实验周期为20天,取样频次为2天/次。取样前将培养体系摇匀,取混合藻液在显微镜下观察两种藻在混合培养体系中的生长情况,将200 mL藻液用0.7 μm的 GF/F玻璃纤维膜(Whatman公司,450 ℃下灼烧4 h)过滤,滤膜用于测定SOD酶、CAT酶活性和叶绿素,将滤液分别装入60 mL的棕色玻璃瓶中并将样品置于-20 ℃下保存,用于测定水体的DOC、TDN和DIN。

表1 米氏凯伦藻、东海原甲藻及两种藻共培养的实验条件
1.3 分析方法
TDN采用总碳/总氮自动分析仪(Multi N/C 3100; Analytik Jena AG, Jena, Germany)高温催化氧化法测定[41]。DIN(NH4-N,NO3-N和NO2-N)使用营养盐自动分析仪(AAⅢ; Bran+Luebe, Norderstedt, Germany)测定[42]。TDN和DIN差减得到DON(DON=TDN-DIN)。使用库仑法[43]和自动电位滴定法[44]分别测得DIC和 TA。用间甲酚紫指示的分光光度法测定海水的pH[45]。将滤膜用90%丙酮萃取后,使用紫外分光光度法测定Chla浓度[46]。
SOD活性以每微克样品的酶单位表示(U·μg-1),依据SOD在光下对抑制氮蓝四唑(nitro-blue tetrazolium,NBT)的还原作用来确定SOD的酶活性[47]。依据CAT可在磷酸缓冲液中催化H2O2,可用H2O2的减少速率来确定CAT的酶活性[48]。
1.4 数据处理方法
浮游植物的生长过程符合Slogistic2生长模型,通过Origin8.5软件(The Microcal Inc.)对生长曲线进行拟合[49]:
其中:Bt为t时刻的生物量(Chla,μg·L-1);Bf为终止生物量(Chla,μg·L-1);B0为初始生物量(Chla,μg·L-1);μmax为最大生长速率(μg·L-1·h-1)。
氮吸收过程采用Monod方程[50],并将其修改为:
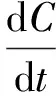
实验结果的显著性采用T检验方法,应用SPSS 22.0软件(SPSS Inc)进行分析,显著性水平设置为α=0.05。
2 实验结果与数据处理
2.1 浮游植物生长
对于单种藻培养体系,东海原甲藻在两种pCO2条件下均较米氏凯伦藻提前5天进入指数生长期(见图1)。在pCO2为380 ppmv的正常条件下,东海原甲藻和米氏凯伦藻的平台期分别持续了约1和4天(见图1(a)和1(b)),而pCO2的升高(800 ppmv)使得东海原甲藻比正常情况下提前1天进入死亡期,同时终止生物量也降低了约40%(见图1(a)和1(d),表2),而米氏凯伦藻则在不同pCO2条件下同步生长和死亡,只是终止生物量低约20%(见图1(b)和1(e),表2)。对于两种藻混合培养体系,进入指数生长期的时间与东海原甲藻一致,而平台期持续时间,在正常条件下约8天,pCO2升高酸化条件下则只有4天,并提前6天到达死亡期,终止生物量降低了约40%(见图1(c)和1(f),表2)。藻分类结果显示,两种藻混合培养下,培养实验的第2天以东海原甲藻占绝对优势,此后米氏凯伦藻逐渐增加,进入第6天后占据对优势。在整个培养实验期间,pH的波动范围为0.1±0.04(见图1)。
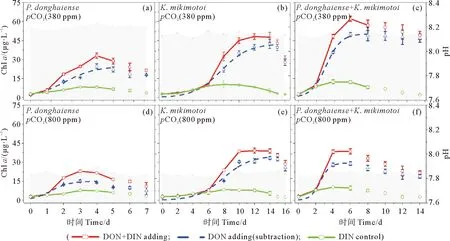
(阴影为pH值,实线是实验测定Chl a浓度,虚线为DON加富培养体系的Chl a浓度减对照培养体系的Chl a浓度,表示单独DON为氮源下浮游植物的生长曲线。Shadow is pH value, the solid lines are Chl a measured by experiment and the dotted line is the growth curve of phytoplankton using dissolved organic nitrogen (DON) as the nitrogen source by subtracting the Chl a of the DIN control treatment from DON enrichment treatment.)
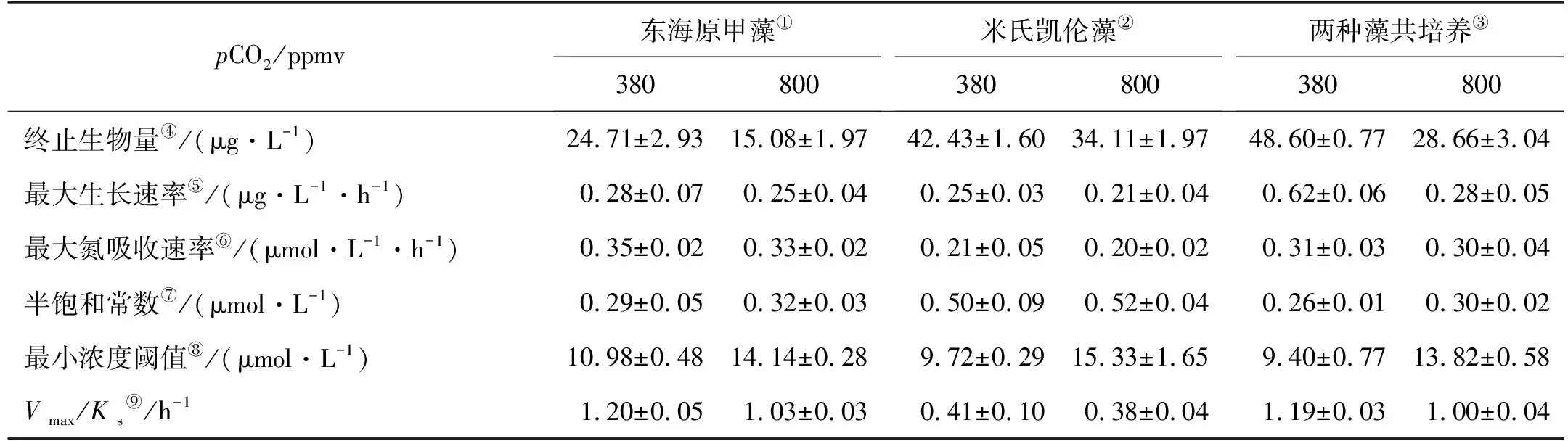
表2 东海原甲藻、米氏凯伦藻和混合藻以DON为氮源在不同pCO2条件下(380和800 ppmv)的生长和氮吸收动力学参数
浮游植物生长动力学拟合结果显示,东海原甲藻的最大生长速率比米氏凯伦藻略快(见表2)。在正常pCO2条件下,二种藻单独培养均显著小于(P<0.05)混合培养下的表观最大生长速率(见表2);而在pCO2升高酸化条件下,三者的最大生长速率没有显著差异(P>0.05)。
2.2 营养盐吸收
东海原甲藻单独培养下,其两种pCO2条件下DON的消耗均快于米氏凯伦藻培养下的(见图2)。这与其吸收动力学拟合结果一致,即东海原甲藻对DON及其降解产物DIN的最大氮吸收速率,在两种pCO2条件下均显著高于(P<0.05)米氏凯伦藻的,同时也显示东海原甲藻对DON吸收的半饱和常数显著低于(P<0.05)米氏凯伦藻的(见表2)。而二种藻混合培养时,DON的消耗与东海原甲藻单独培养接近,较米氏凯伦藻单独培养快(见图2)。这也反映在其吸收动力学上,即两种藻共培养时,其DON的表观最大氮吸收速率和半饱和常数均与东海原甲藻的接近,不存在显著差异(P>0.05),均显著高于(P<0.05)米氏凯伦藻的(见表2)。pCO2升高对东海原甲藻和米氏凯伦藻对DON的最大吸收速率和半饱和常数没有显著影响(P>0.05),但会显著增大(P<0.05)对DON吸收的最小浓度阈值(见表2)。

图2 实验组和对照组在不同pCO2(380和800 ppmv)条件下东海原甲藻(a、d、g)、米氏凯伦藻(b、e、h)和混合藻培养物(c、f、i)中各形态氮浓度变化Fig.2 The nitrogen concentration fluctuations in the Prorocentrum donghaiense (a, d, g), Karenia mikimotoi (b, e, h), and mixed algal cultures (c, f, i) of DON enrichment treatments and DIN control groups under different pCO2 conditions (380 and 800 ppmv)
亲和力指数(Vmax/Ks)可以用来评估浮游植物对营养底物的亲和力,较高的亲和力指数表示浮游植物具有较高的竞争力[52]。实验结果显示,在DON为氮源单藻培养下,米氏凯伦藻的Vmax/Ks在两个pCO2条件下均显著低于东海原甲藻的Vmax/Ks(P<0.05),这表明米氏凯伦藻的竞争力低于东海原甲藻。在两个pCO2条件下,混合藻培养的表观Vmax/Ks值与东海原甲藻Vmax/Ks更加接近,不存在显著性差异(P>0.05),可能与两者共培养下东海原甲藻优先成为优势种有关。
2.3 SOD和CAT酶活性
在pCO2为380 ppmv正常条件下,东海原甲藻培养体系的SOD酶活性随时间先增加后降低,并在第2天达到酶活性最大值(见图3(a));在整个培养实验期间米氏凯伦藻培养体系的SOD酶活性相对恒定(见图3(b));两种藻共培养的SOD酶活性和米氏凯伦藻单独培养具有相同的趋势(见图3(c))。在pCO2为800 ppmv酸化条件下,所有实验组中的SOD酶活性均随时间先增加后降低(见图3)。采用浮游植物指数生长期的平均SOD酶活性来表示其对环境压力的响应(见表3)。结果表明,以DIN实验组为对照,在正常培养条件下,DON的加入对东海原甲藻、米氏凯伦藻和两种藻混合培养下的SOD酶活性没有显著影响(P>0.05)(见表3);酸化增加了米氏凯伦藻的SOD酶活性,而对东海原甲藻的SOD酶活性增加影响不大(见图3)。

图3 在不同pCO2(380和800 ppmv)条件下实验组和对照组的东海原甲藻(a、d)、米氏凯伦藻(b、e)和混合藻(c、f)体系中的超氧化物歧化酶(SOD)Fig.3 Superoxide dismutase (SOD) in the Prorocentrum donghaiense (a, d), Karenia mikimotoi (b, e), and mixed algal cultures (c, f) of the DON enrichment treatments and the DIN control treatments under different pCO2 conditions (380 and 800 ppmv)

表3 在不同pCO2(380和800 ppmv)条件下实验组和对照组的东海原甲藻、米氏凯伦藻和混合藻体系中的超氧化物歧化酶(SOD)和过氧化氢酶(CAT)酶活性Table 3 Catalase (CAT) and Superoxide dismutase (SOD) enzyme activities in the Prorocentrum donghaiense, Karenia mikimotoi, and mixed algal cultures of the DON enrichment treatments and DIN control treatments under different pCO2 conditions (380 and 800 ppmv)
东海原甲藻和米氏凯伦藻单独培养体系的CAT酶活性,在两个pCO2条件下变化趋势基本一致,其中,东海原甲藻培养体系的CAT酶活性随时间降低(见图4(a)),而米氏凯伦藻培养体系的CAT酶活性则先升高后降低,并在第2天达到酶活性最大值(见图4(b))。对混合培养体系的CAT酶活性变化趋势分析发现,酸化条件下和米氏凯伦藻单独培养的变化趋势一致,而在正常条件下和东海原甲藻单独培养的变化趋势一致(见图4(c))。分析指数生长期平均CAT酶活性表明(见表3),相对于DIN对照培养体系,DON的加入对两种藻单独培养和混合培养的CAT酶活性均影响不大,而酸化显著增加(P<0.05)了东海原甲藻和混合藻培养体系的CAT酶活性(见表3)。
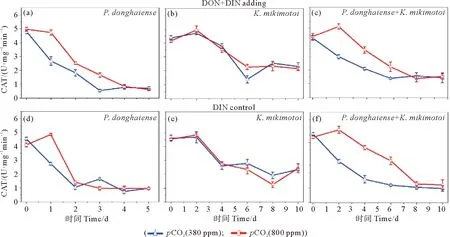
图4 在不同pCO2(380和800 ppmv)条件下实验组和对照组的东海原甲藻(a、d)、米氏凯伦藻(b、e)和混合藻(c、f)体系中的过氧化氢酶(CAT)Fig.4 Catalase (CAT) in the Prorocentrum donghaiense (a, d), Karenia mikimotoi (b, e), and mixed algal cultures (c, f) of the DON enrichment treatments and DIN control treatments under different pCO2 conditions (380 and 800 ppmv)
3 讨论
海洋酸化(pCO2升高)会影响浮游植物的生长和营养盐吸收,本文实验结果显示,米氏凯伦藻和东海原甲藻的生长均明显受到酸化的抑制,而对DON的吸收则影响不大。在pCO2为380 ppmv的正常培养条件下,东海原甲藻较米氏凯伦生长略快,对氮营养盐的吸收则显著快于米氏凯伦藻。而在海洋酸化(pCO2升高)条件下,米氏凯伦藻较东海原甲藻生长速率受抑制更为显著,而终止生物量与东海原甲藻下降幅度相当。有研究表明,pCO2升高致使细胞的能量流通减少,细胞对氮营养盐的吸收降低,进而导致蛋白质的合成效率降低[53],但这与我们实验中氮吸收速率不变而生长变慢,特别是终止生物量显著下降不同。pCO2升高能破坏浮游植物的细胞结构并导致其生理调节机制变化,如营养盐代谢、细胞膜氧化还原和电子转移等[54]。此外,细胞外的pH变化还可能导致细胞内外酸碱失衡,引起细胞酸中毒[55]。这些酸化条件下能量的消耗,可能是本实验中米氏凯伦藻和东海原甲藻营养盐吸收能力受酸化影响较小,而生长受到明显抑制的原因。
海洋酸化对东海原甲藻和米氏凯伦藻生长的抑制作用还体现在抗氧化酶系统上,表现为SOD和CAT等抗氧化酶活性的变化。抗氧化酶在酸化条件下维持细胞内氧化还原平衡中起着重要作用,pCO2水平的升高,导致米氏凯伦藻、东海原甲藻和混合藻培养体系中的CAT或SOD等抗氧化酶活性较正常pCO2水平条件下增加,这与以前的研究结果一致[56]。研究表明,当杜氏藻暴露于盐度胁迫下时,细胞内SOD活性随盐度水平的升高而增加[57];在强光下培养威氏海链藻的ROS产量增加伴随着SOD和CAT酶活性增加[58]。酶活性的变化可能是浮游植物受生长环境胁迫时,引起自身生理特性的适应性调节[59]。尽管大多数氧化损伤可以通过自然防御机制克服,但持续的损伤也可能导致细胞死亡[54]。在我们的研究中,浮游植物的终止生物量都随着pCO2水平升高而降低(P<0.05)。
研究表明,富营养化和海洋酸化可以改变赤潮期间浮游植物的优势种群,并对生态系统功能产生潜在的影响[65]。本文实验结果显示,当以DON作为氮源时,在正常培养条件下,东海原甲藻较快的进入指数生长期并在初期成为优势种,而米氏凯伦藻能够继续利用DON,在后期成为优势种(见图5(a))。在中国福建省沿海地区也常发生东海原甲藻赤潮和米氏凯伦藻赤潮同时或交替发生现象[60],赤潮爆发期间藻优势种变化是一种正常的生态现象并且可能受营养盐的影响[61-62]。在我们的研究中,混合藻的最大生长速率比单一藻培养的最大生长速率快(见图5(a)和(c),表2),可能是东海原甲藻与米氏凯伦藻在共培养体系中,协同性生长,先后或错位吸收环境中的DON[63]。混合藻培养体系的SOD和CAT酶活性值没有明显增加,其中,SOD酶活性和米氏凯伦藻单独培养下有相同的变化趋势,CAT酶活性和东海原甲藻单独培养下有相同的变化趋势,这进一步表明在共培养体系中两种藻可能具有协同作用。pCO2的升高使得东海原甲藻和米氏凯伦藻混合培养的生长速率显著下降,并且酸化条件下的平台期比正常条件下平台期维持的时间要短(见图5(b),表2),表明海洋酸化可能会造成两种甲藻的生态位发生变化,引起米氏凯伦藻提前与东海原甲藻进行竞争,造成营养盐的早期消耗而限制了实验后期米氏凯伦藻的生长(见图5(d))。这也体现在酸化条件下混合藻培养体系的SOD酶和CAT酶活性的显著增加,并且与米氏凯伦藻的SOD酶和CAT酶活性的增加趋势更加接近,表明了pCO2水平升高对共培养体系中米氏凯伦藻生长可能有更大的刺激和抑制作用。
海洋酸化和富营养化对海洋环境产生严重影响,并可能在未来不可逆转地改变海洋生态系统[9,64-65]。藻类优势种的变化是一个相对复杂的过程,受众多环境因素的影响[66]。需要针对海洋酸化和富营养化(例如人为源DON排放增加)对海洋浮游植物的影响开展长期的研究。
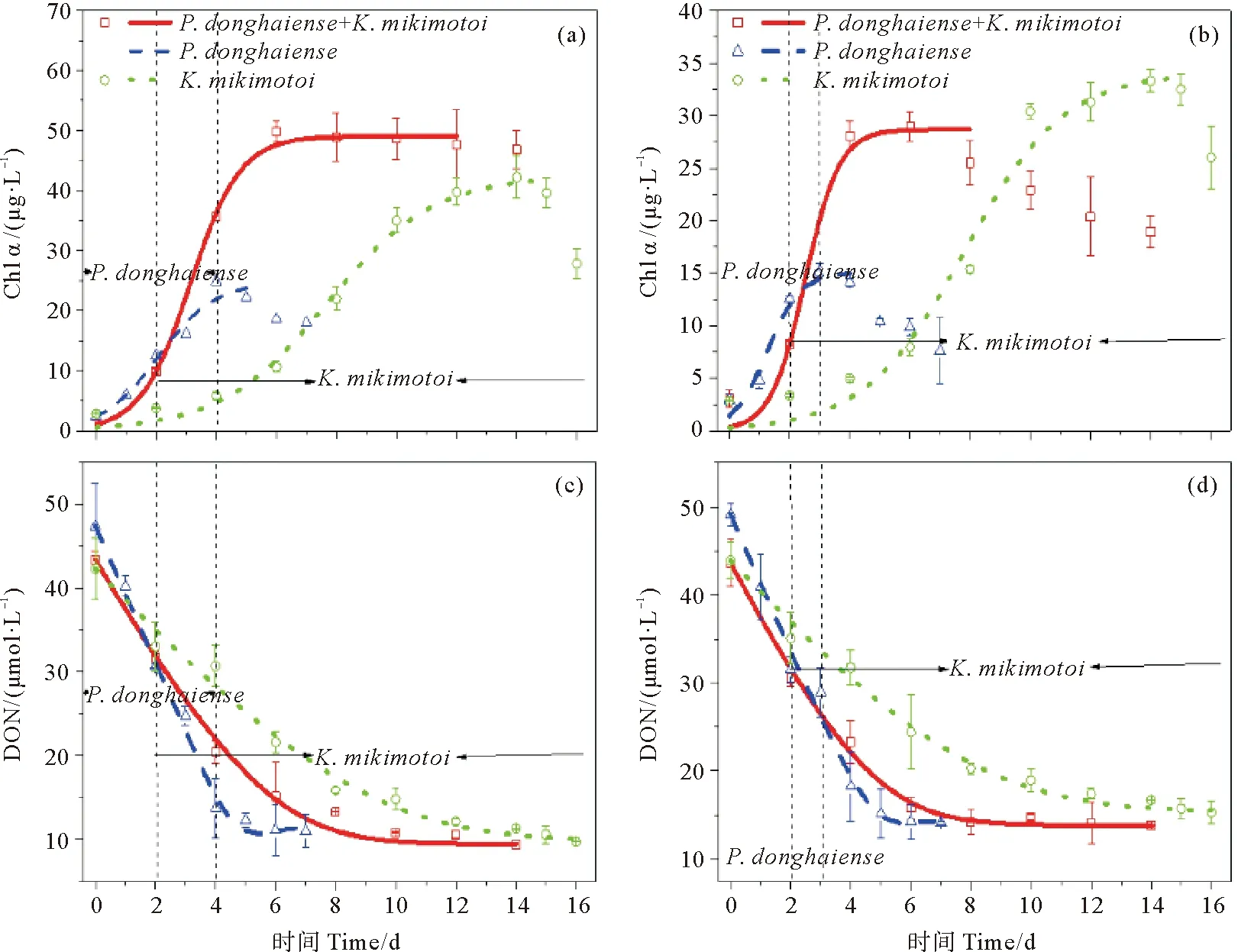
(虚线和实线分别为东海原甲藻和米氏凯伦藻单独培养和二者混合培养的生长曲线和营养盐吸收曲线。左起第一根黑色虚线表示米氏凯伦藻开始生长和开始快速吸收利用DON的时间,左起第二根黑色虚线表示东海原甲藻进入死亡期时间和快速吸收DON终止时间。The dotted line and the solid line are the growth curve and nutrient absorption curve of Prorocentrum donghaiense and Karenia mikimotoi cultured separately and the Prorocentrum donghaiense and Karenia mikimotoi co-culture, respectively. The first black dotted lines from the left indicate the time of Karenia mikimotoi began to grow and to rapidly absorb and utilize DON, the second black dotted lines from the left indicate the time of Prorocentrum donghaiense entered the death period and the end time of the DON was absorbed rapidly by Prorocentrum donghaiense.)
4 结论
本文研究pCO2的升高和人为源DON对米氏凯伦藻和东海原甲藻生长和竞争的影响。采用一次性营养盐加富培养实验,结论如下:
(1)海洋酸化即pCO2升高会抑制东海原甲藻和米氏凯伦藻的生长,但不抑制其对DON的吸收,生长的抑制作用体现在抗氧化酶活性(SOD和CAT)随pCO2水平升高而增加。
(2)在人为源DON加富培养条件下,东海原甲藻比米氏凯伦藻更具有竞争力,优先成为优势种,而米氏凯伦藻可以继续利用DON提供的氮库,并在滞后阶段后成为优势种;升高的pCO2,使得这两种甲藻在竞争条件下生长均受到抑制,特别是米氏凯伦藻受到的影响更大,改变了这两种甲藻的协同交替生长模式。

