BiOI/TiO2纳米棒阵列膜的制备及光催化性能
薛丽梅, 王继文, 梁尔淼
(黑龙江科技大学 环境与化工学院, 哈尔滨 150022)
0 引 言
抗生素广泛用于农牧业中,它进入动物体后绝大多数会被排出体外,进入地下水、地表水中。水体中的抗生素不仅会危害水生生物的生长繁殖,还会影响人类的生命健康[1]。为此,加快对抗生素的降解,缓解其对环境的破坏和对人类健康的危害尤为重要。半导体光催化氧化法是在光照及催化剂等条件作用下对抗生素进行氧化分解,使其成为无毒的小分子的一种方法。因其经济成本低、适用范围广、操作安全、无二次污染等特点,受到了研究者们的关注。二氧化钛(TiO2)以其氧化还原电位高、化学稳定性好、无毒性和低成本等优点被用于半导体光催化研究中[2]。但TiO2禁带宽度约为3.2 eV,可见光对其无响应,光生电子-空穴容易快速复合导致光催化效率和量子效率低,加之TiO2粉末在水体中难回收、活性成分损失大,其应用受到了限制。
将TiO2制成TiO2纳米棒阵列膜(TNAs膜)是一种提高光催化活性和实用性的可行方法[3]。纳米棒阵列膜不需要离心过滤等操作就能快速从水体中分离,从而减少活性成分的损失,提高光催化剂的环境友好性以及实用性。与TiO2纳米球[4]、TiO2纳米管[5]和其他分层微结构[6]相比,TiO2纳米棒阵列(TNAs)结构可获得更大的比表面积,并成为界面间电荷转移的良好电子渗透通道,增加活性位点[7]。纳米棒结构可使TiO2获得量子尺寸效应,让光生电子沿一维的纳米棒有序传输,快速地与表面的活性物质反应,降低光生电子-空穴的复合率,提高其光催化活性[8]。另外,针对TiO2较宽的禁带导致可见光响应差的限制,可以对其进行改性处理,如离子掺杂、贵金属沉积、半导体复合等,获得可见光响应[9]。其中,半导体复合是一种提高可见光响应能力的有效方法,窄带隙的半导体材料与TiO2复合后可降低禁带宽度,拓展光响应范围,并形成异质结结构抑制光生电子-空穴复合,提高光催化活性[10]。BiOI是一种禁带宽度为1.75 eV的窄带隙半导体材料,具有可见光响应能力及高空穴迁移率,在光催化领域有较强的应用潜力[11]。Liu Z Y等[12]通过电化学法在钛网上制备出TiO2纳米管阵列(TiO2NTs),随后通过溶剂热法在其上沉积了BiOI制备出TiO2NTs/BiOI光催化膜,BiOI提高了TiO2纳米管阵列的光响应范围。该光催化膜在模拟太阳光照射下对甲基橙、罗丹明B以及亚甲基蓝的光催化降解率均达到90%以上,而对Cr(VI)的光催化降解率也达到70%以上。Odling G等[13]通过模板法将TiO2固定在FTO玻璃上制备出TiO2膜,随后通过SILAR法将BiOI沉积在TiO2上制备出TiO2/BiOI光催化膜,TiO2膜沉积BiOI后,光响应能力得到了提高,TiO2与BiOI之间形成了n-p异质结,抑制了光生电子-空穴的复合,提高了光催化能力,该光催化膜对罗丹明B以及4-氯酚具有较好的光催化降解能力。可见,窄带隙的BiOI可以拓展TiO2的光响应范围,形成异质结结构,提高光催化活性,但有关TNAs膜与BiOI复合的光催化应用研究却鲜有报道。因此,可将BiOI与TNAs膜复合,获得在太阳光下具有较高光催化活性的BiOI/TNAs膜。
笔者采用一种简单的水热法在FTO玻璃上生长出TNAs膜,通过SILAR法在TNAs上沉积BiOI,制备出BiOI/TNAs膜,并以土霉素为模拟抗生素污染物,探究了BiOI/TNAs膜制备条件对抗生素降解效率的影响。
1 实 验
1.1 材料
实验材料:钛酸四丁酯,AR,上海展云化工有限公司;盐酸,AR,哈尔滨市鑫田科技有限公司;五水硝酸铋,AR,天津市福晨化学试剂厂;碘化钾,AR,天津市永大化学试剂有限公司;乙二醇,AR,国药集团化学试剂有限公司;无水乙醇,AR,哈尔滨市鑫田科技有限公司;土霉素,云南白药集团股份有限公司;去离子水,自制;FTO导电玻璃(7 Ω,100 mm×100 mm×2.2 mm)。
1.2 表征方法
样品的XRD测试在德国Bruker D8 Advance型X射线衍射仪(40 kV,40 mA)上进行,选用Cu-Kα 辐射(λ=0.154 06 nm);表面形貌测试在荷兰Phenom Pro X 扫描电子显微镜上进行,加速电压10 kV;光响应范围测试通过德国耶拿分析仪器股份有限公司生产的Specord Plus型紫外-可见漫反射光谱仪进行,以BaSO4为参比测定样品,扫描范围为380~1 100 nm。
1.3 样品的制备
1.3.1 TNAs膜
将FTO玻璃裁成30 mm×15 mm的尺寸,使用无水乙醇及去离子水清洗、干燥。在磁力搅拌下将钛酸四丁酯逐滴加入30 mL浓盐酸与去离子水体积比为1∶1的盐酸溶液中,继续搅拌至混合溶液变为澄清。将FTO导电面朝下斜靠在50 mL内衬为聚四氟乙烯的水热釜中,将前驱液移入水热釜中,进行水热反应。反应结束后待其冷却,取出样品用去离子水洗去样品表面的残余溶液,在60 ℃下真空干燥2 h,即获得TNAs膜。通过调节钛酸四丁酯添加量V、水热时间t、水热温度θ等条件以获得形态较好的TNAs膜。不同TNAs膜的制备条件如表1所示。
1.3.2 BiOI/TNAs膜
配制0.05 mol/L的硝酸铋溶液及碘化钾溶液,将TNAs膜浸入硝酸铋溶液1 min,使Bi3+吸附在TNAs膜上,随后使用去离子水漂洗10 s,洗去漂浮在膜上未吸附的Bi3+;再将TNAs膜浸入碘化钾溶液1 min,使KI与Bi3+发生反应,在TNAs膜上沉积BiOI,随后使用去离子水漂洗10 s。这样一个步骤称作一次沉积,重复数次即可获得BiOI/TNAs膜,记为BiOI/TNAs-X。其中X为沉积次数,分别为2、4、6、8和10次。
1.4 光催化降解
光催化降解实验以300 W的氙灯(λ=190~1 100 nm)为光源。将样品加入到50 mL模拟污染物(5 mg/L土霉素溶液)中,避光搅拌10 min,达到吸附-脱附平衡后,在氙灯照射下进行光催化降解实验,每隔20 min取土霉素溶液一次。使用紫外可见分光光度仪,在354 nm处测定土霉素溶液的吸光度A,土霉素降解率D的计算公式为
式中:D——降解率,%;
ρ0——土霉素的初始质量浓度,mg/L;
ρt——t时刻土霉素的质量浓度,mg/L;
A0——土霉素的初始吸光度值;
At——t时刻土霉素溶液的吸光度值。
2 结果与分析
2.1 TNAs膜的形貌调控
2.1.1 SEM形貌调控
图1为不同水热温度的TNAs膜的SEM图。当钛酸四丁酯添加量为0.5 mL、水热时间为8 h,水热温度为140 ℃时,TiO2棒分布较为均匀,但仍然会出现倒伏现象,形貌较差(图1a)。图1b为样品T5的正面SEM图。当其他条件不变,水热温度为150 ℃时,TiO2纳米棒在FTO基底上分布均匀,取向一致,纳米棒之间未出现交叉接触,整体排列有序,整体形成纳米棒阵列形貌。图1c为样品T6的正面SEM图。当其他条件不变,水热温度增加到160 ℃时,TiO2纳米棒可以形成阵列形貌,但部分TiO2纳米棒会聚集在一起,形成板块状,不利于光催化的进行。
图2为不同水热时间的TNAs膜的SEM图。图2a为样品T7的截面SEM图。当钛酸四丁酯添加量为0.5 mL、水热温度为150 ℃,水热时间为6 h时,TiO2纳米棒参差不齐,部分纳米棒的生长长度较短,纳米棒阵列形貌较差。图2b为样品T8的截面SEM图。当其他条件不变,水热时间为8 h时,TiO2纳米棒大部分垂直于底部均匀地竖直生长,且生长方向、生长长度一致,具有良好的取向性。图2c为样品T9的截面SEM图。当其他条件不变,水热时间增加到10 h时,纳米棒的生长长度会变长,且生长密度也会增加,纳米棒之间的间隙减少,光催化活性位点减少,从而降低光催化性能。
为获得形貌较好的TNAs膜,在对水热温度及水热时间等条件进行探讨后,继续对钛酸四丁酯添加量进行了研究。图3为不同钛酸四丁酯添加量的TNAs膜的SEM图。

图3 不同钛酸四丁酯添加量的TNAs膜Fig. 3 TNAs films with different addition amounts of tetrabutyl titanate
由图3a可以看出,当钛酸四丁酯添加量为0.25 mL、水热温度为150 ℃、水热时间为8 h时,FTO表面生长的TiO2纳米棒数量较少,生长密度较低,纳米棒出现倒伏现象,不能形成纳米棒阵列形貌。图3b为样品T2正面的SEM图。TiO2纳米棒在FTO基底上分布均匀,取向一致,纳米棒之间未出现交叉接触,整体排列有序,整体形成纳米棒阵列形貌。图3c 为样品T2剥离的单个TiO2纳米棒的SEM图。TiO2呈现纳米棒状结构,长度约为2 μm,直径约为150 nm,为纳米尺寸。图3d为样品T3的SEM图。当其他条件不变,钛酸四丁酯添加量增加到1 mL时,TiO2纳米棒生长过于密集,出现了黏结现象,形成了板块状结构,不能形成纳米棒阵列形貌。
由SEM表征分析可以看出,制备条件为钛酸四丁酯添加量0.5 mL、水热温度150 ℃、水热时间8 h时,TNAs膜的表面形貌最好。在此条件下可制备出TiO2纳米棒生长长度一致、生长间距合适的TNAs膜。
2.1.2 XRD表征
图4为样品T2的XRD谱图。由图4可见,除FTO基底的特征衍射峰外,可以观察到单纯的TiO2晶相特征衍射峰,与四方金红石相TiO2(JCPDS No.760317)特征衍射峰相吻合。主要特征峰位置2θ为36.0°、41.2°、54.3°、62.8°,分别与金红石相TiO2的(101)、(111)、(211)、(002)晶面相对应。而金红石相TiO2的(110)晶面所对应的2θ=27.4°的特征衍射峰大幅降低,(101)晶面对应的2θ=36.0°的特征衍射峰有较大的增强,(002)晶面对应的2θ=62.8°的特征衍射峰显著增强,表明TiO2为单晶且垂直于底面朝着一个晶面取向生长,表现出纳米棒阵列形貌的趋势。这与TNAs膜的SEM表征结果相一致。纳米棒阵列的形成机理,通常认为是由于FTO衬底为四方金红石晶相的SnO2,与四方金红石晶相的TiO2的晶格失配率为2%。这种较小的晶格失配使TiO2很容易在FTO上外延成核及垂直生长,最终形成纳米棒阵列[14-15]。

图4 样品T2的XRD谱Fig. 4 XRD spectra of sample T2
2.2 BiOI/TNAs膜的结构和形貌表征
2.2.1 XRD表征
图5为不同BiOI/TNAs膜的XRD谱图。由图5可见,所有的样品特征衍射峰均较为尖锐,且具有较好的结晶度,所有样品均可以观察到四方金红石相TiO2(JCPDS No.760317)特征衍射峰。此外,2θ为29.7°、31.7°、45.5°、55.3°时出现了新的特征衍射峰,分别与四方晶系BiOI(JCPDS No.732062)的(012)、(110)、(020)、(122)相对应。随着BiOI沉积次数的增加,2θ=31.7°所对应的衍射峰逐渐增高。这表明样品是由四方晶系BiOI与四方晶系金红石相TiO2共同组成的。其中,四方晶系BiOI在2θ=29.7°所对应的(012)晶面的衍射峰有明显的减弱,而2θ=31.7°所对应的(110)晶面衍射峰显著增强,说明BiOI的主要暴露面可能为(001)晶面。

图5 不同BiOI/TNAs膜的XRD谱Fig. 5 XRD spectra of different BiOI/TNAs films
2.2.2 SEM表征
图6为不同BiOI/TNAs膜的SEM形貌。图6a为BiOI/TNAs-2斜截面的SEM图,经过2次BiOI沉积后,较小的BiOI片状颗粒覆盖在TNAs表面,BiOI片状颗粒分散均匀。这可以归因于BiOI沉积次数较少,在TNAs表面随机生长,未形成较大晶核,而TiO2纳米棒阵列形貌未被破坏。图6b为BiOI/TNAs-6正面的SEM图,在经过6次沉积后,BiOI形成丝状以及条状结构覆盖在TNAs表面,部分BiOI进入TNAs的空隙之中,与TNAs的接触面积增多。这有利于TiO2与BiOI之间的电子传输过程。图6c为BiOI/TNAs-10正面的SEM图,在沉积10次BiOI后,TNAs上附着的BiOI明显增多,BiOI形成较大的片状结构,覆盖在TNAs表面,并将部分TiO2纳米棒之间的空隙覆盖,说明经过多次的BiOI沉积后BiOI片状颗粒生长成较大的BiOI片,平均尺寸及厚度也随之增大,TNAs的空隙被盖住。这会导致光催化膜的比表面积减少,以及对紫外光的吸收减弱,降低光催化活性。通过SEM表征可以看出,通过SILAR法,在不破坏TiO2纳米棒阵列形貌的条件下,成功将BiOI沉积在TNAs上,制备出了BiOI/TNAs膜。

图6 不同BiOI/TNAs膜的SEM形貌Fig. 6 SEM morphology of different BiOI/TNAs films
2.2.3 UV-Vis DRS表征
图7为不同光催化膜的紫外可见漫反射吸收光谱图。由图7可以看出,TNAs膜在405 nm出现吸收边,仅在紫外光区域具有光响应。沉积BiOI后的BiOI/TNAs膜在550 nm附近出现了新的吸收边,表现出多带隙结构,对紫外光及可见光均具有光响应,且沉积次数越多,可见光响应强度越强,说明窄带隙BiOI可以有效扩展TiO2的光响应范围。

图7 不同光催化膜的紫外可见漫反射吸收光谱Fig. 7 UV-Vis DRS absorption spectra of different photocatalytic films
根据Kubelka-Munk 方程可以计算出不同光催化膜的禁带宽度,其方程式为
Ahv=c(hv-Eg)2,
式中:A——摩尔吸收系数;
h——普朗克常数;
v——入射光子频率;
c——比例常数;
Eg——光学带隙。
由Kubelka-Munk 方程拟合得出,TNAs膜的禁带宽度为3.00 eV,BiOI/TNAs-2、BiOI/TNAs-4、BiOI/TNAs-6、BiOI/TNAs-8、BiOI/TNAs-10的禁带宽度分别为 2.95、2.90、2.80、2.70、2.40 eV。可见,将TNAs与BiOI复合后,BiOI/TNAs膜的禁带宽度相较于TNAs膜变窄了,降低了电子发生跃迁所需要的能量,扩宽了TiO2的光响应范围。其在可见光区域的光量子效率提高,使光生电子-空穴对更容易发生分离,提高了光生电子-空穴对的生成速率。
2.3 光催化降解评价
图8为不同光催化薄膜对抗生素的光催化降解曲线。在无光催化膜的条件下光照3 h,抗生素有10%左右的降解率。在加入TNAs膜后,光照相同时间,降解率仅为31%。这是由于TiO2仅在紫外区具有光响应,光利用率较低。加入BiOI/TNAs-2后,降解率提高了17%,表明TNAs在复合了窄带隙的BiOI后,禁带宽度变窄,在可见光的照射下即可激发电子跃迁,促进光生电子-空穴对的分离,且BiOI与TiO2之间形成了异质结,抑制光生电子-空穴对的复合,提高了光催化性能[16]。加入BiOI/TNAs-4以及BiOI/TNAs-6后,相较于TNAs膜,降解率分别提高了20%和30%。可见,随着BiOI沉积量的增加,复合膜带隙越窄,可见光利用率越高,光催化活性也会增加。在加入BiOI/TNAs-8及BiOI/TNAs-10后,降解率相较于BiOI/TNAs-6反而下降了2%和18%。这是由于适量的BiOI可以均匀地分布在TNAs表面,当BiOI复合量增大时,BiOI会将TNAs表面覆盖,减少膜表面活性位点,抑制TNAs对光的吸收,减少光生电子空穴对的形成,从而抑制光催化活性[17]。

图8 不同光催化膜对抗生素的光催化降解曲线Fig. 8 Photocatalytic degradation curves of antibiotics by different photocatalytic films
图9为BiOI/TNAs-6光催化降解抗生素溶液在不同时间的吸收光谱。可以看出:抗生素在354 nm波长处具有最高的吸收峰;在光催化的前120 min内,随着光催化的进行,吸收峰的强度下降较快,在光催化进行到120 min后,吸收峰趋于平稳。这说明在光催化降解初期,溶液中的抗生素含量较多,可以充分地吸附在光催化膜上,光催化效率较高,在经过一段时间的光催化降解后,溶液中的抗生素含量降低,吸附在光催化膜上的抗生素减少,导致光催化效率降低,而经过3 h的光催化降解后,大部分抗生素被降解。

图9 BiOI/TNAs-6光催化降解抗生素溶液不同时间的吸收光谱Fig. 9 Absorption spectra of TNAs/BiOI-6 photocatalytic degradation of antibiotic solution at different times
光催化降解低浓度有机污染物的反应为多相表面反应过程。其动力学可以用L-H模型的一级简化形式描述,其方程式为
ln(ρt/ρ0)=kEt,
式中:ρt——t时刻抗生素质量浓度,mg/L;
ρ0——抗生素原始质量浓度,mg/L;
kE——准一级动力学常数;
t——降解时间,min。
图10为不同光催化膜的一级动力学曲线。根据L-H模型计算出光催化膜的一级动力学常数,TNAs膜降解抗生素一级动力学常数为0.001 98 min-1,在沉积BiOI后,BiOI/TNAs-2、BiOI/TNAs-4、BiOI/TNAs-6、BiOI/TNAs-8、BiOI/TNAs-10的一级动力学常数分别为0.003 56、0.004 05、0.004 70、0.004 68、0.002 84 min-1,均高于TANs膜,而BiOI/TNAs-6的一级动力学常数最大,为TNAs膜的2.4倍,有效地提高了光催化活性。

图10 不同光催化膜的一级动力学曲线Fig. 10 First order kinetics curve of different photocatalytic films
2.4 机理分析

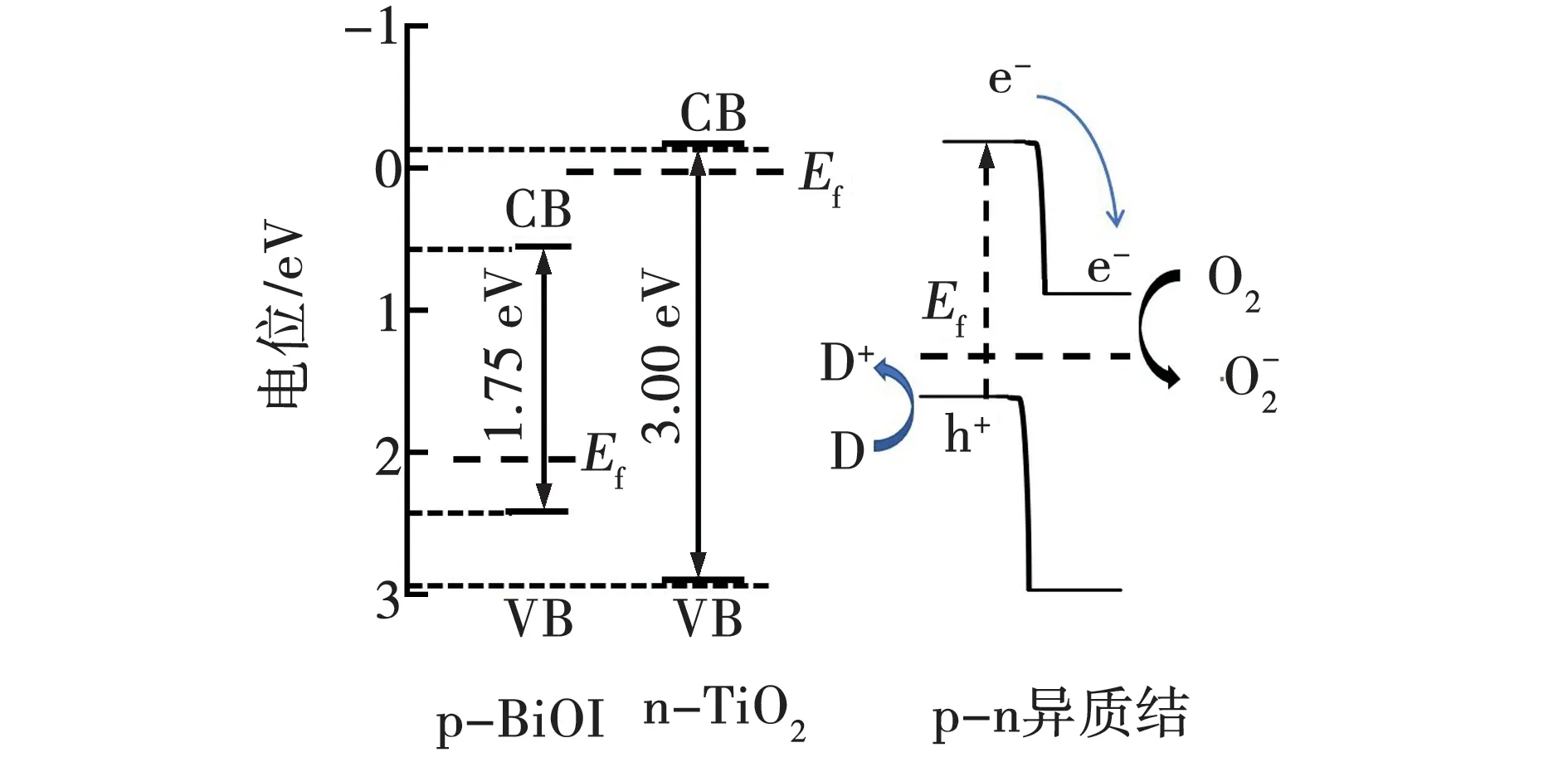
图11 BiOI/TNAs膜的光催化机理Fig. 11 Photocatalytic mechanism of BiOI/TNAs film
3 结 论
(1)利用水热法制备了TNAs膜。通过SILAR法在TNAs膜上沉积了BiOI,成功制备出BiOI/TNAs膜。四方晶系的BiOI均匀的沉积在金红石相的TiO2纳米棒阵列上,提高了TNAs膜的光响应范围,可将禁带宽度降低至2.40 eV,使光生电子-空穴更加容易分离。TiO2与BiOI之间形成了异质结结构,抑制了光生电子-空穴的复合,有效的提高了光催化性能。
(2)BiOI/TNAs膜最佳制备条件为水热温度150 ℃,水热时间8 h,钛酸四丁酯、盐酸、水的体积比为1∶30∶30。BiOI沉积6次时,BiOI/TNAs膜的光催化活性最好,光催化降解率为TNAs膜的2倍。

