多种绿色起爆药的合成方法研究进展❋
高耸松 谢兴兵 王元和
陕西应用物理化学研究所(陕西西安,710061)
引言
在火工品领域中,起爆药具有其他含能材料难以替代的地位。其最重要的特征是极其迅速地将爆燃转换为爆轰(DDT)[1]。常用的经典起爆药有斯蒂芬酸铅(LTNR)、叠氮化铅(LA)等。然而,铅元素具有明显的毒性,对中枢神经系统、肾脏系统和血液都有着极大的危害[2],目前已成为国际上管制最严格的化学物质之一[3]。随着环境保护与可持续发展的理念越来越深入人心,起爆药须朝着无毒且环境友好的方向发展。
绿色起爆药的6条标准:1)对光和水分钝感;2)感度合适(对非爆炸刺激足够敏感,但不应在操作或运输中因太敏感而造成危险);3)200℃以下热稳定;4)储存期内化学稳定,即安定性好;5)不含铅、汞、银、钡、锑等毒性金属;6)不含带毒性的高氯酸盐(有可能是致畸因子且对甲状腺功能有副作用)[4]。
自20世纪90年代起,世界各国已竞相开展绿色起爆药的研究,并先后研制出一系列的新型绿色起爆药,如二硝基苯并氧化呋咱钾盐(KDNP)、5-硝胺基四唑钙盐等。其中的一些已应用在起爆器、雷管、点火元件等火工品中,且取得了较LA与LTNR更优良的试验结果[5]。
根据起爆药的类型,对近年来较有应用前景的绿色起爆药合成时所采用的反应路线与方法进行了整理与综述,并对相关反应机理、药剂性能与用途进行了讨论,为该领域的研究与发展提供参考。
1 叠氮类绿色起爆药
1.1 有机叠氮类绿色起爆药的一般合成方法
合成有机叠氮化物的一般方法是:通过叠氮基与底物分子内π键碳原子上的卤素或硝基发生亲核取代反应,从而得到目标产物。反应在冰水浴中进行,叠氮基负离子一般由叠氮化钠NaN3提供。典型的合成方法如图1所示。三聚氰氯与NaN3反应生成三叠氮基均三嗪(TAT)。该药剂起爆能力强,热稳定性良好,撞击敏感、静电感度显著钝感于LTNR,可有效替代LA与LTNR。目前已被作为起爆药替代NOL-130针刺型雷管与M67手榴弹中的LA,并完成了验证试验[6]。

图1 TAT的合成Fig.1 Synthesis of TAT
1.2 二叠氮基乙二肟(DAG)
2011年,在研究新型富氮炸药TKX-50的过程中,报道了一种具有潜在应用价值的起爆药——二叠氮基乙二肟(DAG)[7]。然而,作为反应的中间体,DAG未经纯化就被用于制备TKX-50的后续反应中。到了2014年,王小军等[8]在成功合成了该起爆药的同时对其予以纯化及表征。DAG的合成方法如图2。乙二醛为初始原料,与盐酸羟胺发生缩合反应,得到乙二肟;随后进行氯代反应,生成二氯乙二肟;该化合物与叠氮化钠发生亲核取代反应,得到目标产物。研究发现:DAG不仅是合成新型富氮炸药的重要中间体,还可用于对抗大规模杀伤性生化武器反战剂战斗部装药[9]。

图2 二叠氮基乙二肟(DAG)的合成Fig.2 Synthesis of diazidoglyoxime(DAG)
2 四唑类绿色起爆药
除叠氮化物外,四唑类化合物是研究最多的绿色起爆药。虽然四唑本身并不适合作为起爆药使用[10],不过,分子内的高含氮量使其本身具有很强的酸性,与金属配位后生成的金属盐具有爆炸性[11]。大部分四唑类化合物具有生成焓高、密度大、热稳定性良好的优点。从环境角度来看,这类化合物分解后产生惰性且无毒的氮气,故可做为一种新型的绿色起爆药[12]。
2.1 四唑类起爆药前体的合成
5-氨基四唑(5-ATZ)具有良好的安全性、耐热性与相容性,且起爆迅速,是合成四唑类起爆药的重要前体[12]。合成方法有两种:Thiele合成法(氨基胍重氮异构法)和Stollé合成法[13]。相较于存在着工艺复杂、反应周期冗长且产率低等问题的Thiele合成法,Stollé等实现了5-ATZ合成方法优化与改进。他们将双氰胺在叠氮酸中分解生成的氰胺与叠氮酸(或甲基叠氮)环化生成5-ATZ(图3)[14]。

图3 Stollé法合成5-ATZFig.3 Synthesis of 5-ATZ by stollémethod
1-烷基取代的5-ATZ一般可通过氮原子上质子的取代反应得到。Joo等[15]报道了合成1-烷基取代的5-ATZ的新方法:烷基取代的胺与叠氮化氰在乙腈溶液中发生亲核加成反应后,发生分子内环化反应得到目标产物(图4,R为烷基,产率52%~84%)。参与反应的叠氮化氰由溴化氰与叠氮化钠在无水乙腈中发生复分解反应制备。此方法简化了1-烷基取代的5-ATZ的合成步骤,提高了反应产率,为合成多种5-ATZ衍生物提供了快捷而高效的途径。

图4 合成1-烷基取代的5-ATZ的新方法Fig.4 The new synthesis method of 1-alkyl-5-ATZ
2.2 硝胺基四唑盐类起爆药
硝胺基四唑盐类起爆药的含氮量大于64%(质量分数),气体产物多为氮气,作用过程中可达到少烟或无烟的效果,具有替代LA的潜力[16]。其前体硝亚胺基四唑可由5-ATZ或1-Me-5-ATZ在质量分数100%的浓硝酸中氧化生成(图5,R为H或Me)[17]。2011年,王杰平等[18]在5-硝亚胺基-1-甲基四唑及其盐的合成研究中发现:在室温下,使用发烟硝酸代替质量分数100%的浓硝酸作为氧化剂,可有效提高反应产率。

图5 硝亚胺基四唑类化合物的合成方法Fig.5 Synthesis of nitriminotetrazolate
2007年,Geisberger等[19]通过硝酸铜中的Cu2+取代了1-甲基-5-硝胺基四唑中的质子,随后在高温、真空的环境中除去分子内的结晶水,合成了二(1-甲基-5-硝胺基四唑)合铜(图6)。该化合物的分解温度为252℃,对撞击敏感(0.7 J),对摩擦钝感(40 N),可在190℃下维持长时间稳定。

图6 二(1-甲基-5-硝胺基四唑)合铜的合成Fig.6 Synthesis of cooper(II)bis-(1-methyl-5-nitriminotetrazolate)
2011年,Fischer等研制并报道了一种新型四唑类绿色起爆药——5-硝胺基四唑钙盐Ca(NATZ)。将氢氧化钙水溶液分批逐滴加入5-硝胺基四唑水溶液中,生成Ca(NATZ)(H2O)5,而后在高温、真空环境下除去结晶水,得到目标产物Ca(NATZ)。合成方法如图7。2013年,佟文超等[20]通过全优化几何构型和轨道能量分析,对Ca(NATZ)的稳定性与分解机理等进行了研究。发现:Ca(NATZ)的分解温度为360℃,热稳定性良好,撞击感度与摩擦感度也较LA钝感,可在电刺激或撞击下起爆,并成功引爆六硝基芪(HNS)。Ca(NATZ)的合成方法简捷,产率(78%)较高,成为目前最有望替代LA的绿色起爆药。

图7 Ca(NATZ)的合成Fig.7 Synthesis of Ca(NATZ)
2.3 硝基四唑类起爆药
硝基四唑类起爆药一般可分为5-硝基四唑盐类起爆药与硝基四唑阴离子为配体的起爆药。自20世纪30年代以来,经过漫长的探索与优化改进,研究人员合成并研究了大量该类起爆药[21]。
2.3.1 硝基四唑类起爆药前体的合成
5-硝基四唑钠盐(NaNT)是合成硝基四唑类起爆药最常用的反应前体[22](图8)。以5-ATZ为底物,在亚硝酸钠的酸性溶液中发生Sandmeyer反应后,生成酮酸盐中间体CuHNT(NT)2·4H2O[23]。该中间体与氢氧化钠溶液混合以沉淀氧化铜,使NaNT留在母液中。随后,可加入正己烷过滤沉淀,或通过蒸馏提纯后重结晶得到目标产物[24]。

图8 NaNT的合成Fig.8 Synthesis of NaNT
为了解决上述工艺在重氮化阶段易发生轻微爆炸的问题,Gilligan等[25]对工艺过程进行了优化,在5-ATZ与硝酸的混合水溶液中加入催化量的Cu(II)盐溶液,以避免爆炸的发生。尽管上述措施优化了NaNT在实验室规模下的合成方法,但随着工艺规模的扩大,合成过程中仍存在着发生爆炸的隐患和凝胶状酸式铜盐的过滤问题。另外,在四唑类起爆药的合成过程中,对NaNT的纯度要求较高,而高纯度NaNT的产率却难以提升[22]。故实现大批量生产NaNT成为了一个极具挑战性的研究方向。
2.3.2 5-硝基四唑盐类起爆药
5-硝基四唑盐类起爆药可通过NaNT与相应的金属盐在水溶液中反应制得,合成过程相当简捷[22]。2008年,Fronabarger等[26]合成并发现了5-硝基四唑亚铜起爆药(DBX-1)。2009年,蒲彦利等[27]对DBX-1进行了合成与表征。DBX-1以自由的单斜晶体形式存在,其合成方法有两种(图9):通过氯化亚铜与NaNT在水溶液中反应得到;以抗坏血酸钠做为还原剂,原位将氯化铜中的Cu(II)还原为Cu(I)后,该Cu(I)与NaNT在水溶液中反应得到[28]。因为第二种方法更易形成具有一定粒度和形貌的晶体,故一般采用该方法进行DBX-1起爆药的合成。反应中的氯化亚铜可由溴化亚铜代替。反应时可以加酸(如盐酸、硝酸、硫酸等)做催化剂,其中加入盐酸时的效果最好。上述反应完全在水溶液中进行,废液主要由氯化钠和水组成,且任何铜离子都可通过加入碱而沉淀成为氧化铜。故该合成工艺亦是环境友好的。

图9 DBX-1的合成Fig.9 Synthesis of DBX-1
DBX-1的撞击、摩擦及静电感度与LA非常接近,起爆能力也与LA相当,在高温、高湿环境下的抗氧化能力比LA更高,可与普通雷管用材料和典型军用炸药兼容。与LA类似的是,DBX-1在水中也会慢慢分解[29]。
2.3.3 硝基四唑阴离子为配体的起爆药
硝基四唑阴离子为配体的起爆药是一种以NH4+、Na+等阳离子与硝基四唑阴离子相结合而形成的配合物[30]。
研究发现,部分上述配合物在水、光和热介质中稳定性强,同时能不被大部分有机溶剂溶解,对静电刺激较钝感[32],且爆炸产物中无有毒气体与金属物质[33],可作为一种性能优越的绿色起爆药[34]。
2.4 5,5'-偶氮四唑为配体的起爆药
5,5'-偶氮四唑金属盐一般感度较高,有作为起爆药的潜力[35]。其分子内的偶氮键不仅提高了氮含量(质量分数大于84%),还增加了分子的生成焓[36]。5,5'-偶氮四唑铜盐和锌盐的制备过程如图10所示。首先,用Thiele碱性氧化法将5-ATZ转化为配合物Na2ATZ·5H2O;随后,加入相应的金属盐溶液,合成目标产物[37]。该类产物一般不溶于水,经抽滤、洗涤后即可提纯。

图10 5,5'-偶氮四唑铜盐和锌盐的合成Fig.10 Synthesis of[Cu(NH3)4]ATZ·2H2 O and ZnATZ
2012年,孙艳苓等[38]对5,5'-偶氮四唑锌(ZnATZ)进行了制备与表征,发现该配合物有良好的火焰感度,撞击感度与斯蒂芬酸铅相当,有望作为点火药和击发药组分。
2014年,谢兴兵等[39]成功合成了偶氮四唑四氨合铜(II){[Cu(NH3)4]ATZ}及其二水合物,并研究了其性能。研究发现:[Cu(NH3)4]ATZ的火焰感度和撞击感度良好,可作为起爆药和击发药,应用前景广阔。
2.5 联四唑类起爆药
随着1,1'-二羟基-5,5'-联四唑(BTO)的问世,自2001年起,研究人员对其离子盐进行了研究[40-41]。2016年,张至斌等[42]首次合成并培养了1,1'-二羟基-5,5'-联四唑钾(BTOK)的单晶,合成方法如图11。DAG在酸性条件下发生分子内环化反应,生成BTO;该化合物与氢氧化钾在水溶液中搅拌,过滤、洗涤后得到高纯度的BTOK。研究发现:BTOK在307℃时开始分解,热稳定性良好,撞击感度低于BNCP、LTNR等,摩擦感度与LTNR相当,对静电火花较钝感,有望成为一种新型绿色耐热起爆药。

图11 BTOK的合成Fig.1 Synthesis of BTOK
3 苯并呋咱盐类绿色起爆药
含有氧化呋咱环(1,2,5-噁二唑-2-氧化物)的化合物及其衍生物大都具备良好的热稳定性与能量水平。当在呋咱盐上引入硝基等高能基团时,其感度将进一步提高,从而具备起爆药的性质。目前已有多种苯并呋咱类起爆药相继问世[43]。
3.1 苯并呋咱环前体的合成机理
合成苯并呋咱环类化合物的前体为邻硝基叠氮苯类化合物及其衍生物。反应机理如图12所示。在酸性条件下,芳环化合物上的叠氮基与其邻位的硝基发生脱氮反应与重排反应,可构建苯并呋咱环。

图12 合成苯并呋咱环的反应机理Fig.12 Reaction mechanism of synthesis of benzofuroxan
3.2 双呋咱-2-硝基酚盐(BFNP盐)
Sitzmann等[44]设计并合成了一种新型的呋咱类起爆药——BFNP盐,如图13。底物为易于购买的3,5-二氯苯甲醚,经硝化反应制得3,5-二氯-2,4,6-三硝基苯甲醚。此化合物在水与碳酸二甲酯(DMC)的双相溶液中与叠氮化钠发生亲核取代反应,生成中间产物3,5-二叠氮基-2,4,6-三硝基苯甲醚。该中间产物含有两对相邻的叠氮基(—N3)与硝基(—NO2),在受热条件下环化生成双呋咱硝基苯甲醚。因π键上的甲氧基在受热环境下易水解,故加热条件下的最终产物即为BFNP[45]。
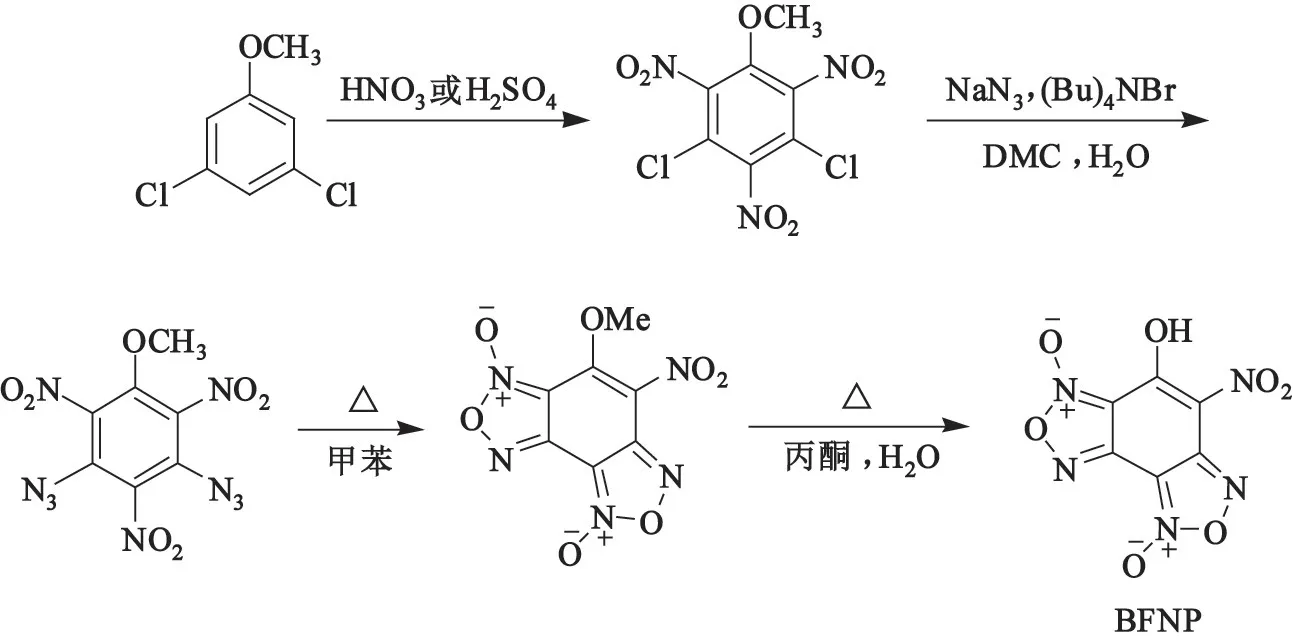
图13 BFNP的合成Fig.13 Synthesis of BFNP
BFNP的盐类可通过其水溶液与相应的乙酸盐、碳酸盐或氢氧化物离子交换得到[46]。具有代表性的是KBFNP的合成方法,如图14[47]。有趣的是,相对于BFNP的其他盐类,KBFNP由两种同分异构体(结构式I和结构式II)以共晶的形式结合(相对占有率51∶49)[48]。KBFNP的热稳定性较低,撞击感度、点火能力和摩擦感度均高于LTNR,点火时间和峰压时间较二硝基苯并氧化呋咱钾(KDNBF)短得多。在替代LTNR方面有着较大的可能性。

图14 KBFNP的合成方法Fig.14 Synthesis of KBFNP
3.3 4,6-二硝基苯并氧化呋咱盐(BFNP盐)
4,6-二硝基苯并氧化呋咱(DNBF)具有一定的酸性,易形成稳定的盐。因其本身亦具有猛炸药的特性,故该化合物的金属盐也有着作为起爆药的潜力。DNBF的合成路线主要有3种[49-50]。鉴于硝化反应较危险且条件苛刻,目前,一般采用图15中的路线进行合成,即从1-氯-2,4,6-三硝基苯出发,经叠氮基取代与脱氮反应生成目标产物[51]。

图15 DNBF的合成Fig.15 Synthesis of DNBF
自20世纪开始,研究人员已合成并研究了如NaDNBF[52]、KDNBF等一系列的金属盐[53]。这类金属盐一般通过DNBF的水溶液或钠盐与其他金属盐的水溶液发生离子交换反应而制备(图16)[54]。图16中,Ni2+,Zn2+,Cd2+;为Al3+,Pb2+,Fe3+,Cr3+,Cu2+。DNBF与不同的金属离子可以结合生成两种结构的Meisenheimer络合物。Sinditskii等[55]经研究后发现:结构式I中的金属离子与硝基氧原子通过离子键结合;结构式II中的金属离子与羟基氧原子通过共价键结合。

图16 4,6-二硝基苯并氧化呋咱盐的合成Fig.16 Synthesis of DNBF salt
KDNBF是一种低毒的绿色起爆药,被广泛应用于商业与军工领域,常与四氮烯混合使用,有时也配合二硝基重氮酚(DDNP)一起使用[56]。纯的KDNBF也可做为雷管火帽装药,或用于汽车的气体发生安全装置[57]。
3.4 7-羟基-4,6-二硝基苯并呋咱盐(DNP盐)
虽然KDNBF的撞击感度和摩擦感度与LTNR相当,但该化合物在217℃时会剧烈分解,分解温度远低于LTNR(分解温度280℃)[58]。因此,KDNBF在高温环境下无法替代LTNR。近年来,通过对KDNBF基团的稍许修饰,改进了其高温易分解这一特性,研发出一种新型呋咱盐类起爆药——DNP盐。
关于KDNP合成方法的报道较早,但一直以来,反应过程中的水分会以一种水合物的形式残留于产物中,致使该药剂不适于处理和装填入起爆装置[58]。2011年,Fronabarger等[59]提出了一种全新而简便的KDNP合成路线(图17):以3-溴苯甲醚做为初始原料,经过硝化反应生成3-溴-2,4,6-三硝基苯甲醚;该分子中的溴被叠氮基取代,在回流条件下生成KDNP。在回流过程中,相较于甲醇,沸点较高的碳酸二乙酯(DEC)做溶剂,更能缩短反应时间。

图17 KDNP的合成Fig.17 Synthesis of KDNP
从分子结构上来说,虽然DNP盐与DNBF盐非常相似,但氢原子位置的微小变化,使得DNP盐的苯并呋喃酮环体系具有芳香性,从而提高了KDNP相对于KDNBF的稳定性(KDNP的分解温度280℃,摩擦感度较LTNR钝感)[59]。KDNP由美国海军与承包商PSEMC联合开发,已在脉冲弹、热桥丝点火起爆系统中进行了多次测试[60]。2017年至2019年,国内学者合成了KDNP,并使用量子化学的计算方法对KDNP的爆轰性能进行了理论预测[61],随后按照国军标测试与评估了其感度性能与爆炸性能。结果表明:KDNP的感度性能和作用时间优于LTNR,是替代LTNR的理想选择。
4 结论与展望
绿色起爆药的合成过程中采用了诸多化学反应,如:叠氮类绿色起爆药常采用叠氮酸根与卤代底物的亲核取代反应制备;四唑类起爆药常通过Thiele合成法或Stollé合成法构建目标产物前体,随后进行基团修饰得到目标产物;呋咱类起爆药常通过脱氮反应与重排反应构建苯并呋咱环等方法进行合成。目前,国内外已成功合成了多种性能优良的新型绿色起爆药,有望替代传统的LTNR与LA。
不过,绿色起爆药的合成步骤较复杂,提纯难度较高。随着研究的逐步深入,成本低廉、制备过程安全稳定、生产规模化、高效化等成为目前合成绿色起爆药亟需解决的问题。另外,尽管一些新型绿色起爆药的性能在试验表征方面优于传统起爆药,但仍处于性能探索的初级阶段。因此,对于绿色起爆药的研究还需要从以下几个方面继续开展:
1)结合各类化学反应与试验仪器,改进与优化绿色起爆药的合成方法,保证其生产过程更加安全、高效;
2)探索绿色起爆药对于相关火工药剂(如点火药等)及火工品(如电起爆器等)的适应性与匹配性,进一步加强与扩大新型绿色起爆药的应用范围;
3)新型绿色起爆药的合成方法与合成工艺正在逐步趋于成熟,可通过对起爆药微观状态下分子构型、起爆机理等方面的探索与研究,进一步设计出性能更加优良的绿色起爆药。
综上所述,绿色起爆药有着良好的环境友好性及热稳定性,具备广阔的发展前景。在军事、民品等行业迅猛发展的同时,新型绿色起爆药的合成方法、性能研究及实际应用也即将成为国内外火工领域中的研究重点。

