靶向药物在HER2阳性乳腺癌患者化疗中的临床应用价值研究
李明 王涛 杨周


【摘要】 目的:研究靶向藥物在HER2阳性乳腺癌患者化疗中的临床应用价值。方法:纳入2012年
3月-2014年3月佳木斯市中心医院收治的60例HER2阳性乳腺癌患者作为研究对象,采取随机数字表法将患者分为观察组和对照组,每组30例。对照组行CEF新辅助化疗,观察组在此基础上联合应用曲妥珠单抗靶向治疗。分别在化疗前后检测两组患者外周血CK19 mRNA水平,记录两组患者治疗效果和不良反应,随访记录两组患者预后。结果:观察组与对照组化疗后4周疾病控制率分别为90.00%与66.67%,两组比较差异有统计学意义(P<0.05)。两组化疗不良反应严重程度比较,差异均无统计学意义(P>0.05)。化疗后,观察组外周血CK19 mRNA显著低于化疗前和对照组,差异均有统计学意义(P<0.05);不同疗效患者外周血CK19 mRNA水平比较,差异有统计学意义(P<0.05)。受试者工作曲线(ROC)分析显示,外周血CK19 mRNA水平判断疗效的AUC为0.816(P=0.003),灵敏度为0.8,特异度为0.6。观察组5年肿瘤无进展生存率显著高于对照组(P<0.05)。结论:曲妥珠单抗靶向药物用于HER2阳性乳腺癌患者有助于提高化疗效果,降低CK19 mRNA水平,提高5年肿瘤无进展生存率,另外监测外周血CK19 mRNA水平有助于判断治疗效果。
【关键词】 靶向药物 HER2阳性乳腺癌 化疗
The Clinical Application Research of Targeted Drugs in Chemotherapy of HER2 Positive Breast Cancer Patients/LI Ming, WANG Tao, YANG Zhou. //Medical Innovation of China, 2022, 19(08): 0-054
[Abstract] Objective: To study the clinical application value of targeted drugs in chemotherapy of HER2 positive breast cancer patients. Method: A total of 60 patients with positive HER2 breast cancer admitted to Jiamusi Central Hospital from March 2012 to March 2014 were included as the research objects, the patients were divided into observation group and control group by random number table method, with 30 patients in each group. The control group was treated with CEF neoadjuvant chemotherapy, and the observation group was treated with trastuzumab on the base of the control group. The levels of CK19 mRNA in peripheral blood of patients in the two groups before and after chemotherapy were detected, the treatment effect and adverse reactions of patients in the two groups were recorded, and the prognosis of patients in the two groups was recorded during follow-up. Result: The disease control rates of the observation group and the control group at 4 weeks after chemotherapy were 90.00% and 66.67%, respectively, the difference between the two groups was statistically significant (P<0.05). There were no significant differences in the severity of chemotherapy adverse reactions between the two groups (P>0.05). After chemotherapy, peripheral blood CK19 mRNA in the observation group was significantly lower than those before chemotherapy and in the control group, with statistical significances (P<0.05); there were statistically significant differences in the levels of CK19 mRNA in peripheral blood of patients with different therapeutic effects (P<0.05). The ROC analysis showed that the area under the curve (AUC) of CK19 mRNA was 0.816 (P=0.003), the sensitivity was 0.8, the specificity was 0.6. The progression-free survival rate at 5 years in observation group was significantly higher than that in control group (P<0.05). Conclusion: Trastuzumab targeted drugs for HER2 positive breast cancer patients can help to improve the effect of chemotherapy, reduce the level of CK19 mRNA, increase the progression free survival rate in 5 years, and monitor the level of CK19 mRNA in peripheral blood to help determine the therapeutic effect.
[Key words] Targeted drug HER2 positive breast cancer Chemotherapy effect
First-author’s address: Jiamusi Central Hospital, Heilongjiang Province, Jiamusi 154002, China
doi:10.3969/j.issn.1674-4985.2022.08.012
乳腺癌是妇科常见恶性肿瘤,随着经济水平提高和生活方式的改变,发病率逐步上升[1]。人类表皮生长因子受体2(human epidermal growth factor receptor 2,HER2)定位于染色体17q12-21原癌基因,通过增加细胞信号传导,刺激肿瘤组织增殖,有报道显示HER2阳性乳腺癌患者恶性程度更高[2]。化疗是乳腺癌患者重要治疗方法,既往报道证实术前新辅助化疗有助于降低患者临床分期,提高保乳率[3]。而靶向治疗作为近年来恶性肿瘤的新型治疗方案,逐渐引起临床重视。曲妥珠单抗是HER2特异性抑制剂,近年已有关于曲妥珠单抗用于HER2阳性乳腺癌的报道[4-5],但有关靶向药物的具体应用临床仍处于探索阶段,本研究纳入60例HER2阳性乳腺癌患者作为研究对象,探讨曲妥珠单抗靶向药物治疗效果及疗效预测指标,观察患者远期预后,为临床提供参考。现报道如下。
1 资料与方法
1.1 一般资料 纳入2012年3月-2014年3月佳木斯市中心医院收治的60例HER2阳性乳腺癌患者作为研究对象,(1)纳入标准:①均经穿刺病理活检证实为乳腺癌,免疫组化检测HER2蛋白表达阳性[6];②患者年龄>18岁。(2)排除标准:①对治疗药物过敏者;②妊娠哺乳期患者;③肝肾功能严重不全者;④已发生远处转移者。采用随机数字表法将60例患者分为观察组和对照组,每组30例。患者均知悉本研究内容,且签署知情同意书。本研究经医院伦理委员会批准。
1.2 方法 观察组:入院确诊后开始CEF新辅助化疗,第1天,静脉滴注环磷酰胺(生产厂家:山西普德药业股份有限公司,批准文号:国药准字H14023686,規格:0.2 g)600 mg/m2,静脉滴注阿霉素(生产厂家:海正辉瑞制药有限公司,批准文号:国药准字H33021980,规格:10 mg)60 mg/m2,静脉滴注5-氟尿嘧啶(生产厂家:南通精华制药股份有限公司,批准文号:国药准字H32022246,规格:10 mL︰0.25 g)500 mg/m2。每3周为1个周期,共治疗4个周期。第1天,静脉滴注曲妥珠单抗(生产厂家:上海罗氏制药有限公司,批准文号:国药准字J20110020,规格:440 mg︰20 mL),首剂量4 mg/kg,以后每周静滴1次,2 mg/kg,连续干预10周。对照组仅接受CEF新辅助化疗,方案同观察组。
1.3 观察指标与评价标准 (1)在化疗结束后4周参照实体瘤疗效标准评价疗效,完全缓解(complete remission,CR):目标病灶完全消失;部分缓解(partial remission,PR):基线病灶直径缩小≥30%;疾病稳定(stabilization disease,SD):基线病灶直径缩小未达到PR,增加未达到PD;疾病进展(progression disease,PD):病灶直径增加≥20%[7]。以(CR+PR+SD)/总例数×100%计算疾病控制率。(2)依据通用不良反应术语标准4.0版标准,记录化疗期间不良反应发生情况及严重程度[8]。(3)分别在化疗前(化疗开始前1 d)和化疗后(化疗后次日)采用实时定量逆转录-聚合酶链反应(quantitative real time-polymerase chain reaction,qRT-PCR)检测两组患者外周血角蛋白19(cytokeratin 19,CK19)mRNA水平,试剂盒由天根生化科技公司提供,操作按试剂盒说明进行。比较不同疗效患者外周血CK19 mRNA水平,分析外周血CK19 mRNA判断治疗效果的价值。(4)化疗结束后进入随访,每4周联系1次,在随访1年后,每3~6个月上门随访1次,记录两组患者5年肿瘤无进展生存率和总生存率。
1.4 统计学处理 选用SPSS 22.0软件对数据进行统计学分析,计量资料以(x±s)表示,组间比较行独立样本t检验,组内比较行配对t检验;计数资料以率(%)表示,组间比较行字2检验;外周血CK19 mRNA判断疗效采用受试者工作曲线(re-ceiver operative characteristic curve,ROC)分析。P<0.05为差异有统计学意义。
2 结果
2.1 两组基本资料比较 两组患者基本资料比较,差异均无统计学意义(P>0.05),具有可比性,见表1。
2.2 两组化疗效果比较 观察组化疗后4周疾病控制率为90.00%,显著高于对照组的66.67%,差异有统计学意义(字2=4.812,P=0.028),见表2。
2.3 两组化疗不良反应比较 两组化疗期间消化道反应、骨髓抑制、血小板降低及红细胞减少等不良反应严重程度比较,差异均无统计学意义(P>0.05),见表3。
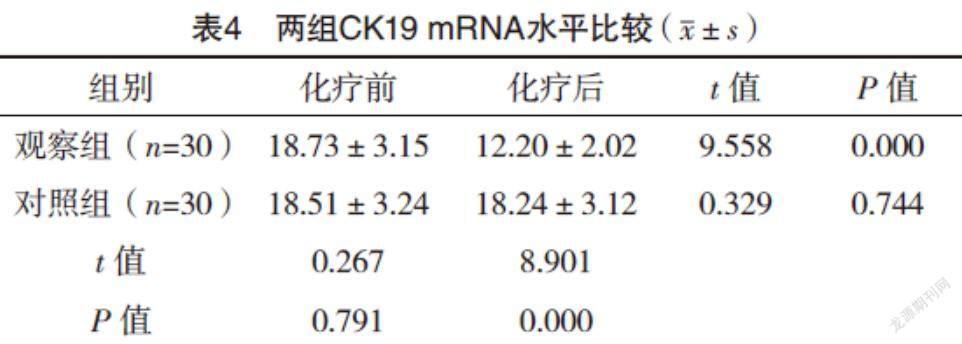
2.4 两组CK19 mRNA水平比较 化疗前,两组外周血CK19 mRNA水平比较,差异无统计学意义(P>0.05);化疗后,观察组外周血CK19 mRNA显著低于化疗前和对照组,差异均有统计学意义(P<0.05)。见表4。观察组中,2例CR,化疗后CK19 mRNA水平为(10.12±1.43),13例PR,CK19 mRNA水平(12.04±1.55),12例SD,CK19 mRNA水平(12.52±1.07),3例PD,CK19 mRNA水平(13.47±1.28)。不同疗效患者CK19 mRNA水平比较,差异有统计学意义(F=8.163,P=0.000)。
2.5 CK19 mRNA水平判断疗效价值分析 以是否达到总缓解(CR+PR)为状态变量,以外周血CK19 mRNA為检验变量,绘制ROC曲线,结果显示其AUC为0.816[95%CI(0.656,0.976),P=0.003],灵敏度为0.8,特异度为0.6,最佳截断值为11.261,见图1。
2.6 两组随访和预后比较 观察组随访期间失访1例,对照组无失访病例,观察组5年肿瘤无进展生存率为58.62%(17/29),显著高于对照组20.00%(6/30)(字2=9.247,P=0.002)。观察组5年总生存率79.31%(23/29),对照组为76.67%(23/30),两组5年生存率比较,差异无统计学意义(字2=0.060,P=0.807)。
3 讨论
乳腺癌以乳腺上皮细胞不典型增生为特点,增长和浸润速度快,新辅助化疗可杀灭肿瘤微转移灶,缩小肿瘤体积,降低肿瘤分期,从而提高保乳率,已在临床普遍开展[9-10],因而本研究以新辅助化疗为基础对照组。靶向治疗是以肿瘤特异性基因或基因表达产物为作用靶点,具有副作用小、特异性高的特点,HER2属血管内皮生长因子,可通过激活下游mTOR和PI3K/Akt信号通路,促进肿瘤细胞增殖和血管生长,增加肿瘤恶性程度[11-12]。因而,对于HER2阳性乳腺癌患者,通过抗HER2靶向药物干预可降低肿瘤侵袭性,改善患者预后。
曲妥珠单抗是国内首个针对HER2人源化单克隆抗体靶向药物,它将曲妥珠单克隆抗体与美登素类衍生物偶联[13],增强抗肿瘤活性,提高疗效。国外大规模临床研究还显示曲妥珠单抗能显著降低乳腺癌复发风险[14-15],本研究也显示观察组化疗效果及5年肿瘤无进展生存率高于对照组。
CK19属上皮特异性分布蛋白质,既往报道显示CK19与肿瘤微血管数量呈显著相关性,CK19是判断乳腺癌肿瘤微血管转移的良好指标[16]。本研究发现化疗后,观察组外周血CK19 mRNA水平显著低于化疗前(P<0.05),提示曲妥珠单抗靶向治疗可通过降低外周血CK19 mRNA水平,抑制肿瘤血管生长,诱导肿瘤细胞凋亡,这可能是其提高疗效的途径之一[17]。研究结果还显示不同疗效患者CK19 mRNA水平比较,差异有统计学意义(P<0.05),为进一步探讨CK19 mRNA在曲妥珠单抗靶向治疗中的作用,本研究将治疗后达到CR与PR患者作为观察对象分组,进行ROC分析,结果显示CK19 mRNA判断疗效的灵敏度达0.8,说明通过监测外周血CK19 mRNA水平有助于预测曲妥珠单抗靶向治疗效果,这可为下一步手术或其他治疗提供依据。
综上所述,曲妥珠单抗靶向治疗用于HER2阳性乳腺癌疗效确切,不良反应无明显增加,可降低CK19 mRNA水平,延长5年肿瘤无进展生存率,另外监测外周血CK19 mRNA水平有助于判断疗效,为临床提供依据。
参考文献
[1]曹明丽.基于分子分型的乳腺癌流行病学新认识[J].中国肿瘤临床,2017,44(9):449-451.
[2]张艳秋,王昳凡,王简.HER-2阳性乳腺癌的新辅助治疗现状及展望[J].临床肿瘤学杂志,2017,22(3):264-271.
[3] SWISHER S K,VILA J,TUCKER S L,et al.Locoregional control according to breast cancer subtype and response to neoadjuvant chemotherapy in breast cancer patients undergoing breast-conserving therapy[J].Ann Surg Oncol,2016,23(3):749-756.
[4]李洪涛,裴效瑞,窦宗山,等.曲妥珠单抗融合UL16结合蛋白2激活自然杀伤细胞治疗乳腺癌[J].中华实验外科杂志,2018,35(1):61-64.
[5] BEITSCH P,WHITWORTH P,BARON P,et al.Pertuzumab/Trastuzumab/CT versus trastuzumab/CT therapy for HER2+ breast cancer: results from the prospective neoadjuvant breast registry symphony trial (NBRST)[J].Ann Surg Oncol,2017,24(3):2539-2546.
[6] EDGE S B.AJCC cancer staging manual[J].Jama-J Am Med Assoc,2010,304(15):1726-1727.
[7]杨学宁,吴一龙.实体瘤治疗疗效评价标准—RECIST[J].循证医学,2004,4(2):85-90.
[8]皋文君,刘砚燕,袁长蓉.国际肿瘤化疗药物不良反应评价系统——通用不良反应术语标准4.0版[J].肿瘤,2012,32(2):142-144.
[9]阮思妮,胡亚飞.彩色多普勒超声在乳腺癌患者新辅助化疗疗效评估中的应用价值[J].医学临床研究,2018,35(3):504-507.
[10] WEISS A,BASHOUR S I,HESS K,et al.Effect of neoadjuvant chemotherapy regimen on relapse-free survival among patients with breast cancer achieving a pathologic complete response: an early step in the de-escalation of neoadjuvant chemotherapy[J].Breast Cancer Res,2018,20(1):27-30.
[11]陈静瑶,周杰,李飞,等.飞燕草素通过AKT/mTOR通路诱导HER-2+乳腺癌细胞自噬[J].中南大学学报(医学版),2017,42(3):264-270.
[12]刘娟妮,李俊海,白国栋,等.PI3K/AKT信号通路相关蛋白在乳腺癌中的表达及其临床意义[J].癌症进展,2016,14(5):438-440.
[13]耿凤勇,金克敏.曲妥珠单抗联合新辅助化疗对乳腺癌患者术后临床疗效及相关指标的影响[J].中国药房,2017,28(11):1532-1534.
[14] VESCI L,CAROLLO V,ROSCILLI G,et al.Trastuzumab and docetaxel in a preclinical organotypic breast cancer model using tissue slices from mammary fat pad: Translational relevance[J].Oncol Rep,2015,34(3):1146-1152.
[15]崔剑锋.曲妥珠单抗联合长春瑞滨治疗HER-2阳性晚期乳腺癌患者的疗效分析[J].实用药物与临床,2017,20(7):759-762.
[16]孙凯,孙松,胡恩伟,等.联合CK19、hMAM、SBEM检测乳腺癌外周血循环肿瘤细胞及其与分子分型和临床病理特征的相关性分析[J].临床和实验医学杂志,2018,17(3):270-273.
[17]吕勉,潘小明,王慧玲,等.循环肿瘤细胞数量的变化情况对HER2阳性早期乳腺癌患者治疗效果及预后的影响[J].癌症进展,2019,17(14):1659-1664.
(收稿日期:2021-09-03) (本文编辑:张爽)

