e-ATRP水相制备温度响应高分子微凝胶
——有关高分子微凝胶的新实验设计与实践
张来英,康玮,徐浩金,赵浩博,王蔷薇,吴伟泰
厦门大学化学化工学院,福建 厦门 361005
实验教学是化学类专业本科教学中不可或缺的部分,不仅有助于加深学生对化学理论知识的理解,还可以培养学生学以致用和动手实践的能力。随着新时代科技创新人才培养的深化推进,学生在掌握基础化学理论知识、具备基本动手实践能力的同时,更需要紧跟科研前沿和社会高质量发展需求,养成学科交叉融合思维和环保意识,锻炼科技创新实践能力。
高分子化学本科教学中已涉及原子转移自由基聚合(Atom Transfer Radical Polymerization,ATRP)等可控/活性聚合概念,但是并未深入挖掘,较欠缺相关实验[1-5]。ATRP是目前最重要的可控/活性聚合方法之一[6,7],广泛用于高分子结构设计以及功能高分子材料的合成,例如刺激响应高分子(也称智能高分子)微凝胶的聚合制备[8]。高分子微凝胶兼具高分子、凝胶和胶体性质,在食品、生物医药等方面得到广泛应用,赋予其智能响应特性是前沿热点之一,在生物传感器、物质运输等领域具有很好的应用前景。ATRP方法用于合成刺激响应高分子微凝胶,可实现对结构、粒径等的可控,已成为相关领域研究常用方法。鉴于ATRP主要利用铜离子价态转变来催化反应的进行,其中还原剂被氧化后会生成副产物,研究者发展了电化学原子转移自由基聚合(Electrochemical Atom Transfer Polymerization,e-ATRP),即用电子代替还原剂来控制聚合反应[9,10]。相较于一般ATRP方法,e-ATRP所需金属催化剂可低至10-6级别,在降低成本的同时更绿色环保,还可通过改变电流、电位等来控制反应,大大提高了反应的可控性。
基于此,笔者结合自身多年从事高分子化学教学和科研的经历[11],以大学生创新实验为背景,设计了e-ATRP水相制备刺激响应高分子微凝胶的基础实验。本实验选取温度响应高分子作为实验体系,以研究起步较早、受广泛关注且较深入已有较多验证的温度响应微凝胶作为具体实验对象,在一定程度上反映可控/活性聚合、电合成、刺激响应高分子等知识。本实验结合了前沿性、综合性和环保性等特点,且便于操作,提供常用实验方法的基础训练,可为学生深入相关领域学习和研究奠定基础。在教学过程中,还结合曾在厦门大学任教的钱人元先生擅长开拓边缘学科新领域等事迹,以及厦门大学在电化学服务国家重要需求等方面的事例,深入挖掘身边的思政元素,潜移默化地影响学生,激发学生科技报国的家国情怀和使命担当,实现价值引领和知识传授的同频共振。
1 实验目的
(1)学习和掌握高分子化学知识,理解可控/活性聚合的操作过程;
(2)掌握电合成方法;
(3)了解紫外-可见分光光度计和动态激光光散射法在高分子研究中的运用。
2 实验原理
2.1 ATRP原理
ATRP方法以有机卤化物为引发剂、卤化亚铜和有机配体形成的络合物为催化剂,通过引发剂与CuI-L+反应得到自由基R·,进而引发聚合反应得到链自由基R-M·,同时生成X-CuIIL+;链自由基R-M·也可以与X-CuIIL+发生链终止反应得到R-M-X与CuI-L+。整个反应过程中,活性种R-M·与休眠种R-M-X之间的相互转化始终存在,而CuI-L+和X-CuIIL+之间的可逆转化有效降低了活性种R-M·的浓度,从而实现可控/活性聚合(如图1所示)[1]。
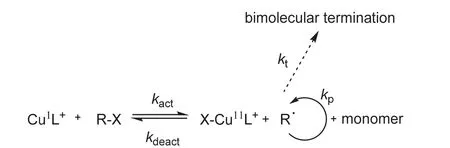
图1 传统ATRP聚合机理示意图
但上述方法存在一系列的问题:反应中需保持CuI-L+一定浓度,需在无氧体系中进行,需较大量的催化剂。为了解决这些问题,Krzysztof Matyjaszewski课题组提出了一种改良方法AGET-ATRP。相较于传统ATRP,其创新之处在于向体系中间歇性地加入了过量还原剂不断还原X-CuIIL+生成CuI-L+,有效降低了催化剂的使用量,使得反应可以在少量氧气存在的体系之中进行。然而,AGET-ATRP过程中,还原剂被氧化后会生成副产物,可能对聚合物性能有不良影响,也无法对聚合过程实时控制。
2011年,Krzysztof Matyjaszewski课题组基于AGET-ATRP,提出了一种全新的ATRP方法,即e-ATRP (图2)[8]。e-ATRP方法使用电子尤其是电流代替还原剂,通过电化学反应将在空气中较为稳定的X-CuIIL+还原成CuIL+来进行ATRP控制聚合反应。相较于一般ATRP方法,e-ATRP具有聚合速率可控性更好、催化剂用量更低、无需还原剂、更加环保等优点。在此工作的基础之上,Krzysztof Matyjaszewski课题组进一步发展了可用于水相合成的e-ATRP方法[9]。
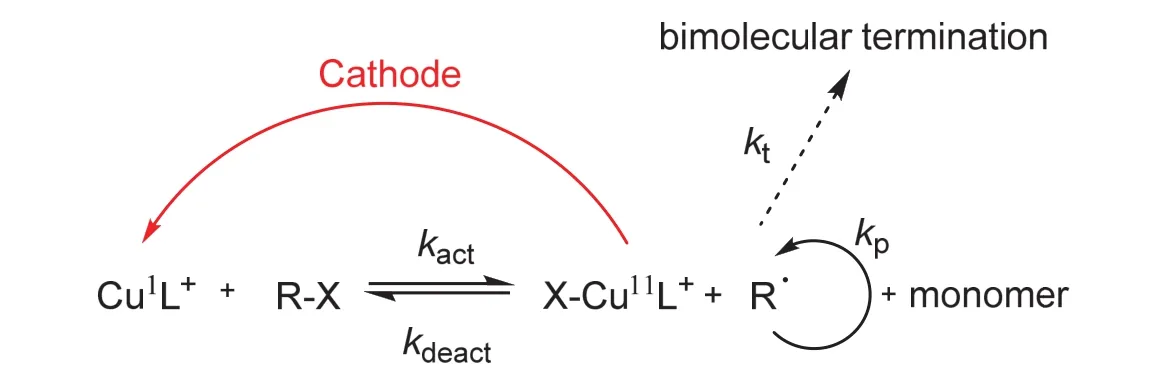
图2 e-ATRP聚合机理示意图
2.2 合成原理
本实验基于水相e-ATRP体系,以EO2为单体、PEGDMA为交联剂,采用电化学方法,在水相体系中一锅制备一种具有温度响应的高分子微凝胶,反应机理如图3所示。Cu(I)的配合物与EO2反应生成自由基,自身被氧化为Cu(II)。之后自由基引发链增长过程,同时与交联剂PEGDMA发生交联反应,形成交联的高分子微凝胶。同时,Cu(II)的配合物在阴极上发生还原反应,重新回到Cu(I)继续产生自由基。以α-溴苯乙酸乙酯为引发剂,通过其与[CuI(Me6TREN)]+的反应得到自由基引发聚合反应,生成[CuII(Me6TREN)]+。在整个反应过程中,[CuI(Me6TREN)]+与[CuII(Me6TREN)]+之间的相互转化始终存在,有效降低了活性中心-自由基的浓度,同时通过电化学还原[CuII(Me6TREN)]+的方法保证[CuI(Me6TREN)]+始终保持在一定浓度,减少了催化剂的使用。
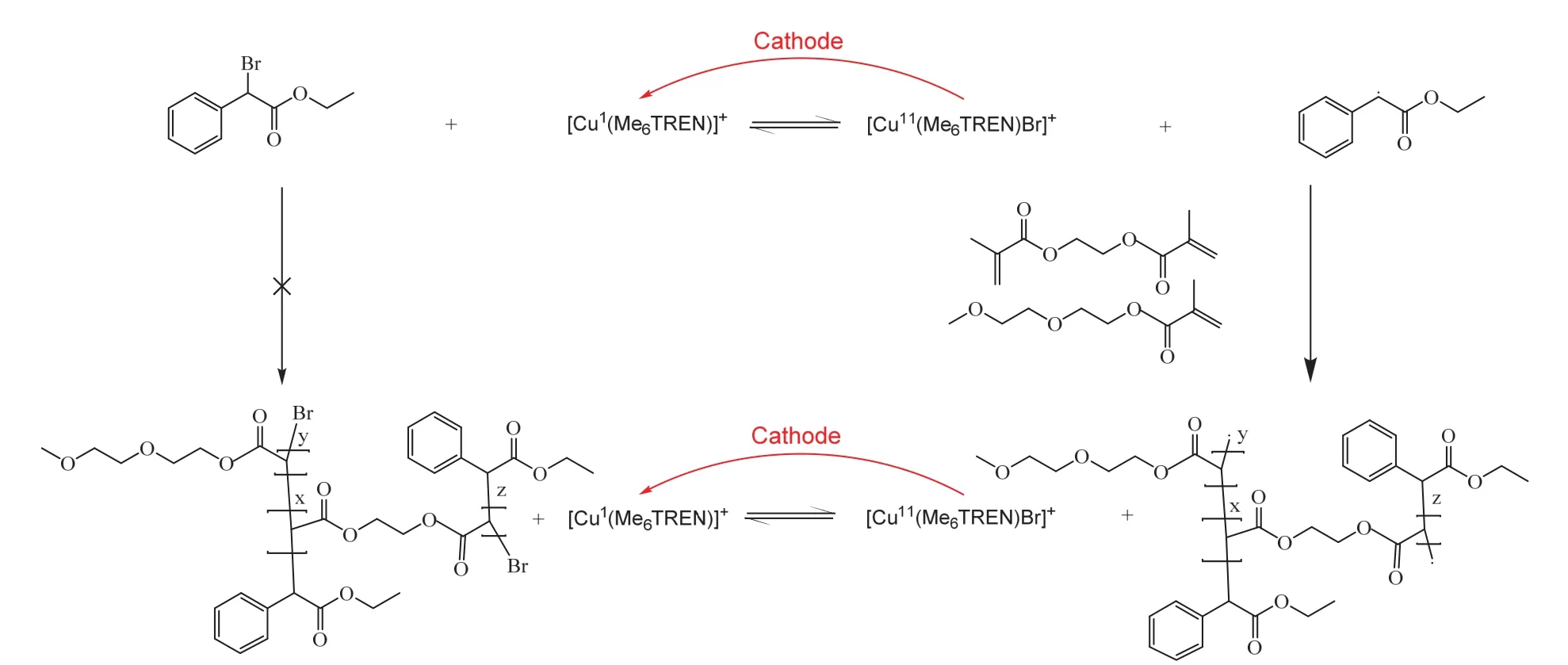
图3 本实验反应机理图
3 实验仪器和试剂
3.1 实验仪器
铂片电极、银/氯化银电极、铂丝电极;分析天平、磁力搅拌器、磁子;标准磨口四颈瓶(100 mL/19#mm × 4)、橡皮塞、封口膜、4个10 mL容量瓶、1个50 mL容量瓶、3个25 mL小烧杯、大烧杯、移液枪、滴管若干。
电化学工作站(上海辰华仪器有限公司),紫外-可见分光光度计(Thermo Sxientific公司,Multiskan GO全波长酶标仪);动态激光光散射仪器(BI-200SM, Brookhaven公司)。
3.2 实验试剂
2-甲基-2-丙烯酸-2-(2-甲氧基乙氧基)乙酯(EO2,Aldrich),聚乙二醇二甲基丙烯酸酯(PEGDMA,Aladdin),溴化铜(ALFA),三(2-二甲氨基乙基)胺(Me6TREN,迈瑞尔),α-溴苯乙酸乙酯(毕得医药),溴化钾(ALFA),N,N-二甲基甲酰胺(DMF,国药集团药业股份有限公司),试剂纯度均为分析纯。
4 实验步骤
4.1 电极反应液的配制
(1)聚乙二醇二甲基丙烯酸酯溶液:用移液枪移取90 μL PEGDMA于10 mL容量瓶中,加入纯水定容至刻度线,贴上标签注明①;
(2) Cu2+/Me6TREN溶液:称取22.3 mg溴化铜于25 mL小烧杯中,加入少量纯水搅拌溶解,再加入30 μL Me6TREN,搅拌,转移到10 mL容量瓶中,洗涤2-3次,将洗涤液并入容量瓶中,加入纯水定容至刻度线,贴上标签注明②;
(3) α-溴苯乙酸乙酯DMF溶液:用移液枪移取36 μL α-溴苯乙酸乙酯于10 mL容量瓶中,加入DMF定容至刻度线,贴上标签注明③;
(4)溴化钾溶液:称取595 mg溴化钾于25 mL小烧杯中,加入少量纯水搅拌溶解,转移到10 mL容量瓶中,洗涤2-3次,将洗涤液并入容量瓶中,加入纯水定容至刻度线,贴上标签注明④;
(5)反应液:用移液枪移取185 μL EO2于50 mL 容量瓶中,再加入1.0 mL ①溶液,1.0 mL ②溶液,0.5 mL ③溶液和20 μL ④溶液,加入纯水定容至刻度线,摇匀备用。
上述(1)-(4)待用反应液如图4所示。

图4 待用溶液图
4.2 电极处理、装置搭建和电化学反应
(1)铂电极的预处理:将铂电极置于热的(1 + 1) HNO3中浸泡,再用纯水冲洗干净,滤纸吸干备用;
(2)用纯水冲洗参比电极和对电极,滤纸吸干备用;
(3)按照反应装置图(图5)接好仪器:在洗净干燥的四口瓶中,加入配制好的反应液约25-30 mL,放入搅拌磁子,分别插入洗净的铂片电极(工作电极)、银/氯化银电极(参比电极)和对电极(注意:反应液要没过电极,搅拌磁子不能和电极碰撞),用封口膜缠紧三个电极对应的瓶口;
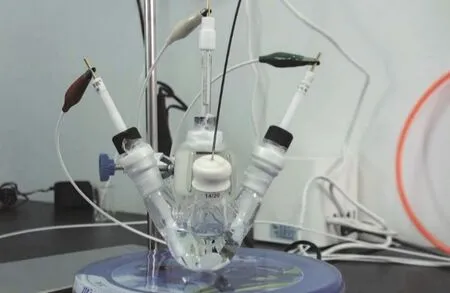
图5 反应装置图
(4)在四口瓶的剩余一口上装上橡皮塞,取一长针头插入反应液,针头另一端连接气路,先打开氮气钢瓶阀门,再缓慢打开气路阀门,控制气流大小为正常鼓泡,通氮气30 min;
(5)打开电化学工作站,检测设备是否正常,接好电极与相应导线,进行循环伏安法测试(CV),确定合适的反应电压;
(6)设定反应电压为-0.5 V,开始反应,持续电解1 h。反应结束,抽出通气针头,关闭气阀和气瓶,拆除导线和电极,倒出反应液备用。
4.3 表征和测试
(1)干净的样品瓶中,加入微凝胶分散液0.5 mL和纯水20.0 mL,使用涡旋振荡器分散5 min,然后静置0.5 h。
(2)用紫外-可见分光光度计测量不同温度下微凝胶稀溶液的吸光度。
(3)用干净的玻璃针筒注射器和针头式过滤器,过滤、除尘。用动态激光光散射仪测量不同温度下微凝胶的尺寸和粒径分布。
5 结果与讨论
5.1 吸光度测试
用紫外-可见分光光度计测试微凝胶稀溶液对400 nm波长处光的吸收值,数据详见表1。
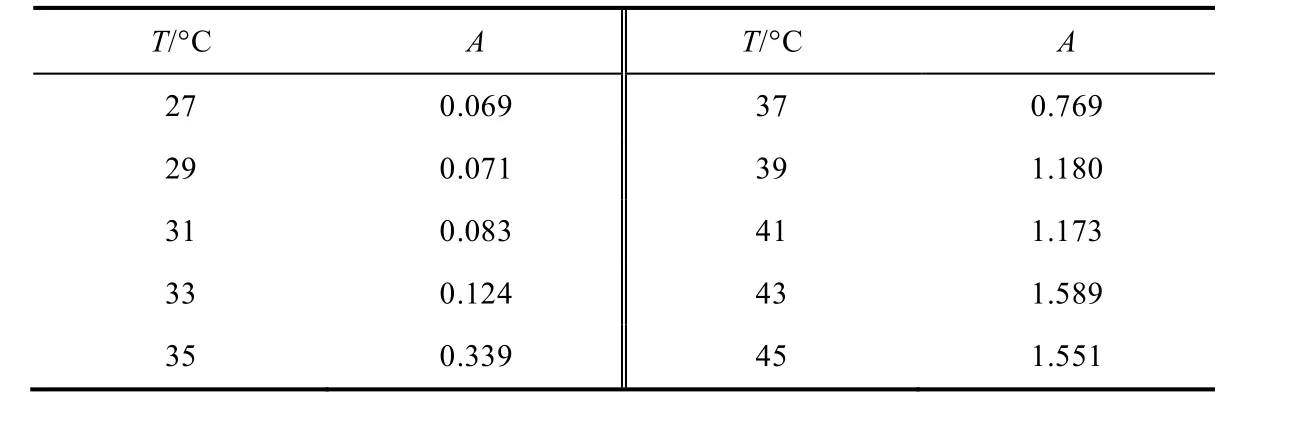
表1 不同温度下微凝胶稀溶液对400 nm波长处光的吸收值
从不同温度下微凝胶稀溶液对400 nm波长处光的吸光度的结果(图6)可以看出:随着温度的升高,吸光度先上升后趋于平稳。这代表溶质微凝胶的密度随温度上升逐渐增大随后基本保持不变。对400 nm吸光度-温度曲线进行求导并再次拟合,得到相转变温度应为37.02 °C。

图6 微凝胶溶液对400 nm波长光吸光度-温度图(左)及其一阶导数图(右)
5.2 动态激光光散射仪测试
如图7所示,随着温度上升,S型曲线整体向下偏移,代表微凝胶的水合粒径随着温度上升而逐渐下降,随后基本保持平稳,与吸光度测定结果一致。
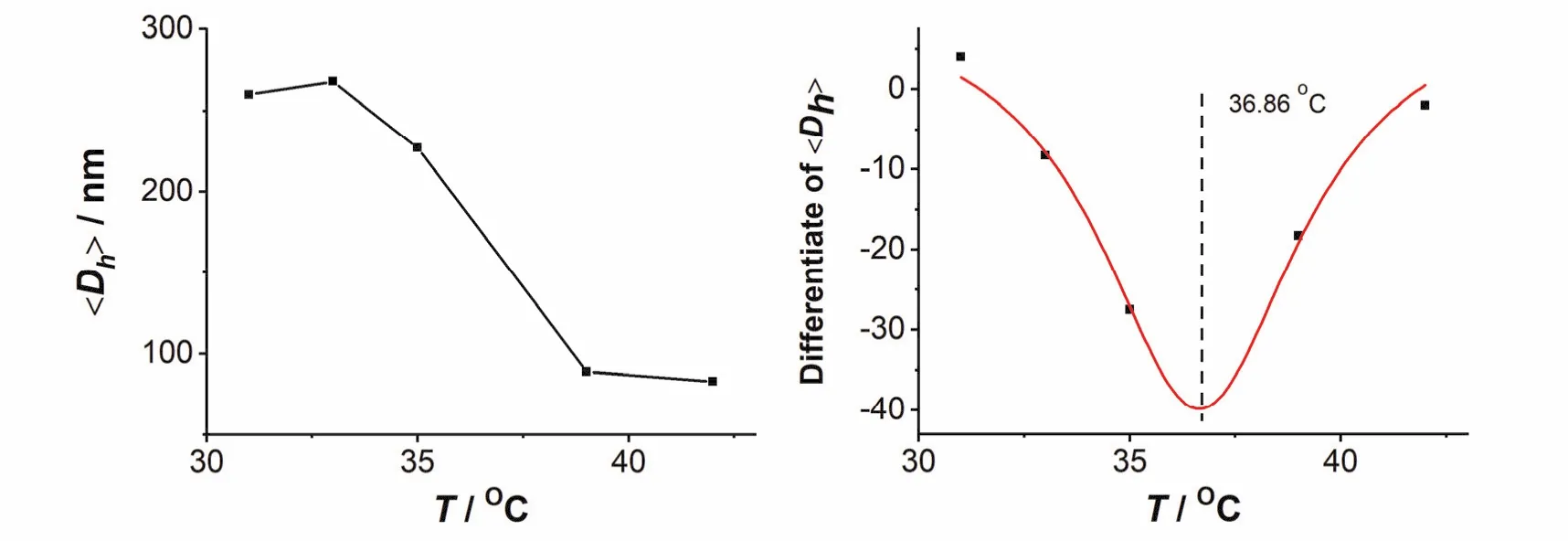
图7 不同温度下微凝胶的自相关函数(归一化)变化图(左)及其局部放大图(右)
上述分析结果在图8之中得到了印证,实验进一步对粒径<Dh>求导后进行拟合,得到相转变温度为36.86 °C。这一结果与前述吸光度测试结果相一致。
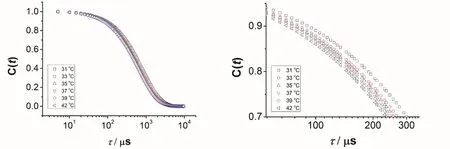
图8 不同温度下微凝胶的水合粒径图(左)及其一阶导数图(右)
综合上述分析结果,可以得出以下结论:在较低温度下,随着温度的升高,一开始粒径基本没有变化,聚合物链与水之间存在较强的氢键,微凝胶处于较好的溶胀状态;当温度进一步提高以后,聚合物链与水之间的氢键逐渐被破坏,聚合物链与聚合物链之间的疏水相互作用逐渐成为主导,使微凝胶发生收缩,微凝胶的粒径变小,即微凝胶发生体积相转变,直至达到新的平衡。
6 思考题
(1)在ATRP可控/活性聚合方法中,还原剂的选择原则是什么?
(2)化学合成实验之前,为什么要确定合适的反应电压?简述电压的选取原则。
(3)简述e-ATRP如何使用电化学技术控制聚合反应。还有哪些电化学技术可以用于控制反应?
(4)在ATRP可控/活性聚合方法中,所使用的金属催化剂是否会污染最终样品?如果你认为会,如何从根本上解决金属催化剂带来的不利影响。
(5)结合之前学习的化学知识,本实验可以拓展到其他哪些高分子的合成?
7 实验组织运行建议
本实验一共5学时左右,其中制备2学时、表征3学时,学生单人单套操作,可以作为基础实验引入。本实验涵盖高分子化学、电合成与仪器分析等领域,较适合高年级本科生在修读完高分子化学、物理化学、分析化学等课程后开展,并可从以下多方面对学生知识、素质和能力展开训练:
(1)在实验之前,指导学生通过查阅相关文献了解实验和仪器相关原理和步骤等,做好预习工作,培养学生的自主学习意识及文献检索阅读能力。
(2)在实验开展之初,将可控/活性聚合、电合成、刺激响应高分子等领域的最新科研成果及发展方向引入课程背景介绍,拓展学生视野,激发学生的科研兴趣。
(3)合成过程不仅可以帮助学生巩固可控/活性聚合、电合成、刺激响应高分子等化学理论知识,使学生理解各学科之间的内在联系,构建连贯的知识体系,培养学科交叉融合思维,同时提供常用实验方法的基础训练,掌握电合成装置等常规科研设备的使用,提升学生的科研素养。
(4)温度响应特性的表征过程可以帮助学生熟悉紫外-可见分光光度计和动态光散射仪等科研仪器的原理及数据分析过程,培养学生理论联系实验、学以致用的创新思维。
(5)在数据整理及实验报告撰写过程中,要求学生运用所学的相关基础知识解释实验现象,了解科研基本思路和方法,为学生深入相关领域学习和研究奠定基础。
本实验是厦门大学化学化工学院综合化学实验“温度响应高分子微凝胶的水相制备与表征”[11]的并行实验之一。以后者为主的实验,自2012年以来已经运行10轮,实验开设初衷是为“拔尖计划”大三学生提供必修实验训练,授课形式为实验研讨课:实验前讲授实验方法、原理和实验技术等相关知识和要求,实验过程中即时研讨实验现象。此外,该实验[11]合成侧重传统自由基聚合;与此不同,本实验合成聚焦可控/活性聚合、电合成。
8 结语
可控/活性聚合是高分子合成最重要的方法之一,已成为相关领域研究常用方法。高分子化学本科教学中已涉及ATRP等可控/活性聚合概念,但是并未深入挖掘,也较欠缺相关实验。基于此,我们设计了e-ATRP水相制备刺激响应高分子微凝胶的基础实验,选取温度响应高分子作为实验体系,以研究起步较早、受广泛关注且较深入而已有较多验证的温度响应微凝胶作为具体实验对象,并在一定程度上反映可控/活性聚合、电合成、刺激响应高分子等知识。本实验涉及高分子化学、电合成与仪器分析等领域,涵盖面较广,有助于学生在深化理解相关理论知识和增强动手实践能力的同时,初步感受科研魅力,开阔视野与科研前沿接轨,强化综合运用知识能力,培养学科交叉融合思维和环保意识,锻炼创新实践能力,为将来学习深造、解决实际问题奠定基础。
本实验采用电合成装置在水相中进行微量合成,简便易行,绿色环保、安全可靠并且成本较低。本实验具有较好普适性和较强的可设计性,允许拓展其他高分子的合成,也可在现有基础上进一步尝试各种电化学技术,因而适合于不同院校根据实际情况开展相关教学工作。

