前列腺中央腺体癌磁共振检查ADC值对定性判断及癌灶风险程度的预测价值
赵 雪 张明辉
1.北京怀柔医院医学影像科 (北京 101400)
2.临沂市人民医院影像科(山东 临沂 276002)
前列腺癌是男性常见、多发疾病[1],患病年龄多在50岁以上。目前关于前列腺癌发生机制尚未完全明确[2],可能与遗传、雄激素分泌异常等有关。前列腺癌分为腺癌、导管腺癌、尿路上皮癌、腺鳞癌等[3]。早期前列腺癌临床症状不典型,缺少特性。中晚期前列腺癌发展较快,严重影响患者生活质量。前列腺中央腺体癌是前列腺癌主要类型之一,大部分确诊时已是中晚期,错失最佳治疗时机[4]。及早诊断前列腺中央腺体癌在指导治疗、提升预后上均有价值。磁共振弥散加权成像临床较常用,在诊断恶性肿瘤占位情况上有优势[5]。本研究选取医院2017年1月至2019年6月收治的前列腺中央腺体癌患者,依据相关诊断标准,采用磁共振弥散加权成像检查,分析ADC值,为临床治疗提供可靠依据。
1 资料与方法
1.1 一般资料 选取医院2017年1月至2019年6月收治的前列腺中央腺体癌患者60例,年龄41~69岁,平均年龄(59.14±7.28)岁,病程1~37个月,平均病程(22.69±1.79)个月。分化程度:高分化14例、中分化20例、低分化26例。肿瘤直径:1cm~5cm47例,6cm~10cm10例,>10cm3例。临床分期:T1期31例、T2期7例、T3期7例、T4期15例。转移类型:淋巴结转移19例、骨转移23例、未转移18例。诊断标准[6]:参考WHO制定的前列腺中央腺体癌相关标准。
纳入标准:知情同意;自愿参加;接受手术治疗;手术病理确诊。排除标准:合并其他前列腺疾病患者;合并严重性基础疾病患者;粒子植入术治疗的患者;手术禁忌证患者。
1.2 方法 所有患者接受磁共振弥散加权成像检查,仪器是飞利浦3.0T磁共振检查仪,基本组成部分有磁体、诊断床、系统电源柜、操作台。使用体部线圈检查,先进行常规扫描,包括T1WI、FSE、T2WI、DWI。DEI成像为自旋平面回波成像序列,扫描范围是前列腺与精囊平面,获取其弥散敏感系数b值。T1WI射频重复时间为517ms,射频回波时间7.3ms,参数视野36mm×36cm,矩阵288mm×192mm,层厚4mm。FSE射频重复时间为4500ms,射频回波时间111.9ms,参数视野36mm×36cm,矩阵288mm×192mm,层厚4mm。T2WI射频重复时间为3300ms,射频回波时间111.9ms,参数视野32mm×32cm,矩阵288mm×192mm,层厚4mm。DWI射频重复时间为4000ms,射频回波时间87ms,参数视野32mm×32cm,矩阵140mm×140mm,层厚3.5mm。以上指标激励次数均为2。随访6个月,统计患者预后情况。
1.3 图像处理 所有图像传送至电脑工作站,自动生成诊断图片后由2位专业影像学医生测量感兴趣区ADC值,选取平均值。诊断时要尽可能避开患者前列腺周围血管、脂肪等组织,感兴区为4~20个,测量范围40~3020mm2,记录肿瘤情况,判断分期及分化,记录ADC值。
1.4 统计学方法 本文全部数据资料均使用SPSS 27.00软件分析,前列腺中央腺体癌患者的年龄、ADC值以(±s)形式表示,采用t检验。患者的分期、分化情况等计数资料使用(%)表示,采用χ2检验,以P<0.05表示比较结果差异有统计学意义。
2 结 果
2.1 前列腺中央腺体癌预后分析 随访6个月,60例患者中有14例(23.33%)预后不良,46例(76.67%)预后较佳。不良预后的患者中复发患者7例(50.00%)、转移患者4例(28.57%)、死亡患者2例(14.29%),复发伴远处转移1例(7.14%)。
2.2 不同预后患者的ADC值结果比较 预后较佳的患者的中央腺体区ADC值低于不良预后患者(P<0.05),见表1。
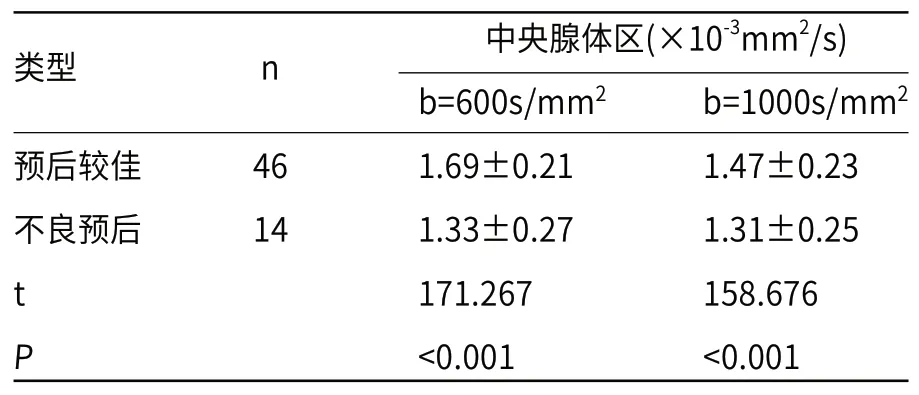
表1 不同预后患者的ADC值结果比较
2.3 磁共振弥散加权成像诊断分化与病理结果比较 磁共振弥散加权成像诊断高分化、中分化、低分化结果与病理结果符合情况分别是10例、18例、23例。将3例高分化患者误诊为中分化,1例误诊为低分化;2例中分化误诊为低分化,1例低分化误诊为高分化、2例低分化误诊为中分化。高分化、中分化、低分化符合率及误诊率差异比较有统计学意义(P<0.05),见表2。
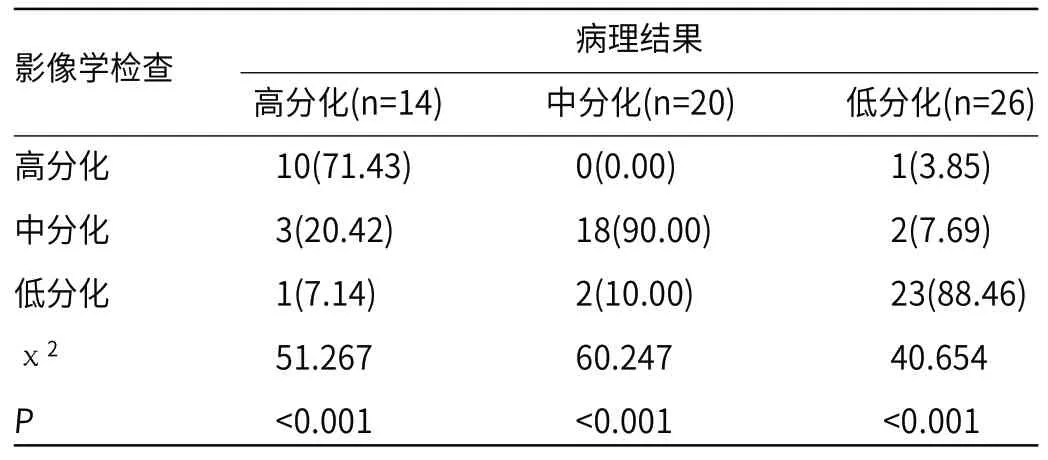
表2 磁共振弥散加权成像诊断分化与病理结果比较[n(%)]
2.4 磁共振弥散加权成像诊断分化与病理结果比较 磁共振弥散加权成像诊断T1期、T2期、T3期、T4期结果与病理结果符合情况分别是27例、6例、4例、3例。磁共振弥散加权成像将2例T1期患者误诊为T2期,1例误诊为T3期,1例误诊为T4期;1例T2期误诊为T1期;2例T3期误诊为T2期,1例T3期误诊为T4期;1例T4期误诊为T1期,1误诊为T3期;不同分期符合率及误诊率差异比较有统计学意义(P<0.05),见表3。
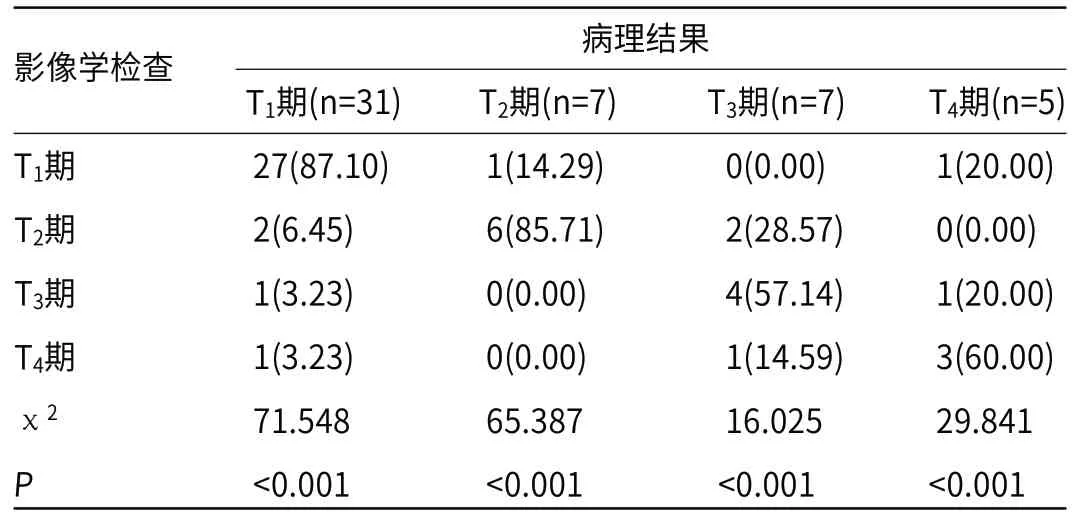
表3 磁共振弥散加权成像诊断分化与病理结果比较[n(%)]
2.5 磁共振弥散加权成像ADC值对前列腺中央腺体癌灶风险程度预测价值 分析发现,ADC值在b值为600s/mm2时敏感度为0.711、特异度为0.714、标准误为0.0079、P<0.001、95%CI=0.577~0.0885、曲线下面积=0.731;ADC值在b值为1000s/mm2时敏感度为0.934、特异度为0.643、标准误为0.063、P<0.001、95%CI=0.721~0.969、曲线下面积=0.845,见表4及图1。
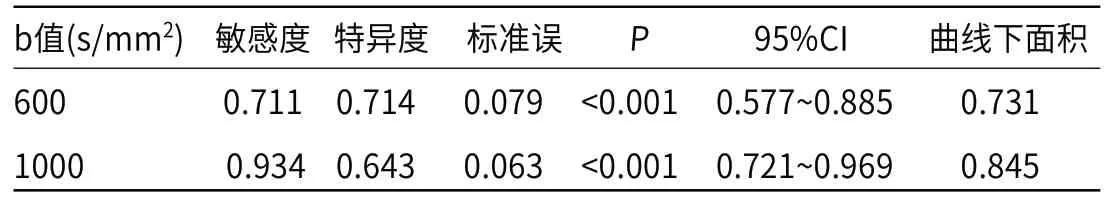
表4 磁共振弥散加权成像ADC值对前列腺中央腺体癌灶风险程度预测价值

图1 预测价值图
2.6 特征分析 前列腺中央腺体癌灶:T2WI序列为低信号,T1WI序列为等信号,较小时不易与前列腺增生鉴别,DWI序列与ADC图有助于鉴别诊断,DWI序列上清晰可见病灶位置,呈高信号,ADC图像为低信号(图2~图5)。
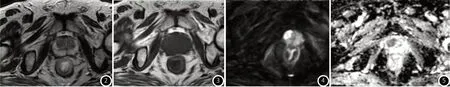
图2 T2WI结节呈低信号。图3 T1WI呈等信号。图4 DWI呈高信号。图5 ADC值明显减低。
3 讨 论
前列腺中央腺体癌是前列腺癌中较常见的类型[7],占前列腺癌30%。前列腺中央腺体癌影像学表现较复杂[8]。正常前列腺外周带上的腺泡会沿着尿道呈现放射状分布,因其腺体及管状结构丰富,因而T2WI信号为高信号。朱望舒等[9]研究发现,前列腺中央腺体癌发生后,中央区域内会出现大量的癌变腺体值、细胞紧密排列。经检查发现检黏蛋白激液体的含量会明显减少,因此T2WI信号是低信号。前列腺中央腺体癌常合并急性或慢性前列腺炎[10]、出血及钙化,因此常规影像学较难鉴别。磁共振弥散加权成像临床较常用,在鉴别肿瘤恶性程度、浸润上有价值。有文献报道,磁共振弥散加权成像不受脂肪、血液、脓液影响,通过T1WI、FSE、T2WI、DWI图像分析肿瘤恶性风险[11],并采用ADC值反映肿瘤组织内水分子弥散情况。前列腺中央腺体癌腺体型的T2WI信号较高[12],基质型形态不规则、无包膜结节。DWI能反映活体水分子弥散情况,可指导临床明确肿瘤组织的细胞组成、细胞密度、结构等信息。ADC图形成与DWI水分子弥散运动特性密切相关[13]。ADC图在观察水分子扩散变化上更直接、更准确。王宪等[14]研究认为磁共振弥散加权成像前列腺癌ADC图呈低信号,DWI为高信号。弥散敏感因子b值能直接影响DWI参数及ADC图信号。B值越大表示组织扩散能力越强,微循环灌注效应越差。b值越小说明组织弥散效应差,微循环灌注效应好。
前列腺中央腺体癌组织中的腺上皮的正常分泌能力受损,肿瘤细胞大量取代正常腺管结构,出现较高的核质比、间隙液体减少,因此前列腺中央腺体癌水扩散运动明显受限,DWI高信号。本研究结果显示,23.33%前列腺中央腺体癌患者预后不良,76.67%预后较佳,提示前列腺中央腺体癌仍在较高概率的预后不佳情况,包括复发、转移及死亡。Tafuri等[15]研究认为磁共振弥散加权成像ADC值、b值能提示预后,判断病灶恶性程度,反映不良预后。本研究结果显示,不良预后前列腺中央腺体癌患者b=600s/mm2、b=1000s/mm2ADC值较高,说明水分子弥散运动较明显,微循环灌注较差。进一步分析发现,磁共振弥散加权成像诊断前列腺中央腺体癌分化程度与病理结果高分化符合率为71.43%、中分化90%、低分化88.46%,但高分化、中分化及低分化均存在一定分误诊情况。病灶分化程度越高,其细胞与组织异型性越低,故而细胞代谢及增殖较慢,ADC值低。磁共振弥散加权成像诊断前列腺中央腺体癌分期与病理结果T1期、T2期、T3期、T4期符合率为87.10%、85.71%、57.14%、60%,但不同分期均存在一定误诊情况。同时,磁共振弥散加权成像600s/mm2、1000s/mm2ADC值对前列腺中央腺体癌灶风险程度预测价值较高,表明分析磁共振弥散加权成像ADC值能提示前列腺中央腺体癌患者预后。
综上所述,前列腺中央腺体癌磁共振弥散加权成像检查ADC值能帮助临床判断预后、指导治疗,推荐使用。

