乙肝病毒YMDD突变小鼠模型的建立及复制能力研究*
雷 君,张少军,王黎黎
(长江航运总医院感染科,湖北武汉 430010)
乙肝病毒(HBV)感染呈世界性流行,全球约有2.57亿慢性HBV感染者,每年有88.7万人死于HBV感染。我国慢性HBV感染者约7 000万,其中慢性乙型肝炎患者2 000万~3 000万。对于慢性乙型肝炎患者根据病情、家族史及伴随疾病等因素,适时启动抗病毒治疗是延缓病情进展的最有效手段。核苷(酸)类似物是最主要的抗乙肝病毒药物,受到经济条件的限制,我国最早上市的拉米夫定(lamivudine,LAM)和阿德福韦酯(adefovir,ADV)仍在临床上广泛应用。长期服用拉米夫定的患者HBV DNA聚合酶P区可发生变异,简称YMDD变异[1],5年发生率可高达70%,YMDD变异对拉米夫定产生耐药,对恩替卡韦的敏感性下降,需要及时调整抗病毒治疗方案[2]。
小鼠乙肝模型是目前研究HBV感染及治疗最常用的动物模型,采用尾静脉高压法注射复制性质粒建立短期HBV模型,相对简单易行[3]。本研究通过建立乙肝病毒YMDD突变小鼠模型,进行HBV复制水平及药物敏感性研究,为后续耐药研究奠定基础。
1 材料与方法
1.1 质粒 采用的野生型HBV质粒为具备复制能力的PH-BV 4.1 kb质粒(四川大学感染性疾病研究室),包含1.3拷贝的HBV基因组(ayw亚型)。突变型HBV质粒是在野生型PH-BV 4.1 kb质粒的基础上,使用Quik Change Multi Site-Directed Mutagenesis Kit试剂盒(上海英骏生物技术有限公司)进行rtM204I位点突变,通过引物设计、PCR扩增、转染、培养、摇菌后行质粒抽提,并完成质粒测序鉴定[4]。
1.2 小鼠模型建立及分组处理 选取雄性BALB/c小鼠16只,6~8周龄,体重18~20 g,合格证号SCXK(川)2020-030,饲养于武汉大学实验动物中心,许可证号SYXK(鄂)2019-0013。随机分为野生型组和突变型组,每组8只。预先将10μg质粒溶于2 mL PBS,经尾静脉分别注射野生型和突变型HBV质粒,5~8 s内注射完毕。每组小鼠再分成2个亚组各4只,分别给予生理盐水(空白对照)和拉米夫定灌胃处理,连续3 d。参考文献报道及前期预实验结果[4-5],拉米夫定灌胃剂量为500 mg/kg·d,空白对照组小鼠给予相同容量生理盐水灌胃[6]。
1.3 标本留取及处理 灌胃处理3天后处死各组小鼠,留取肝脏标本,保存于液氮中待测。抽提小鼠肝脏HBV-DNA复制中间体,进行Southern杂交检测。
1.4 统计学处理 采用SPSS 25.0统计学软件进行数据分析。HBV复制水平通过Imagine J进行灰度统计分析,计量资料中的HBV-DNA复制中间体水平为连续变量,两组之间的比较均采用t检验,P<0.05为差异有统计学意义。
2 结 果
2.1 rtM204I突变质粒测序 测序结果显示,HBV突变质粒出现rtM204I位点突变,其他位点序列与野生型质粒一致。见图1。
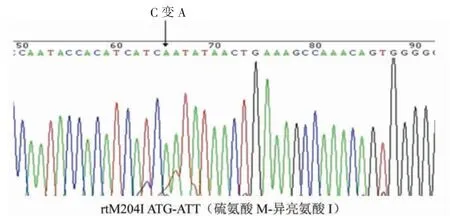
图1 拉米夫定耐药突变株测序图
2.2 突变质粒生物学特性研究 Southern杂交发现,两组小鼠体内均检测到HBV复制,但突变型组HBV复制水平较野生型组降低,见图2,提示rtM204I位点突变影响HBV的复制能力。

图2 野生型和YMDD突变型小鼠HBV复制能力
2.3 拉米夫定处理后两组HBV-DNA复制中间体水平比较 野生型组小鼠在拉米夫定灌胃处理后,HBV-DNA复制中间体水平较空白对照组明显下降(P<0.05),表明拉米夫定对野生型HBV-DNA的复制有很好的抑制作用;但突变型组小鼠给予拉米夫定灌胃后,HBV-DNA复制中间体水平与空白对照组比较,差异无统计学意义(P>0.05),见图3,表明rtM204I位点突变影响拉米夫定对HBV-DNA复制的抑制作用。
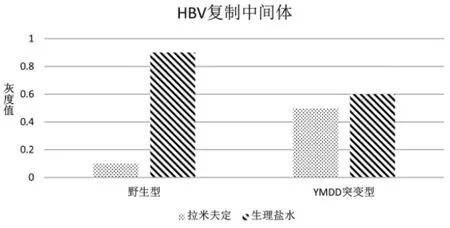
图3 拉米夫定处理后野生型和YMDD突变型小鼠的HBV-DNA复制中间体水平
3 讨 论
乙肝病毒感染导致肝炎、肝硬化及肝癌的发生,严重威胁人类健康。我国乙肝病毒感染患者群体基数较大,长期稳定地抑制乙肝病毒复制是延缓慢性乙肝患者病情进展的唯一方法,一旦出现耐药,后续抗乙肝病毒药物的选择变得更加棘手,乙肝耐药一直是临床关注的热点问题[7]。耐药突变是指在药物选择压力下,HBV基因组上某些位点发生突变,导致药物对HBV的抑制作用减弱或消失[8]。为了进行药物敏感性研究,建立有效的体内研究模型尤为重要。拉米夫定为最早应用的核苷类抗病毒药物,其rtM204I位点突变是最早发现的耐药突变位点,患者在使用拉米夫定6个月后即可检测到,用药2年的检出率达25%~40%,且该位点也是恩替卡韦耐药的重要突变位点,一旦rtM204I位点突变,则恩替卡韦耐药的风险明显增加,2年耐药发生率可达到16%[9-10]。
YMDD变异主要是rtM204I/V变异,rtM204I/V株较野生株复制能力低,rtL180M的出现使突变株HBV的复制接近野生株的水平,故rtM204I/V变异通常与突变rtL180M联合出现;180位点的变异能够使dNTP的结合位点重排,从而使突变的HBV复制恢复到野生株水平,但单独rtL180M变异并不能引起拉米夫定耐药[11-12]。本研究单独对rtM204I突变位点进行研究,其突变株的HBV-DNA复制能力较野生株有所下降,对拉米夫定的敏感性也明显降低,符合YMDD变异的生物学特性。然而,单一突变位点的研究有局限性,后续将进一步构建rtM204VI+rtL180M联合突变位点小鼠模型,研究其相关生物学特性。
综上所述,本研究构建乙肝病毒rtM204I突变质粒,通过小鼠尾静脉注射突变质粒建立HBV突变小鼠模型,并进行HBV-DNA复制能力及药物敏感性的检测,为今后深入开展乙肝病毒突变位点相关研究奠定基础。

