3D打印、计算机建模及人工智能在结构性心脏病中的应用
徐臣年,李 泽,刘 洋,杨 剑
结构性心脏病(structural heart disease,SHD)介入治疗需要对围手术期心脏病理生理学和介入器械进行深入了解,传统的影像学检查已无法满足这些要求。经导管介入手术中仍存在专用器械研发、医学教育、医疗成像以及护理配合等方面的短板,对人体的3D、4D和解剖生理关系的理解上也存在差异[1]。为了弥补虚拟现实之间的差距、整合计算机科学和生物医学工程优势,3D打印、计算机建模和人工智能(artificial intelligence,AI)可能会发挥其优势作用。本文就以上领域新技术进行综述。
1 3D打印简介
3D打印,也称为“快速原型制造或增材制造”,是通过在数字化定义的几何图形上沉积多层材料,将数字对象转换为三维物理复制品的一种制造技术。3D打印建模是一个连续的过程,制作患者特定的3D打印模型源于采集高质量的成像数据,并将其转换为适合进一步图像处理的医学数字成像与通信(digital imaging and communication in medicine,DICOM)格式。将DICOM图像导入专门的图像处理软件中,通过分割过程构建特定解剖部位,然后进行3D模型的绘制和数字建模。3D数字解剖模型以立体光刻(stereolithography,STL)文件格式保存,其中包含适合3D打印的复杂几何体表面网格信息,并可通过计算机辅助设计建模和分析进行修饰。
1.13D打印技术概述 3D打印技术已经应用于心血管医学。立体光固化成型(stereo lithography appearance,SLA)技术是上世纪80年代发展起来的第一代3D打印技术,它利用紫外(ultraviolet,UV)激光以逐层方式固化基底材料(一种光敏液体树脂)来生产3D零部件。根据设计要求,SLA在一个模型中只能使用一种材质,并且需要额外打印支撑结构。SLA是制作大型、高精度和透明心脏和血管模型的理想选择,可用于教育、训练和测试。选择性激光烧结(selective laser sintering,SLS)是一种利用高功率红外激光熔接尼龙、金属和陶瓷等小颗粒热敏材料的技术[2]。SLS主要应用于制造业,不常用于心血管领域。熔融沉积建模(fused deposition modeling,FDM)是一种成本相对较低的3D打印技术,适用于家庭或办公室使用。FDM成本低,是生产刚性模型的理想选择。喷墨3D打印技术的工作原理类似于2D喷墨打印机,它沉积了彩色液体粘合剂的微小液滴,以连接和固化粉末层,形成一个全彩色模型。喷墨只能使用一种基材。是制作复杂彩色心血管结构的理想选择。Stratasys公司(Rehovot,以色列)开发的Polyjet技术在某种程度上是SLA和喷墨技术的结合,它逐层沉积可紫外光固化的光聚合物以产生3D模型(图1),通过混合两种或两种以上的基材,可以打印具有广泛颜色和物理特性的“数字材料”。Polyjet技术最近被用于打印带有刚性部分的顺应性心血管模型,如带有钙化病变的主动脉根部[2-4](图1)。

图1 Stratasys J850打印机制作3D打印心脏模型
1.23D打印数据采集原理 立体图像的采集在3D打印中起着至关重要的作用,不仅决定了3D模型的几何精度,而且还可描述组织特性,指导选择合适的打印材料。许多现代心血管成像技术被用于获取3D打印的图像数据。计算机断层扫描(computed tomography,CT)的时间分辨率在75~200 ms之间,由于其快速采集、高空间分辨率以及组织特征识别能力,已成为3D打印最常用的影像数据来源。与CT相比,3D心脏磁共振(cardiac magnetic resonance,CMR)的空间分辨率较低、采集时间较长。然而,由于没有电离辐射,不受呼吸影响,CMR成像常用于儿童和年轻患者的心腔和大血管的3D打印建模。超声心动图适用性广、时间分辨率高,并易于床边进行,在许多研究中,超声心动图已被用于获取3D打印图像数据[5]。3D超声心动图的主要局限性在于信噪比相对较低,不利于图像后处理和3D建模。此外,由于声学窗口和时空分辨率的限制,利用超声心动图对完整的心脏解剖结构进行3D重建仍然有困难。
1.3数据分割和图像生成原理 在医学图像中描绘目标心脏结构边界过程通常被称为图像分割,是心脏计算机建模的第一步,也是最费力的一步。对SHD患者DICOM图像进行3D处理需要借助专业的3D分割和建模软件。然而,多数情况下,需要手动分割与编辑,因为大多数分割工具都基于简单的强度阈值和区域增长,无法分割具有相似阈值心脏结构。已发表的研究报告通常会使用一些商业、免费工具[6-7]以及内部研发工具[8],其中基于AI的更复杂的图像分割技术具有广阔的应用前景[9]。用于计算机建模的心脏组织的材料特性的数据主要来源于动物组织和/或人类尸体的体外生物力学试验[10]。然而,值得注意的是,活体人体组织的力学性能不同于动物组织或尸体。此外,受试者的年龄、性别和病理学特性在决定组织性质方面起着关键作用。尽管在心脏的计算机模型中经常使用特定患者的形态学特征,只有少数研究增加了特定患者的材料特性[11]。
2 SHD的3D打印
2.1经导管主动脉瓣置换术的3D打印 患者个体化3D打印模型可用于经导管主动脉瓣置换术(transcatheter aortic valve replacement,TAVR)的术前计划、TAVR器械尺寸选择和发生瓣周漏可能性的风险评估[12-14]。主动脉的3D打印模型已被证明可用于模拟患者的血流动力学状况和体外植入TAVR装置。Maragiannis等[15]开发了一系列患者特异性、柔性、多材料组合的3D打印主动脉瓣狭窄模型,该模型在柔性的主动脉弓内可有钙化结构。3D模型使用柔性材料打印主动脉瓣叶和主动脉弓的几何结构,而主动脉瓣叶内的钙化结构则由硬质材料制成。将3D打印的主动脉模型置于患者特定的血流动力学条件下,从而证明其在体外个体化模拟患者血流动力学参数以及采集患者超声心动图参数的可行性[16-18]。笔者所在中心通过术前3D打印模拟主动脉根部结构以及手术模拟辅助TAVR术前影像学评估,取得了3D打印技术应用于主动脉瓣狭窄及关闭不全TAVR手术的初步经验[2]。对于瓣膜钙化较为严重的主动脉瓣狭窄患者,行TAVR术后钙化瓣膜阻塞冠状动脉风险增加,术前3D打印模拟患者主动脉根部解剖结构以及瓣叶钙化点的分布情况,在体外模拟术中球囊扩张等操作,初步判断钙化瓣叶阻塞冠脉的风险程度,可以辅助TAVR术前决策。而对于主动脉瓣关闭不全并伴有升主动脉扩张的患者,介入瓣膜的锚定问题也可通过体外3D打印模拟进行预测,通过在体外3D打印主动脉根部模型模拟植入不同型号的瓣膜,通过比较不同型号以及类型瓣膜的锚定力、瓣膜释放后的稳定程度,个体化的选择最佳介入器械。见图2。

图2 计算机模拟及3D打印技术在TAVR中的应用
2.23D打印技术在经导管二尖瓣修复术中的应用二尖瓣介入修复手术的迅速发展,促进了二尖瓣3D打印的创新应用。最初将3D打印的二尖瓣瓣环和瓣叶用于正常和病变瓣膜结构的解剖学观察。功能完整的二尖瓣模型包括瓣环、瓣叶、腱索和乳头肌,对于提供一个功能性工具来测试和模拟患者个体化器械是必要的。Vukicevic等[19-20]开发了一种多材料3D打印二尖瓣模型,适用于使用MitraClip装置进行经皮二尖瓣修补的手术模拟和规划。在外科培训中,基于高端3D打印的手术模拟使受训人员能够在实际手术之前获得更多关于修复技术的实践经验。
2.3经导管二尖瓣置换术的3D打印与虚拟仿真在经导管二尖瓣置换术(transcatheter mitral valve replacement,TMVR)中,对“neo”-LVOT(left ventricular outflow tract,左心室流出道)的理解首先是通过在患者个体化3D打印中模拟器械开始的,该3D打印可以模拟流出道阻塞风险的相关LVOT解剖结构[21]。3D打印模型可作为可视化沟通工具来测试TMVR器械定位在患者二尖瓣平面的位置,以及评估TMVR后新的LVOT大小。在患者身上获得TMVR术前和术后CT,neo-LVOT的概念就能够从实物3D打印发展到虚拟3D打印瓣膜植入,并进行模拟[22]。
2.43D打印在左心耳封堵术中的应用 左心耳(left atrial appendage,LAA)临床试验和早期可行性研究不需要使用3D打印;然而,一旦开始商业化应用,在没有手术经验的情况下,在早期操作人员的会有一个学习曲线,以确定器械尺寸和器械植入位置等新技术[23]。将3D打印应用于LAA围手术期规划,有助于了解患者解剖结构内不同LAA器械释放位置,并有助于优化器械尺寸、导管和器械选择[24](图3)。

图3 3D打印技术在左心耳封堵术前对左心耳及周围解剖结构的模拟
2.53D打印用于经导管三尖瓣修复和置换 经皮介入治疗三尖瓣(tricuspid valve,TV)最近引起了广泛关注[25]。由于TV器械本身的结构复杂性,包括瓣环非平面性、不同数量的瓣叶、腱索、乳头肌的位置以及右心房和心室周围和内部结构的变异性;传统的成像方式不足以评估右心解剖结构和TV器械的复杂性。目前有几项研究报道了从多模态图像中提取TV用于术前计划和解剖可视化研究[26-27]。Muraru等[26]证明了利用3D经食道超声心动图(transesophageal echocardiogram,TEE)数据提取正常和异常三尖瓣叶和瓣环的几何结构的可行性,其模型是3D打印的固体材料,适用于术前测量和定量分析。此外,Harb等[28]重建了一系列由多模态图像构建的右心模型,包括CT图像、3D-TEE、以及MRI数据中提取的混合模型,用以评估TV形态、TV与周围解剖结构及血流动力学等因素的相互作用,制订术前计划[28]。Cabasa等[27]使用右心3D打印模型来设计一个使用Sapien XT假体(Edward Life sciences,Irvine,CA)的经导管三尖瓣环植入术,演示如何从CT数据重建3D打印模型,用于选择最佳手术器械尺寸和测试植入。
2.63D打印辅助患者教育与医患沟通 3D打印对心脏团队的价值不仅仅局限于围术期手术规划,在临床访视期间,患者与医师之间利用3D打印模型可以进行治疗方案的讨论、患者参与度和满意度的医学调研。传统的术中知情同意沟通需要患者理解医学二维图像,以及医师口头或书面描述。在患者教育中采用3D打印技术,能够提高患者对手术知情同意书的理解。见图4。
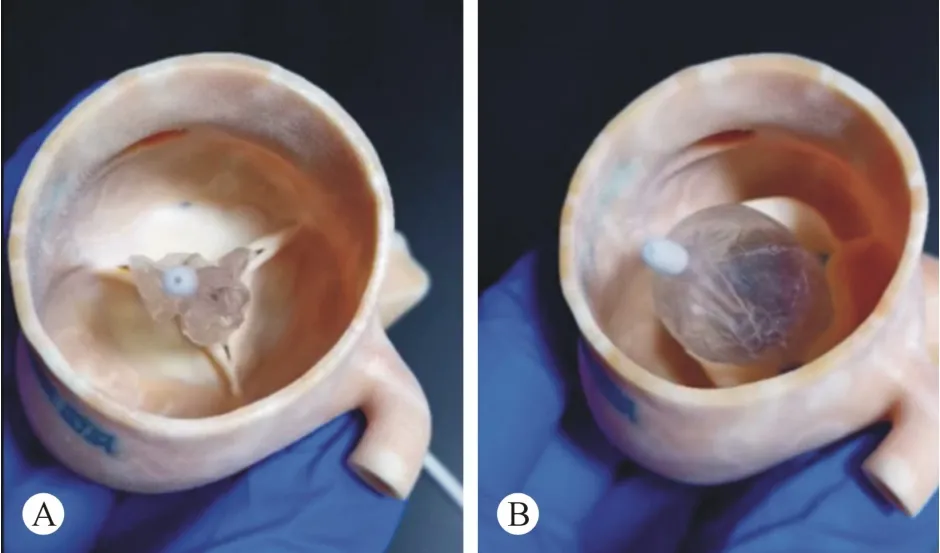
图4 利用3D打印模型在TAVR术前进行球囊预扩模拟
3 计算机建模和AI基础
心血管3D打印模型可以模拟活体器官的外观和机械性能。对于体外试验或手术模拟,最理想的3D打印模型应模拟整个心动周期内的心血管活动;然而,这些材料无法模拟组织学特性,因此寻找与生物组织完全匹配的材料仍然是一个挑战。有报道称4D打印技术可以制作主动变形的3D物体[29]。而打印方向和后处理方法能显著影响模型的力学行为[30]。利用3D打印制作生理和生物学上的精确模型,需要对组织打印材料进行进一步的研究。
静态3D打印模型正在为研发团队应用,可减少新器械从概念到临床应用的过渡时间。静态打印结合体外模拟患者特定血流动力学条件,形成功能性3D打印模型,是模拟介入心脏瓣膜装置和输送系统的理想测试环境。然而,3D打印无法模拟心脏生理搏动,如心脏组织生物力学特性、组织变形、流体力学等。计算机模拟可使用数值分析方法,如有限元分析(finite element analysis,FEA)和计算流体力学(computational fluid dynamics,CFD),这些技术已广泛应用于量化模拟心脏组织的应力和变形[31]以及心脏血流模式。全过程术前模拟可能需要数小时至数天时间,取决于解剖结构的复杂程度以及心脏组织和血流之间的潜在相互作用,进而达到结构-流体力学的完美耦合[32]。因此,FEA和CFD的成本较贵,特别是涉及到大的组织变形和流体-结构相互作用时。计算机模拟的一个局限性是它对简化建模过程所采用的数值假设非常敏感,例如,许多研究将左心室的心内膜模拟成光滑的表面,这种简化可能会导致心室内血流模型与实际不符。目前还缺乏商业化用于临床的FEA和CFD的计算机建模工具,这些技术的实施需要特殊的编程、工程技能,因此主要还停留在研究机构进行。在临床实践中,于心脏计算机模型上模拟经导管植入心脏瓣膜是一种捷径,利用这种技术可以测试各种瓣膜尺寸和锚定深度。瓣膜植入后的新的LVOT也可以在TMVR前进行评估[21]。TMVR术后LOVT梗阻不仅由新LVOT几何结构决定,也可受左心室的血流动力学影响。然而,在这样的限定条件下没有展示物理相互作用的模型,也不能观察到瓣膜或组织的变形。
3.1AI在SHD中的应用 AI对医疗保健的潜在影响巨大。近年来,AI方案在该领域的商业投入激增,这些解决方案提供了改善医疗保健和实现精确诊疗的能力,并在大型医疗公司中大规模采用AI。如前所述,SHD是一个以大量已使用、未使用和未测量的参数为特征的领域,3D结构和“4D”生理可视化并不理想,患者之间在年龄、性别和种族上存在显著差异,这为AI方案提供了巨大应用潜力,可以提高患者护理的有效性、提高效率并降低成本。AI,具体说就是机器学习,不同于经典的计算机编程,因为它面对的是未知领域,从示例中学习而不依赖程序定义规则。因此,机器学习模型可以从大量数据中学习极其复杂的关联,而不需要常识[33]。
3.2基于AI方法,改善SHD介入手术 AI与3D
打印相结合,可以制作患者个性化解剖结构模型,这对精准医学做出了重大贡献[34-35]。Engelhardt等通过内窥镜学习网络,提高了微创手术能力。通过计算机网络可以从二尖瓣修补的内窥镜实例中了解术中关键信息,并在模拟测试中学习。AI可以通过虚拟增强现实提高手术训练过程的真实性。
3.3介入医师和介入影像医师培训 超现实主义和AI模拟的应用将为未来新技术研发发训练奠定基础。在手术模拟中利用3D打印心脏瓣膜模型,可以提高操作人员对手术操作的信心[22,36]。AI在介入手术TEE训练中的应用,能够为数字化图像分级,并使获取TEE图像反馈成为可能。在TAVR介入医师培训中,基于动作分析和手术操作模式的AI自动化评估证明新晋和专家级手术医师之间在手术时间、技术水平等的差异[36]。未来将实时3D-TEE数据集、机器学习以及AI相结合,可以构建更强大的可扩展模块,用于培训介入影像医师、技师。
深度学习可能有助于AI在现实世界中的整合,深度学习在医学影像中最重要的应用之一是分割领域。将心脏CT、MRI数据分割,可以获取心脏大小、形状和功能等重要信息[37]。AI的应用有助于①自动化过程,消除操作人员之间的差异。②在临床可操作的时间范围内获取快速准确的结果。其临床潜力在于它能够分析不同来源的结构化数据组合,从而在临床决策中发挥价值。通过将待处理信息与深度学习方法相结合,可以发现数据中未被发现的知识,进而制定更可靠的临床决策。每种类型数据可以独立分析,也可以与不同类型算法协同分析,产生创新性的应用效果。例如,经导管二尖瓣夹合术(MitraClip)手术模拟可以使操作者选择感兴趣的瓣叶部位进行夹持,并评估虚拟夹植入后形成二尖瓣接合区,以获得最佳手术效果。术中监测这些不同类型的数据可以进行实时预测,避免不良事件。③AI还可用于构建、共享和检索世界各地许多外科医师和介入医师收集的大量手术视频、术中成像和电子医疗记录[38],形成一个实践技术数据库。推进机器学习和AI能够改进和创建更多可复制解剖模型,应用于实时3D-TEE成像。AI有助于识别罕见的解剖病例,整合术前、术中和术后数据。
4 展 望
3D打印、计算机模拟建模和深度学习在SHD手术中具有重要作用,这些技术的早期应用有可能减少操作人员对于新技术的早期学习曲线。未来,计算机建模和深度学习的应用需要将患者手术数据集成到医疗记录和数据采集共享平台。多模态心血管成像的未来需要心脏病理生理学的临床知识、生物医学工程技术与计算机软件开发相结合,而不再仅仅是临床专业知识。

