长链非编码RNA与心肌凋亡*
何娟娟 综述 刘立新 审校
(济宁医学院临床医学院,济宁 272013;济宁医学院附属医院,济宁 272029)
长链非编码RNA(long non-coding RNA,lncRNA)作为复杂分子网络中的一部分,在心血管疾病、自身免疫性疾病及肿瘤等的发生发展中具有重要作用。lncRNA在急性心肌梗死(acute myocardial infarction,AMI)中的研究进展比较多,但lncRNA在心肌细胞凋亡中的作用及分子机制研究尚未见系统叙述。心肌凋亡是多种心血管疾病的重要病理过程,本文围绕lncRNA在不同原因导致的心肌凋亡作用及分子机制做一综述,旨在进一步分析lncRNA通过调节心肌细胞凋亡影响心血管疾病的作用。
1 lncRNA概述
lncRNA是转录本长度超过200个核苷酸且不具有功能性蛋白质编码能力的RNA转录物。lncRNA可以执行多个生物功能:1)可以作为调控染色质状态因子的支架、桥梁和绳索进行表观遗传调控;2)可通过作用于靶基因的转录因子或者抑制因子进行转录调控;3)核分区-维持核结构;4)通过与mRNA碱基结合或作为mRNA结合蛋白的辅助因子或竞争对手进行转录后基因调控[1]。lncRNA在心血管疾病中的表达存在差异,并通过各种机制调节心血管疾病的发生和发展,其中在AMI、心脏发育、心力衰竭(heart failure,HF)、扩张型心肌病、动脉粥样硬化及血脂异常等过程中发挥重要的作用。此外,循环中的lncRNA结构相对稳定,在外周血单核细胞、血浆、血清、尿液等体液中易于检测其存在。
2 心肌细胞凋亡在心血管疾病中的作用
细胞凋亡是一种高度调控的细胞死亡过程,可由细胞膜、线粒体和内质网中的死亡受体介导。参与凋亡过程的相关基因有几十种,其中Bcl-2、Bcl-XL、Bcl-AL等基因有抑制凋亡作用,Bad、Bax、Bak、P53等基因有促进凋亡作用,c-myc等基因可能具有双向调节作用,生长因子充足时促进细胞增殖,生长因子缺乏时引起细胞凋亡[21]。心肌细胞凋亡是多种心血管疾病的重要病理过程。心肌细胞凋亡的增加会促进心肌梗死、HF和扩张型心肌病等多种心血管疾病的发生发展,而限制细胞凋亡对心脏有保护作用。lncRNA通过作用于凋亡相关通路影响凋亡蛋白的表达,从而调控心肌细胞凋亡,在多种心血管疾病的发病机制中发挥重要作用。
3 lncRNA与心肌凋亡
在不同机制导致的心肌细胞凋亡中lncRNA表达有变化,MIAT、MIRF、circANKRD36等在心肌细胞凋亡中表达升高,而UCA1、CARL、ENSMUST00000134285等表达降低,同时还有一些lncRNA 亚型如MALAT1、ANRIL、TUG1、XIST、ROR在调控心肌细胞凋亡中存在双向调节作用,它们既能促进心肌细胞凋亡也能抑制心肌细胞凋亡,这可能与不同心肌细胞类型、不同作用条件或者不同信号通路有关。这些lncRNA通过不同机制发挥不同功能,促进及抑制心肌细胞凋亡。
3.1 lncRNA促进心肌凋亡
3.1.1心肌梗死相关转录本(myocardial infarction associated transcript,MIAT) MIAT是首个被确定为具有心肌梗死风险的一种lncRNA。MIAT通过海绵作用抑制miR-22-3p来上调DAPK2的表达,从而促进心肌细胞凋亡[2]。而且在缺氧/复氧(hypoxia /reoxygenation,H/R)诱导的H9C2心肌细胞中发现MIAT的表达增加[3]。Yao等[4]通过对房颤(Atrial fibrillation,AF)大鼠模型用特定的shRNA慢病毒注射下调MIAT,可使具有心脏保护作用的miR-133a-3p表达增加,导致AF持续时间缩短,并且有效减少AF诱导的心肌细胞凋亡和心房纤维化。见图1。
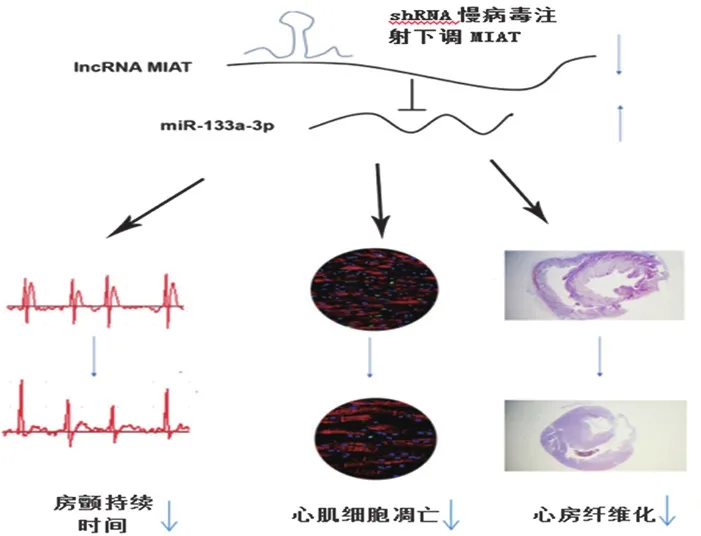
图1 AF大鼠模型MIAT/miR-133a-3p通路示意图[4]
3.1.2心梗调控因子(myocardial infarction-regulatory factor,MIRF) MIRF参与心肌梗死病理过程,但是关于其具体机制的研究尚少。Su等[5]研究揭示了lncRNA MIRF-miR-26a-Bak1轴在心肌梗死中的分子机制。MIRF可通过抑制miR-26a的表达,进而上调Bak1的表达,导致心肌细胞凋亡;敲除MIRF可以减轻AMI小鼠的心肌损伤并改善心功能。
自噬是心肌细胞抗缺血损伤的保护因子。近期一项研究[6]提出了心肌梗死期间MIRF相关的自噬信号机制,心脏应激通过上调MIRF来抑制miR-26a的表达,进而解除对抗自噬蛋白USP15的抑制作用,阻断自噬,减轻内在的心脏保护活性,增加心肌细胞凋亡,最终导致缺血损伤和心功能不全,表明MIRF是一种新的抗自噬lncRNA,为其他自噬相关疾病的研究提供了依据。
3.1.3circANKRD36 环状RNA(circRNA)是属于非编码RNA(ncRNA)的一种新型RNA,在心肌病及心力衰竭中发挥重要作用。circANKRD36属于circRNA中的一种,在炎症损伤中通过吞噬微小核糖核酸(如miR-15、miR-138等)发挥作用。Wang等[7]研究发现circANKRD36通过吞噬作用负调节miR-15水平,而miR-15具有抗炎损伤活性,在心脏缺血性损伤中发挥保护作用,而MyD88是miR-15的靶基因,miR-15通过靶向MyD88发挥作用;沉默circANKRD36可通过调节miRNA-15/MyD88通路减轻脂多糖(lipopolysaccharide,LPS)诱导的炎症损伤。沉默circANKRD36还可通过上调H9c2细胞中的miR-138,抑制p38MAPK /NF-κB通路,减轻LPS激活的心肌细胞凋亡和炎症反应[8]。
3.2 lncRNA抑制心肌凋亡
3.2.1UCA1 UCA1包含3个外显子,长度为1.4kb,最初在人膀胱移行细胞癌中被发现的一种lncRNA。UCA1在成人心脏中特异性表达,表明UCA1可能在维持正常心肌功能方面发挥重要作用,并可作为心脏病(如AMI)的生物标志物。UCA1通过抑制miR-143/MDM2/p53轴来抑制心肌细胞凋亡,发挥心血管保护因子的作用[9]。而在心肌梗死大鼠模型中,也证实了UCA1抑制心肌凋亡作用,UCA1通过靶向作用于miR-873,降低miR-873对其靶点XIAP的抑制作用,并升高抗凋亡蛋白Bcl-2水平,从而减轻心肌细胞凋亡[10]。
3.2.2心脏凋亡相关lncRNA (cardiac apoptosis-related lncRNA,CARL) CARL通过调节心肌细胞凋亡参与心脏疾病的发生发展,但是目前关于其分子机制的研究尚少。Wang等[11]揭示了CARL可抑制线粒体裂变和凋亡,而这种作用主要依赖于miR-539和PHB2。CARL通过下调miR-539来增加 PHB2 的表达,从而抑制线粒体分裂和心肌凋亡。此外,Li等[12]发现CARL在大鼠原代心肌内皮细胞中过表达可提高细胞活力,降低细胞凋亡。
3.2.3ENSMUST00000134285 2018年,Chun等[13]鉴定出ENSMUST00000134285是调控细胞凋亡的一种lncRNA。ENSMUST00000134285可增加下游的MPAK11活性,MAPK11通过抑制ROS形成发挥促存活作用。敲低H/R心肌细胞模型小鼠ENSMUST00000134285可抑制MAPK11的活性,增加心肌细胞凋亡;推测miRNA760可能是ENSMUST00000134285和MAPK11之间的中介,但是目前尚未得到进一步证实。
3.3 lncRNA双向调节心肌凋亡
3.3.1转移相关肺腺癌转录本1 (metastasis-associated lung adenocarcinoma transcript 1,MALAT1) MALAT1是一个长度为8000 nt的lncRNA,位于染色体11q13上。近年来,MALAT1在心血管疾病方面的作用被重视,并发现它可以通过多种途径参与调节心肌凋亡。下调MALAT1可减少糖尿病大鼠心肌细胞凋亡,改善左心室功能[14]。MALAT1介导的组蛋白甲基转移酶EZH2向miR-22启动子募集导致miR-22的转录受到抑制;低水平的miR-22可上调ABCA1的表达,ABCA1可通过影响细胞炎症因子分泌来增加糖尿病大鼠心肌细胞的凋亡(图2)。MALAT1在自噬调节中也能发挥作用,MALAT1通过TSC2启动子区招募EZH2诱导核小体组蛋白(H3K27me3)来表观抑制TSC2转录,从而诱导mTOR激活并抑制自噬,降低自噬对心脏的保护作用[15]。但是部分研究也表明H9C2细胞中,MALA起到抑制凋亡的作用。Yao等[16]指出敲低MALAT1可上调miR-217的表达,进而降低Sirt1的表达,加重缺氧诱导的H9C2细胞凋亡。MALAT1可通过海绵作用下调miR-558的表达,进而减少异丙肾上腺素(ISO)诱导的 H9C2心肌细胞凋亡[17]。

图2 MALAT1在糖尿病心肌病中的作用机制图[14]
3.3.2ANRIL ANRIL是一种长3.8kb的反义非编码RNA,转录自人类9号染色体P21的短臂上。目前已经确定ANRIL是一种与冠状动脉心脏病(CHD)密切相关的生物标志物[18]。Yang等[19]研究发现在AMI小鼠模型中,下调ANRIL可通过IL-33/ST2途径减轻心肌细胞凋亡,促进心肌细胞存活,减少梗死面积、纤维化,改善心肌功能。但是,Shu等[20]研究揭示了ANRIL通过调节miR-7-5p/SIRT1轴,在缺氧诱导的H9c2细胞损伤中发挥保护作用。ANRIL通过与miR-7-5p竞争性结合,正向调控Sirt1表达,从而减少了心肌细胞凋亡。
3.3.3LncRNA牛磺酸上调基因1(Taurine-upregulated gene 1,TUG1) TUG1位于染色体22q12上,最初被确定为牛磺酸处理的小鼠视网膜细胞中上调的转录本。TUG1可通过影响成骨细胞凋亡在骨质疏松中发挥重要作用。TUG1通过上调 Bcl-2 来抑制地塞米松诱导的小鼠 MC3T3-E1 细胞凋亡,表明TUG1 可能是糖皮质激素诱导的成骨细胞凋亡的保护性因子[21]。而近年来关于TUG1影响心肌缺血操作的研究表明,TUG1在心肌细胞凋亡中也起到重要作用。Wu等[22]研究发现TUG1竞争性结合miR-340加速心肌缺血再灌注损伤(myocardial ischemia-reperfusion injury,MIRI)。
另外,TUG1-miR-9a-5p轴通过靶向KLF5促进心肌细胞凋亡,导致心肌缺血损伤。TUG1通过竞争性结合miR-9a-5p来促进KLF5的表达;上调的KLF5通过刺激线粒体死亡通路,导致心肌细胞凋亡增加[23]。此外,敲低 TUG1可通过调控miR-532-5p/Sox8轴来减轻缺血缺氧诱导的心肌细胞炎症和凋亡[24]。而Jiang等[25]研究发现,在缺氧诱导的H9C2细胞中上调TUG1可减轻心肌细胞损伤。TUG1通过靶向下调miR-124的表达,降低了miR-124对Hic-5抑制作用,过表达的Hic-5激活Sp1/Survivin信号通路,最终减轻缺氧诱导的心肌细胞凋亡。
3.3.4非X活性特异性转录本(X-inactive specific transcript,XIST) XIST位于人Xq13.2染色体上,是一个17kb的lncRNA。XIST在心肌梗死、糖尿病心肌病及脓毒症心肌损伤等疾病中发挥重要作用。XIST可通过靶向miR-101a-3p上调FOS和凋亡相关蛋白水平,促进心肌细胞凋亡[26]。下调XIST可改善LPS诱导的心肌损伤,减少凋亡[27]。Peng等[28]研究提示XIST可以抑制H9C2心肌细胞凋亡。XIST通过吸附miR-122-5p来促进FOXP2表达,而FOXP2过表达可上调Bcl-2表达,抑制HIF-alpha、Bax和cleaved-caspase 9蛋白的表达,从而减少心肌细胞凋亡。
4 小结与展望
心肌凋亡是包括心肌梗死、心力衰竭、扩张型心肌病在内的多种心血管疾病重要的病理基础,而lncRNA种类众多,目前关于lncRNA与心肌凋亡的关系仍在研究阶段,lncRNA调节心肌凋亡的具体机制尚不完全明确。因此,针对lncRNA调节心肌凋亡的研究仍是非常有必要的。这将有助于挖掘更多心血管疾病的潜在的生物标志物和治疗靶点,为医师把握患者病情及较早采取治疗措施提供帮助,从而改善预后。
利益冲突:所有作者均申明不存在利益冲突。

