奥沙利铂+吉西他滨联合索拉非尼对晚期原发性肝癌患者的疗效分析
黄 维,杨 庆,黄江远
[南方医科大学顺德医院(佛山市顺德区第一人民医院)肿瘤科,广东 佛山 528300]
原发性肝癌属于一种恶性肿瘤,我国属于肝病大国,肝癌的发病率也较高,早期疾病症状不显著,至发现时多数已经处于局部晚期或者发生远处转移阶段,以致错过手术最佳时机,生存率较低,对患者生命健康造成严重威胁[1]。索拉非尼是国家认可的多靶点治疗药物,用于不可手术切除的晚期肝细胞癌治疗,但是该药物在治疗的过程中有效率较低,容易出现疾病恶化,并易产生耐药性,因此需要对治疗方法进行改进,使用更加有效的药物对疾病进展进行控制[2]。奥沙利铂属第3代铂类药物,在肝癌的治疗中效果较好,能够对控制疾病的发展起到一定的积极作用;吉西他滨作为一种化疗药物,是核糖核苷酸还原酶的一种抑制性酶的替代物,化疗效果显著,因此将其与索拉非尼联用可提高患者的临床治疗效果[3]。本研究选择50例晚期原发性肝癌患者作为研究对象,旨在探讨奥沙利铂+吉西他滨联合索拉非尼对晚期原发性肝癌患者血清肿瘤标志物指标水平的影响,现将结果报道如下。
1 资料与方法
1.1 一般资料 按随机数字表法将2019年3月至2020年6月南方医科大学顺德医院(佛山市顺德区第一人民医院)收治的50例晚期原发性肝癌患者分为两组。对照组(25例)中男、女患者分别为20、5例;年龄42~68岁,平均(55.11±3.23)岁;肝细胞癌19例,肝细胞/胆管混合型6例;肝外转移23例,未转移2例;试验组(25例)中男、女患者分别为19、6例;年龄41~68岁,平均(54.56±3.34)岁;肝细胞癌20例,肝细胞/胆管混合型5例;肝外转移22例,未转移3例。两组患者一般资料比较,差异无统计学意义(P>0.05),组间可实施对比。纳入标准:符合《原发性肝癌诊断标准》[4]中的诊断标准者;均实施影像学检查、病理诊断确诊者;预计生存期>2个月者等。排除标准:实验前1个月接受重大手术者;存在严重精神类疾病,无法配合实验者;中途退出研究者;存在相关药物过敏史者;存在颅内出血、血管畸形病史者等。患者及家属均签署知情同意书,且本研究获南方医科大学顺德医院(佛山市顺德区第一人民医院)医学伦理委员会审核批准。
1.2 治疗方法 对照组患者给予甲苯磺酸索拉非尼片(Bayer AG,注册证号HJ20160201,规格:0.2 g/片)口服治疗,0.2 g/次,2次/d。试验组患者在其基础上接受注射用奥沙利铂(江苏恒瑞医药股份有限公司,国药准字H20000337,规格:50 mg/支)1 000 mg/m2联合注射用盐酸吉西他滨(江苏豪森药业集团有限公司,国药准字H20030104,规格:0.2 g/支)1 000 mg/m2静脉滴注,1次/周,连续治疗3周,休息1周,每4周重复1次;索拉非尼使用剂量仍为0.2 g/次,2次/d。对病程发展程度进行观察,如存在病情进展的情况则按照既定FOLFOX4或者XELOX化疗方案进行化疗,FOLFOX4方案:在第1天给予奥沙利铂静脉滴注,剂量为85 mg/m2;在第1、2天给予注射用亚叶酸钙(江苏恒瑞医药股份有限公司,国药准字H32022391,规格:100 mg/支)静脉滴注,剂量为200 mg/m2;给予氟尿嘧啶注射液(上海旭东海普药业有限公司,国药准字H31020593,规格:10 mL∶0.25 g)静脉注射,剂量为400 mg/m2,同时进行氟尿嘧啶静脉滴注,剂量为600 mg/m2,均1次/d;XELOX方案:第1天给予奥沙利铂静脉滴注,剂量为130 mg/m2,1次/d。第1~14天给予卡培他滨片(上海罗氏制药有限公司,国药准字H20073024,规格:0.5 g/片)口服,剂量为1 250 mg/m2。上述化疗均持续3周为1个周期,共化疗4个周期,且两组患者均随访1年。
1.3 观察指标 ①临床疗效。完全缓解:治疗后症状与病灶均消失;部分缓解:症状消失,病灶的最大直径和体积缩小30%及以上;稳定:症状部分消失,病灶最大直径与体积缩小低于30%;进展:如症状部分消失,病灶最大直径和体积在治疗后扩大超过20%[4]。总有效率=完全缓解率+部分缓解率。②血清肿瘤标志物。分别于两组患者治疗前后清晨空腹状态下,抽取静脉血5 mL,以3 000 r/min转速离心10 min取血清,用全自动生化分析仪检测血清甲胎蛋白(AFP)水平,用酶联免疫吸附实验法检测两组患者血清糖链抗原(CAl99)、癌胚抗原(CEA)水平。③生存指标与临床结局评估。生存指标包括疾病进展期、总生存期。临床结局评估:治疗后对两组患者进行随访,统计生存情况。④不良反应评估。包括白细胞减少、血小板减少、肝功能损伤、恶心呕吐、腹泻、周围神经毒性等发生情况。
1.4 统计学方法 应用SPSS 23.0统计软件分析数据,计量资料(血清肿瘤标志物与生存指标)与计数资料(临床疗效、临床结局及不良反应)分别以(±s)及[ 例(%)]表示,分别用t及χ2检验。以P<0.05为差异有统计学意义。
2 结果
2.1 临床疗效 试验组患者治疗总有效率为32.00%,与对照组的4.00%比显著升高,差异有统计学意义(P<0.05),见表 1。

表1 两组患者临床疗效比较[ 例(%)]
2.2 血清肿瘤标志物 治疗后两组患者血清AFP、CA199、CEA水平与治疗前比均显著下降,且试验组与对照组比显著降低,差异均有统计学意义(均P<0.05),见表2。
表2 两组患者血清肿瘤标志物指标水平比较( ±s)
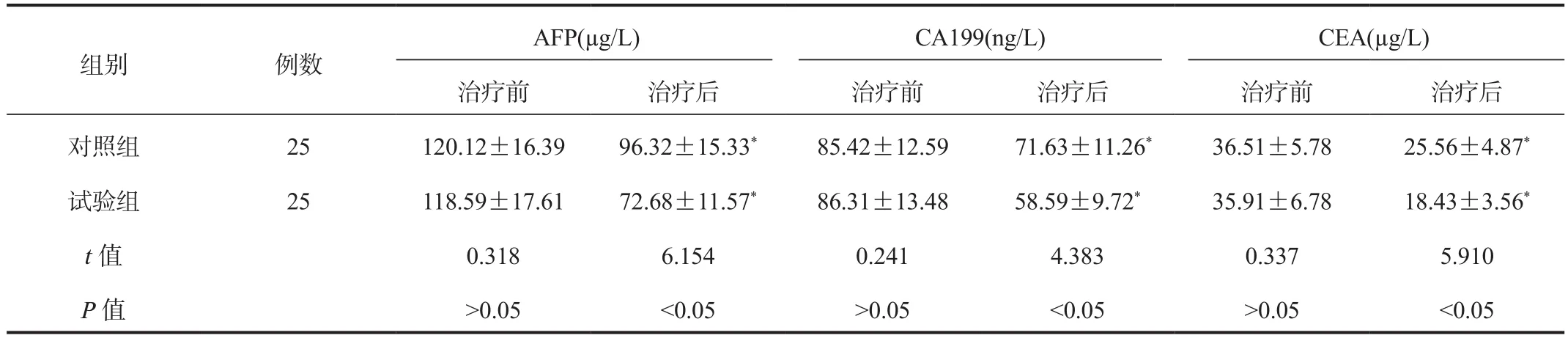
表2 两组患者血清肿瘤标志物指标水平比较( ±s)
注:与治疗前比,*P<0.05。AFP:甲胎蛋白;CA199:糖链抗原;CEA:癌胚抗原。
AFP(μg/L) CA199(ng/L) CEA(μg/L)治疗前 治疗后 治疗前 治疗后 治疗前 治疗后对照组 25 120.12±16.39 96.32±15.33* 85.42±12.59 71.63±11.26* 36.51±5.78 25.56±4.87*试验组 25 118.59±17.61 72.68±11.57* 86.31±13.48 58.59±9.72* 35.91±6.78 18.43±3.56*t值 0.318 6.154 0.241 4.383 0.337 5.910 P值 >0.05 <0.05 >0.05 <0.05 >0.05 <0.05组别 例数
2.3 生存指标与临床结局评估 随访期间试验组患者疾病进展期、总生存期与对照组比均显著延长;试验组患者生存率与对照组比显著升高,死亡率显著降低,差异均有统计学意义(均P<0.05),见表3。

表3 两组患者生存指标与临床结局评估
2.4 不良反应 两组患者化疗期间白细胞减少、血小板减少、肝功能损伤、恶心呕吐、腹泻、周围神经毒性等不良反应发生率比较,差异均无统计学意义(均P>0.05),见表4。
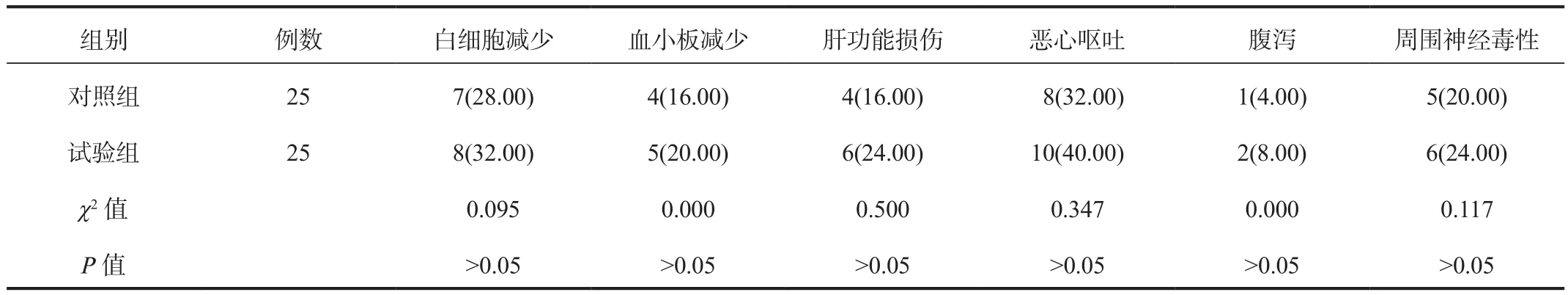
表4 两组患者不良反应发生率比较[ 例(%)]
3 讨论
原发性肝癌属于消化系统肿瘤,该病早期症状不明显,大部分患者在确诊时已经处于中晚期,失去手术治疗机会,仅能通过非手术方案治疗,因此需要选择更加有效的疾病治疗方案,对肿瘤进行控制。索拉非尼是一种多靶点的治疗药物,可以对肿瘤进行较好的控制,该药物可以阻断有丝分裂原活化蛋白激酶信号通路,对肿瘤细胞的生长进行抑制,但长期使用会产生耐药性,整体疗效欠佳[5]。
奥沙利铂属于第三代铂类药物,该药物对于多种肿瘤细胞均具有较好的控制效果,可有效抑制肿瘤活性,其主要成分为左旋反式二氨环已烷草酸铂,患者接受给药后,通过铂原子结合细胞内的DNA链,从而形成互联效果,切断其复制和转录途径,阻碍肿瘤的进展扩散;吉西他滨能够抑制脱氧胞嘧啶脱氨酶,减少细胞内代谢物的降解,发挥自我增效作用[6-7]。本研究中,试验组患者治疗总有效率及随访期间生存率与对照组比显著升高,死亡率显著下降;疾病进展期、总生存期与对照组比均显著延长,提示晚期原发性肝癌患者以奥沙利铂+吉西他滨联合索拉非尼治疗,可以提高治疗有效率,延长生存时间,降低死亡率。
AFP是诊断肝癌的一种重要分子,也是筛选肝癌的主要手段之一,其水平与原发性肝癌严重程度呈正相关;CA199、CEA是一种黏蛋白型的糖类蛋白肿瘤标志物,其水平在肝病、胰腺癌等疾病中异常升高[8-9]。奥沙利铂在用药15 min内即可完成与肿瘤细胞内DNA链的结合,速率更快,结合作用更加牢固,因此对肿瘤细胞的毒性作用更为明显,用于晚期原发性肝癌治疗中有着较好的肿瘤抑制作用,对于肿瘤的进一步进展可以有效控制。吉西他滨进入人体后由脱氧胞嘧啶激酶活化,由胞嘧啶核苷脱氨酶代谢,对降低患者机体内肿瘤标志物水平也具有重要意义[10]。本研究中,治疗后试验组患者血清肿瘤标志物水平与对照组比均显著下降,提示晚期原发性肝癌患者以奥沙利铂+吉西他滨联合索拉非尼治疗,可在提高其治疗有效率的同时,有效降低患者血清肿瘤标志物水平。
药物不良反应在治疗中也是需要重点关注的问题,奥沙利铂药物使用中主要的不良反应为恶心呕吐和骨髓抑制(白细胞减少),因此在治疗期间需定期进行检查,同时用药过程中要少食用冰冷刺激食物,并通过对症治疗可以减少恶心、呕吐等不良反应;而周围神经毒性反应则主要出现在化疗中,属于一种急性反应,通过对症治疗也可得到及时恢复[11]。本研究结果显示,两组患者各项不良反应发生率比较,差异均无统计学意义,提示晚期原发性肝癌患者以奥沙利铂+吉西他滨联合索拉非尼治疗,未增加不良反应,安全有效。
综上,以奥沙利铂+吉西他滨联合索拉非尼治疗晚期原发性肝癌患者,可以提高其治疗有效率,有效降低机体的血清肿瘤标志物水平,延长生存时间,降低死亡率;同时未增加不良反应,安全有效,具有较高的临床推广普及价值。

