赤黄止痢颗粒中赤芍的薄层色谱鉴别与含量测定方法的建立
尚静雪,苏岳乐,张鹏举,蔡小利,张远达,战 文,何鸿毅,付丽云,李海华,陈志强*
(1.内蒙古华天制药有限公司,内蒙古赤峰 024070;2. 内蒙古自治区兽药监察所,呼和浩特 010020;3. 赤峰市药品检验所,内蒙古赤峰 024000)
大肠杆菌和痢疾杆菌是导致痢疾最为常见的病原菌[1],目前,临床上采用的常规抗菌西药疗法收到的效果并不理想[2]。刘筱[3]的药效学和安全性研究试验结果显示赤黄止痢颗粒有效率高达100%,治愈率可达80%,临床效果明显,开发该中兽药复方制剂不仅可为养殖市场提供“无抗药”,满足消费者对食品安全的要求,而且能够推动和发展“传统中兽药新制法”的科学疗法和健康养殖的理念,具有广阔的发展前景。
赤黄止痢颗粒是由赤芍和黄柏2味中药提取浓缩后,添加一定辅料制备而成的中药复方颗粒,主治畜禽痢疾。方中赤芍始载于《神农本草经》,列为中品,其曰:“主邪气腹痛,除血痹,破坚积,寒热疝瘕,止痛[4]”。黄柏始载于《神农本草经》原名“果木”,列为上品,属于清热燥湿类药物[5]。《阎氏小儿方论》中记载:赤芍四钱、黄柏半两,具清热止痢的功能。实验室又通过大量中药体外抑菌试验发现,赤芍、黄柏两味药联用对大肠杆菌和沙门氏菌菌的药敏试验中,其FIC<0.5,具有联合抑菌作用。本文主要研究赤黄止痢颗粒中赤芍的薄层鉴别和含量测定项的分析方法。为使产品安全、有效、质量可控,制定合理的质量标准很重要。
1 材料与方法
1.1 材料
1.1.1 试验样品 赤黄止痢颗粒(批号200701、200702、200703)为内蒙古华天制药有限公司制备的3批样品。
1.1.2 主要试剂及仪器 芍药苷对照品(来源:中国食品药品检定研究院,批号:110736-201943);甲醇为色谱纯购自国药集团化学试剂有限公司;水为超纯水,乙醇、甲醇等其余试剂均为国产分析纯。
超声波清洗器(SK1200H)购自上海科导超声仪器有限公司;电子天平(TD10002C)购自天津天马衡基仪器有限公司; 电子分析天平(BT-125D)购自赛多利斯科学仪器有限公司;水浴锅(HH-4)购自江苏省金坛市荣华仪器制造有限公司;高效液相色谱仪(LC-2030C Plus)购自岛津公司;色谱柱:C18(250 mm×4.6 mm,5 μm);购自岛津公司、北京绿百草科技发展有限公司和安捷伦科技有限公司。
1.2 方法
1.2.1 赤黄止痢颗粒的定性鉴别方法
1.2.1.1 赤芍的鉴别 取本品适量研磨成细粉,取细粉1 g,加乙醇10 mL,超声20 min,滤过,滤液蒸干,残渣加乙醇2 mL使溶解,作为供试品溶液。另取芍药苷对照品,加乙醇制成每1 mL含2 mg的溶液,作为对照品溶液。照薄层色谱法试验,吸取上述两种溶液各5 μL,分别点于同一硅胶G薄层板上,以三氯甲烷-乙酸乙酯-甲醇-甲酸(40∶5∶10∶0.2)为展开剂,展开,取出,晾干,喷以5%香草醛硫酸溶液,加热至斑点显色清晰。供试品色谱中,在与对照品色谱相应的位置上,显相同的蓝紫色斑点。
1.2.1.2 专属性考察 取赤黄止痢颗粒样品和分别缺少赤芍的阴性样品,按上述相应方法进行检测,根据试验结果考察该方法对药材的薄层鉴别是否具有专属性。
1.2.1.3 重复性考察 取3批样品,按上述相应方法检测,考察该方法的重复性。
1.2.1.4 耐用性考察 取赤黄止痢颗粒样品按上述相应方法检测,分别点于3个不同厂家的薄层板上,考察该方法的耐用性。
1.2.2 赤黄止痢颗粒含量测定方法
1.2.2.1 赤芍色谱条件 色谱柱:用十八烷基硅烷键合硅胶为填充剂(Agilent 4.6 mm×250 mm,5um),以甲醇为流动相A,以0.1%磷酸溶液为流动相B;按(36∶64)进行等度洗脱,流速为1.0 mL/min,检测波长230 nm,理论板数按芍药苷峰计算不应低于2000。
1.2.2.2 对照品溶液的制备 取经五氧化二磷减压干燥器中干燥36 h的芍药苷对照品适量,精密称定,加甲醇制成每1 mL含0.5 mg的溶液,即得。
1.2.2.3 供试品溶液的制备 取本品适量研磨成细粉,取细粉1 g,精密称定,置具塞锥形瓶中,精密加入甲醇25 mL,称定重量,超声冷却20 min,放冷,再称定重量,用甲醇补足减失的重量,摇匀,滤过,取续滤液,即得。
1.2.2.4 阴性样品溶液制备 取缺赤芍的处方药材制备成缺赤芍的赤黄止痢颗粒样品,同“1.2.2.3”方法制成阴性样品溶液。
1.2.2.5 精密度试验 精密吸取供试品溶液各10 μL,连续6次注入液相色谱仪,记录色谱图。
1.2.2.6 专属性试验 精密吸取对照品溶液、供试品溶液和阴性样品溶液各10 μl,注入液相色谱仪,记录色谱图。
1.2.2.7 线性关系试验 精密称取芍药苷对照品适量,制成不同浓度的对照品溶液,按上述色谱条件进样,记录峰面积,以对照品浓度为横坐标(x),峰面积为纵坐标(y)绘制标准曲线并进行线性回归分析。
1.2.2.8 稳定性试验 精密吸取供试品溶液10 μL,分别在制备后0、2、8、12、18和24 h测定芍药苷的峰面积。
1.2.2.9 重现性试验 精密称取同一批颗粒剂样品6份研磨成细粉,每份取细粉0.5 g,照供试品溶液制备项下方法制备,分别进样10 μL,按上述“1.2.4.1”项中色谱条件进行测定。
1.2.2.10 回收率试验 取已知含量的同一批赤黄止痢颗粒样品9份(含量为0.50%),每份分别按赤黄止痢颗粒中含有芍药苷量的80%、100%和120%加入对照品溶液,各3份,再按供试品溶液制备项下方法制备,精密吸取5 μL,按上述色谱条件测定芍药苷的峰面积,计算平均回收率。
1.2.2.11 耐用性试验 精密吸取供试品溶液5 μl,测定芍药苷的峰面积并计算芍药苷含量,分别考察不同厂家(岛津、绿百草和安捷伦)色谱柱、不同流速(0.8、1.0 mL/min)和不同柱温(20、25和30 ℃)对芍药苷含量测定的影响。
1.2.2.12 样品含量测定 取3批样品,各批次三份平行样品,按对照品、供试品溶液制备方法制备好对照品和供试品溶液,精密吸取供试品溶液及对照品溶液各5 μL,注入液相色谱仪,按“1.2.4.1”中色谱条件进样、测定、记录峰面积。计算样品中芍药苷含量。
2 结果与分析
2.1 赤黄止痢颗粒中赤芍的定性鉴别结果
2.1.1 专属性和重现性 赤芍的薄层鉴别:由图1可知,赤黄止痢颗粒样品色谱在与对照药材色谱相应的位置上,显相同的蓝紫色斑点。缺赤芍的阴性样品色谱在与相同的位置上无相应斑点,斑点清晰,方法具有专一性。

1,5:对照品;2:阴性样品;3~4:样品
2.2.2 耐用性考察结果 赤芍的耐用性结果见图2,在3个不同厂家的硅胶G薄层板上3批赤黄止痢颗粒样品色谱与芍药苷对照品色谱相应的的位置上,均显示相同的蓝紫色斑点。
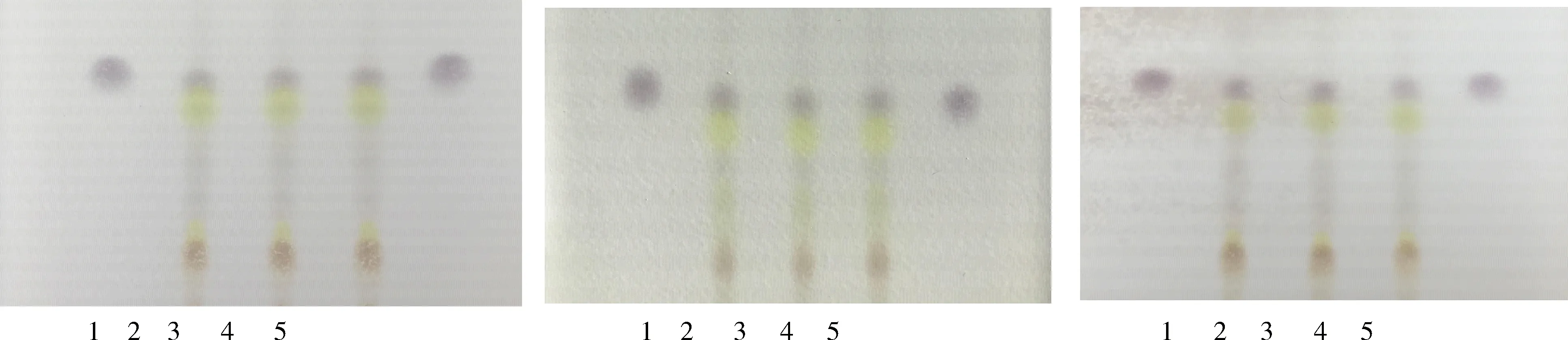
1,5:芍药苷对照品;2~4:赤黄止痢颗粒;3:批样品
2.3 赤黄止痢颗粒的含量测定结果
2.3.1 精密度试验 芍药苷峰面积6次进样结果分别为:2637993、2643986、2635589、2646308、2654697和2667774,RSD=0.45%(n=6),表明精密度良好。
2.3.2 专属性试验 专属性试验结果见图3,芍药苷的保留时间为8.638 min,阴性样品对测定干扰,结果表明专属性良好。
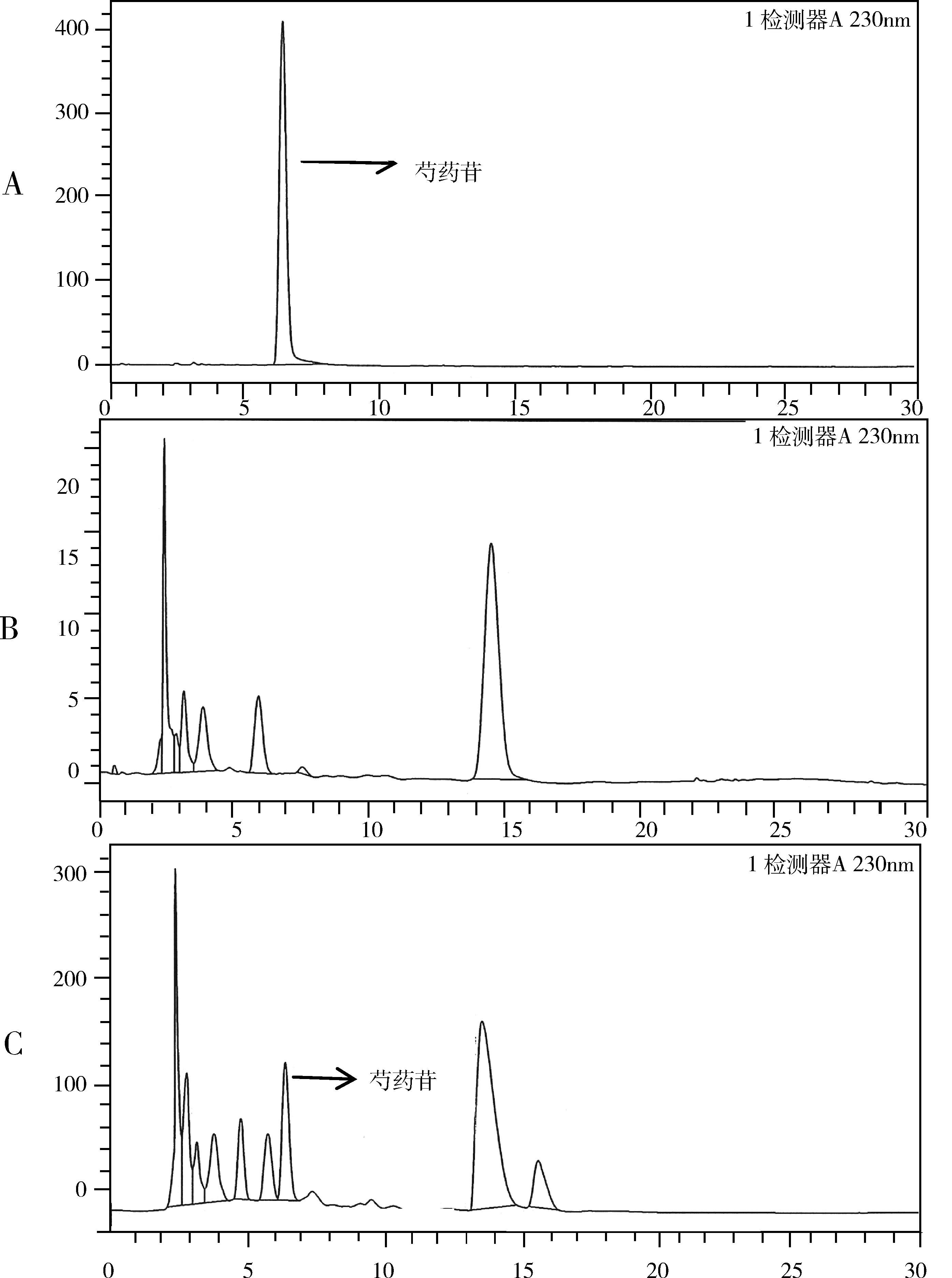
A:对照品溶液;B:阴性对照品溶液;C:供试品溶液
2.3.3 线性关系试验 通过线性关系分析得到回归方程:15115057.2000x + 152337.2667, R2=0.9996。结果表明,芍药苷在0.25~2.0 mg范围内与其色谱峰峰面积呈良好的线性关系,回归曲线见图4。

图4 芍药苷回归曲线
2.4.4 稳定性试验 放置0、2、8、12、18和24 h的赤黄止痢颗粒中芍药苷峰面积分别为2933920、3031287、2865617、2934849、2983689和2953168,RSD为1.93%,表明样品溶液在24 h内稳定。
2.3.5 重现性试验 由表2可知,RSD为0.81%,表明样品重现性良好。
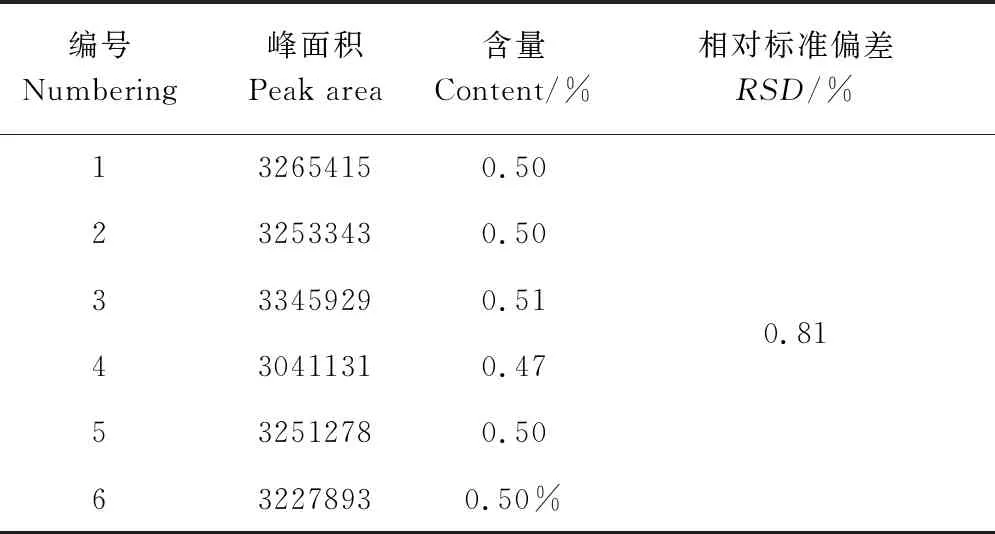
表1 重现性试验结果
2.3.6 回收率试验 通过测定芍药苷的峰面积,计算平均回收率,结果见表3,芍药苷平均回收率为99.74%,RSD为1.95%(n=9),表明该方法准确可信。
2.3.7 耐用性试验 试验结果显示,色谱柱为岛津和绿百草的分离度小于1.5且拖尾因子大于1.05,色谱柱为安捷伦的分离度大于1.5且拖尾因子在0.95~1.05之间,表明赤黄止痢颗粒中赤芍含量测定适用于安捷伦色谱柱;不同流速进样测定试验芍药苷的峰面积,其含量平均值为0.54%,RSD为1.71%,表明流速变化±0.2 mL/min耐用性良好;不同柱温进样测定芍药苷的峰面积,计算得芍药苷的含量平均值为0.52%,RSD为1.69%,表明柱温变化±5 ℃的耐用性良好。
2.3.8 样品含量测定 3批赤黄止痢颗粒样品各批次三份平行样品的测定结果见表4,计算含量平均值为0.51%,RSD为0.041%。参照《中国兽药典》含量限度的一般要求,并结合赤黄止痢颗粒各批次含量测定结果,将赤黄止痢颗粒含量限度拟定为:本品含赤芍以芍药苷(C23H28O11)计不得少于0.4%。
3 讨论与结论
3.1 有关薄层色谱鉴别方法 赤黄止痢颗粒应工艺制备需求在处方中需添加适量辅料,故在薄层色谱鉴别预试验中供试品溶液的制备考虑使用中性氧化铝柱[14]和未使用中性氧化铝柱对其影响,试验结果发现:经中性氧化铝柱前处理的供试品溶液较未使用中性氧化铝柱的供试品溶液薄层鉴别斑点颜色较浅,说明使用中性氧化铝柱前处理对芍药苷的薄层鉴别有少许影响。因此,芍药苷供试品溶液不需要经中性氧化铝柱前处理。参照药典中赤芍药材的鉴别方法,对其进行专属性、重现性和耐用性等方面考察,结果表明该TLC方法稳定、可行,适用于赤黄止痢颗粒中赤芍药材的鉴别。同时,李柯[15]等对芪芍化纤柔肝汤中赤芍参照药典方法进行薄层鉴别,结果显示鉴别效果较好。
3.2 有关含量测定项检测方法 赤芍为毛茛科植物赤芍或川赤芍的干燥根,具有清热凉血,散瘀止痛的功效[6]。现代药理学研究发现其主要化学成分为芍药苷,主要占比约3.1%~7.0%[16],本研究为更好地控制制剂质量,采用HPLC法建立赤黄止痢颗粒中芍药苷的含量测定。
波长的选择:取供试品溶液在紫外分光光度计中200~400 nm区间扫面,结果在230 nm处芍药苷的吸光度最大,故选用230 nm为检测波长。
色谱柱的选择:试验考察了不同色谱柱对芍药苷色谱峰分离的影响,色谱柱厂家分别为岛津、绿百草和安捷伦。结果表明色谱柱为Agilent (4.6 mm×250 mm,5um)时供试品色谱峰的分离度大于1.5且拖尾因子在0.95~1.05之间,因此色谱柱选择Agilent (4.6 mm×250 mm,5um)。
流动相的选择:文献[17-20]报道,高效液相色谱法测定中药芍药苷的流动相系统有乙腈-0.1%磷酸溶液、乙腈-水、甲醇-水、甲醇- 0.1%磷酸溶液、甲醇-0.05 mol/L磷酸二氢钾溶液等,考察其分离度和峰形等,试验发现甲醇- 0.1%磷酸溶液为流动相时峰面积的分离度与峰形较好。
3.3 结论 本试验建立的赤黄止痢颗粒中赤芍的薄层色谱鉴定方法,分离效果好,专属性强、重复性高;建立的赤黄止痢颗粒中芍药苷含量测定的HPLC分析方法,结果准确、专属性强、精密度高,选择的流动相降低对仪器系统和色谱柱的损伤,可用作赤黄止痢颗粒中芍药苷的含量测定。因赤黄止痢颗粒为内蒙古华天制药有限公司自主研发的新中兽药复方制剂,主要用于治疗畜禽痢疾。检索有关资料,未发现本制剂相关检测数据,故本试验建立的赤黄止痢颗粒中赤芍的薄层色谱鉴别方法和含量测定分析方法,为赤黄止痢颗粒质量标准的制定提供了方法学依据。

