常规施肥对土壤水稳性团聚体镉吸附解吸特性及化学形态的影响研究
秦秦 ,段海芹 ,宋科,孙丽娟,孙雅菲,周斌,薛永*
1.上海市农业科学院生态环境保护研究所,上海 201403;2.农业农村部绿色低碳重点实验室,上海 201403;3.上海海洋大学海洋生态与环境学院,上海 201306;4.上海市设施园艺艺术重点实验室,上海 201403
镉(Cd)是一种毒性较高的重金属元素,早在1993年就被国际癌症研究机构列为Ⅰ类致癌物。随着工农业的迅猛发展,中国农田土壤Cd污染日益严重。2014年《全国土壤污染状况调查公报》显示,Cd是目前中国土壤中污染程度最高的重金属污染物之一,点位超标率达7%。农田土壤中的Cd主要会产生两方面的危害,一方面是被作物根系吸收,在植株器官内富集并产生毒害,导致作物生长发育受阻,降低作物产量,造成农业经济损失(Gu et al.,2019);另一方面是在作物可食用部位累积,并通过食物链进入人体,诱发癌症、痛痛病和神经退化性等一系列疾病,威胁人类健康(Tinkov et al.,2018)。因此,如何降低Cd在农田土壤中的可移动性和生物活性,一直是国内外Cd污染土壤修复研究的重点。
土壤颗粒表面的吸附解吸反应决定了重金属在土壤中的移动性、毒性和生物有效性(McLaren et al.,1998)。土壤团聚体是土壤颗粒的一种主要存在形式,是矿物质、有机质和生物体相互作用在特定条件下的组合。由于不同粒径土壤团聚体颗粒与有机质和矿物质结合方式不同,它们对重金属在土壤微域环境中的吸附解吸行为以及生物有效性等方面会产生明显影响(王润珑等,2018;罗谦等,2020)。不同粒径团聚体颗粒对土壤重金属Cd吸附解吸行为的影响存在不同观点:一部分认为细颗粒团聚体对 Cd具有更高的初始吸附率和最大吸附量(Zhang et al.,2004;蒲昌英等,2018)。原因在于细颗粒团聚体比表面积大以及存在较多负电荷,会提供较大的接触力和吸附力,使得更多的重金属牢靠附着在细小颗粒团聚体表面(Li et al.,2020)。如Huang et al.(2014)和姜强等(2014)研究发现Cd等重金属元素主要向<53 µm 的粉-黏团聚体颗粒中富集。然而,另一部分学者却发现,一些新输入的重金属 Cd首先倾向于被粒径较大的粗颗粒团聚体吸附。如龚仓等(2012)和王润珑等(2018)发现,黑土中250—1000 µm的粗颗粒团聚体对Cd等重金属元素的负载因子最高,富集贡献率最大。可见,现有不同粒径团聚体颗粒对 Cd吸附解吸影响的研究结果不一,这可能与其自身理化特性差异有关。然而,目前关于不同粒径团聚体自身理化特性对 Cd吸附解吸行为的研究尚不充分,特别是对其吸附Cd化学形态的影响研究相对较少。施肥措施会影响土壤理化特性,导致土壤养分富集,改变有机质与土壤矿物之间的相互作用,增加团聚体颗粒之间的吸引力使土壤团聚体粒径组成和化学特性发生变化(刘哲等,2021),从而影响土壤重金属的移动性和生物活性。为此,本文通过两种施肥处理影响团聚体理化特性,比较研究不同理化特性的各粒径团聚体颗粒对 Cd吸附、解吸和赋存形态的影响,以期为农田土壤中Cd污染的预防、治理以及修复提供理论依据。
1 材料与方法
1.1 土壤样品采集与预处理
供试土壤为潮土,质地砂壤,试验点位于上海市奉贤区庄行镇上海市农业科学院综合实验站露天菜田土壤(30°53′39″N,121°23′47″E),主栽蔬菜作物为花菜。于2021年5月花菜收割后,按照“S”形5点混合采样法,分别采集不施肥和常规施肥(表1)两种处理(小区面积25 m2,灌溉及病虫害防治等其他田间管理方式均相同)的0—20 cm耕层土壤样品。将采集的土壤样品分别装袋带回实验室,拣去石砾、植物根系和碎屑残渣等,沿土壤的自然结构轻掰成直径为1 cm左右的小土块,经自然风干后,一部分用于土壤理化性质的测定;另一部分于−4 ℃冰箱保存,用于不同粒径水稳性团聚体的提取。

表1 各处理的施肥量Table 1 Fertilizers application rate relative to each treatment kg·hm−2
1.2 各粒径水稳性团聚体颗粒的提取
采用Cambardella et al.(1994)介绍的湿筛法筛分不同粒径的水稳性团聚体,将获得 2000—250 μm、250—53 μm、<53 μm 3种粒径范围的水稳性团聚体进行冷冻干燥后,备用。
1.3 原土及各粒径团聚体理化特性测定
参照鲁如坤(2000)的方法,原土及其各粒径团聚体 pH采用无二氧化碳蒸馏水浸提(水土质量比为 2.5꞉1),酸度计测定;全氮采用凯氏定氮法测定;有效磷采用0.5 mol·L−1碳酸氢钠溶液浸提,钼锑抗比色法测定;速效钾采用1 mol·L−1醋酸铵溶液浸提,火焰光度计法测定;有机质采用重铬酸钾容量法-外加热法分析测定;游离氧化铁用连二亚硫酸钠-柠檬酸三钠-碳酸氢钠(DCB)法测定;无定形氧化铁通过酸性草酸-草酸铵缓冲溶液浸提测定。
1.4 等温吸附解吸实验
利用氯化镉(CdCl2·5H2O)配制质量浓度为 1 g·L−1的Cd2+母液,根据实验需要稀释成质量浓度为2、5、10、20、30 mg·L−1的 Cd2+溶液,以 0.01 mol·L−1NaCl溶液作为支持电解质。准确称取两种施肥处理的原土及上述3种粒径土壤团聚体各0.50 g于若干50 mL塑料离心管中,加入25 mL配制的不同质量浓度的Cd2+溶液,每组实验设置4个平行样。然后,将离心管置于恒温(25 ℃)水浴震荡器以 180 r·min−1振荡 24 h,以 4000 r·min−1离心 10 min,取上清液过0.45 µm滤膜,利用火焰原子吸收分光光度计(Spectrum 3530AA型,上海光谱,中国) 测定溶液中Cd2+浓度。
解吸试验组别设计同上述吸附实验,在吸附平衡后,分别向离心管中加入25 mL空白NaCl溶液(0.01 moL·L−1),置于恒温(25 ℃)水浴震荡器以180 r·min−1继续振荡 24 h 后,以 4000 r·min−1离心10 min,取上清液过0.45µm滤膜,利用火焰原子吸收分光光度计(Spectrum 3530AA型,上海光谱,中国)测定溶液中Cd2+浓度。
1.5 原土及各粒径团聚体中Cd的赋存形态提取及测定
上述等温吸附解吸实验完成后,离心管中的残渣经冷冻干燥48 h后,参照Tessier(1979)五步提取法对两种施肥处理原土及其各粒径团聚体中Cd2+的5种赋存形态(可交换态、碳酸盐结合态、铁锰氧化物结合态、有机质结合态和残渣态)进行提取测定,用于分析各粒径团聚体固持Cd2+的化学形态变化。
1.6 原土及各粒径团聚体对Cd2+吸附解吸参数计算及模型拟合
1.6.1 吸附量、解吸量和解吸率计算
所有试验数据采用Microsoft Excel、SPSS 13.0和Origin 2018进行统计分析。两种施肥处理原土及各粒径团聚体对溶液中 Cd2+的吸附量按式(1)进行计算,解吸量按式(2)计算,解吸率按式(3)计算,具体公式如下:
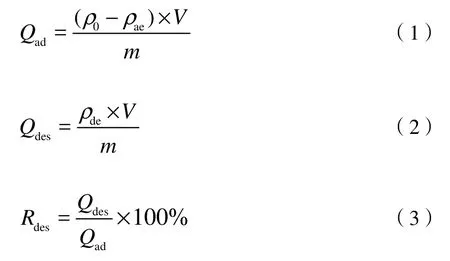
式中:
Qad和Qdes——Cd2+的吸附量和解吸量(mg·kg−1);
Rdes——Cd2+的解吸率(%);
ρ0——背景溶液中 Cd2+的初始质量浓度(mg·L−1);
ρae——吸附平衡后背景溶液中 Cd2+的残留质量浓度(mg·L−1);
ρde——解吸平衡后背景溶液中 Cd2+的质量浓度(mg·L−1);
V——吸附溶液的体积(mL);
m——土壤样品的质量(g)。
1.6.2 吸附/解吸等温模型
两种施肥处理原土及不同粒径团聚对溶液中Cd2+的等温吸附/解吸过程采用Langmuir方程(4)和Freundlich方程(5)进行拟合,拟合方程如下:
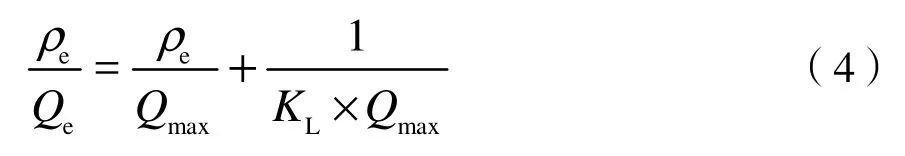

式中:
ρe——吸附/解吸平衡后背景溶液中残留 Cd2+质量浓度;
Qe和Qmax——平衡吸附/解吸量和最大吸附/解吸量;
KL——Langmuir模型参数,代表Cd2+最大吸附/解吸能量;
KF、n——Freundlich常数和Freundlich常数的亲和力值,分别代表吸附/解吸容量和吸附/解吸能力大小。
1.6.3 滞后系数的计算
滞后系数计算公式如下:

式中:
H——滞后系数;
n和ndes——Freundlich方程吸附和解吸过程中的吸附常数值。
2 结果与分析
2.1 土壤水稳性团聚体粒径分布及其理化特性
重金属的富集与土壤团聚体粒径分布及其理化特性存在密切关系。从表2中可以看出,常规施肥与未施肥处理土壤中各粒径团聚体颗粒总体分布规律相似,即大粒径团聚体(2000—250 µm)所占比例最高(>40%),<53 µm的粉-黏团聚体颗粒所占比例最小,但二者各粒径团聚体的组成比例存在一定差别。例如,经过常规施肥处理后,土壤中2000—250 µm大团聚体和250—53 µm的微团聚体含量均显著增加(P<0.05),增幅分别为 8.89%和10.6%,而<53 µm 的粉-黏团聚体含量却显著下降(P<0.05),降幅为 34.2%。表明长期投入肥料有利于土壤中微团聚体胶结成大团聚体,这与以往研究结果一致。如郭菊花等(2007)通过对水稻土进行不同施肥措施研究发现氮、磷等化学肥料进入土壤后会改变土壤团聚结构,导致土壤中大团聚体占比显著增加。刘哲等(2021)研究发现外源有机肥的输入,增加了土壤有机质等有利于团聚体形成稳定的重要胶结物质,促使微团聚体向大团聚体的胶结团聚,从而增加大团聚体的含量。
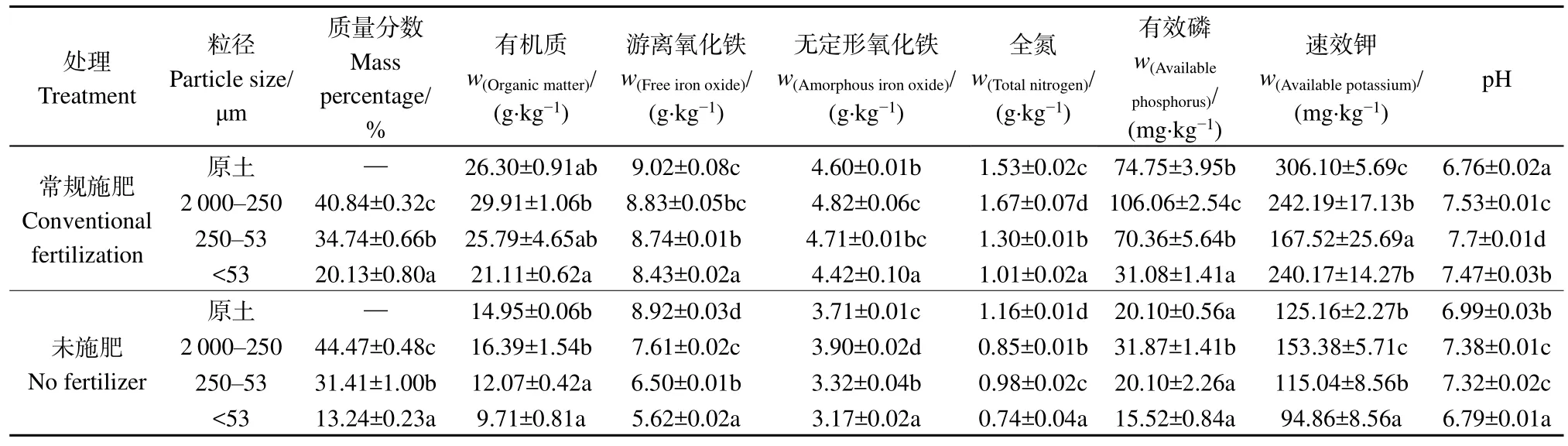
表2 不同施肥处理下原土及各粒径团聚体的理化性质Table 2 Effects of different fertilization treatments on physicochemical properties of bulk soil and different particle size aggregates
土壤有机质与污染物具有强络合能力,而团聚体是土壤有机质分解、转化及腐殖质形成的重要场所。常规施肥处理能够显著增加原土和各粒径团聚体颗粒的有机质含量,相比未施肥处理,增幅可达75.9%—117%。然而,随着团聚体粒径的减小,有机质含量呈现下降趋势,在<53 µm的粉-黏团聚体中有机质含量最少,表明有机质主要存储在大团聚体中,这与梁利宝等(2019)和刘旭等(2022)研究认为大团聚体有机碳含量较高的研究结果一致。另外,铁氧化物的吸附作用也是土壤重金属离子保留的主要机制之一。常规施肥处理能够增加原土和各粒径团聚体颗粒的游离氧化铁(特别是无定形氧化铁)含量。各粒径团聚体颗粒的游离氧化铁含量分布与有机质较为类似,即<53 µm的粉-黏团聚体颗粒组中游离氧化铁含量最少。
Kirkham(2006)研究认为,除有机质外,土壤pH是影响土壤重金属形态的另一个重要因素。本研究中,相比未施肥处理,常规施肥原土pH呈现下降趋势,但在团聚体层级,团聚体颗粒pH呈上升趋势,且>53 µm粒径团聚体pH显著高于<53 µm粒径,表明常规施肥能够促使酸性土壤团聚体(特别是大粒径团聚体)pH升高。产生这种结果的主要原因可以用原土及其各粒径团聚体的游离氧化铁含量及组成来解释。土壤中微生物分解有机质释放大量的电子和质子,使游离氧化铁(特别是无定形氧化铁)等氧化性物质接受电子发生还原,同时也消耗大量的质子,导致酸性土壤pH升高(贺前锋等,2016)。与翟龙波等(2019)研究结果一致,常规施肥处理能够显著提高原土及其团聚体的全氮、有效磷和速效钾含量,且不同粒径土壤团聚体之间存在显著差异。其中,2000—250 µm粒径团聚体的全氮、有效磷和速效钾含量显著高于<53 µm粒径团聚体,表明大粒径团聚体对于氮、磷、钾等矿质营养的存储能力更大。
2.2 不同粒径水稳性团聚体中Cd2+的吸附特性
不同粒径土壤团聚体对 Cd2+的吸附行为,将影响其在土壤中的环境风险。由图1可以看出,原土及其各粒径团聚体对 Cd2+的吸附量随着平衡溶液中Cd2+浓度的增加而增加,各粒径团聚体对 Cd2+的吸附量高于原土,但随着粒径的减小吸附量逐渐降低,说明在大粒径团聚体中 Cd2+存在明显的富集现象。这与以往研究认为小粒径颗粒比表面积大以及存在负电荷(Lombi et al.,2000;龚仓等,2012),对Cd2+的吸附能力更高的结果不一致。产生这种分歧的主要原因,可能与各粒径团聚体中有机质的含量有关(Lund et al.,1991)。在本研究中,2000—250 μm 的大团聚中有机质含量最高(表1)。通常有机质含量与吸附量成正相关(王润珑等,2018)。土壤颗粒有机质含量越高,不仅产生物理吸附的能力越强,更重要的是其他各种吸附的吸附点位也会越多,从而吸附能力越大(陈朕等,2013)。本研究中,Cd2+吸附量均以高有机质含量的常规施肥处理土壤颗粒组最大(图1c和图1d),也验证了上述推测。
土壤颗粒对 Cd2+的吸附主要包括离子交换吸附、络合吸附和物理吸附等。络合吸附和物理吸附等往往被认定为专性吸附,对 Cd2+的固定意义较大;而离子交换吸附认定为非专性吸附,相比专性吸附而言,所固定的 Cd2+稳定性较弱。在本研究中,不同粒径团聚体对 Cd2+的吸附趋势变化总体一致。即当平衡溶液中 Cd2+浓度较低时,原土及各粒径团聚体对 Cd2+的吸附均呈快速上升的趋势,但随着平衡溶液 Cd2+浓度的增加,上升趋势逐渐减缓,吸附速率减小(图1)。这主要是由于土壤颗粒表面不均一,产生了两种不同吸附位点,即高能吸附位点和低能吸附位点(熊东等,2012)。在吸附开始时,低浓度的 Cd2+优先与土壤颗粒表面的高能吸附位点结合,对 Cd2+的亲和力较大,吸附速度较快,吸附过程以专性吸附为主,随着平衡液中 Cd2+浓度的增加,土壤颗粒表面的高能吸附位点被逐渐占据,Cd2+被低能吸附位点吸附,非专性吸附能力增强。当土壤颗粒表面的吸附点位全部被覆盖,溶液中的 Cd2+和土壤颗粒中的 Cd2+形成了动态平衡(Huang et al.,2014)。
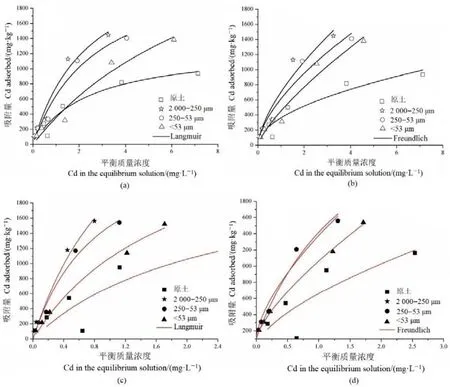
图1 原土及各粒径团聚体对Cd2+的等温吸附曲线Figure 1 Adsorption isotherm of Cd2+ in bulk soil and different particle size aggregates
将原土及各粒径团聚体吸附过程进行Langmuir方程(图1a和图1c)和Freundlich方程拟合(图1b和图1d),拟合参数列于表3。从表3可以看出,两种方程均能较好地模拟土壤颗粒对Cd2+的吸附过程,但常规施肥处理原土及各粒径团聚体对Cd2+的吸附过程更符合Freundlich方程,而未施肥处理原土及各粒径团聚体对 Cd2+的吸附过程更符合Langmuir方程,表明常规施肥处理后,由于有机质和铁氧化物等胶结物质含量的增加(表1),Cd2+在原土及各粒径团聚体表面可以达到多层吸附,包含复杂的专性吸附作用,吸附发生在表面与内层(刘桃妹等,2021),而未施肥处理原土及各粒径团聚体表面为单层吸附。在Freundlich方程中,KF值越大,表示土壤颗粒对Cd2+的吸附能力越强,即土壤吸附能力大小顺序为 2000—250 μm 粒径>250—53 μm粒径> <53 μm粒径>原土,表明大粒径团聚体(2000—250 μm)对Cd2+的吸附能力更强。在Langmuir方程中,KL与Qmax的乘积(MB,C)通常用于表征吸附剂对Cd2+的最大缓冲容量,表示土壤对重金属元素的缓冲性能,可以作为环境重金属容量的评价指标(龙新宪等,2000)。从表3可以得出,常规施肥处理的原土和各粒径团聚体颗粒Cd2+的缓冲容量分别为 995.38 mg·kg−1(原土)、2817.78 mg·kg−1(2000—250 μm)、2195.63 mg·kg−1(250—53 μm)、1665.18 mg·kg−1(<53 μm),比未施肥处理依次高出90.4%、165.8%、149%、215%,这说明常规施肥处理后,原土和各粒径团聚体颗粒对Cd2+的缓冲能力明显提升,其中 2000—250 μm大粒径团聚体的缓冲能力最强。

表3 原土及不同粒径团聚体对Cd2+的等温吸附方程拟合参数Table 3 Parameters of isothermal adsorption of Cd2+ in bulk soil and different particle size aggregates
从原土及各粒径团聚体对 Cd2+的最大吸附量与其理化性质的相关分析结果(表 4)来看,无论施肥与否,各粒径团聚体对 Cd2+的吸附量与有机质、游离氧化铁(特别是无定形氧化铁)及有效磷含量呈现显著甚至极显著的正相关。由此推测,本研究中大粒径团聚体(2000—250 μm)对Cd2+的吸附能力较高,与其有机质、游离氧化铁(特别是无定形氧化铁)和有效磷含量较高有着直接关系。有机质是决定颗粒组吸附Cd2+的重要因素之一,主要通过改变颗粒组表面负电荷数量以及与 Cd2+发生不同的化学反应(如络合、螯合和离子交换)而起作用。游离氧化铁是Cd2+的络合吸附剂,游离氧化铁含量越高,对Cd2+的络合吸附作用越强。研究发现有机质或游离氧化铁(特别是无定形氧化铁)含量减少,专性吸附下降,黄壤原土及各粒径团聚体对Cd2+的吸附作用力减弱(熊东等,2012)。当磷浓度增加,团聚体表面净负电荷量增大(文勤亮等,2014),通过静电作用吸附的 Cd2+也越多。与此相同,许海波等(2013)也研究发现外源磷肥施入可增加土壤胶体表面净电荷,进而不断加强粒级中Cd2+的静电吸附作用。因此,常规施肥处理的大团聚体颗粒比其未经施肥处理的对 Cd2+的吸附缓冲能力更高。此外,土壤团聚体颗粒对Cd2+的吸附量与pH和全氮、速效钾等矿质养分含量也存在一定相关性,但相关程度受施肥处理的影响。如常规施肥处理后,土壤全氮与各粒径团聚体对Cd的吸附量呈极显著正相关(P<0.01),相关系数为0.985,这可能是因为含氮化肥的施入增加了土壤团聚体对 Cd的吸附。张洪等(2009)研究氮肥对团聚体Cd吸附影响的研究也得到类似的研究结果。

表4 不同粒径团聚体对Cd2+最大吸附量与其理化性质的相关性Table 4 Correlation analysis between maximum adsorbance of Cd2+ and physicochemical properties of different particle size aggregates
2.3 不同粒径水稳性团聚体对Cd2+解吸特性的影响
解吸量/解吸率通常用来表征胶体表面活性吸附位点与重金属离子结合牢固程度,Cd2+在土壤中的解吸状况将直接影响其对地下水、土壤生物及作物的潜在污染风险。由图2可知,Cd2+在各粒径团聚体中的解吸量趋势相同,解吸量均随着吸附量的增加而增大,且呈正相关,这与吸附过程有密切的关系。当Cd2+添加浓度较低时,团聚体颗粒与Cd2+的络合反应以专性吸附为主,在离子水合作用之外,共价键或氢键也在起作用,与Cd2+的结合能力较强,这部分专性吸附具有不可逆性,解吸困难(李春玲等,2009)。随着吸附量的增加,团聚体颗粒对Cd2+的专性吸附逐渐减少,离子交换吸附的 Cd2+逐渐增加,表面吸附点位与Cd2+的结合能力逐渐减弱,解吸作用增强(徐温新等,2008)。本研究发现,常规施肥处理后原土和各粒径团聚体对Cd2+的解吸量(图2b)明显低于未施肥处理(图2a),常规施肥原土及各粒径团聚体对Cd2+的解吸量由小到大依次为2000—250 µm 粒径<原土<250—53 µm 粒径<<53 µm 粒径,与熊东等(2012)对水稻土解吸特性研究结果相似,表明大粒径团聚体颗粒对 Cd2+的固持能力大于其它粒径,在土壤 Cd2+迁移风险阻控方面起到最关键的作用。当 Cd2+添加浓度为 2—30 mg·L−1时,常规施肥处理的原土及各粒径团聚体中Cd的解吸率也偏低于未施肥处理,分别为0.37—13.5%、未检出—14.2%、未检出—17.2%、3.54%—20.1%(表5),以大团聚体(2000—250 µm)中Cd2+的解吸率最低,说明常规施肥处理后,各粒径团聚体颗粒与 Cd2+的结合能力增强,特别是大粒径团聚体吸附的 Cd2+稳定性较高,不易于发生因解吸而导致的二次污染。
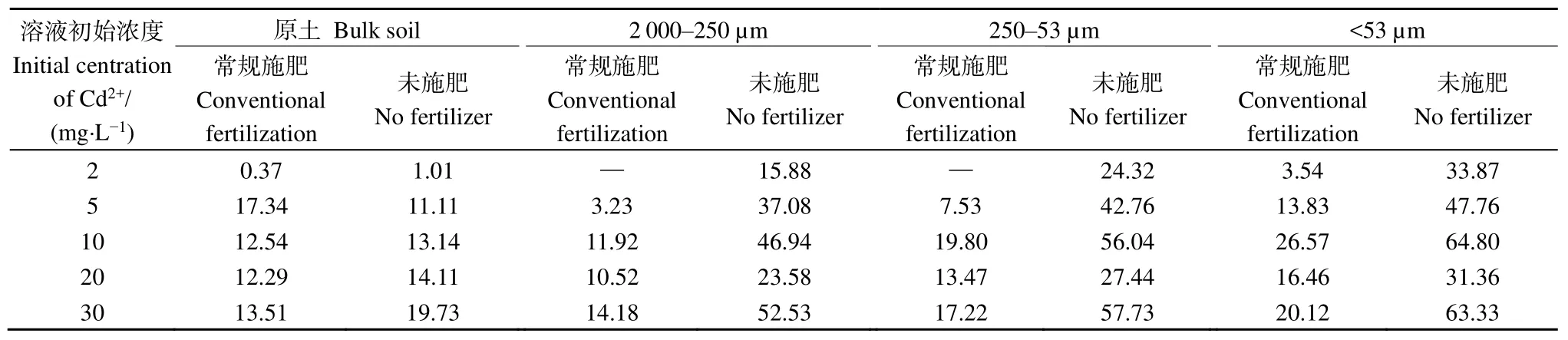
表5 原土及各粒径团聚体对Cd2+的解吸率Table 5 Desorption rates of Cd2+ by bulk soil and different particle size aggregates %

图2 原土及各粒径团聚体对Cd2+解吸量与吸附量的关系Figure 2 The relationship between Cd2+ desorption and adsorption capacity by bulk soil and different particle size aggregate relative to treatments
相比吸附等温线,原土和各粒径团聚体的解吸等温线呈轻微非线性(图3),非线性弱于吸附等温线,表明其解吸过程并非吸附的可逆过程,解吸过程具有明显的迟滞效应。相比未施肥处理,常规施肥处理的各粒径团聚体Cd解吸滞后系数更大(表6)。滞后性越强,Cd2+在固相介质中解吸释放越难,Cd2+在同一施肥处理的3种粒径团聚体中的解吸难易程度为:2000—250 µm 粒径>250—53 µm 粒径>53 µm粒径。这种解吸现象会导致Cd在常规施肥土壤特别是大粒径团聚体中的短暂停留,减少Cd污染的扩散。
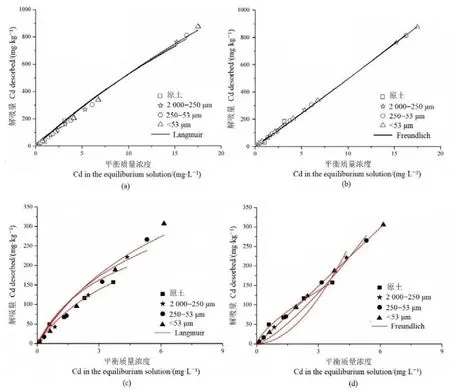
图3 原土及各粒径团聚体对Cd2+的等温解吸曲线Figure 3 Desorption isotherm of Cd2+ in bulk soil and different particle size aggregate
将以上解吸过程进行Langmuir方程和Freundlich方程拟合,拟合参数列于表 6。从表中可以看出,Langmuir方程对未施肥处理的原土和各粒径团聚体中Cd2+的解吸数据拟合效果较好,而常规施肥处理原土和各粒径团聚体中Cd2+的解吸数据用Freundlich方程拟合更好。表明常规施肥处理原土及各粒径团聚体主要以表面非均匀多层解吸为主,而表面单层均匀吸附比例低于前者。根据 Langmuir方程中的Qmax可知,相比未施肥处理,Cd2+在经施肥处理的原土及不同粒径团聚体中的最大解吸量理论值相对较低,由低到高的顺序依次为2000—250 µm粒径<原土<250—53 µm粒径<53 µm粒径,这与试验研究结果一致,表明 2000—250 µm 大团聚体对Cd2+的固持能力更强,原土和 250—53 µm 微团聚体颗粒居中,而53 µm粉-黏团聚体颗粒对Cd固持能力较低,环境迁移释放风险更高。施肥能够影响土壤理化特性,改善土壤团聚结构,从而影响重金属固持能力。通过分析原土及各粒径团聚体中Cd2+最大解吸量与其理化性质的相关性发现,与吸附过程相反,各粒径团聚体对Cd2+的解吸量与颗粒组中的游离氧化铁(特别是无定形氧化铁)、有效磷和有机质含量呈显著甚至极显著负相关(P<0.01)(表7)。表明土壤游离氧化铁(特别是无定形氧化铁)、有效磷和有机质含量等理化性质是导致各粒径团聚体对Cd2+固持能力差异的主要原因。本研究中,大粒径团聚体中这些胶结物质及矿质营养元素含量较高,因此其对Cd2+具有很强的固定能力,从而降低Cd2+的环境迁移风险。此外,pH、全氮和有效钾含量也与各粒径团聚体对Cd2+的解吸量存在一定相关性,但相关程度受施肥的影响。未施肥处理土壤各粒径团聚体对Cd2+的解吸量与其pH和有效钾含量呈显著负相关,与全氮含量无显著相关关系;常规施肥处理土壤各粒径团聚体对Cd2+的解吸量却与其全氮含量呈极显著负相关,这说明由常规施肥导致的氮素营养增加也是促使大粒径团聚体对Cd2+固持能力增强的主要原因之一。
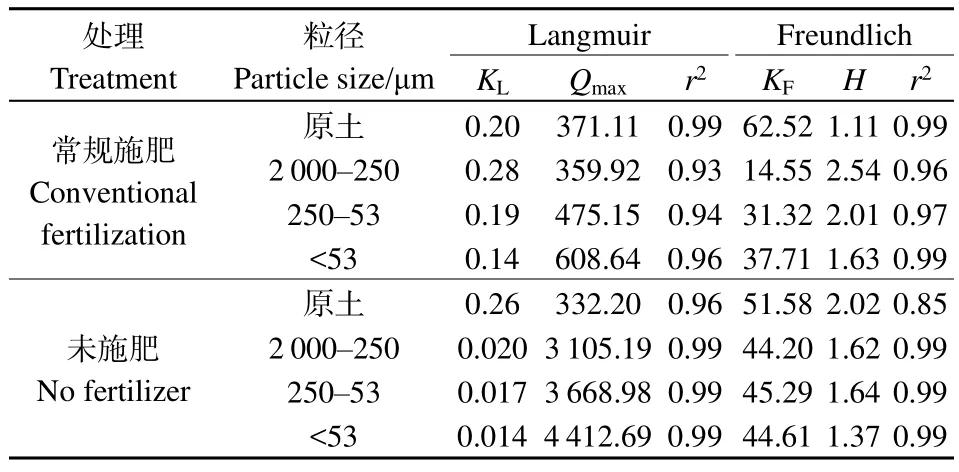
表6 原土及不同粒径团聚体对Cd2+的等温解吸方程拟合参数Table 6 Parameters of isothermal desorption of Cd2+ in bulk soil and different particle size aggregates

表7 不同粒径团聚体对Cd2+解吸量与其理化性质的相关性Table 7 Correlation analysis between maximum desorption capacity of Cd2+ and physicochemical properties of different particle size aggregates
2.4 不同粒径水稳性团聚体Cd2+的形态分析
外源重金属进入土壤后,通过溶解、沉淀、络合吸附等各种反应,可形成不同的化学形态,对植物表现出不同的生物活性和毒性。本研究对解吸后常规施肥与未施肥处理的原土及不同粒径团聚体中固持 Cd2+的化学形态进行分析,结果如图 4所示。由图4a可知,未施肥处理土壤的各粒径团聚体中Cd2+各形态含量和比例与原土规律相似,主要以交换态为主,其中,2000—250 μm、250—53 μm、<53 μm 团聚体上交换态的 Cd所占比例分别为66.0%、73.5%、72.9%,可见2000—250 μm大团聚体中残留的交换态Cd所占比例相对较低,说明大粒径团聚体上固持的Cd更稳定,生物活性更低。常规施肥处理(图4b)后,2000—250 μm、250—53 μm、<53 μm粒径团聚体中可交换态Cd所占比例分别降低了41.1%、16.9%、10.3%;碳酸盐结合态Cd所占比例分别增加了80.1%、48.3%、136%;铁锰氧化物结合态Cd所占比例分别增加了116%、20.7%、43.7%;有机结合态Cd所占比例分别降低了17.7%、26.3%、33.7%;残渣态Cd所占比例分别增加了75.7%、56.6%、3.83%。表明土壤经过常规施肥处理后,团聚体(特别是2000—250 μm粒径)中固持的交换态Cd和有机结合态Cd含量显著降低(P<0.05),而碳酸盐结合态Cd、铁锰氧化物Cd和残渣态Cd含量显著增加(P<0.05)。这说明施肥处理增加了团聚体组分的有机胶结物质,改善了土壤结构(Huang et al.,2010),从而促使各团聚体组分中固持的 Cd由易于被植物吸收的交换态Cd转化为不易于被植物吸收的碳酸盐结合态,再逐渐通过土壤胶体吸附、络合和化学反应转化为难于被植物吸收的铁锰氧化物结合态和残渣态形式(岳平等,2008)。相比可交换态形式,结合态和残渣态Cd的植物利用潜力更低,特别是残渣态较为稳定,在自然条件下不易释放出来,难以被植物利用(Heet al.,1994;Yuan et al.,2011)。本研究发现常规施肥处理Cd结合态部分的增加主要来自粒径2000—250 μm的大团聚体。这主要是大粒径团聚体中的有机质、游离氧化铁相对含量较高,易于发生络合或螯合作用、胶体吸附、专性吸附等,导致更多的 Cd2+因吸附作用而存在于团聚体中,从而导致结合态Cd含量增加。郁红艳等(2016)也研究发现,pH、有机质含量和 CEC提高将促使团聚体层级更多交换态Cd向结合态转化。但值得注意的是,相比大团聚体,本研究中小粒径团聚体中残留的 Cd交换态比例更高,而且较少向活性较低的结合态Cd转化,由于交换态 Cd更易于被植物吸收或迁移至深层土壤或地下水中,在外部因素(如降雨、灌溉、施肥等)的影响下,这些小粒径团聚体携带的Cd存在局部富集的可能,因此需要引起足够的重视。
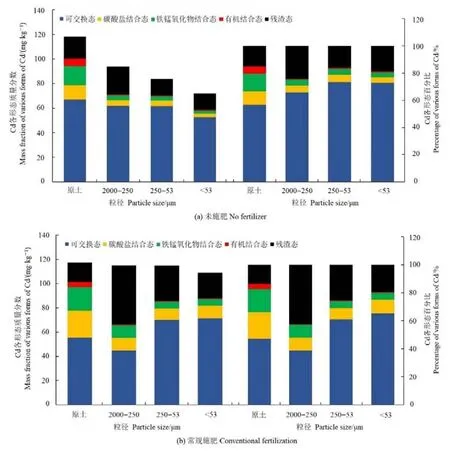
图4 原土与各粒径团聚体中各形态Cd分布Figure 4 Distribution of Cd in bulk soil and different particle size aggregate
3 结论
本文以长期常规施肥方式改变土壤团聚体理化特性,研究原土及各级粒径团聚体对Cd2+的吸附解吸特性及其形态赋存情况,得出以下结论:
(1)无论施肥与否,2000—250 µm粒级团聚体占比最高,有机质、游离氧化铁(包括无定形氧化铁)、全氮、有效磷和速效钾等团粒胶结物质优先存储于2000—250 µm粒级团聚体中。相比未施肥处理,常规施肥处理能够促使大粒径团聚体(>53 µm)结构生成,增加其有机质、游离氧化铁等上述团粒胶结物质含量。
(2)常规施肥处理的团聚体颗粒对Cd2+的吸附等温线符合Freundlich方程,Cd2+在团聚体颗粒表面可以发生多层吸附。随着Cd2+初始浓度增加,各粒径团聚体对Cd2+吸附量增加,吸附量由大到小依次为 2000—250 μm 粒径>250—53 μm 粒径>(<53 μm)粒径>原土,吸附能力主要与各粒级有机质含量、游离氧化铁(包括无定形氧化铁)含量、有效磷含量和全氮含量呈显著正相关,Cd2+的解吸率与此顺序相反。土壤中2000—250 μm粒级团聚体对Cd2+的固持能力较强,<53 μm 粒级团聚体颗粒中Cd2+释放风险更高。
(3)各粒径团聚体固持的Cd2+主要以活性较高的交换态形式存在,相比于大粒径团聚体,小粒径团聚体上固持交换态Cd比例更高。常规施肥处理能够促使团聚体固持的交换态Cd向更稳定的结合态和残渣态Cd转化,但Cd结合态增加部分主要来自于粒径2000—250 μm的大团聚体,而小粒径团聚体中固持的Cd较少向结合态转化,因此需要对小粒径团聚体固持Cd的环境风险进行重点关注。

