左炔诺孕酮宫内缓释系统对子宫腺肌病痛经患者卵巢功能及神经生长因子、转化生长因子β1的影响
王兵


[摘要] 目的 探討左炔诺孕酮宫内缓释系统对子宫腺肌病痛经患者卵巢功能及神经生长因子(NGF)、转化生长因子(TGF)-β1表达的影响。 方法 选取2018年1月至2020年5月大连市妇女儿童医疗中心(集团)收治的90例子宫腺肌病患者分为观察组与对照组各45例。对照组给予常规治疗,观察组给予常规治疗联合左炔诺孕酮宫内缓释系统治疗。比较两组治疗前后子宫内膜厚度、两组治疗不同时间点的VAS评分、两组治疗前后血清CA125含量及两组治疗前后血清NGF、TGF-β1含量。 结果 两组治疗后的子宫内膜厚度[(7.14±1.02)mm和(9.43±1.85)mm]低于治疗前[(12.89±3.82)mm和(12.74±4.15)mm](P<0.001),观察组低于对照组[(7.14±1.02)mm vs.(9.43±1.85)mm](P<0.05)。观察组治疗第1个月[(4.14±0.21)分vs.(6.24±0.17)分]、2个月[(3.40±0.15)分vs.(5.25±0.42)分]、3个月[(4.15±0.44)分vs.(2.87±0.27)分]的痛经VAS评分低于对照组(P<0.05)。两组治疗后的血清CA125值[(11.84±4.89)×103U/L和(31.67±3.81)×103U/L]低于治疗前[(77.42±33.87)×103U/L和(77.10±28.48)×103U/L](P<0.001),观察组低于对照组[(11.84±4.89)×103U/L vs. (31.67±3.81)×103U/L](P<0.001)。两组治疗后的血清NGF、TGF-β1含量高于治疗前(P<0.001),观察组高于对照组(P<0.001)。 结论 左炔诺孕酮宫内缓释系统在子宫腺肌病患者的应用能缓解痛经程度,改善患者的卵巢功能,抑制NGF、TGF-β1的释放,减少子宫内膜厚度。
[关键词] 左炔诺孕酮宫内缓释系统;子宫腺肌病;痛经;卵巢功能;神经生长因子;转化生长因-β1
[中图分类号] R711.74 [文献标识码] B [文章编号] 1673-9701(2022)01-0077-03
Effect of levonorgestrel releasing intrauterine system on ovarian function, nerve growth factor and transforming growth factor-β1 in patients with adenomyosis and dysmenorrhea
WANG Bing
Outpatient Operating Room, Dalian Women and Children Medical Center (Group), Dalian 116021, China
[Abstract] Objective To investigate the effect of levonorgestrel releasing intrauterine system(LNG-IUS) on the ovarian function and expressions of nerve growth factor (NGF) and transforming growth factor (TGF)-β1 in patients with dysmenorrhea of adenomyosis. Methods A total of 90 patients with adenomyosis admitted to Dalian Women and Children Medical Center (Group) from January 2018 to May 2020 were divided into observation group and control group, with 45 cases in each group. The control group were given conventional treatment, and the observation group were given conventional treatment combined with LNG-IUS. The endometrial thicknesses before and after treatment, VAS scores at different time points of treatment, serum CA125 levels before and after treatment, and serum NGF and TGF-β1 levels before and after treatment were compared between the two groups. Results The endometrial thicknesses in the two groups after treatment [(7.14±1.02) mm and (9.43±1.85) mm] were lower than those before treatment[ (12.89±3.82) mm and (12.74±4.15) mm] (P<0.001). The endometrial thickness in the observation group was lower than that in the control group [(7.14±1.02) mm vs. (9.43±1.85) mm] (P<0.05). The VAS scores of dysmenorrhea in the observation group at 1, 2 and 3 months after treatment were lower than those in the control group [(4.14±0.21) points vs. (6.24±0.17) points, (3.40±0.15) points vs. (5.25±0.42) points, (4.15±0.44) points vs. (2.87±0.27) points] (P<0.05). The serum CA125 levels in the two groups after treatment [(11.84±4.89)×103U/L and (31.67±3.81)×103U/L] were lower than those before treatment [(77.42±33.87)×103U/L and (77.10±28.48)×103U/L] (P<0.001). The serum CA125 level in the observation group was lower than that in the control group [(11.84±4.89)×103U/L vs. (31.67±3.81)×103U/L] (P<0.001). Serum NGF and TGF-β1 levels in the two groups after treatment were higher than those before treatment (P<0.001). Serum NGF and TGF-β1 levels in the observation group were higher than those in the control group (P<0.001). Conclusion LNG-IUS can relieve the degree of dysmenorrhea, improve the ovarian function, inhibit the release of NGF and TGF-β1, and reduce the endometrial thickness in patients with adenomyosis.
[Key words] Levonorgestrel releasing intrauterine system; Adenomyosis; Dysmenorrhea; Ovarian function; Nerve growth factor; Transforming growth factor-β1
子宫腺肌病作为一种常见的妇科良性病变,除了伴随有严重痛经外,也存在卵巢异常,主要临床特点是经期较长、出血量较多且周期不规律。目前学者对子宫腺肌病的发病原因尚不明确,可能与激素、炎症因子过量分泌或内分泌失调等引起,少数患者会存在恶变的风险。子宫切除是子宫腺肌病患者的主要治疗手段,但是对于患者的创伤比较大[1-2]。子宫腺肌病患者当前在临床上常用口服药物治疗,主要适应于有生育要求的患者,但是目前无根治性的有效药物[3]。左炔诺孕酮宫内缓释系统(levonorgestrel releasing intrauterine system,LNG-IUS)是一种外观呈“T”形带有尾丝的宫内节育器,也被称为曼月乐,其能直接作用于子宫内膜,间接抑制前列腺素和血栓素A2的合成,使异位内膜萎缩、退化,从而达到临床治疗作用[4-5]。神经生长因子(nerve growth factor,NGF)广泛分布于机体各组织器官,是维持机体神经系统正常功能的重要因子[6]。转化生长因子(transforming growth factor,TGF)-β1可调节机体炎症因子表达水平,也可影响机体的内分泌功能[7]。本研究通过探讨左炔诺孕酮宫内缓释系统对子宫腺肌病痛经患者卵巢功能及NGF、TGF-β1的影响,现报道如下。
1 资料与方法
1.1 一般资料
选择2018年1月至2020年5月在大连市妇女儿童医疗中心(集团)诊治的90例子宫腺肌病患者,纳入标准:①患者年龄28~50岁,处于经期;②根据临床表现及B超确诊为子宫腺肌病[1];③患者或家属知情同意本研究,经医院医学伦理委员会批准同意;④患者依从性好,同意并能按要求定期随访;⑤大连市妇女儿童医疗中心(集团)批准了本研究。排除标准:①伴有子宫肌瘤、宫颈癌或子宫内膜癌等者;②合并严重心肝肾异常者;③具有生殖道急性炎症者;④近期进行免疫抑制剂治疗者;⑤合并子宫附件区囊肿者;⑥伴有严重精神疾病,患者精神状态不佳,无法配合治疗者[2]。根据随机信封抽签原则将患者分为观察组与对照组各45例,两组患者一般资料比较,差异无统计学意义(P>0.05),具有可比性。见表1。
1.2 方法
1.2.1 对照组 给予常规治疗,于经期皮下注射醋酸亮丙瑞林微球(北京博恩特药业有限公司,国药准字H20093809,规格:3.75 mg/支),1个月注射1次,共3次。
1.2.2 观察组 在对照组治疗的基础上给予左炔诺孕酮宫内缓释系统治疗,于月经期4~5 d宫内放置左炔诺孕酮宫内缓释系统(商品名:曼月乐,拜耳制药有限公司,国药准字J20140088)。
1.3 观察指标及评价标准
①采用视觉模拟评分法(visual analogue scale,VAS)在治疗第1、2、3個月进行痛经评估,按疼痛等级计为0~10分[8];②在治疗前后抽取患者空腹肘静脉血2~3 ml,室温静置30 min后,3000 rpm/min离心10 min,取上层血清,采用化学发光法检查卵巢癌相关抗原(ovarian cancer associated antigen,CA125)水平;③取上述血清学指标,采用酶联免疫法检测血清NGF、TGF-β1含量;④在治疗前后测定与记录患者的子宫内膜厚度。
1.4 统计学方法
采用SPSS 21.0统计学软件进行数据分析,计量资料以均数±标准差(x±s)表示,组间比较采用t检验,组内不同时间点行重复测量方差分析;计数资料以[n(%)]表示,组间比较采用χ2检验,P<0.05为差异有统计学意义。
2 结果
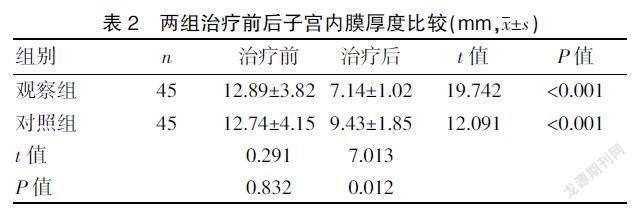
2.1 两组治疗前后子宫内膜厚度比较
两组治疗后的子宫内膜厚度低于治疗前(P<0.001),观察组低于对照组(P<0.05)。见表2。
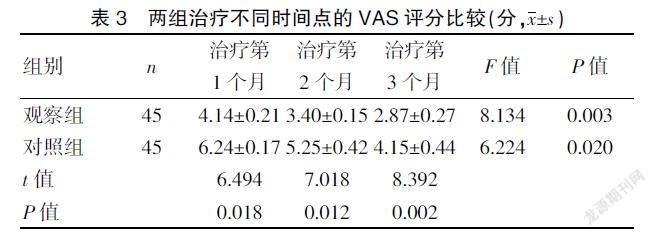
2.2 两组治疗不同时间点的VAS评分比较
观察组治疗第1、2、3个月的痛经VAS评分低于对照组(P<0.05)。见表3。
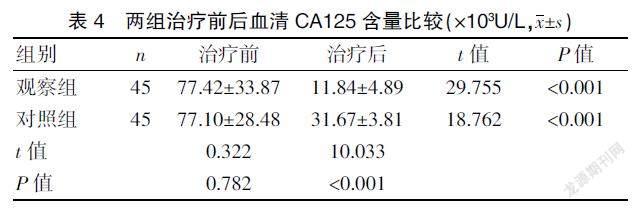
2.3 两组治疗前后血清CA125含量比较
两组治疗后的血清CA125低于治疗前(P<0.001),观察组低于对照组(P<0.001)。见表4。
2.4 两组治疗前后血清NGF、TGF-β1含量比较
两组治疗后的血清NGF、TGF-β1含量高于治疗前(P<0.001),观察组高于对照组(P<0.001)。见表5。
3 讨论
子宫腺肌病作为一种常见性的良性妇科疾病,多见于育龄期女性,是指子宫内膜腺体和间质侵入子宫肌层形成的弥漫或局限性病变。临床表现为月经量明显增多、痛经、慢性盆腔炎、子宫增大等。该病的发生机制还不明确,在病理上可表现为子宫肌层内弥漫性生长,子宫肌层出现内膜周期性增生,影响到子宫肌壁的收缩,使子宫壁增厚与子宫增大,从而使患者在临床上出现内膜周期性增生、出血,临床对该病尚缺乏统一规范的治疗方案,对病情轻者以各种保守治疗;病情重者以子宫切除为主[8]。在药物治疗中,亮丙瑞林治疗效果最好,但是不宜长期使用,很多患者在停药后容易复发;同时亮丙瑞林的使用费用也一直比较高,也影响其在临床的应用。本研究显示,两组治疗后的子宫内膜厚度低于治疗前(P<0.001),观察组低于对照组(P<0.05);观察组治疗第1、2、3个月的痛经VAS评分低于对照组(P<0.05)。从机制上分析,左炔诺孕酮宫内缓释系统环作为宫内节育器之一,其含有左炔诺孕酮,形状为“T”形,其表面有一层专用的控释膜覆盖,可以长时间释放出少量的左炔诺孕酮(20 μg/24 h,可维持5年左右),并且能够保持平衡状态,从而有利于缓解患者的疼痛程度,降低子宫内膜厚度[9-10]。并且能够直接在患者的宫腔内进行局部作用,增强子宫的血管阻力,减少子宫出血量,抑制机体释放的前列腺素进而促进患者的病灶退化,使子宫平滑肌萎缩,其次通过左炔诺孕酮宫内缓释系统环携带的激素作用能抑制体内的雌激素受体活性,起到拮抗子宫内膜增生,促进子宫变薄的作用。
子宫肌腺病是富血管性疾病,对缺血、缺氧比较敏感,病灶的生长需要血液的供应和血液中性激素及其他生长因子的刺激。相关研究显示,子宫腺肌症患者的卵巢功能代谢可出现紊乱现象,使雌激素受体与孕激素受体呈现过高表达,会引起其雌激素与孕激素比例平衡状态受破坏,从而导致严重并发症的发生[11]。也有研究显示,雌激素与孕激素的异常状态很有可能引起子宫腺肌病的出现,缓解二者的异常表达能改善患者的预后[12]。本研究显示,两组治疗后的血清CA125低于治疗前(P<0.001),观察组低于对照组(P<0.001),表明左炔诺孕酮宫内缓释系统在子宫腺肌病患者的应用能改善患者的卵巢功能。从机制上分析,左炔诺孕酮宫内缓释系统环可以减轻子宫内膜雌激素、孕激素受体的免疫活性,可以利用二者水平的调节而发挥阻滞内膜增生的作用,从而调节机体性激素分泌平衡。NGF及其受体广泛分布于中枢神经系统,有利于减轻或防止继发性病理损害的发生[13]。TGF-β1水平可反映机体的炎症平衡状态,可以促进成骨细胞的增殖分化[14-15]。本研究显示,两组治疗后的血清NGF、TGF-β1含量高于治疗前(P<0.001),观察组高于对照组(P<0.001),表明左炔诺孕酮宫内缓释系统在子宫腺肌病患者中的应用能促进NGF、TGF-β1的释放。不过长期应用左炔诺孕酮宫内缓释系统可减轻孕激素依赖性前列腺素脱氢酶活性,导致血管脆性提高,在临床上也需要慎重使用。同时本研究也存在一定的不足,随访观察的时间比较短,纳入患者的数量比较少,将在后续研究中进行探讨。
综上所述,左炔诺孕酮宫内缓释系统在子宫腺肌病患者的应用能缓解痛经程度,改善患者的卵巢功能,抑制NGF、TGF-β1的释放,减少子宫内膜厚度。
[参考文献]
[1] 杜洁贤,王康,田彩,等.不同预处理方式对曼月乐治疗弥漫性大子宫腺肌病效果的影响研究[J].中国妇幼保健,2020,35(2):199-202.
[2] 柴瑞瑞.促性腺激素释放激素激动剂联合曼月乐治疗巨大子宫腺肌病的效果[J].河南医学研究,2020,29(9):1654-1655.
[3] 胡倩,黄帅,吕秋波,等.左炔诺孕酮宫内释放系统治疗子宫腺肌病的下移率及其相关因素的分析[J].生殖医学杂志,2020,29(3):354-357.
[4] 杨赛花,陈滢.曼月乐联合GnRH-a對子宫腺肌病患者子宫内膜容受性的影响[J].中国妇幼保健,2020,35(13):2382-2385.
[5] 贺凤,付丹.醋酸亮丙瑞林缓释微球对子宫腺肌病患者月经量与子宫体积的影响[J].山西医药杂志,2019,48(7):810-812.
[6] 吴晓虹,张文杰,武冬娜.子宫腺肌病患者采用曼月乐联合小剂量米非司酮治疗的效果及对血清神经生长因子可溶性CD147血管内皮生长因子水平变化的影响[J].河北医学,2019,25(1):50-54.
[7] 张丽凤,杨慧,张信美,等.左炔诺孕酮宫内节育系统治疗子宫腺肌病患者的疗效和不良反应观察[J].浙江大学学报(医学版),2019,48(2):130-135.
[8] Baboo Kalianee Devi,陈正云,张信美.子宫腺肌病患者药物治疗进展[J].浙江大学学报(医学版),2019,48(2):142-147.
[9] 许艳萍,张惠文,黄水英,等.GnRH-a联合宫腔镜及曼月乐治疗围绝经期子宫腺肌病的疗效[J].中国妇幼保健,2019,34(3):602-604.
[10] 孙菁,黄杰萍,叶湘萍,等.錨固定曼月乐治疗大子宫腺肌病的临床研究[J].中华生物医学工程杂志,2019,25(2):233-236.
[11] 王笑妍,韩旭.子宫腺肌病病灶切除术联合曼月乐环及GnRH-a治疗的比较研究[J].医学研究杂志,2019,48(6):148-151,156.
[12] 楼俊瑶,黄秀峰,张丽凤,等.第二代子宫内膜消融术可提高左炔诺孕酮宫内节育系统对子宫腺肌病患者的疗效[J].浙江大学学报(医学版),2019,48(2):136-141.
[13] 徐秋霞,赵相军.曼月乐联合散结镇痛胶囊对子宫腺肌病患者子宫体积、痛经及月经的影响[J].世界中医药,2018,13(8):1918-1920,1924.
[14] 郗晓丽,冯敏,李万胜.左炔诺孕酮宫内节育系统联合桂枝茯苓丸治疗子宫腺肌病的临床评价[J].河北医药,2017,39(9):1362-1364.
[15] 赵淑云,梁慧.腹腔镜术后联合达菲林及曼月乐环治疗子宫腺肌病伴不孕的疗效分析[J].中国妇幼保健,2017, 32(2):333-335.
(收稿日期:2021-02-20)
——既能避孕又能治病的环

