经皮冠状动脉腔内成形术后应用降压药对肾功能的影响
姜慧妍,严思敏,葛卫红(南京大学医学院附属鼓楼医院药学部,南京 210008)
随着放射诊断技术与介入治疗手段的发展,造影剂的使用越来越广泛。相对的,造影剂所引起的急性肾功能损伤也日益受到临床关注。造影剂肾病(contrast-induced nephropathy,CIN)是接受冠状动脉造影或经皮冠状动脉腔内成形术(percutaneous transluminal coronary angioplasty,PTCA)后常见的不良后果[1]。由于涉及多种危险因素,CIN 发病率为0%~24%不等[2]。临床因血管疾病而接受造影的患者,通常合并高血压。《2018 美国放射协会手册》指出需要药物治疗的高血压病史且为造影剂肾病的危险因素之一,可能需要在使用碘造影剂前进行肾功能的评估[3]。但降压药物对肾功能具体的影响以及造影术前是否需要停用这些药物还未得到严格的证实。近年来,肾素-血管紧张素-醛固酮系统抑制剂(renin-angiotensin-aldosterone system inhibitors,RAASi)包括血管紧张素转化酶抑制剂(angiotensin convening enzyme inhibitor,ACEI)和血管紧张素受体拮抗剂(angiotensin receptor blockers,ARB)对造影剂急性肾损的影响尚存在争议。一项纳入12 篇文献包含4 493 名患者的meta 分析发现,在接受RAASi 和未接受RAASi 治疗的患者之间,CIN 的发生率没有差异[4],反而术前接受RAASi可降低造影剂急性肾损伤的发生率和医院病死率[5],但也有部分学者认为ACEI/ARB 会增加CIN 的发生率[6-7]。β 受体阻滞剂作为危险因素常被认为与造影剂的过敏样反应相关[3,8],而对肾功能的影响鲜有研究。另外,在造影前使用CCB 类的降压药物预防CIN 的作用也存在争议[9],还需进一步考察。本研究回顾分析了常见抗高血压药物对PTCA术后患者短期肾功能的影响,探讨其对CIN 的作用及安全性,以期为临床用药提供更多的循证医学证据。
1 对象与方法
1.1 研究对象
选取2020 年1 月至2020 年12 月南京鼓楼医院心血管内科疑似冠心病行冠脉造影术的193 例住院患者为研究对象,所有患者在PTCA 治疗前后均接受了标准水化治疗。纳入标准:①年龄在18 周岁以上。②冠脉造影后行PTCA 术的患者。③术前均规律(≥7 d)服用ACEI/ARB、β 受体阻滞剂或CCB 类药物。排除标准:①同时服用两种及以上降压药的患者。②术前术中使用袢利尿剂患者。③碘过敏试验阳性或2 周内静脉使用过对比剂。④严重肾功能不全:eGFR<30 ml/(min·1.73 m2)。⑤存在其他导致急性肾功能损伤的病因(如使用肾毒性药物、慢性肾功能不全、血容量不足、心力衰竭)。⑥患有自身免疫性疾病、严重感染及肿瘤者。试验分组:根据时间顺序依次纳入,分为4 组,不服用降压药物或至少停药2 周的单纯水化组(50 例)、ACEI/ARB 组(50 例)、β 受体阻滞剂组(47 例)、CCB 组(46 例)。
1.2 方法
冠脉造影及介入治疗通过有经验的心内科介入医师在标准程序下完成,所有患者均使用碘海醇为造影剂。回顾性收集患者的临床资料,包括患者的年龄、性别、体重、身高、血压、血脂、血糖、尿酸、造影剂用量、造影前及造影48 h 后的血肌酐(Scr)、尿素氮(BUN)、Cockcroft-Gault 法计算肌酐清除率(Ccr)、MDRD 法计算肾小球滤过率(eGFR)。CIN 诊断标准[10-11]为:排除其他影响肾功能因素,造影暴露后48 h 内,SCr 水平绝对值增加44.2 μmol/L 或超过基础值25%以上。所有患者在造影前静脉滴注0.9%氯化钠注射液250 ml 进行水化治疗。
1.3 统计学方法
数据采用SPSS 22.0 统计学软件进行分析。计量资料用(±s)表示。统计指标均进行正态性及方差齐性检验,造影前后连续变量的比较采用配对t检验。多组间连续变量的比较采用单因素方差分析,方差齐采用LSD 检定,方差不齐采用Games-Howell 检验。计数资料采用Fisher 确切概率法,用[n(%)]表示。所有统计分析,以P<0.05 表示数据存在差异,具有统计学意义。
2 结果
2.1 一般资料比较
本研究一共纳入193 例患者,如表1 所示,4 组患者在年龄、性别、BMI、血压、血脂、血糖、尿酸、造影剂用量以及基础肾功能指标等方面,差异均无统计学意义(P>0.05)。
表1 4 组患者基本资料比较[n(%),±s]
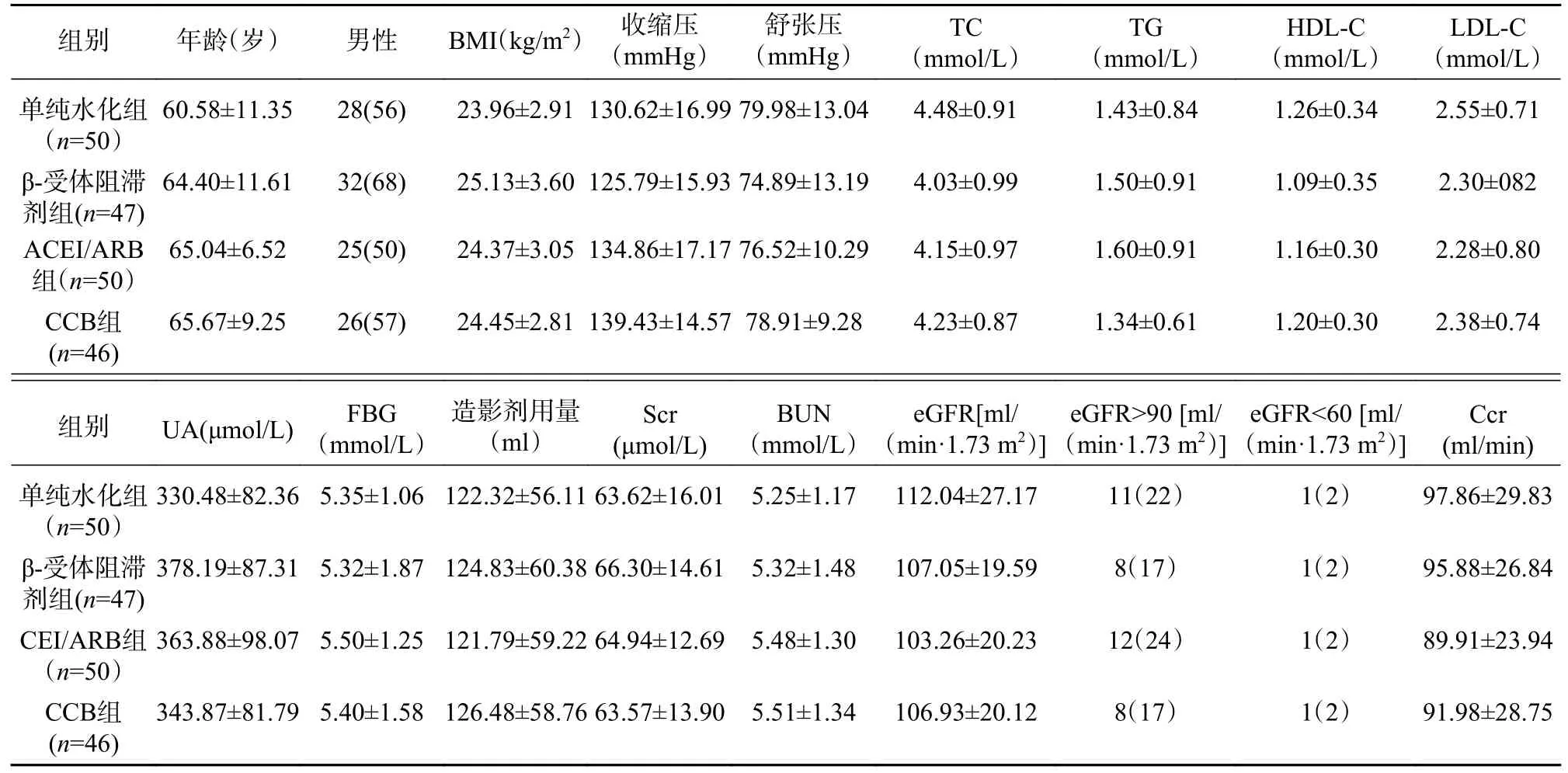
表1 4 组患者基本资料比较[n(%),±s]
2.2 患者应用造影剂前后肾功能变化情况
应用造影剂48 h 后肾功能指标变化如表2 所示。CIN 发生率为0%,4 组患者的Ccr 在手术前后均无变化,组间也无差异。除了单纯水化组,服用抗高血压药物组BUN 皆有一定幅度的下降,其中,β 受体阻滞剂组术后与术前相比具有显著差异。并且,β 受体阻滞剂组术后BUN 水平与单纯水化组、CCB 组之间也存在组间差异。另外,与术前相比,β 受体阻滞剂组患者的eGFR 水平在术后也显著降低。差异具有统计学意义(P<0.05)。

表2 4 组患者造影前后肾功能指标的比较
2.3 β 受体阻滞剂组不同血压水平造影前后肾功能指标的比较
将β 受体阻滞剂组患者按照血压水平分级,比较不同血压水平下的肾功能情况,结果如表3 所示。SBP≥140 或DBP≥90 的患者在使用造影剂之前,Scr 与Ccr 水平均显著高于SBP<140 且DBP<90 的患者(P<0.05)。

表3 β 受体阻滞剂组不同血压水平造影前后肾功能指标的比较
3 讨论
CIN 的危险因素有很多,包括:年龄>60 岁、肾功能不全、高血压、糖尿病、造影剂剂量大、使用具有肾毒性的药物等[12],其中最危险的因素是存在慢性肾脏病,且疾病发展严重程度与发生CIN 风险有关。当eGFR<30 ml/(min·1.73 m2)时,患者CIN发病率是正常人群的3 倍[13]。本研究纳入的患者肾功能基础水平均处于正常值,造影前均进行了标准水化治疗,且造影剂用量低于易发生CIN 的200 ml[14],又排除了其他对肾功能有影响的药物,因此未观测到CIN 的发生。
Scr、BUN、eGFR、Ccr 都是常见的用以评价肾功能的指标。其中,Scr 受年龄、饮食、肌肉指数等众多因素影响,其浓度上升需要时间且只有在eGFR 下降到50%时才升高,因此难以用于早期预测CIN 的发生[15]。BUN 与Scr 相似,灵敏度与特异性较差。除了肾功能之外,BUN 的浓度还取决于每日膳食蛋白摄入量、肾血流量、肝功能和患者的水合作用。有趣的是,在本研究中,除了单纯水化组以外,服用抗高血压药的患者在使用造影剂的短期内BUN 水平都有轻微幅度的下降,这可能是因为其影响肾功能血流量,导致肾功能短暂性的失调,临床意义不大。在造影前评估基础肾功能损害(主要依靠eGFR)是预测患者发生CIN 危险的最重要的标志。本研究中,除了β 受体阻滞剂组eGFR 水平在造影后有轻微下降,其余ACEI/ARB、CCB 组未见明显变化。但β 受体阻滞剂组的下降是在正常范围内且β 受体阻滞剂作为冠心病患者用来降低心率的基础用药,并不建议术前停用。但对于发生急性肾损伤或eGFR<30 ml/(min·1.73 m2)的患者,在临床可行的情况下,还是应当谨慎去除非必要的潜在肾毒性药物[16]。另外,根据研究结果,应当格外关注那些本身基础血压控制不佳的人群,在确定无CIN 发生的前提下,肾功能恢复至基线水平后,再重新启动药物治疗。
此外,作为一项回顾性分析,本研究也存在一定的局限性。①未探讨造影剂对不同肾功能损伤患者的影响。②评估的是短期内肾功能的变化,而未长期动态跟踪造影剂术后一段时间内降压药对肾功能的影响。③CIN 的早期预测指标不够全面,目前研究发现的一些更敏感的生物标记物,如肾阻力指数(RRI)、肾损伤分子(KIM-1)、胱抑素C(CysC)可被选择。④未对高血压药物详细再分类,且药物使用周期未进行分层分析,忽略了长期用药对结果可能产生的影响。因此,期待未来有更多前瞻性的、大样本量的研究去进一步指导临床安全用药。

