2019—2020年天津市津南区多环芳烃和有机磷阻燃剂气固分配特征及健康风险评价
薛倩倩,魏 扬,田瑛泽,2*,冯银厂,2
1. 南开大学环境科学与工程学院, 国家环境保护城市空气颗粒物污染防治重点实验室, 天津 300350
2. 中国气象局-南开大学大气环境与健康研究联合实验室, 天津 300074
大气中存在多种有机化合物,且具有不同程度毒性[1],其中多环芳烃(polycyclic aromatic hydrocarbons,PAHs)是大气中浓度较高且危害性较大的有机污染物之一,其化学性质相对稳定且具有致癌性、致畸性和致突变性[2]. 人为源及自然源均可排放PAHs,大气中的PAHs主要由含碳物质的不完全燃烧产生,如化石燃料燃烧以及生物质等不完全燃烧[3-5]. 由于溴代阻燃剂的禁用,有机磷酸酯(organic phosphorus esters,OPEs)阻燃剂作为替代品应运而生[6-8]. OPEs常被添加到人们日常生活消费品中,如塑料、电子设备、家具、纺织品和建筑材料,以防止燃烧和减缓火灾蔓延[8-9]. OPEs多作为添加剂混合到材料中而非通过化学键键合到材料中,因此更易通过挥发、溶解和磨损从材料中释放到环境空气中[6]. 大量研究[6-9]证明,OPEs可在食物链中进行生物积累并对人体产生不良影响. 因此,近年来对于PAHs及OPEs的生成、分配行为及其对人类的健康风险引起了越来越多的关注[3-9].由于PAHs和OPEs都属于半挥发性有机物(SVOCs),受化合物本身性质、大气环境温度以及大气颗粒物特性(浓度、粒径及有机组成)等因素影响,其在大气中能够通过吸收/吸附等物理过程进入颗粒态,也可以经挥发过程形成气态,从而达到气/固分配平衡状态[10]. 研究[10-11]表明,蒸汽压较高的PAHs和OPEs易以气态形式存在,而蒸汽压较低的PAHs和OPEs更易存在于颗粒态中,且随着大气温度的降低,这些化合物的气态浓度降低. 不同相态下有机污染物的风险可能不同. 然而,目前对PAHs及OPEs进行的风险评估中,多关注颗粒态的PAHs及OPEs[2-3,6-8,12-14].如Chen等[13]对中国台湾彰化县颗粒态PAHs造成的过度癌症风险进行评估; Zhang等[7]讨论了OPEs的气固分配行为,但只对颗粒态OPEs进行了风险评价.PAHs和OPEs进入大气后,可富集在颗粒物中,同时也以气态存在,在计算健康风险评价时,只考虑颗粒物载带的PAHs及OPEs含量,而忽略其气态浓度,会低估其对人体健康的风险. 所以在进行PAHs及OPEs的风险评价时,综合考虑气态和颗粒态的PAHs及OPEs更有利于风险的全面评价;其次,不同组分受气固分配的影响不同,因此研究不同组分的气固分配特征,并分析不同组分的气固分配对风险的影响至关重要. 鉴于此,该研究分析了天津市津南区PAHs和OPEs的组分分布特点及其气固分配特征,并对其人体暴露水平的健康风险进行了预测,以期为大气环境中PAHs及OPEs浓度模拟和预测以及健康风险评价研究提供依据.
1 材料与方法
1.1 样品采集
样品采集点位于天津市津南区南开大学大气环境综合观测站楼顶(38°59'40″N、117°20'6″E). 天津市津南区位于天津市东南部,又称天津市南郊区. 截至2018年,全区常住人口89.60×104人,总面积为387.84 km2. 属于暖温带半湿润季风型大陆性气候,主要呈春季干燥多风少雨,夏季炎热多雨,冬季寒冷干燥少雪等特征. 采样点直线距离500 m内为中等车流量的同德路,采样点5 km范围内除居民生活以及交通运输等活动外无其他污染源.
PM2.5样品采用中流量大气颗粒物采集器(TH-150C型,武汉市天虹仪表有限责任公司)于2019年9月-2020年8月进行每周一次样品采集,采样流速为100 L/min. 秋冬季(9月-翌年1月)与夏季(6-8月)分别连续采集47和95 h. 采样过程中同时采集颗粒态样品(石英滤膜,直径90 mm,QFFs PALLFLEX,美国)和气态样品(聚氨酯泡沫,PUF,直径65 mm、高75 mm,Tisch,美国). 最终收集有效样品22组(颗粒态及气态样品各22个). 样品采集后,避光储存于-20 ℃的冰箱中用于后续试验分析.
1.2 样品分析
1.2.1 颗粒态样品前处理
为了分析颗粒态的PAHs和OPEs,将1/2的90 mm石英滤膜切成碎条放入试管中,加入20 mL正己烷和丙酮(体积比为3∶1)混合溶液. 超声提取(100 kHz,加冰)3次,每次10 min并更换溶剂,将萃取后溶液合并收集于圆底烧瓶中,用旋转蒸发仪浓缩至1 mL. 然后,将萃取液转移到活化后的固相萃取小柱〔Florisil,1 g/(12 mL)〕. PAHs和OPEs组分通过固相萃取步骤分别进行洗脱收集,首先用正己烷和二氯甲烷(体积比为1∶1)混合液洗脱柱子并将流出液记为洗脱液A(PAHs),然后用8 mL乙酸乙酯对小柱进行洗脱,该部分流出液记为洗脱液B (OPEs). 最后,将洗脱液A与B分别用氮气吹到近干,洗脱液A加入50 μL PAHs内标(5种氘代PAHs,2 μg/mL),用正己烷定容至1 mL,待上机分析;洗脱液B加入20 μL OPEs内标(氘代磷酸三丁酯,0.5 μg/mL),用异辛烷定容至0.5 mL,并置于-20 ℃保存,1个月内完成上机分析.
1.2.2 气态样品前处理
吸附在聚氨酯泡沫(PUF,直径为 6.5 cm,长度为7.5 cm,Tisch, 美国)上的气态PAHs和OPEs通过加速溶剂(ASE)萃取(BuchiE-916, 步琦,瑞士)进行提取. 将1/2 PUF切碎并置于底部带有滤膜的40 mL萃取槽中. ASE萃取条件:萃取池40 mL,萃取溶剂为正己烷和丙酮(体积比为3∶1),温度为100 ℃,压力为10.3 MPa,静态萃取5 min,萃取循环2次,60%的溶剂冲洗,吹脱120 s. ASE萃取液保存于60 mL棕色样品瓶中,浓缩方法、试验条件与颗粒态PAHs和OPEs一致.
1.2.3 气态色谱质谱联用仪分析
预处理得到的样品通过GC-MS (7890B/5977B,安捷伦科技有限公司,美国)进行定性定量分析,使用的色谱柱为DB5-MS (厚度0.25 μm,内径0.25 mm,长度30 m). 气态色谱质谱运行条件:载气为高纯氦气,载气流量为1.0 mL/min;进样方式为不分流进样,进样量为1 μL;根据不同物质保留时间不同对目标物进行定性分析;定量分析采用选择离子模式,利用内标定量法进行定量计算. 对于多环芳烃的分析方法参考文献[3-5]. 对于OPE的分析,GC的初始温度设置为90 ℃并保持2 min;然后以10 ℃/min升温至170 ℃,并以3 ℃/min升温至 240 ℃,保温2 min;最后以20 ℃/min升温至310 ℃,保持4 min. 离子源和传输线的温度分别设置为230和 300 ℃.
1.3 质量控制与质量保证
石英滤膜及PUF在采样前均需要进行预处理以消除基质中背景值的影响. 采样前,石英滤膜在马弗炉中500 ℃焙烧2 h,冷却后,置于恒温恒湿〔温度为(25±1)℃,相对湿度为50%±5%〕环境平衡48 h后用1/100 000精密电子天平(XPE105型,瑞士METTLER TOLEDO)称量. PUF则通过索氏提取法加入正己烷和二氯甲烷溶液洗脱48 h,约24 h需更换一次溶剂.将清洗后的PUF用铝箔包裹后装入铝箔袋中,放入冰箱冷藏备用. 用方法空白、空白加标和平行样对数据进行质量控制. 样品分析中进行空白样回收率测定. 每一批样品进行一次平行检测和空白加标回收试验. PAHs和OPEs标准曲线的线性系数在0.99以上.PAHs的回收率在60%~85%之间,OPEs的回收率在60%~130%之间.
1.4 气固分配模型
1.4.1 气固分配系数实测模型
气固分配行为是决定SVOCs在大气环境中迁移和归趋的重要因素,主要受温度、颗粒物浓度、颗粒物粒径及颗粒物中有机组分等因子影响. 实际环境中这种行为可以通过气固分配系数(Kp,单位为m3/μg)来确定[15-16],计算公式:

式中:Cp和Cg分别表示颗粒态和气态有机污染物的浓度,ng/m3;CTSP为空气中总悬浮颗粒物(TSP)的浓度,μg/m3,该研究采用PM2.5浓度代替大气环境中的TSP浓度.
1.4.2 气固分配系数预测模型
国内外学者在SVOCs的气固分配预测模型方面开展了广泛研究[10-11,15,17-19],发现SVOCs在大气中主要存在3种气固分配平衡机制:①吸附机制,即目标物被颗粒物表面所吸附,主要受范德华力、化学键等多种吸附作用力影响,应用最广泛的为Junge-Pankow(J-P)吸附模型[7,10,17,20];②1998年Harner和Bidleman提出的基于KOA值的理论模型[21-23],该模型提出SVOCs受吸收机制影响;③烟尘-气吸附吸收双模型是近年来应用比较广泛的气固分配模型,是有机质(OM)和炭黑吸附的二重模型[24-25].
1.5 健康风险评价模型
该研究基于US EPA (美国环境保护局)提出的健康风险评价模型对成人通过呼吸暴露途径进行暴露风险评价,计算公式:
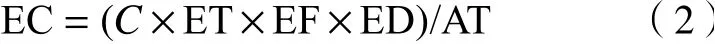
式中:EC为非致癌/致癌日均暴露浓度,mg/m3;C为大气中PAHs和OPEs各单体浓度,mg/m3;ET为暴露时间,24 h/d;EF为暴露频率,365 d/a;ED为暴露持续时间,30 a;AT为平均暴露时间,计算致癌风险时取70×365×24 h,计算非致癌风险时取30×365×24 h[3-5].
因OPEs没有呼吸暴露途径风险参考值(RfC,mg/m3)[3],且部分PAHs缺少RfC参数. 为更直观、清晰地对比化合物的非致癌暴露风险结果,按照US EPA提供的方法将已有化合物的每日参考剂量〔RfD, mg/(kg·d)〕转化为RfC进行非致癌风险的计算,转换方法[26]如下:
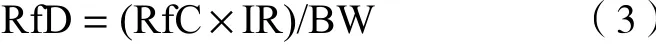
式中:IR为人体吸气量,m3/d,成人一般取值为20 m3/d;BW为体质量,kg,成人体质量一般取70 kg.
对于非致癌物,其非致癌风险商(HQ)计算公式:
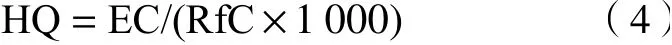
式中,HQ为非致癌风险商,表示PAHs和OPEs经呼吸途径对人体造成的非致癌风险. PAHs和OPEs的RfC值如表1所示.

表1 PAHs和OPEs的RfC及IUR值[27-28]Table 1 The RfC and IUR values of PAHs and OPEs[27-28]
PAHs及OPEs致癌风险(incremental lifetime cancer risk,ILCR)的计算公式:

式中,IUR为致癌PAHs或OPEs的单位风险,(μg/m3)-1,取值如表1所示.
2 结果与讨论
2.1 大气气态和颗粒态多环芳烃及有机磷阻燃剂水平
天津市津南区2019-2020年∑G-PAHs (气态PAHs总和)年均浓度为36.7 ng/m3,PM2.5中∑P-PAHs(颗粒态PAHs总和)年均浓度为7.3 ng/m3,气态和颗粒态中16种PAHs (∑PAHs)年均浓度为44.1 ng/m3.该地区秋冬季∑G-PAHs平均浓度为51.6 ng/m3,PM2.5中∑P-PAHs平均浓度为13.4 ng/m3,高于2015年我国北方背景点PM2.5中PAHs浓度(3.3~7.0 ng/m3)[29],低于2017年10月-2018年3月天津市郊区PM2.5中PAHs年均浓度(26.7 ng/m3)[30]. 由于津南区工业主要涉及橡胶和塑料制品业、黑色金属冶炼、压延加工业和通用设备制造业,其次机动车排放也相对严重,因此相较于背景点,该地区PAHs浓度较高. 天津市津南区夏季∑G-PAHs平均浓度为21.9 ng/m3,PM2.5中∑P-PAHs平均浓度为1.2 ng/m3. 该地区大气环境中∑PAHs浓度低于昆明市主城区2018-2019年大气环境中的PAHs浓度〔(94.4±38.9)ng/m3〕[31]. 由图1可见,∑P-PAHs及∑G-PAHs浓度均呈秋冬季高于夏季的趋势. 一方面可能是秋冬季PAHs排放源较夏季强;另一方面可能是夏季高温及强太阳辐射有利于PAHs光解和氧化等二次反应的发生. ∑G-PAHs浓度占∑PAHs浓度的比例为87.0%,即大气环境中总PAHs的相分布特征为气态占优型,可能是由于大气环境中PAHs以低环、易挥发的单体为主,导致PAHs以气态分布为主. 高分子量(5~6环)的PAHs相分布特征为颗粒态占优型,而低分子量(2~4环)的PAHs相分布特征为气态占优型,这主要由于分子量低的PAHs较高分子量的PAHs挥发性强,更趋向于分布在气态所致.
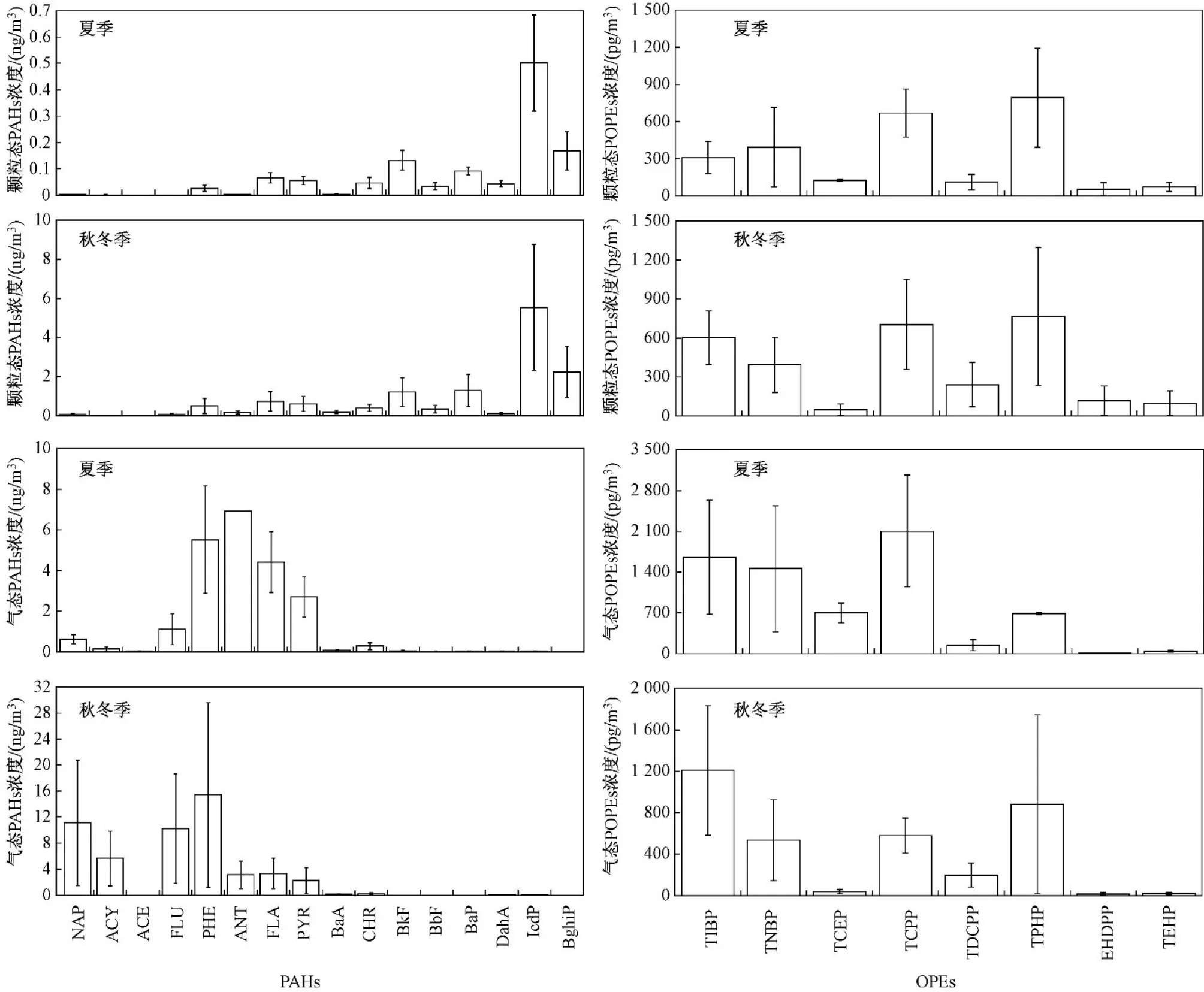
图1 秋冬季和夏季气态、颗粒态PAHs及OPEs的浓度Fig.1 The concentration of PAHs and OPEs in the gaseous and particulate in different seasons
天津市津南区2019-2020年∑G-OPEs (气态OPEs总和)年均浓度为5 142.0 pg/m3,PM2.5中∑P-OPEs (颗粒态OPEs总和)年均浓度为2 752.0 pg/m3. 该地区PM2.5中∑P-OPEs年均浓度与2015年1-12月新乡市城区PM2.5中8种OPEs年均浓度〔(2 780±3 000)pg/m3〕接近[32]. 天津市津南区气态和颗粒物态中7种OPEs (∑OPEs)年均浓度为7 894.0 pg/m3,低于成都市大气PM2.5中7种OPEs的年均浓度(市区为6 460 pg/m3,郊区为9 380 pg/m3)[9],高于2016年4月-2017年3月天津市大气环境中的8种OPEs (气态+颗粒态)浓度(中位值为1 590 pg/m3)[7,33],说明天津市不同区域OPEs浓度相差较大,津南区OPEs本地排放不容忽视. 天津市津南区秋冬季和夏季气态∑G-OPEs平均浓度分别为3 480.0和6 803.0 pg/m3,PM2.5中∑P-OPEs平均浓度分别为2 977.0和2 527.0 pg/m3. ∑G-OPEs浓度占总∑OPEs浓度的65.1%,即大气环境中总OPEs的相分布特征为气态占优型,尤其是在夏季,说明OPEs浓度在一定程度上受温度的影响.
采样期间的气象条件以及气象条件与污染物浓度之间的相关关系如图2、3所示. 由图2可见,夏季温度及相对湿度均较冬季大,秋冬季风速较夏季大,风向多为东南风,其中温度与相对湿度呈正相关(P<0.05). 由图3可见,温度与∑PAHs浓度、∑P-PAHs浓度和∑G-PAHs浓度均呈线性负相关(P均小于0.05),温度与∑P-OPEs浓度呈线性负相关(P<0.05),与∑OPEs浓度和∑G-OPEs浓度关系则呈“U型”曲线关系. 温度越低或温度越高,∑G-OPEs浓度越高,说明气态OPEs浓度在一定程度上受温度的影响[7,34].
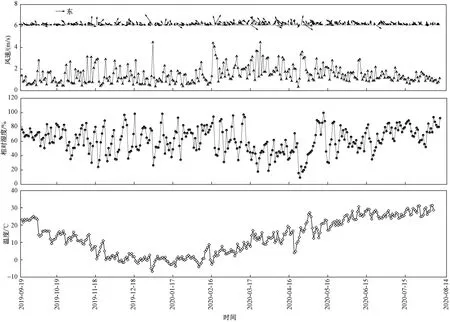
图2 采样期间风速、风向、温度和相对湿度的变化情况Fig.2 Variation of wind speed, wind direction, temperature and relative humidity during the sampling period

图3 采样期间温度与不同相态污染物浓度的关系Fig.3 The relationship between temperature and the concentration of pollutants in different phases during the sampling period
2.2 PAHs和OPEs气固分配机制研究
PAHs的lgKp测量值和预测值如图4所示. 由图4可见:模型预测值与实际测量值趋势相近,尤其是烟尘-空气吸收吸附双模型. 对于低分子量PAHs,Junge-Pankow吸附模型拟合程度优于Harner-BidlemanKOA吸收模型;对于高分子量PAHs,Harner-BidlemanKOA吸收模型拟合程度优于Junge-Pankow吸附模型. 通过比较3种模型预测值与实际测量值的差异,可以推测该地区PAHs在两相中的整体分布机制(包括吸收和吸附机制). 低分子量PAHs主要在吸附机制作用下完成气态与颗粒态的转化,而对于高分子量PAHs,主要受有机物吸收机制的影响.
OPEs的lgKp实际测量值和模型预测值如图4所示. 由图4可见:3种预测模型的趋势相似,Harner-BidlemanKOA吸收模型与烟尘-空气吸收吸附双模型的预测结果几乎一致. 对于lgKOA>10的化合物(EHDPP、TDCPP),3种预测模型模拟的效果均较好;对于lgKOA<10的化合物(TNBP、TCEP、TPHP、TCPP),预测模型模拟结果存在明显低估现象,与Zhang等[7]研究结果相似. Junge-Pankow吸附模型对7种OPEs lgKp值的预测值均显著低于实际测量值.因此,推测该地区OPEs主要受有机物吸收机制的影响. 此外,对比3种模型预测的PAHs和OPEs的lgKp值发现,烟尘-空气吸收吸附双模型预测的lgKp值更接近实际测量值.
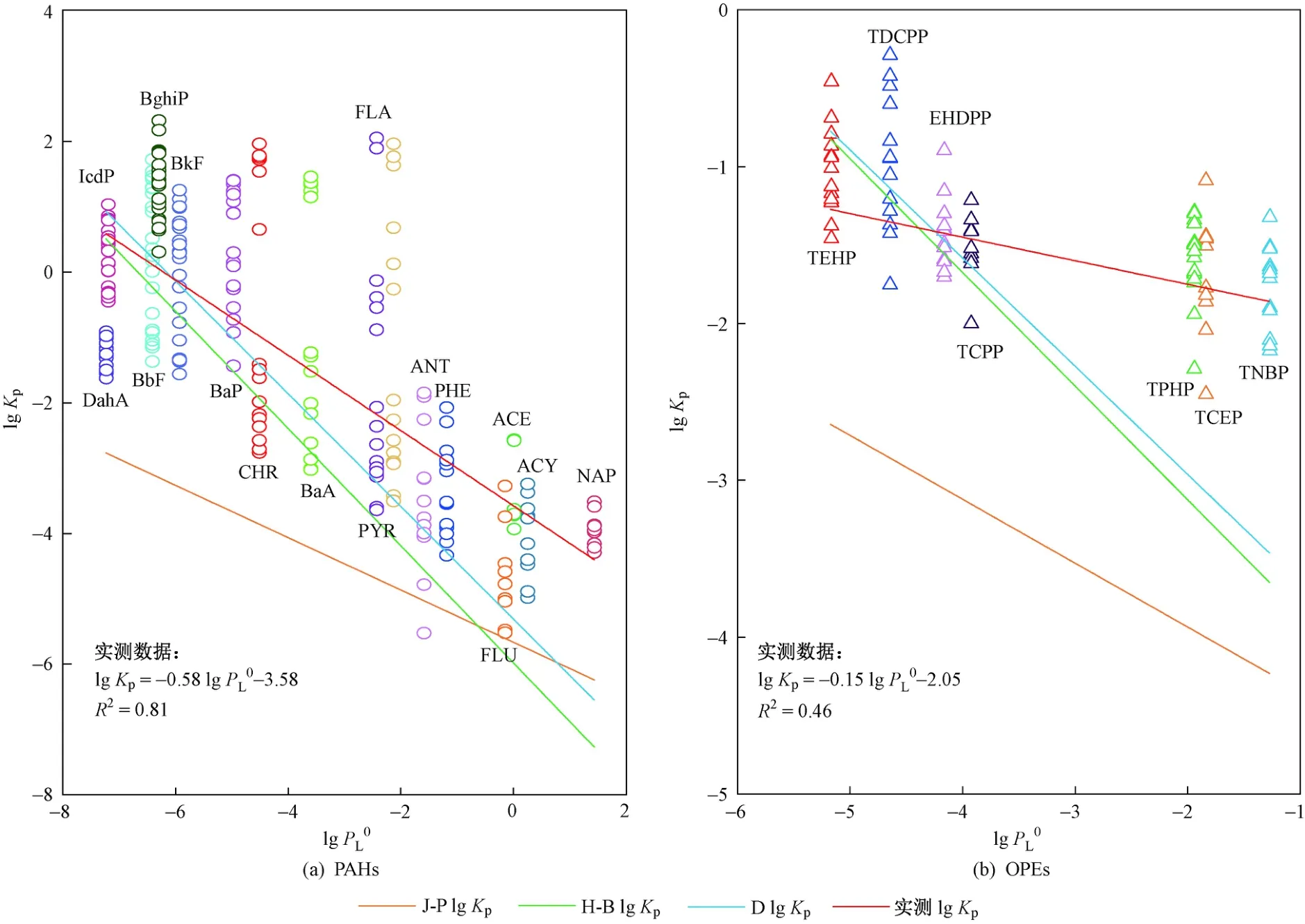
图4 基于预测及实测气固分配模型的天津市津南区大气中PAHs和OPEs的lg Kp预测及实际测量值Fig.4 lg Kp values of PAHs and OPEs based predicted and experimental gas/particle partitioning model
为了验证PAHs和OPEs的分配机制是否正确.Dachs and Eisenreich提出利用基于烟尘碳吸附模型的贡献与基于颗粒物中有机物吸收模型的贡献的比值(r)来判断SVOCs的气固分配机制[35], 计算方法如式(6)所示. 当r≥5时,影响SVOCs气固分配的主要机制是烟尘碳吸附;当0.2<r<5时,有机物吸收和烟尘碳吸附共同影响SVOCs气固分配;当r≤0.2时,影响SVOCs气固分配的主要机制是有机物吸收.

式中:fEC和fOM分别为EC和OM占颗粒物的比例,%;KSA为烟尘/空气分配系数,L/kg;δoct为辛醇的密度,kg/L;KOA为辛醇空气分配系数.
由表2可见,多数PAHs (除ANT和PYR外)的r值在0.2~5.0之间,表明吸收和吸附行为共同影响其气/固分配行为. 而OPEs的r值除TNBP和TCEP外,其他均接近或小于0.2,表明OPEs的气/固分配整体主要受有机物的吸收机制影响;TNBP和TCEP受吸附机制影响的主要原因可能是在真实环境中,因温度较低,TNBP会更趋向于从气态吸附到颗粒态中[36],而TCEP具有强极性,可能更趋向于吸附到颗粒物或采样过程中使用的玻璃纤维膜上[37].
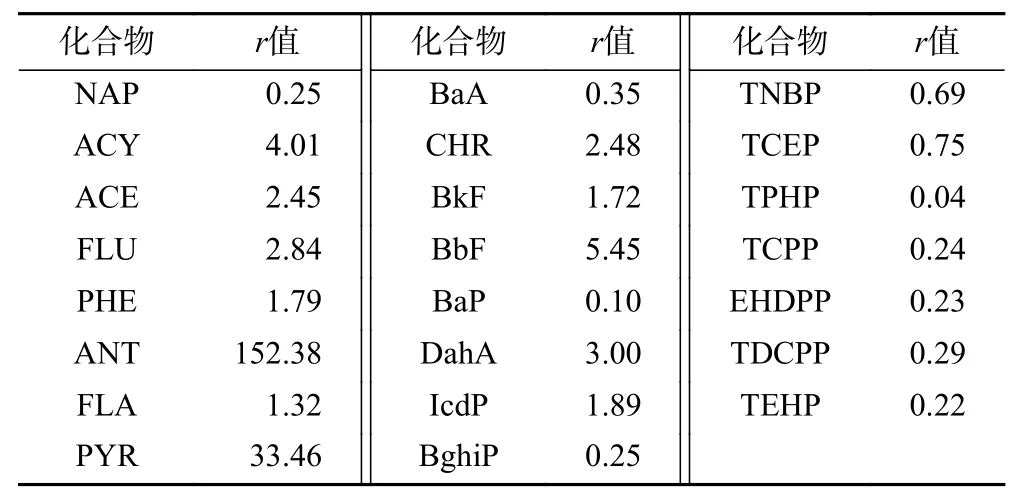
表2 PAHs和OPEs的r值Table 2 The ratio values of each substance in PAHs and OPEs
2.3 大气PAHs及OPEs健康风险评价
利用各单体PAHs年均浓度计算致癌风险及非致癌风险,将计算结果与US EPA非致癌风险的阈值(HQ=1)对比发现, PAHs的颗粒态及气态非致癌风险值分别为0.55和0.01,颗粒态及气态PAHs的非致癌风险值加和为0.56,且颗粒态PAHs非致癌风险占PAHs非致癌风险总和的98.0%. PAHs的颗粒态及气态致癌风险值分别为9.7×10-7和2.7×10-7,颗粒态及气态PAHs的致癌风险值加和为1.3×10-6,颗粒态PAHs致癌风险占PAHs致癌风险总和的76.0%.由于缺少OPEs的单位致癌风险参数IUR,因此仅对OPEs的非致癌风险进行分析对比. 颗粒态及气态的OPEs非致癌风险值分别为1.5×10-7和2.4×10-7,颗粒态及气态OPEs的非致癌风险值加和为3.9×10-7. 由于OPEs的非致癌风险远低于PAHs的非致癌风险,因此OPEs和PAHs的HQ值加和为0.56. 与PAHs不同的是,气态OPEs非致癌风险占总OPEs致癌风险的比例(62.0%)远高于气态PAHs非致癌风险占总PAHs非致癌风险的比例(2.0%)以及气态PAHs致癌风险占总PAHs非致癌风险的比例(22.0%),表明气态OPEs和颗粒态PAHs对人体健康的影响较显著.
利用颗粒态PAHs及OPEs各单体年均浓度计算其致癌及非致癌风险. 由图5可见,颗粒态的2~3环PAHs、4环PAHs和5~6环PAHs的非致癌风险占全态PAHs非致癌风险的比例分别为0.01%~8%、1%~31%和62%~98%,其致癌风险值占全态PAHs致癌风险的比例分别为0.2%~1.5%、3%~71%和70%~99%.结果表明,随着PAHs环数的增加,PAHs分子量增加,而其挥发性降低,颗粒态PAHs的致癌和非致癌风险占全态PAHs风险值的比例均增加.

图5 颗粒态PAHs及OPEs的致癌及非致癌风险占比Fig.5 The ratio of the risk value in the particulate phase of OPEs and PAHs to the risk value in the total phase
颗粒态TNBP、TCEP、TCPP、TPHP和TDCPP的非致癌风险占全态TNBP、TCEP、TCPP、TPHP和TDCPP非致癌风险的比例分别为36%(范围为10%~58%)、40%(范围为11%~72%)、45%(范围为13%~67%)、51%(范围为38%~75%)和49% (范围为37%~60%).结果表明,随着OPEs分子量的增加,其挥发性降低,颗粒态OPEs非致癌风险占全态OPEs非致癌风险的比例均增加.
2.4 不确定性分析
该研究的不确定性主要来自PAHs和OPEs有机物仪器测量及分析操作过程. 主要涉及以下5个方面:①PAHs和OPEs颗粒态和气态分别采用膜和PUF进行,采样方式不同可影响2个相态污染物的平衡,可能会造成采样过程中两相之间发生转化;②采样过程中,由于采样环境温度及相对湿度的变化,会导致之前收集到的颗粒态和气态PAHs和OPEs重新进行分配,影响污染物原始气固分配平衡;③最终收集到的气态和颗粒态的PAHs和OPEs可能不饱和,在收集完成后仍会发生气固分配过程;④采样期间,PAHs和OPEs可能会发生二次转化,且两相之间反应速率不同,造成损失;⑤PAHs和OPEs分析过程中涉及较为复杂的有机物前处理分析,人为分析操作本身会带来一定的不确定性.
3 结论
a)该地区大气环境中PAHs的相分布特征为气态占优型,气态PAHs浓度占PAHs总浓度的87.0%;大气环境中总OPEs的相分布特征为气态占优型,气态OPEs浓度占OPEs总浓度的65.1%.
b)研究期间,该地区PAHs在两相中的整体分布机制包括吸收和吸附机制. 低分子量PAHs主要在吸附机制作用下完成了气态与颗粒态的转化. 对于高分子量PAHs,吸收是气固分配的重要机制. 该地区OPEs气固分配主要受有机物吸收机制影响. 此外,PAHs和OPEs的lgKp实测值和预测值的差异表明,烟尘-空气吸收吸附双重模型预测的lgKp值更接近实测值.
c)随着PAHs环数及分子量的增加,其挥发性降低,颗粒态PAHs的致癌/非致癌风险占全态PAHs致癌/非致癌风险的比例增加. PAHs的致癌/非致癌风险呈颗粒态大于气态的特征. 随着OPEs分子量的增加,其挥发性降低,颗粒态OPEs非致癌风险占全态OPEs非致癌风险的比例增加. 与PAHs不同,气态OPEs的非致癌风险大于颗粒态OPEs的非致癌风险.

