GB/T 7139—2002方法中是否须加入硝酸钠探讨
李岩松,高旭东
(锦西化工研究院有限公司,辽宁 葫芦岛 125000)
在GB/T 7139—2002《塑料 氯乙烯均聚物和共聚物 氯含量的测定》燃烧瓶法的7.2.5步骤中,要求在燃烧后的吸收溶液中加入约1 g硝酸钠固体;但在燃烧弹法的相关操作中,并未要求加入硝酸钠。在燃烧瓶法中是否有必要加入硝酸钠,标准使用者多有质疑,但未见相关的研究报道。笔者先模拟配制燃烧瓶法样品燃烧后的溶液,进行加与不加硝酸钠的电位滴定对比试验,但是试验的仪器条件不可缺。结果发现,在这种仪器条件下,样品溶液中可以不加入硝酸钠。
1 模拟溶液试验
模拟燃烧瓶法CPE、PVC、CPVC样品燃烧后的溶液进行配制:分别量取25、50、60 mL浓度0.01 mol/L的盐酸到烧杯中,加适量水使体积达到60 mL。这3种溶液分别相当于氯质量分数为35%的CPE 25.25 mg、氯质量分数为56%的PVC 31.56 mg、氯质量分数为67%的CPVC树脂样品31.65 mg燃烧后的吸收溶液。各加2.5 mL浓度2 mol/L的硝酸溶液到3种试样中。
试验各分成2组,一组加入1 g硝酸钠,另一组不加硝酸钠。用浓度0.050 1 mol/L的硝酸银标准溶液滴定。使用的电位滴定仪以银电极为指示电极,双盐桥饱和甘汞电极为参比电极。空白试验硝酸银标准滴定溶液滴定体积为0。
氯含量计算公式为:
其中:V1为滴定时消耗的硝酸银标准滴定溶液的体积,mL;V0为滴定空白溶液时消耗的硝酸银标准滴定溶液的体积,mL;c为硝酸银标准滴定溶液的浓度,mol/L;m为试样的质量,g。
滴定结果见表1~表6。
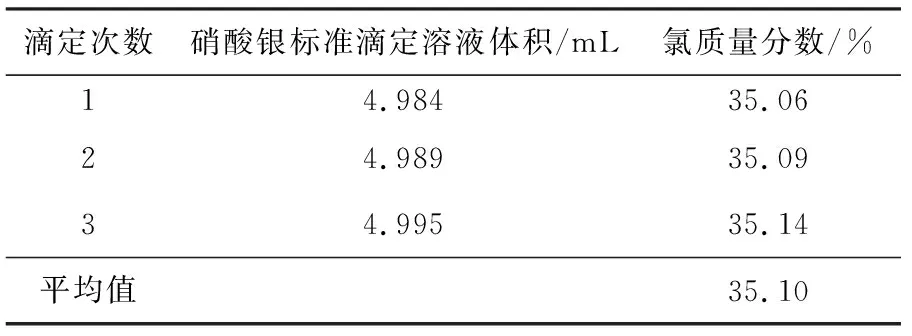
表2 模拟氯含量35%、质量25.25 mg样品,加入硝酸钠的试验结果Table 2 Test results of sodium nitrate added solution simulating 25.25 mg sample of hlorine mass fraction 35%

表3 模拟氯含量56%、质量31.56 mg样品,未加入硝酸钠的试验结果Table 3 Test results of no-sodium nitrate added solution simulating 31.56 mg sample of chlorine mass fraction 56%
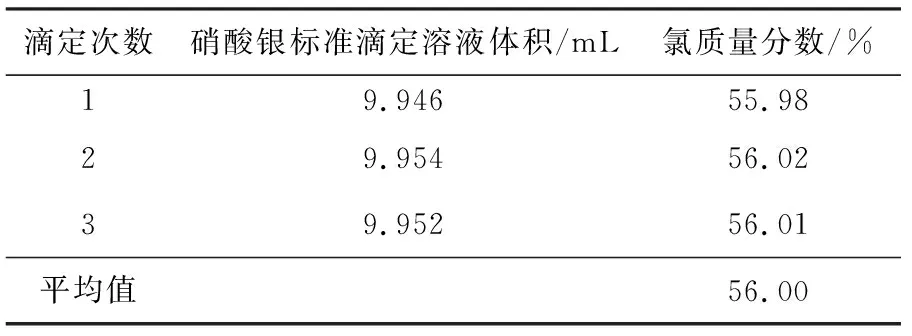
表4 模拟氯含量56%、质量31.56 mg样品,加入硝酸钠的试验结果Table 4 Test results of sodium nitrate added solution simulating 31.56 mg sample of chlorine mass fraction 56%
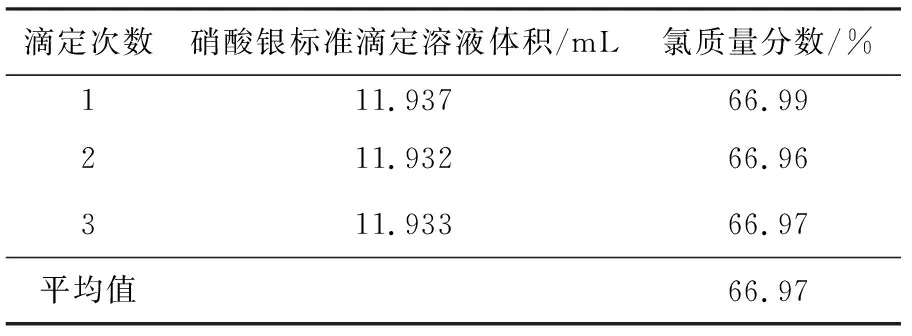
表5 模拟氯含量67%、质量31.65 mg样品,未加入硝酸钠的试验结果Table 5 Test results of no-sodium nitrate added solution simulating 31.65 mg sample of chlorine mass fraction 67%
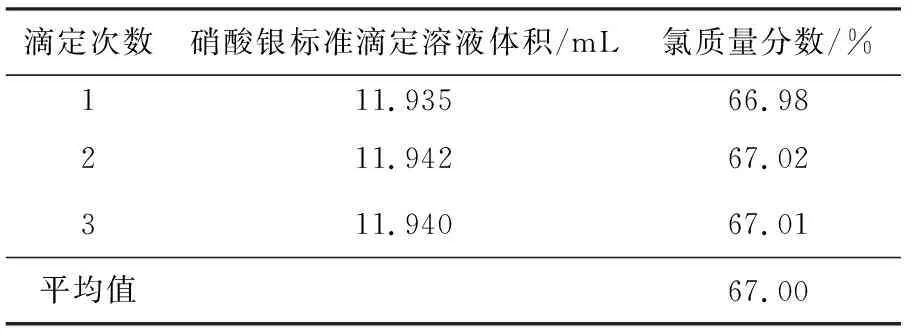
表6 模拟氯含量67%、质量31.65 mg样品,加入硝酸钠的试验结果Table 6 Test results of sodium nitrate added solution simulating 31.56 mg sample of chlorine mass fraction 56%
表1~表6试验结果表明:是否加入硝酸钠,对模拟溶液的滴定结果无影响。
2 实际样品对比试验
试验样品为某公司SG8型PVC,硝酸银滴定液浓度0.050 1 mol/L。试验分为A、B两组。A组按照GB/T 7139—2002方法B(燃烧瓶法)进行前处理;B组在步骤7.2.5时,不加入硝酸钠,其他试验条件与A组相同。试验结果见表7、表8。
A、B两组滴定曲线平滑,突跃明显,定点准确无异常。滴定曲线分别见图1、图2。
实际样品滴定对比试验结果也表明:在这种仪器条件下,样品溶液中可以不加入硝酸钠。

表7 加硝酸钠的滴定结果Table 7 Test results of samples with added sodium nitrate
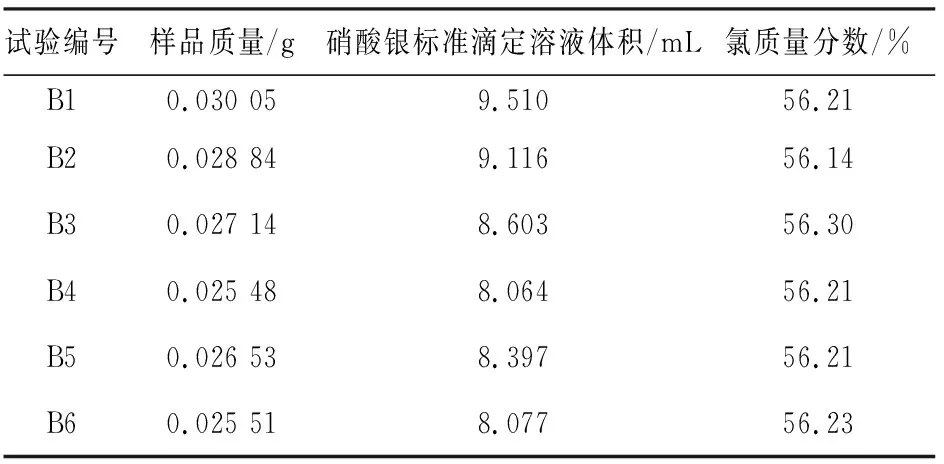
表8 不加硝酸钠的滴定结果Table 8 Test results of samples without added sodium nitrate
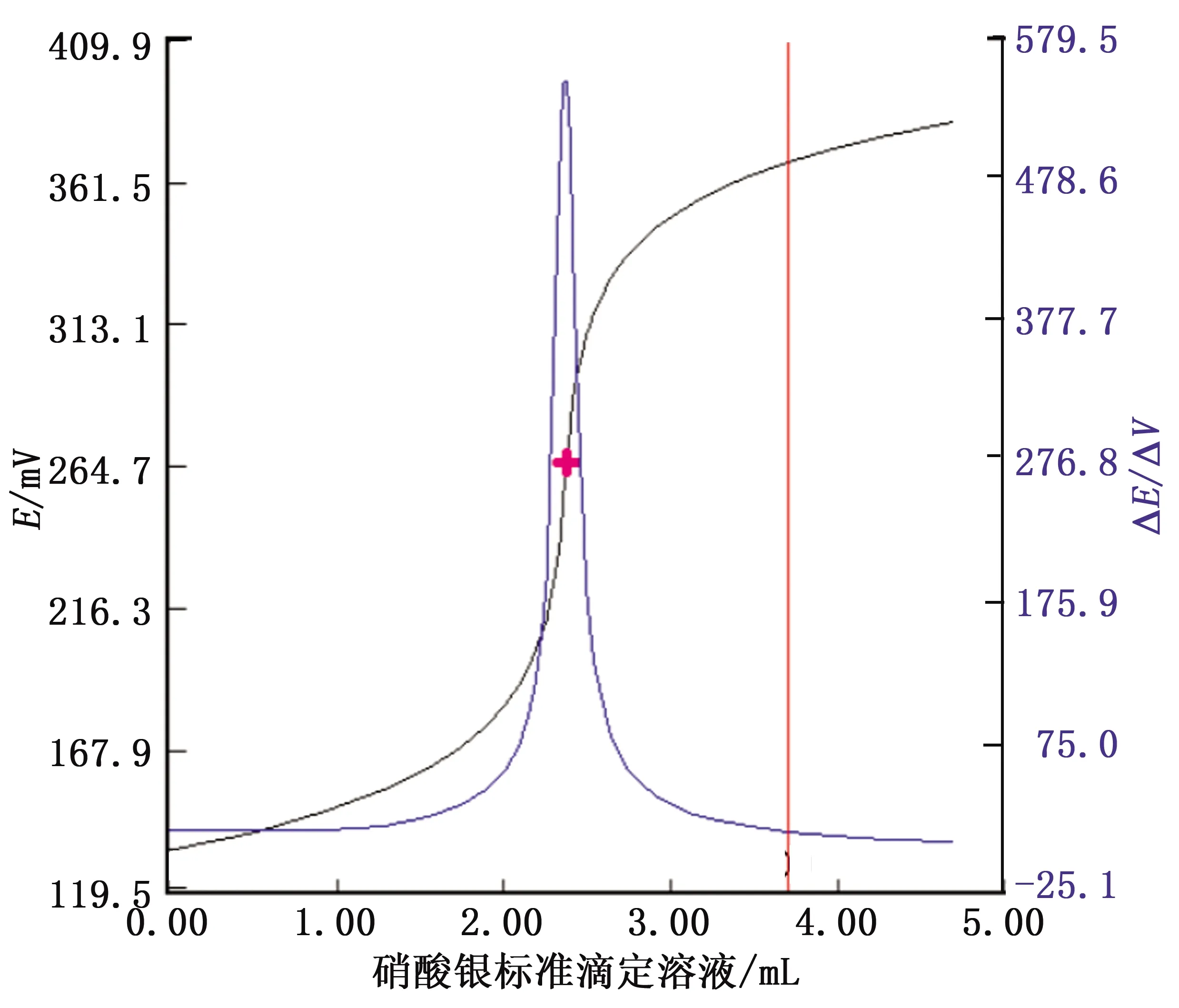
图1 加入硝酸钠的滴定曲线Fig.1 Titration curve with added sodium nitrate
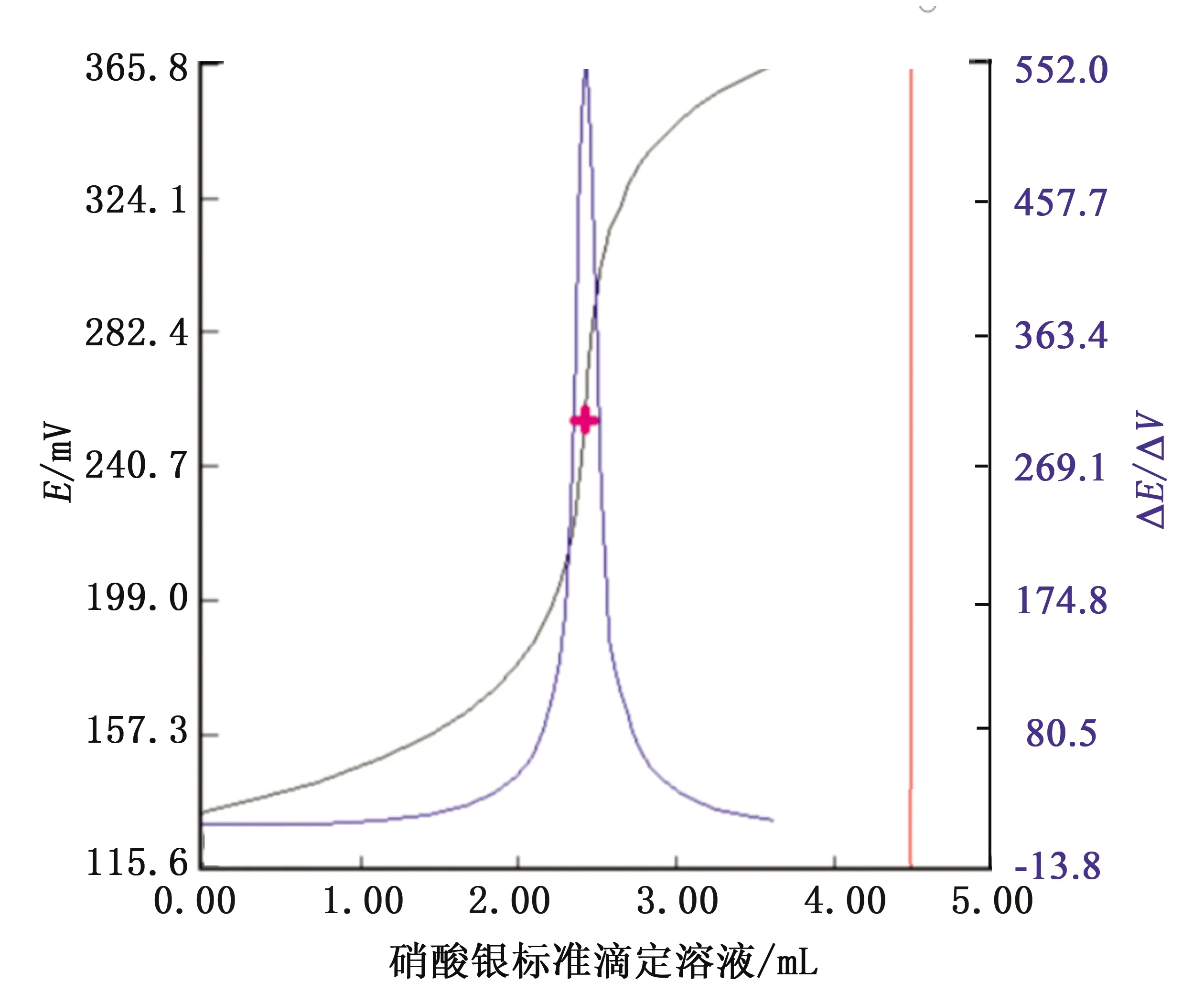
图2 未加入硝酸钠的滴定曲线Fig.2 Titration curve without added sodium nitrate
3 是否应加入硝酸钠的进一步思考
GB/T 7139—2002是等效采用国际标准 ISO 1158:1998(E)《塑料 氯乙烯均聚物和共聚物 氯含量的测定》。ISO 1158:1998(E)起草时在燃烧瓶法中加入硝酸钠是出于什么目的,笔者没有找到该标准的编制说明,因此没有找到明确答案。但笔者有如下的思考。
(1)该标准的燃烧瓶法中只说加入约1 g硝酸钠,采用电位滴定法或佛尔哈德法滴定,但并未指明电位滴定法时用哪种参比电极和指示电极。如果以氯离子电极为指示电极,有的要求溶液中有0.1 mol/L的硝酸钠[1],有的用0.2 mol/L硝酸钠溶液作氯电极活化液,并且在滴定中加入硝酸钠,滴定前溶液浓度也是0.2 mol/L[2]。在GB/T 7139—2002燃烧瓶法中,加入硝酸钠后溶液中硝酸钠浓度也同为0.2 mol/L,但本试验中使用的是银电极,不需要硝酸钠活化。文献[2]中的方法是确定终点电位值滴定,在滴定前加入硝酸钠是为了使被测液和活化液组成与浓度尽量一致,以保证终点电位值一致;而笔者采用的仪器是动态电位滴定,无须准确确定终点电位。
(2)GB/T 3050—2000 《无机化工产品中氯化物含量测定的通用方法 电位滴定法》、GB/T 15453—2008 《工业循环冷却水和锅炉用水中氯离子测定》、QB 1036—91 《工业用三聚磷酸钠 氯化物含量测定 电位滴定法》、DB61/T 1036—2019 《水质 氯化物的测定 全自动电位滴定法》、GB 5009.44—2016 《食品安全国家标准 食品中氯化物的测定 电位滴定法》中以银电极为指示电极,双液型饱和甘汞电极为参比电极,都未要求加入硝酸钠。
(3)在GB/T 7139—2002燃烧瓶法中,煮沸前的溶液中存在氯离子、碳酸根离子、硝酸根离子、氢离子、钾离子、过氧化氢和溶解在溶液中的少量氧气分子。硝酸钠溶液化学性质稳定,并不与溶液中的任何离子发生化学反应。在煮沸过程中温度不超过100 ℃,硝酸钠溶液在此温度下化学性质稳定,没有发生化学反应。
(4)GB/T 7139—2002中燃烧弹法没有加入硝酸钠,说明在燃烧瓶法中加入硝酸钠值得商榷。在燃烧弹法中,按加入10 g过氧化钠计,溶液中硝酸钠的浓度为1.28 mol/L,而燃烧瓶法中为0.2 mol/L,显然差别很大。
(5)使用佛尔哈德滴定法滴定时,笔者认为理论上也不须加入硝酸钠,但笔者未进行试验验证。

