疏血通注射液联合依达拉奉治疗急性脑出血患者的临床疗效
李新华
(民权县人民医院 神经内科,河南 商丘 476800)
急性脑出血是血管破裂引起出血,时间窗通常在3天内,急性期致死、致残率较高,且预后效果较差[1-2]。依达拉奉是一种自由基清除剂,亲脂性高,且血脑屏障透过率较高,能够有效抑制细胞的过氧化作用,降低神经细胞凋亡速率,在急性脑出血的治疗中效果较好,但容易出现血小板减少、弥散性血管内凝血等不良反应[3-4]。疏血通注射液作为中药制剂,具有活血化瘀的功效,用于急性脑出血患者的治疗中,疗效显著[5-6]。为探究依达拉奉和疏血通联合治疗急性脑出血患者的效果,选择民权县人民医院收治的156 例急性脑出血患者进行研究。
1 资料与方法
1.1 一般资料
选择本院2016年8月至2020年4月收治的156 例急性脑出血患者作为研究对象,将其按照随机数字表法分为对照组和观察组,各78 例。对照组男性41 例,女性37 例;年龄60 ~79 岁,平均年龄(68.49±3.71)岁;脑叶出血46 例,丘脑出血17 例,其他部位出血15 例;平均出血量(19.89±3.87) mL。观察组男性42 例,女性36 例;年龄60 ~79 岁,平均年龄(67.92±3.56)岁;脑叶出血44 例,丘脑出血17 例,其他部位出血17 例;平均出血量(20.03±3.89) mL。两组一般资料比较,差异无统计学意义(P>0.05)。本研究经本院医学伦理委员会批准。
纳入标准:①均符合《中国脑血管病影像应用指南2019》[7]中急性脑出血的诊断标准;②年龄≥60 岁;③患者家属签署知情同意书。
排除标准:①有脑出血史;②伴有精神疾病者;③伴有肝肾功能障碍;④入组前2 周内行外科手术者;⑤伴有心脏系统疾病者;⑥同时参与其他研究者。
1.2 治疗方法
两组患者入院后均给予抗血小板聚集、补液、降血压等常规处理。
对照组静脉滴注依达拉奉注射液( 国药准字H20080056,国药集团国瑞药业有限公司,规格:30 mg)30 mg,30 mg/ 次,2 次/d。治疗2 周后观察疗效。
观察组采用依达拉奉联合疏血通治疗,依达拉奉用法用量及治疗周期同对照组,疏血通注射液( 牡丹江友搏药业,国药准字:Z20010100,规格:2 mL/ 支)6 mL加入0.9% 生理盐水注射液250 mL 中静脉滴注,现配现用且于0.5 h 内滴注完全,1 次/d。治疗2 周后观察疗效。
1.3 观察指标
神经功能:分别于治疗前后,采用美国国立卫生院卒中量表(NIHSS)[8]评估两组患者的神经功能。NIHSS评分范围为0 ~42 分,分数越高神经受损越严重。
血小板参数:分别于治疗前后,采集患者清晨空腹静脉血4 mL,使用全自动血细胞分析仪( 济南正荣医疗器械有限公司,型号:HF-3800)测定血小板计数(PLT)、血小板分布宽度(PDW)、血小板平均体积(MPV)。
凝血指标:比较两组患者治疗前后凝血酶原时间(PT) 及活化部分凝血活酶时间(aPTT) 水平,试剂盒及其相关试剂均购自上海酶联生物科技有限公司。
血清炎性因子指标:分别于治疗前后,采集患者外周空腹静脉血4 mL,离心分离10 min 后( 离心半径:13.5 cm,离心率:3 000 r/min),取上清,分别以胶乳增强免疫比浊法及循环酶法完成血清高敏C 反应蛋白(hs-CRP) 及半胱氨酸(Hcy) 水平检测。试剂盒均购自上海酶联生物科技有限公司。
不良反应发生率:比较两组患者用药后的不良反应发生率,包括过敏、血小板减少、血管内凝血。
1.4 统计学分析
使用SPSS19.0 统计学软件对研究数据进行分析,计数资料以n(%) 表示,行χ2检验;符合正态分布的计量资料以±s表示,行t检验;P<0.05 表示差异有统计学意义。
2 结 果
2.1 两组患者治疗前后神经功能比较
治疗后,两组患者的NIHSS 评分均低于治疗前,且观察组低于对照组,差异有统计学意义(P<0.05),详见表1。
表1 两组患者治疗前后神经功能比较(± s ,分)Table 1 Comparison of neurological function before and after treatment between the two groups (± s ,points)
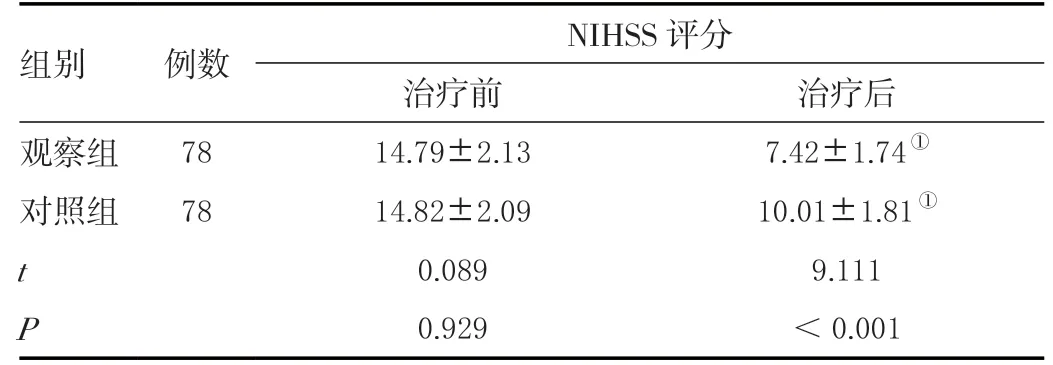
表1 两组患者治疗前后神经功能比较(± s ,分)Table 1 Comparison of neurological function before and after treatment between the two groups (± s ,points)
注:与同组治疗前相比,①P <0.05。
组别 例数 NIHSS 评分治疗前 治疗后观察组 78 14.79±2.13 7.42±1.74①对照组 78 14.82±2.09 10.01±1.81①t 0.089 9.111 P 0.929 <0.001
2.2 两组患者治疗前后血小板参数比较
治疗前,两组各项血小板参数比较,差异均无统计学意义(P>0.05)。治疗后,两组PDW、MPV 指标均低于治疗前,且观察组低于对照组;两组PLT 指标均高于治疗前,且观察组高于对照组,差异均有统计学意义(P<0.05),详见表2。
表2 两组患者治疗前后血小板参数比较(± s )Table 2 Comparison of platelet parameters before and after treatment in the two groups(± s )
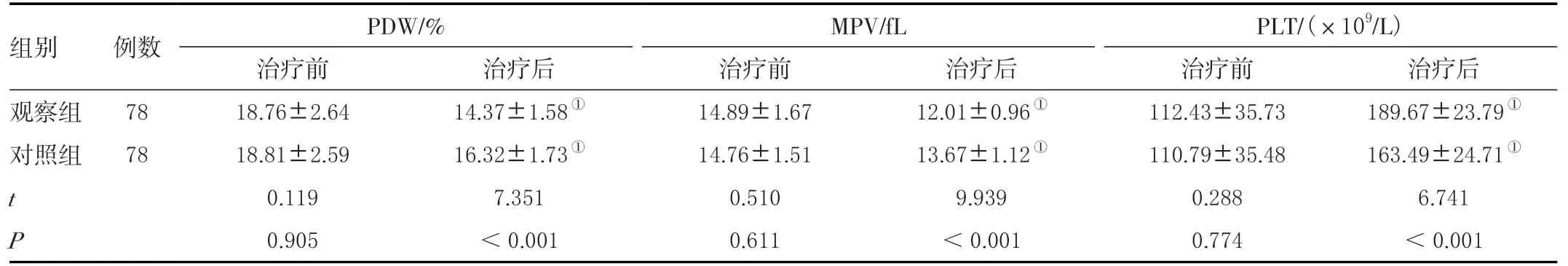
表2 两组患者治疗前后血小板参数比较(± s )Table 2 Comparison of platelet parameters before and after treatment in the two groups(± s )
注:与同组治疗前相比,①P <0.05。
组别 例数 PDW/% MPV/fL PLT/(×109/L)治疗前 治疗后 治疗前 治疗后 治疗前 治疗后观察组 78 18.76±2.64 14.37±1.58① 14.89±1.67 12.01±0.96① 112.43±35.73 189.67±23.79①对照组 78 18.81±2.59 16.32±1.73① 14.76±1.51 13.67±1.12① 110.79±35.48 163.49±24.71①t 0.119 7.351 0.510 9.939 0.288 6.741 P 0.905 <0.001 0.611 <0.001 0.774 <0.001
2.3 两组患者治疗前后aPTT 及PT 水平比较
治疗前,两组患者的aPTT 及PT 水平比较,差异无统计学意义(P>0.05);治疗后,两组患者的aPTT 及PT 水平均高于治疗前,且研究组均高于对照组,差异均有统计学意义(P<0.05),详见表3。
表3 两组患者治疗前后aPTT 及PT 水平比较(± s ,s)Table 3 Comparison of aPTT and PT levels before and after treatment in the two groups(± s ,s)

表3 两组患者治疗前后aPTT 及PT 水平比较(± s ,s)Table 3 Comparison of aPTT and PT levels before and after treatment in the two groups(± s ,s)
注:与同组治疗前相比,①P <0.05。
组别 例数 aPTT PT治疗前 治疗后 治疗前 治疗后观察组 78 28.34±4.15 38.54±2.76① 12.51±3.46 17.53±3.14①对照组 78 28.79±4.21 31.22±2.83① 12.68±3.81 13.06±3.37①t 0.672 16.354 0.292 8.571 P 0.502 <0.001 0.771 <0.001
2.4 两组患者治疗前后血清hs-CRP 及Hcy 水平比较
治疗前,两组患者的血清hs-CRP 及Hcy 水平比较差异无统计学意义(P>0.05);治疗后,两组患者的血清hs-CRP 及Hcy 水平较治疗前均降低,且研究组均低于对照组,差异有统计学意义(P<0.05),详见表4。
表4 两组患者治疗前后血清hs-CRP 及Hcy 水平比较(± s )Table 4 Comparison of serum hs-CRP and Hcy levels before and after treatment in the two groups(± s )

表4 两组患者治疗前后血清hs-CRP 及Hcy 水平比较(± s )Table 4 Comparison of serum hs-CRP and Hcy levels before and after treatment in the two groups(± s )
注:与同组治疗前相比,①P <0.05。
组别 例数 hs-CRP/(mg/L) Hcy/(μmol/L)治疗前 治疗后 治疗前 治疗后观察组 78 19.02±3.06 13.14±1.12① 25.37±4.41 15.69±2.85①对照组 78 18.98±2.76 14.79±1.01① 25.44±4.32 19.21±3.02①t 0.085 9.662 0.100 7.487 P 0.932 <0.001 0.920 <0.001
2.5 两组患者不良反应发生率比较
观察组出现过敏2 例,血小板减少1 例,不良反应发生率为3.85%;对照组出现过敏1 例,血小板减少1 例,血管内凝血2 例,不良反应发生率为5.13%;两组患者的不良反应发生率比较,差异无统计学意义(P>0.05),详见表5。

表5 两组患者不良反应发生率比较[n(%)]Table 5 Comparison of the incidence of adverse reactions between the two groups [n(%)]
3 讨 论
急性脑出血主要与脑血管病变有关,患者情绪激动或受到过度刺激时易发病,死亡率很高,且预后较差,易出现运动障碍、认知障碍、语言障碍等并发症,严重影响患者的生活质量[9-10]。依达拉奉作用于急性脑出血,自由基清除率较高,能够有效抑制脂质过氧化,从而避免或降低神经细胞氧化损伤,临床治疗过程中疗效显著,但易诱发血管凝血及血小板减少等并发症,严重影响预后效果[11-12]。疏血通注射液从水蛭等生物中提取,是临床常用于抗凝血、扩张血管的中药制剂,活血化瘀作用较强,应用于急性脑出血的临床治疗过程中,疗效显著且安全性较高[13-14]。
本研究治疗后观察组NIHSS 评分低于对照组(P<0.05),两组不良反应发生率相近,表明疏血通注射液联合依达拉奉治疗急性脑出血患者,能够有效改善神经功能恢复情况,促进病情康复,安全性较高。陈钫等[15]研究认为疏血通注射液治疗急性脑出血,具有抗凝血和抗血小板聚集、减少脑缺血范围的功效,能够有效改善血小板相关指标水平,促进神经功能恢复。
本研究治疗后两组PDW、MPV 指标均低于治疗前,且观察组低于对照组;两组PLT 指标均高于治疗前,且观察组高于对照组,表明疏血通注射液联合依达拉奉治疗急性脑出血患者,能够有效改善血小板相关指标水平。
本研究结果显示,治疗后,两组患者的aPTT 及PT水平均高于治疗前,且研究组均高于对照组,差异均有统计学意义(P<0.05),表明疏血通注射液联合依达拉奉治疗急性脑出血患者,可有效升高患者的aPTT 及PT水平,改善凝血功能。研究分析疏血通注射液以水蛭和地龙提取物入药,其水蛭中含有的水蛭素是特效特异性凝血酶抑制剂,且及地龙中含有蚓激酶能够有效激活纤溶酶原,降解纤维蛋白,对调节患者的aPTT 及PT 水平具有重要作用[16]。hs-CRP 是机体应对入侵微生物及细菌或病毒感染的急性反应蛋白,可通过介导单核细胞等对血管内皮的黏附作用,促进血液粥样硬化斑块形成,继而加重神经功能损伤[17]。Hcy 是机体内含硫氨基酸的一个重要的代谢中间产物,可间接激活胆固醇氧化及血小板聚集,对急性脑出血患者的不良预后具有促进作用[18]。本研究治疗后,两组患者的血清hs-CRP 及Hcy 水平较治疗前均降低,且研究组均低于对照组,差异有统计学意义(P<0.05),提示疏血通注射液联合依达拉奉治疗急性脑出血患者,能够有效调节患者血管内皮相关炎症因子水平,进而有助于改善患者预后。急性脑出血临床表现为意识障碍、口舌歪斜和语言障碍等症状,中医理论究其症状列入“中风”之列,认为急性脑出血由气滞血瘀、血随气逆所致,中医主张祛风通络、化痰熄风、活血化瘀之法。疏血通注射液中水蛭可消肿解毒、破血通经;现代医学研究认为水蛭提取物为水蛭素,可抑制凝血酶活性,从而减少神经细胞损伤和凋亡,改善神经系统功能。地龙可清热定惊、通络平喘。诸剂合用共奏活血化瘀、通经活络之功[19]。
综上所述,疏血通注射液联合依达拉奉治疗急性脑出血患者,能够有效改善神经功能,恢复血小板相关指标,促进病情康复,安全性较高。

