基于网络药理学研究止嗽散治疗咳嗽变异性哮喘的分子机制
陈丽君,阚红星,丁 然,侯 俊,杨银凤
(安徽中医药大学医药信息工程学院,安徽 合肥 230012)
咳嗽变异性哮喘(cough variant asthma,CVA)通常表现为气道反应过度,嗜酸性炎症和咳嗽。CVA是哮喘的前兆。据统计,有50%~80%的儿童和10%~33%的CVA成人会发展为典型的哮喘。CVA的发病机制及病理生理表现与典型哮喘相似,均为多种炎症细胞和炎症递质参与的慢性呼吸道炎症性疾病。目前治疗CVA的药物有激素和支气管扩张剂,但此类药物长期使用存在毒性和不良反应,而且停药后易复发。
止嗽散收载于清代程钟龄《医学心悟》中,对CVA具有显著的疗效。该方由桔梗、甘草、白前、紫菀、荆芥、陈皮、百部组成。方中紫菀、百部味苦,止咳化痰,共为君药;桔梗开宣肺气,白前降气化痰,共为臣药;荆芥疏风解表,陈皮理气化痰,共为佐药;甘草调和诸药,配桔梗又有利咽止咳之功,共为佐使药。
本研究旨在通过整合药物代谢动力学数据,进行多重药物靶点预测和分子对接分析,以探究止嗽散治疗CVA的作用机制。
1 方法
1.1 活性成分的筛选 通过中药系统药理学数据库和分析平台(traditional Chinese medicine systems pharmacology database and analysis platform, TCMSP)、中国中药整合数据库(traditional Chinese medicine integrated database,TCMIP)和文献检索收集止嗽散中7味中药的分子数据集。同时,将口服生物利用度(oral bioavailability,OB)、类药性(drug likeness,DL)、药物半衰期(half life,HL)的阈值分别设置为OB≥30%,DL≥0.2,HL≥4,以同时满足这3个条件的化合物作为止嗽散方中潜在的活性成分。
1.2 靶点的预测 运用TargetNet、Swiss Target Prediction和基于支持向量机(support vector medicine,SVM)、随机森林法(random forest, RF)的SysDT(Systems drug targeting,SysDT)模型预测靶点。在SysDT方法中,将同时满足RF≥0.7和SVM≥0.8的化合物-靶点相互作用视为有效靶点。此外,将化合物的简化分子线性输入规范(simplified molecular input line entry system,SMILES)值输入Swiss Target Prediction和TargetNet数据库,以补充获取活性成分的靶基因信息。
1.3 CVA致病候选基因的获取 结合GeneCards和OMIM两大疾病数据库,以“cough variant asthma”为关键词进行检索,获取CVA的致病基因。
1.4 网络构建 将活性成分作用靶点与致病候选基因取交集后的靶点导入蛋白互作平台数据库(String),以获取蛋白与蛋白相互作用(protein-protein interaction,PPI)关系,并利用Cytoscape 3.7.2软件绘制PPI网络和“活性成分-靶点-疾病(C-T-D)”网络。最后,运用“Network Analyzer”功能计算PPI和C-T-D网络的“度(degree)”和“介数(betweenness)”值。
1.5 生物学功能富集分析 为了进一步探讨止嗽散治疗CVA的分子作用机制,将上述获得的潜在靶点导入到DAVID 6.8数据库(http://david.abcc.ncifcrf.gov),采用京都基因与基因组百科全书(Kyoto encyclopedia of genes and genomes,KEGG)进行富集分析。
1.6 分子对接 为进一步探索止嗽散的活性成分与其靶点的结合模式,从PPI网络获取的关键靶点中随机选择3个靶点与其相应的关键活性分子进行分子对接验证。这些靶蛋白的X射线晶体结构从蛋白质数据(protein data bank,PDB)(http://www.rcsb.org)获取。然后,采用AutoDock Vina软件进行分子对接,得到结合能,并绘制活性分子和蛋白的结合模式图。
2 结果
2.1 止嗽散活性成分筛选 根据前面设置的阈值,尽管部分化合物的OB、DL和HL值很低,但这些化合物如柚皮素、β-谷甾醇等已有相关文献报道其药理学活性,故入选有效化学成分库,最终筛选出止嗽散的潜在活性成分有97个,止嗽散的部分活性成分见表1。
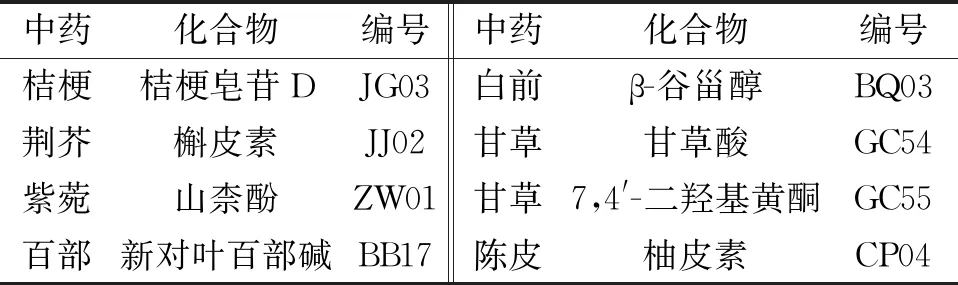
表1 止嗽散部分活性成分
2.2 交集靶点筛选结果 通过多重药物靶点预测方法对这97个化合物进行打靶,共获取2 118个靶点,与CVA对应的1 250个致病候选基因取交集后,最终获得共有基因靶点144个。
2.3 网络构建 为了探讨止嗽散对CVA治疗的分子机制,构建PPI和C-T-D网络。图1展示由143个节点和1 884个边组成的PPI网络。分析该网络拓扑参数,得到靶基因的平均度值为26.35,度值越大,节点大小越大,对应的重要程度越高。取度值前10位的靶基因作为核心靶点(见表2)。

图1 止嗽散治疗CVA的核心基因的PPI网络
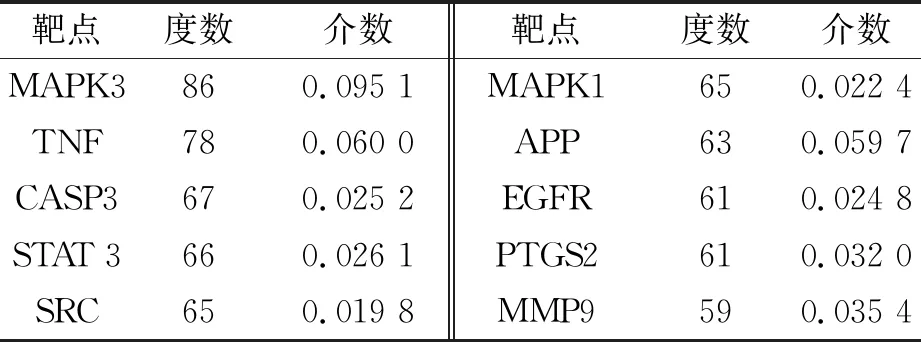
表2 止嗽散靶基因中排名前10的潜在靶点
此外,通过分析C-T-D网络,得到该网络节点的平均度值为8.73。其中,排名前列的分别是白前苷元C、7,4′-二羟基黄酮、甘草酸、新对叶百部碱、β-谷甾醇等(见表3)。例如,甘草中甘草酸可以通过减轻哮喘小鼠模型的气道炎症缓解哮喘症状。此外,Chung等发现,百部中新对叶百部碱对豚鼠咳嗽模型的镇咳作用最强。因此,将这些化合物作为止嗽散治疗CVA的关键成分。
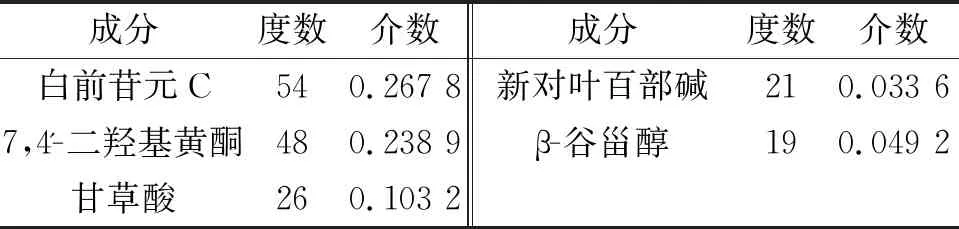
表3 止嗽散治疗CVA的关键化合物信息
2.4 生物学功能富集分析 对144个潜在靶点进行生物学功能富集分析,图2提示止嗽散治疗CVA的主要通路是PI3K/Akt信号通路、核因子-κB(nuclear factor kappa B,NF-κB)信号通路和缺氧诱导因子-1(hypoxia-inducible factor-1,HIF-1)信号通路。为了进一步阐明止嗽散治疗CVA的分子机制,笔者将止嗽散的潜在靶点映射到这3条关键信号通路(见图3)上。

图2 生物学功能富集分析弦图

注:“→”表示激活,“┥”表示抑制
2.5 分子对接 从止嗽散有效成分中选取度值和介数靠前的核心成分,筛选出与CVA相关的3个核心靶点进行分子对接(见表4)。从表4发现,这3个关键的靶点与其关键的化合物的结合能均为负值,表示两者间具有一定的结合活性。而当结合能小于-5 kJ/mol时,两者具有较强的结合活性;当结合能小于-7 kJ/mol时,两者具有强烈的结合活性。对接结果说明止嗽散中关键化合物与核心靶点均具有较强的结合活性。

表4 关键化合物和关键靶点的结合能
选取结合力排名靠前的化合物β-谷甾醇与其关键靶点EGFR,作出两者的空腔结合图(见图4)。从图4可见,位于EGFR蛋白结合空腔中,分子β-谷甾醇与EGFR周围的氨基酸残基SER-720形成一个氢键作用,长度为0.29 nm。正是这些氢键形成的作用力使这些化合物牢牢地固定在活性位点处。

图4 止嗽散关键化合物β-谷甾醇与其关键靶点EGFR的结合空腔图
3 讨论
本研究发现,止嗽散治疗CVA的关键活性成分有桔梗皂苷D、白前苷元C、新对叶百部碱、β-谷甾醇、甘草酸和7,4′-二羟基黄酮等。其中,桔梗皂苷D具有祛痰和抗炎活性。此外,白前中β-谷甾醇可以抑制Th2细胞因子的升高,防止气道炎症,具有治疗过敏性哮喘的作用。而甘草中7,4′-二羟基黄酮显著降低嗜酸性粒细胞性肺部炎症患者血清IgE、IL-4、IL-13水平。因此,止嗽散治疗CVA的机制与其活性成分减少气道炎症反应,降低气道高反应,抑制气道重塑有关。
在核心靶点中,甘草酸和7,4′-二羟基黄酮作用于前列腺素内过氧化物合酶2(prostaglandin-endoperoxide synthase 2,PTGS2),而PTGS2与哮喘的炎症反应有密切的联系。此外,7,4′-二羟基黄酮可作用于基质金属蛋白酶9(matrix metalloproteinase-9,MMP-9)和表皮生长因子受体(epidermal growth factor receptor,EGFR)。MMP-9属于蛋白酶超家族,可降解构成肺泡壁和基底膜的蛋白成分。研究表明,气道炎症部位的MMP-9活性较高,是气道重塑的重要标志物。哮喘患者支气管上皮中EGFR高表达,EGFR信号通路的过度激活通常参与气道黏液过度分泌,并在慢性气道炎症中引发ERK1/2、PI3K、Akt激酶的激活。因此,可以推测7,4′-二羟基黄酮对PTGS2、MMP-9、EGFR的靶向作用可能是止嗽散治疗CVA的作用机制。
生物学功能富集结果显示,止嗽散治疗CVA的主要信号通路有PI3K-Akt、NF-κB和HIF-1信号通路等。首先,PI3K/Akt信号通路在细胞的生长、增殖、转移、凋亡和炎症递质的形成过程中产生重要的作用。经PI3K激活的Akt利用磷酸化作用抑制或激活其下游Caspase9、Bad等靶基因,对细胞的增殖、凋亡、分化等起调控作用。例如,在PI3K/Akt信号通路中, Bad的磷酸化减少Bad与Bcl-2或Bcl-xl的结合,使Bad的促凋亡作用减轻,而Akt磷酸化可以继续磷酸化Caspase 9,使其活性消失,同样可以减轻促凋亡作用。这些表明活化后的Akt能维持气道平滑肌细胞的增殖与凋亡的平衡状态。另有文献报道,PI3K/Akt通路与哮喘病程有关联,PI3K可影响气道平滑肌的增殖以及嗜酸性粒细胞的招募,并影响肺部炎症和感染的有害反应和保护性反应之间的平衡,调节粒细胞的募集、活化、凋亡。同时,有研究发现,调节PI3K/Akt信号通路中基因的表达,可有效减轻哮喘老鼠的气道重塑,从而达到治疗哮喘的目的。
其次,NF-κB是细胞中重要的转录调节因子。NF-κB在哮喘发病机制和急慢性炎症反应机制中起到重要作用,与树突状细胞、上皮细胞和嗜酸性粒细胞的生长、分化、炎症因子的释放、基因的表达有关。例如,在哮喘大鼠肺组织中NF-κB p65、NF-κB p50表达水平较高,IκBα表达水平较低,而止嗽散中柚皮素能下调NF-κB p65、NF-κB p50的表达水平,上调IκBα的表达水平,从而减轻哮喘大鼠的气道炎症及细胞损伤。
此外,HIF-1由HIF-1α和HIF-1β两个亚基组成,在低氧状态下可激活多种靶基因的转录,并且对于细胞生长发育和生理应激及在某些病理过程中起着重要作用。当前已发现在过敏性气道炎症发展中HIF-1α存在过表达。王莉等通过药物进行干预,使HIF-1α表达水平下调,结果哮喘小鼠气道炎症的症状得到明显缓解。这与本研究结果一致。所有这些结果都表明,止嗽散可能通过抑制HIF-1信号通路治疗CVA。最后,分子对接结果显示,止嗽散中潜在活性成分与其关键靶点的良好结合力是由其结合位点处稳定的氢键导致的,进而验证了本研究靶点预测方法的可靠性。
综上,本研究通过整合药物代谢动力学数据进行多重药物靶点预测和分子对接分析,对止嗽散治疗CVA的分子作用机制进行多途径、多靶点研究,今后仍需要对止嗽散中关键成分抗CVA的作用进行验证。

