蛞蝓多糖的鉴定及其含量测定*
韦秀莎,黄金石,吴娅妮,高雨桐,陈 铭,黄仁彬
(广西医科大学药学院,南宁 530021)
蛞蝓(Limax)属腹足类腹足纲蛞蝓科,一种有肺的软体动物,俗称“鼻涕虫”。《神农本草经》卷四下品、《本草纲目》、《中药大辞典》等中医药书籍对蛞蝓性味归经、功效主治均有记载,主治蜈蚣咬伤、痔热肿痛、脚胫烂疮、清热祛风、消肿解毒、破痰通经、中风歪僻、筋脉拘挛、惊痫、喘息、喉痹、咽肿、痈肿、丹毒、经闭、症瘕等。药理研究发现,蛞蝓提取物具有抗肿瘤、平喘等多方面的作用,且其毒性较低[1-3]。现代研究表明,蛞蝓含蛋白、多糖等多种成分。陈亮等[4]研究发现,蛞蝓抗癌有效成分不是蛋白,有可能是多糖。但目前缺乏对水溶性蛞蝓多糖的结构及其含量的研究,因此,本组对水提法获得的蛞蝓多糖进行鉴定,初步确定其结构,测定其含量,为研究蛞蝓多糖的药理作用奠定基础。
1 材料与方法
1.1 试药和仪器
蛞蝓,采自广西百色,经广西中医药研究院赖茂祥教授鉴定,确定为腹足类腹足纲蛞蝓科蛞蝓(Limax)。低温高速冷冻离心机(德国Eppendorf 公司);倒置显微镜(日本Olympus 公司);万分之一电子天平(梅特勒一托利多公司);紫外可见分光光度计(上北京谱析TV-1901);傅里叶红外光谱仪(美国珀金埃尔莫Spectrum 100)。所用到的化学试剂均为分析纯。
1.2 蛞蝓的性状鉴别与显微鉴别[5]
根据《中国药典》2020版的项目要求第15项,对本次实验采集的蛞蝓全虫大小、颜色、器官、气味等特征进行性状观察。将蛞蝓全虫置于4%甲醛溶液中固定,24 h后,进行标本修剪、漂洗、脱水、透明、透蜡、包埋、切片与展片、烘片,中性树脂封片,苏木精—伊红(HE)染色后,通过显微镜对蛞蝓横切面组织形态进行观察。
1.3 蛞蝓多糖的提取
称取蛞蝓全虫1 kg,液料比2∶1加入蒸馏水进行破壁匀浆,4 000 r/min低温离心15 min,弃上层漂浮物和下层沉淀,得粗提液,加80%乙醇醇沉24 h,离心,收集沉淀,低温真空干燥,研磨均匀,过40 目筛,得蛞蝓粗多糖[6]。
1.4 蛞蝓多糖的鉴定试验[7]
取200 mg的蛞蝓多糖溶解于10 mL蒸馏水中,超声助溶30 min,得蛞蝓多糖溶液。采用Molish 反应和斐林反应鉴定蛞蝓多糖。Molish 反应:分别取1 mL 的蒸馏水阴性对照溶液和蛞蝓多糖溶液于试管中,然后加4滴α-萘酚试剂,摇匀后沿管壁缓缓滴加浓硫酸1 mL,观察液面交界处是否有紫环。斐林反应:分别取1 mL的蒸馏水阴性对照溶液和蛞蝓多糖溶液于试管中,再分别往试管滴加事先配好的斐林试剂1 mL,沸水浴10 min,观察试管底部是否有砖红色沉淀。
1.5 蛞蝓多糖的组成分析[8-9]
样品a溶液的制备:称取蛞蝓全虫1 kg,液料比2∶1 加入蒸馏水进行破壁匀浆,4 000 r/min 低温离心15 min,弃上层漂浮物和下层沉淀,得粗提液,冷冻干燥得样品a 溶液。样品b 溶液的制备:同“1.3项”。样品酸水解:于20 mL 具塞试管中,分别加入125 mg 样品a 溶液和样品b 溶液,后加入10 mL 2 mol/L的硫酸,混匀,置于105 ℃的烘箱水解4 h,冷却至室温,加入碳酸钡中和水解液,然后离心20 min(10 000 r/min),吸取上清液,过滤,分别得样品a、b水解液,置于4 ℃冰箱保存备用。标准糖溶液的制备:分别称取100 mg的L-阿拉伯糖、D-半乳糖、L-鼠李糖、D-核糖、D(+)-无水葡萄糖对照品,加10 mL水,配制成10 mg/mL 的标准单糖溶液。分别吸取0.5 μL 标准糖溶液,3 μL 样品a、b 水解液点样于同一硅胶G 薄层板上,以正丁醇—甲醇—氯仿—冰乙酸—蒸馏水(25∶9∶5∶3∶3)作为展开剂展开,取出后待薄层板晾干,喷以苯胺—二苯胺磷酸溶液,105 ℃加热至斑点清晰,于日光下检视。
1.6 蛞蝓多糖红外光谱结构鉴定[6,10]
称取0.5 mg蛞蝓多糖样品,与110 mg溴化钾研磨成粉末,混匀,按照仪器条件进行测定。
1.7 含量测定[11-15]
1.7.1 对照品与供试品的制备 对照品溶液的制备:精密称取葡萄糖对照品1.0 mg,加蒸馏水定容至10 mL,得浓度为0.1 mg/mL 的葡萄糖对照品溶液。供试品溶液的制备:称量50 mg蛞蝓多糖,加蒸馏水定容至10 mL,超声30 min,过滤,量取滤液1 mL,定容至10 mL,备用。
1.7.2 测定波长的选择 以蒸馏水为空白,取葡萄糖对照品与样品溶液按标准曲线“1.7.4项”操作,于400~600 nm波长范围内扫描。
1.7.3 显色条件的考察 6%苯酚用量考察:分别在7个试管内加入对照品1.0 mL,逐管加入6%苯酚溶液0.6 mL、0.8 mL、0.9 mL、1.0 mL、1.1 mL、1.3 mL,摇匀,迅速加入5 mL 浓硫酸,沸水浴15 min,冷却,测定波长485 nm处的吸光度值。浓硫酸用量考察:分别在5 个试管内加入对照品1.0 mL、6%苯酚溶液1.0 mL,摇匀,逐管迅速加入浓硫酸3.0 mL、4.0 mL、5.0 mL、6.0 mL、7.0 mL,沸水浴15 min,冷却,测定波长485 nm 处的吸光度值。水浴温度考察:分别在5 个试管内加入对照品溶液1.0 mL、6%苯酚溶液1.0 mL,摇匀,迅速加入浓硫酸5.0 mL,分别于水温为25 ℃、40 ℃、60 ℃、80 ℃、100 ℃条件下反应15 min,冷却,测定最大波长485 nm 处的吸光度值。显色时间的考察:分别在4 个试管内加入对照品溶液1.0 mL、6%苯酚溶液1.0 mL,摇匀,迅速加入浓硫酸5.0 mL,分别于沸水反应15 min、30 min、45 min、60 min,冷却,测定485 nm处的吸光度值。
1.7.4 标准曲线的制备 精密吸取葡萄糖对照品0.1 mL、0.2 mL、0.3 mL、0.4 mL、0.5 mL、0.6 mL、0.7 mL、0.8 mL、0.9 mL、1.0 mL,用蒸馏水补足体积至1 mL,加入6%苯酚溶液1 mL,摇匀,迅速精密量取5 mL 浓硫酸滴加入试管,沸水浴15 min,冷却。测定波长485 nm处的吸光度值。
1.7.5 方法学考察 稳定性试验:取一份蛞蝓多糖,同“1.7.1 项”法制备供试品,分别于0 min、30 min、60 min、90 min、120 min 同“1.7.4 项”法测定波长485 nm 处吸光度值,并计算RSD 值。重复性试验:取6份同一批次蛞蝓多糖,同“1.7.1项”法制备供试品,同“1.7.4 项”法测定485 nm 波长处的吸光度,并计算RSD 值。精密度试验:精密称定50 mg蛞蝓多糖,同“1.7.1 项”法制备供试品,同“1.7.4 项”法在485 nm波长处连续重复测定6次吸光度值,并计算RSD 值。加样回收率:按表2 精密称取6 份已知多糖含量的蛞蝓多糖,同“1.7.1项”法制备成供试品溶液,分别按表2加入不同含量的葡萄糖标准品,同“1.7.4项”法测定485 nm波长处的吸光度,根据吸光度值,计算得平均回收率。
1.7.6 蛞蝓多糖含量测定 取1 mL 供试品溶液,同“1.7.4项”法在485 nm波长处测定吸光度,根据吸光度值计算以葡萄糖计的多糖百分含量。
2 结果
2.1 蛞蝓性状鉴别与显微鉴别
蛞蝓呈长梭状,两头小,中间大,体长30~55 mm,体宽6~12 mm;体表呈灰褐色,同时伴有零星又细小的褐色斑点,体表光滑有黏液;头部有两对触角,前端一对各有眼一个,后端一对较长,触角可以自由伸缩;其右侧附近有椭圆形生殖孔,气腥味咸,见图1。通过显微镜对蛞蝓横切面组织形态进行观察,可以看到蛞蝓最外层为表皮组织,紧贴着是大量的粘液腔,还有大而散列的消化腔,泄殖腔器官明显,见图2。

图1 蛞蝓外观图

图2 蛞蝓HE染色图(×200)
2.2 蛞蝓多糖的鉴定试验
蒸馏水的Molish 反应虽然有分层,但无紫环,而蛞蝓多糖液面交界处有清晰可见的紫环;蛞蝓多糖的斐林反应有明显有砖红色沉淀,而蒸馏水的斐林反应呈现与斐林试剂相同的颜色,无沉淀,提示提取物是含有还原糖的多糖,见图3。

图3 蛞蝓多糖的鉴定试验
2.3 蛞蝓多糖的组成分析
通过薄层色谱分析蛞蝓多糖的单糖成分,观察到蛞蝓多糖主要由葡萄糖和半乳糖组成,见图4、表1。

表1 蛞蝓多糖水解物和标准单糖的Rf值

图4 蛞蝓多糖薄层色谱图
2.4 蛞蝓多糖红外光谱结构鉴定
该样品在4 000.00~600.00 cm-1区域内具有多糖类物质的一般特征。3 420.17 cm-1附近的强吸收峰是糖分子中—OH 的伸缩振动吸收峰;2 961.37 cm-1和2 930.63 cm-1分别为C—H 的2 个伸缩振动吸收峰;1 648.05 cm-1处的强吸收峰说明蛞蝓多糖含有糖醛酸;1 545.63 cm-1处出现振动吸收是N—H键的弯曲振动;1 401.23 cm-1处吸收峰为=CH2的变形吸收峰;1 385.24 cm-1处的吸收峰是C—H 变角振动峰;1 240.15 cm-1处吸收峰是C—O 伸缩振动峰;在1 077.69 cm-1处的吸收峰是吡喃糖环羟基的变角振动吸收峰;929.12 cm-1处吸收峰说明含有α和β-吡喃环型糖苷键,见图5。以上结果表明,蛞蝓多糖是含有吡喃环型糖苷键和酰胺键的酸性多糖。

图5 蛞蝓多糖红外光谱图
2.5 含量测定
样品和对照液的最大吸收波长均为485 nm,因此本次试验选择485 nm为测定波长,见图6。随着6%苯酚的用量增加,吸光度值先升高后降低,当6%苯酚用量为1.0 mL 时,吸光度达到峰值,因此,本次实验6%苯酚的用量为1.0 mL;随着浓硫酸的用量增加,吸光度值先升高后降低,当浓硫酸用量为5.0 mL 时,吸光度达到峰值,因此,本次实验浓硫酸选择的用量5.0 mL;在40~80 ℃的吸光度值变化趋于平缓,在100 ℃时,吸光值达到峰值,故本次实验选择的水浴温度为100 ℃;随着反应时间的延长,吸光度值呈下降趋势,故本次实验选择的沸水浴反应时间为15 min,见图7。以吸光度为纵坐标,浓度为横坐标,绘制标准曲线,得线性回归方程式A=0.0104C-0.0305(R2=0.9994)。在方法学考察中,稳定性试验RSD 值为0.10%(n=6),重复性试验RSD值为1.75%(n=6),精密度试验RSD 值为0.08%(n=6),加样回收率为98.70%,RSD为1.13%(表2)。以葡萄糖计蛞蝓多糖的平均含量为18.47%。

表2 加样回收试验结果n=6
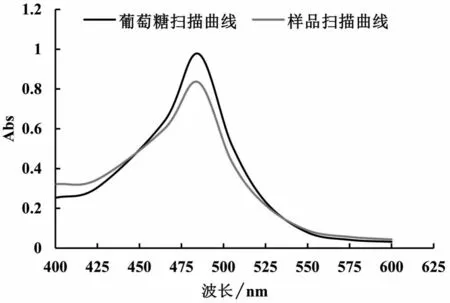
图6 葡萄糖对照品与样品的波长扫描图

图7 显色条件的考察
3 讨论
在进行多糖的鉴别实验前,先对蛞蝓药材进行性状鉴别,显微鉴别,保证药材的可靠性。多糖的常用鉴别方法有Molish 和斐林反应。Molish 反应虽不具有专属性,但可鉴别药品中是否含有糖类,斐林反应可以鉴别药品中是否含有还原糖,根据实验结果得知提取物含有还原糖的多糖。薄层色谱实验过程中,为了寻找合适的鉴别条件,实验前期对展开系统、展开距离、耐用性进行了考察,最终确定展开条件为:展开剂为正丁醇—甲醇—氯仿—冰乙酸—蒸馏水(25∶9∶5∶3∶3);上行展开距离为8 cm,选择硅胶G板为薄层板、苯胺—二苯胺磷酸为显色剂,日光下检视,25 ℃条件下跑板。在多糖的水解实验前期探索了氢氧化钠,强氧化钡,碳酸钡的中和效果,发现碳酸中和得到的斑点比较集中清晰。用碳酸钡中和水解液,容易降低单糖的浓度,只有含量高的单糖斑点易显现出来,为了避免这种情况发生,本次实验选择了2 种样品水解液进行多糖组成成分分析,最终确定蛞蝓多糖主要由半乳糖和葡萄糖组成。红外光谱技术在中药的鉴别中非常重要,本研究通过傅里叶红外光谱仪检测,证实提取物质含有吡喃环型糖苷键和酰胺键的酸性多糖。在测定多糖含量前期,已经对6%苯酚的用量,硫酸的用量,反应温度,显色时间进行考察,最终得出6%苯酚用量为1 mL,浓硫酸用量为5 mL,显色时间为15 min,显色温度为100 ℃为最佳反应条件。选择苯酚—硫酸法测定蛞蝓多糖含量,因为该法简便,且重复性、稳定性良好。
本研究先用观察法、HE 染色法对蛞蝓药材进行鉴别,再用molish 反应、斐林反应、薄层色谱法,傅里叶变换红外光谱法和苯酚—硫酸法对蛞蝓多糖进行鉴别、组成、结构和含量测定,可为将来研究蛞蝓多糖的结构以及药理作用提供参考。

