基于UPLC-Q-TOF-MS/MS分析多物料多流程炮制对半夏化学成分的影响
崔美娜,钟凌云*,兰泽伦,张大永,杨 明*
基于UPLC-Q-TOF-MS/MS分析多物料多流程炮制对半夏化学成分的影响
崔美娜1,钟凌云1*,兰泽伦2,张大永2,杨 明1*
1. 江西中医药大学,江西 南昌 330004 2. 四川新荷花中药饮片股份有限公司,四川 成都 611731
应用超高效液相色谱串联四级杆飞行时间质谱(UPLC-Q-TOF-MS/MS)定性分析多物料多流程炮制半夏的化学成分,分阶段探究不同物料和流程对其成分的影响。比较成分差异性,为阐明多物料多流程炮制对化学成分的变化规律提供参考。将通过不同物料和炮制流程得到的半夏阶段产物分为4组,分别为浸漂半夏、石灰制半夏、甘草制半夏、法半夏,以生半夏作为对照。以5种样品醇提液为供试品溶液,采用Waters Acquity BEH C18色谱柱,乙腈-0.1%甲酸水为流动相进行二元梯度洗脱,质谱采用电喷雾离子化源(ESI),正、负离子全扫描的一级和二级质谱信息。通过一级精确质荷比和二级的碎片数据,参考文献、数据库以及质谱裂解规律,对5组样品所含成分进行鉴定。鉴定了101个化学成分,分别为7个生物碱类、5个氨基酸类、5个酰胺类、14个醇胺类、26个黄酮类、6个溶血磷脂酰胆碱类、14个脂肪酸甘油脂类、6个有机酸类、7个皂苷类及11个其他类型化合物。通过UPLC-Q-TOF-MS/MS对5组样品化学成分进行分析,发现半夏炮制前后化学成分存在明显差异,物料甘草为半夏引入了甘草黄酮、三萜皂苷类成分,而物料石灰对成分引入影响不大,推测出石灰的加入是为了在不影响药效成分的前提下减轻半夏毒性。与生品相比,浸漂后的半夏成分减少,推测浸漂的过程中,会使成分有所损失。而经过多物料多流程炮制的法半夏减少了刺激性毒性成分,增加了甘草黄酮类成分。该方法快速、准确,为探究半夏多物料多流程炮制机制提供一种新的策略,对其药效物质深入研究及质量控制具有重要意义。
半夏;法半夏;超高效液相色谱串联四级杆飞行时间质谱;多物料多流程炮制;甘草黄酮
半夏(Thunb.) Breit为天南星科植物半夏的干燥块茎。其性温,味辛,有毒,归脾、胃、肺经。具有燥湿化痰、降逆止呕、消痞散结的功效。生用毒性大,一般炮制加工后使用。法半夏是半夏炮制品中最为常用的品种,采用多物料多流程炮制而成,具有燥湿化痰之功效。用于痰多咳喘、痰饮眩悸、风痰眩晕、痰厥头痛等[1]。多物料多流程是半夏炮制方法的核心,法半夏通过浸漂、浸泡,加入甘草、石灰进行炮制而成,其长于祛痰止咳[2-4],在炮制过程中功效发生了改变。本研究主要探讨多物料多流程炮制对半夏化学成分的影响,将法半夏的炮制分为几个阶段,将中间产物也作为样品进行研究,分别为浸漂半夏、甘草半夏、石灰半夏、法半夏。并与生品进行比对,分析不同流程、物料炮制成分差异性,以期为阐明半夏经多物料多流程炮制成为法半夏后功效发生变化的物质基础及其临床合理应用提供依据。
半夏中含有多种生物活性成分,如生物碱类、醇醚类、脂肪酸及酯类、多糖、挥发油、氨基酸、半夏蛋白和无机元素等[5],具有止咳化痰、抗肿瘤、抗炎等药理作用。而法半夏经过炮制后增加了甘草成分,其中包括三萜皂苷类成分、黄酮类成分[6]。目前,国内外对半夏及其炮制品中的化学成分差异进行了大量的研究,为半夏的现代应用研究提供一定的理论依据。然而半夏不同物料不同流程分阶段考察物质基础未见有研究报道。虽有许多学者分别对生品和炮制品做过一定的分离研究,但是单一物料、单一流程分别对化学成分的影响仍是未知的。为了明确其活性成分并阐述多物料多流程的物质基础和作用机制,其全成分分析研究十分必要。本实验首次应用超高效液相色谱串联四级杆飞行时间质谱(UPLC-Q-TOF-MS/MS)技术,对半夏多物料多流程不同阶段炮制品进行了研究分析,根据色谱保留时间、精确相对分子质量、分子碎片峰和相关文献,对主要色谱峰的来源进行了归属,并对其化学结构进行了推断和鉴定。本研究比较全面地阐明了其化学组成,为以后药效物质基础研究和质量控制奠定了基础。
1 材料与仪器
Triple-TOFTM5600+型质谱仪(配有ESI源和APCI,Triple-TOFTM5600+System),AnalystTF 1.6 software数据采集软件,Peakview 1.2 Software 数据处理软件系统(美国AB Sciex);30AD型高效液相色谱系统(包括DGU-30A3在线真空脱气机,LC30AD泵,SIL-30AC自动进样器,CBM-30A控制器,CTO-30A色谱柱温箱,日本岛津公司)。
生半夏购自中国药材市场,批号20180816,由江西中医药大学葛菲教授鉴定为天南星科植物半夏(Thunb.) Breit.的块茎,甘草批号20181224,产自内蒙古,由江西中医药大学葛菲教授鉴定为豆科植物甘草Fisch的干燥根和根茎。屈臣氏蒸馏水;乙腈(质谱级,德国Merck公司),甲酸(质谱级,美国ACS公司)。
2 方法
2.1 色谱条件
采用Waters Acquity BEH C18色谱柱(100 mm×2.1 mm,1.7 μm),0.1%甲酸水溶液(A)-乙腈(B)为流动相,梯度洗脱(0~8 min,5%~30% B;8~12 min,30%~56% B;12~20 min,56%~58% B;20~28 min,58%~72% B;28~38 min,72%~75% B;38~41 min,75%~80% B;41~46 min,80% B;46~56 min,80%~85% B;56~60 min,85% B;60~67 min,85%~90% B;67~72 min,90% B;72~77 min,90%~95% B;77~79 min,95%B;79~79.1 min,95%~5% B;79.1~82 min,5% B~100% A)。柱温40 ℃,进样量5 μL,体积流量0.25 mL/min。
2.2 质谱条件
离子喷射电压5500 V;去簇电压分别为100 V;碰撞电压分别是40 eV;去溶剂温度500 ℃;雾化气50 kPa;辅助加热气50 kPa;气帘气40 kPa;离子模式正离子;电喷雾离子源;质量扫描范围/100~1000;碰撞活化扫描15 eV。
2.3 样品炮制方法及供试品溶液的制备
2.3.1 浸漂半夏 称取半夏100 g,用水浸泡至内无干心,约14 h。
2.3.2 甘草半夏 称取半夏100 g,用水浸泡至内无干心。另取甘草15 g,加水煎煮2 h至药液充分煎出呈金黄色,加入半夏,浸泡5 d。
2.3.3 石灰半夏 称取半夏100 g,用水浸泡至内无干心。另取10 g 生石灰,加120 mL水,再加入半夏,搅匀,浸泡5 d。
2.3.4 法半夏 称取半夏100 g,用水浸泡至内无干心(每日换水1次)。另取甘草10 g,加1.5倍水煎煮2 h,即得甘草煎汁。加入15 g生石灰,搅匀,再加入浸透的半夏,浸泡5 d,至剖面淡黄色,口尝微有麻舌感即可。将炮制好的法半夏至干燥箱中70 ℃干燥至干。在炮制过程中pH值保持在12以上。
2.3.5 供试品溶液的制备[5]分别称取上述炮制品及生半夏各2 g,加入10倍量70%乙醇,浸渍30 min,微沸状态下回流提取60 min,滤过,再加入5倍量的70%乙醇到药渣回流30 min,滤过,合并提取液,静置,吸取10 min,经4000 r/min离心15 min,取上清液,稀释,0.22 μm微孔滤膜滤过即得供试品溶液。
3 结果
3.1 UPLC-TOF-MS对5种半夏中各类成分的快速鉴别
在色谱条件和质谱条件下,对总离子流图的色谱峰进行分析,见图1。采用Peakview 1.2软件鉴定推断化学成分并对其成分进行归类,对其主要碎片离子信息进行归属,见表1。根据ESI离子源的工作原理可知,化合物在ESI电离过程中采用正离子模式会得到准分子离子[M+H]+;当化合物经过离子源轰击后其结构中特定的化学键会发生断裂,产生相应的离子碎片。由于同一类化合物具有相近的化学键断裂方式,其共有的断裂碎片就可作为一类化合物的特征碎片离子,作为这类化合物结构鉴定的依据[6]。本研究根据化合物准确相对分子质量、准分子离子、特征碎片离子及其他碎片离子等信息,参考相关文献数据,初步定性101个化学成分,其中包括7个生物碱类、5个氨基酸类、5个酰胺类、14个醇胺类、26个黄酮类、6个溶血磷脂酰胆碱类、14个脂肪酸甘油脂类、6个有机酸类、7个皂苷类成分。结果见表1。

1-生品 2-浸漂半夏 3-甘草半夏 4-石灰半夏 5-法半夏
3.2 氨基酸类化合物的裂解规律
氨基酸为含有氨基和羧基的一类有机化合物,在正离子模式下,准分子离子脱去NH3或COOH是氨基酸类化合物典型的质谱裂解规律[7]。有些氨基酸会丢失NH3,但是此实验没有检测到此碎片离子,因此推测此类氨基酸中N为NH[5]。通过数据库分析,在样品中共鉴定出5个氨基酸类成分。如化合物oleoylglycine,软件给出的分子式C20H37NO3,质谱信号显示准分子离子为/340.284 6 [M+H]+,丢失COOH后得到二级碎片/294.284 3 [M+H-COOH]+。综上信息,结合文献报道,故推测为油酰甘氨酸质谱信息,二级质谱和裂解方式见图2。用相同方法鉴别氨基酸类化合物。
3.3 酰胺类化合物的裂解规律
结合数据库查询分析与相关文献报道[5],共鉴定出半夏中酰胺类化合物5个,以化合物amide HPL为例,通过数据库匹配得到该成分分子式为C16H33NO,其准分子离子为/256.263 5 [M+H]+,通过Peakview 1.2对二级全扫描质谱分析,发现很多二级质谱碎片产生130.123 3 [M+H-C9H17]+、116.108 4 [M+H-CH2]+、102.093 7 [M+H-CH2]+、88.079 3 [M+H-CH2]+、74.063 3 [M+H-CH2]+特征碎片离子。结合文献报道,此类化合物的特征裂解途径为酰胺键、酯键断裂生成相应的碎片离子[8],故推测为酰胺质谱信息,其二级质谱图与质谱可能裂解途径分别见图3。

表1 半夏及其炮制品中化学成分UPLC-Q-TOF-MS/MS分析
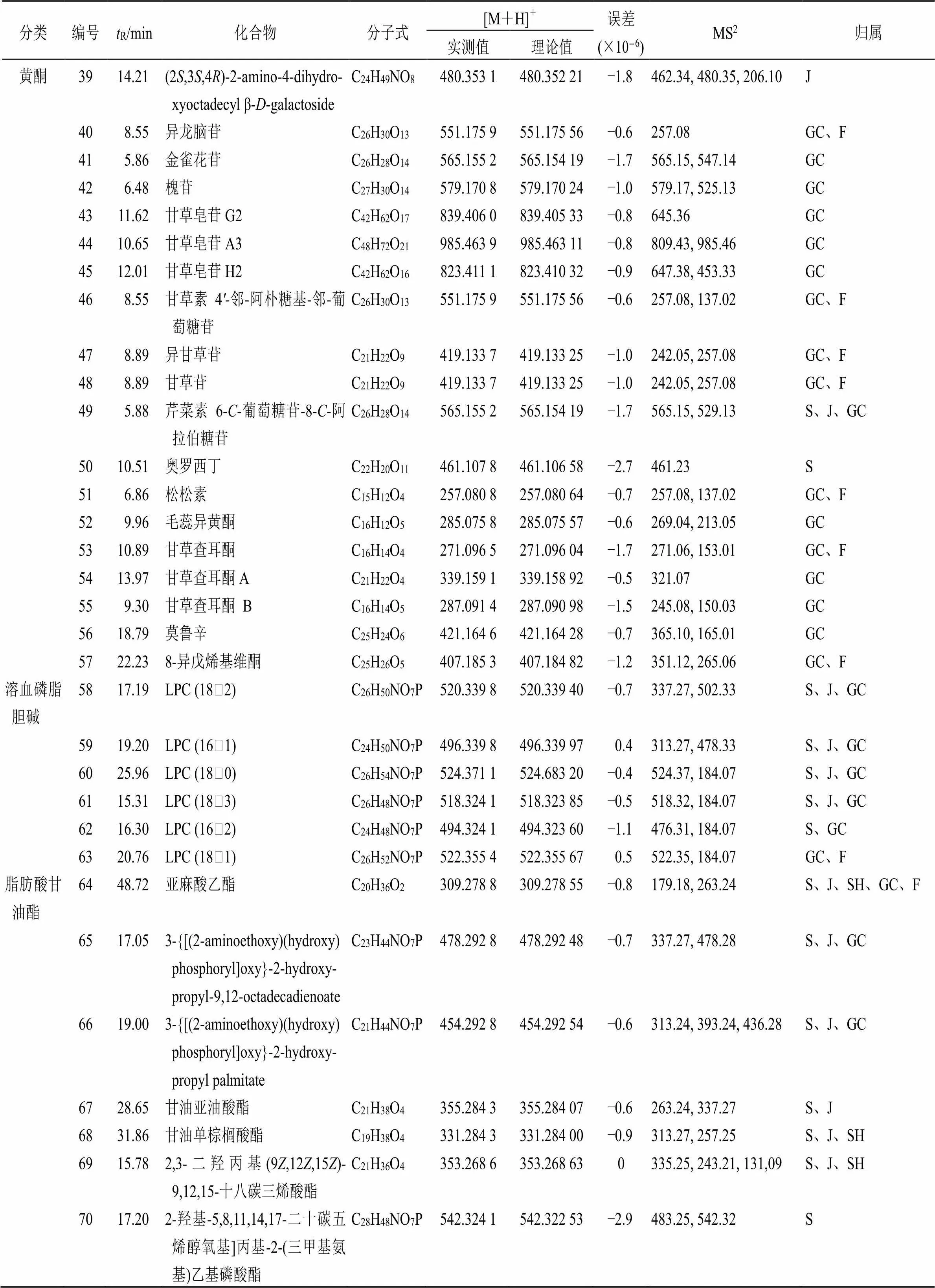
续表1

续表1
S-生品半夏 J-浸漂半夏 SH-石灰制半夏 GC-甘草制半夏 F-法半夏
S-J- Soaked and bleachedSH-made of lime GC-licorice pinellia F-
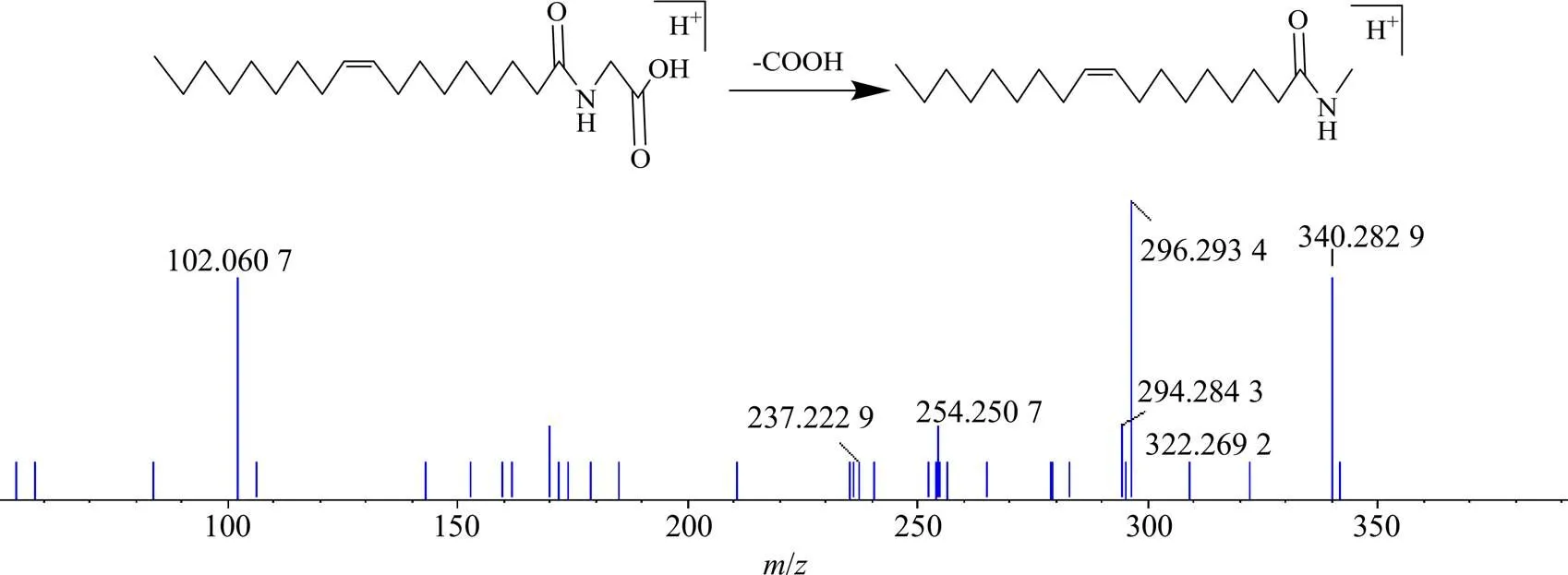
图2 Oleoylglycine的二级质谱图和可能的裂解途径
3.4 黄酮类化合物的裂解规律
关于此类化合物,RDA裂解是其典型的质谱裂解规律之一[9],物料甘草引入许多甘草黄酮成分,以化合物licochalcone A为例,通过数据库匹配得到该成分分子式为C21H22O4,根据其裂解规律可以判断结构中存在糖取代基,其准分子离子为/339.159 1 [M+H]+,通过RAD裂解得到二级碎片离子/271.100 1 [M+H-C5H7]+,107.050 6 [M+H-C14H15O3]+,与文献报道的质谱信息相符[9]。其二级质谱图与质谱可能裂解途径分别见图4。
3.5 溶血磷脂胆碱类化合物的裂解规律
溶血磷脂酰胆碱也称溶血卵磷脂,不溶于丙酮、乙醚,有强溶血作用[5]。以化合物LPC (18∶3)为例,通过数据库匹配得到该成分分子式为C26H48NO7P。通过Peakview 1.2对二级全扫描质谱分析,发现很多二级质谱产生/184.073 5 [M+H-C21H39O3]+特征碎片离子,如图5所示,推测其为溶血磷脂酰胆碱类化合物。

图3 Amide HPL的二级质谱图和可能的裂解途径
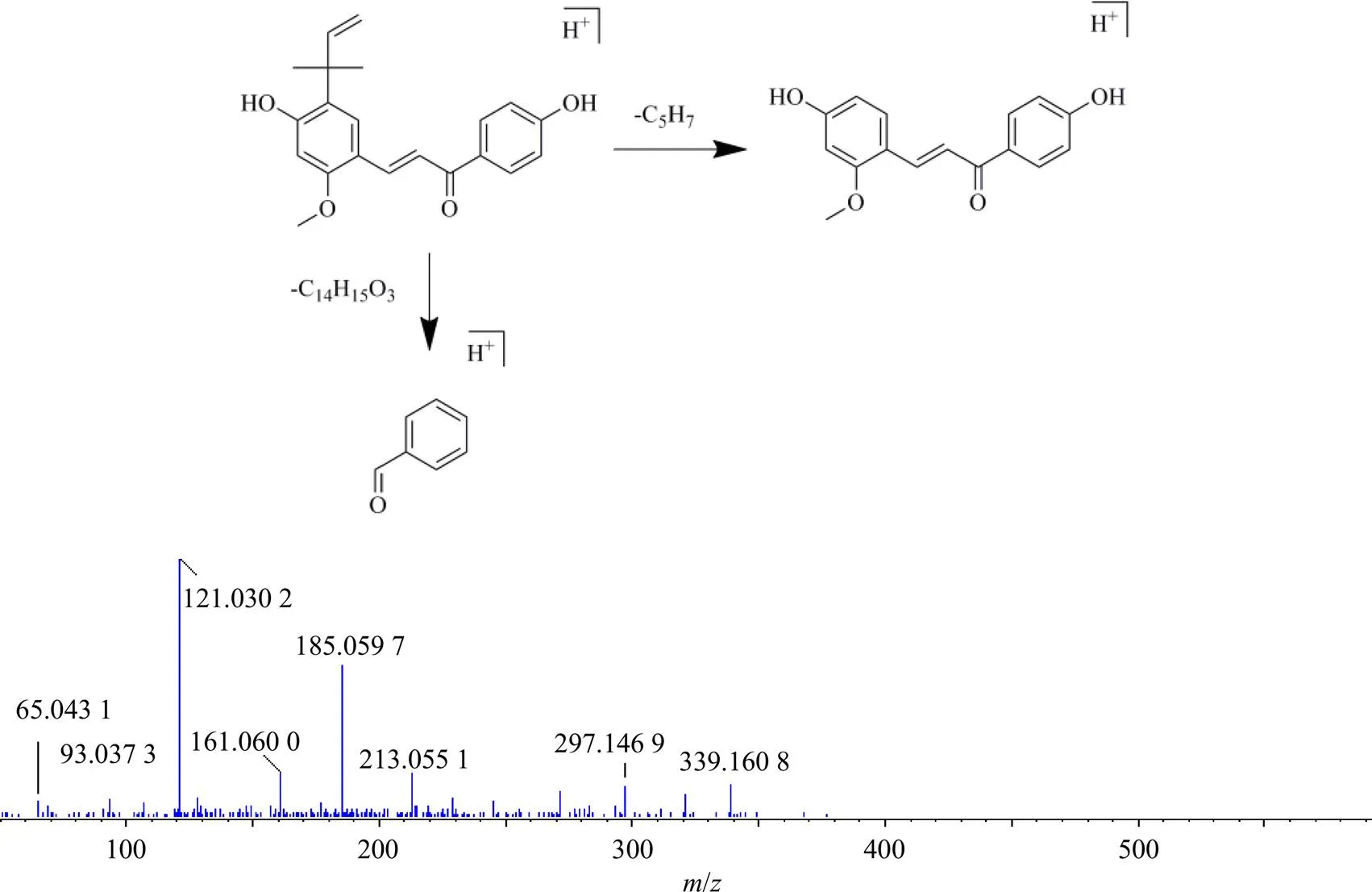
图4 licochalcone A的二级质谱图和可能的裂解途径

图5 LPC (18∶3) 的二级质谱图和可能的裂解途径
3.6 皂苷类化合物的裂解规律
三萜皂苷类化合物为甘草的主要成分[11-13],甘草制半夏和法半夏中甘草三萜皂苷在ESI正离子源轰击下产生准分子离子[M+H]+。以化合物glycyrrhizic acid为例,通过数据库匹配得到该成分分子式为C42H62O16,其准分子离子为/823.411 1 [M+H]+,二级碎片分别为471.345 7 [M+H-C12H15O12]+、647.375 1 [M+H-C6H7O6]+。综上信息,结合文献报道,故推测为皂苷类质谱信息,二级质谱和可能的裂解方式见图6。
4 讨论
本研究从5组样品中鉴定出101个化学成分,半夏炮制前后化学成分存在明显的差异,半夏在不同物料不同流程炮制的过程中,化学成分发生改变。物料甘草增加了甘草黄酮、三萜皂苷类成分,石灰无增加。其中,甘草酸为主要的皂苷类成分,其在口服后会水解为甘草次酸,对小鼠氨水引咳、二氧化硫引咳模型均有明显的镇咳作用[13-14]。此外,黄酮类化合物中甘草苷、异甘草素[15]及芹糖甘草苷[16]均有文献研究证实具有祛痰止咳平喘的功效。由此可见,法半夏中含有的2类甘草成分可能是其炮制后长于祛痰止咳的物质基础。而浸漂对半夏成分会有损失,因此在炮制过程中,应减少浸漂时间,即浸漂至内无干心即可。

图6 glycyrrhizic acid的二级质谱图和可能的裂解途径
石灰虽然对成分增加无影响,但其在解毒方面作用显著。有研究发现,石灰水的强碱性可使半夏的草酸钙针晶结合蛋白变性,不再具有刺激性作用;石灰水本身可以使半夏中部分针晶发生絮凝,使少量可能仍有刺激性的针晶混凝在大量淀粉粒或黏液细胞当中,无法释放,从而使半夏的刺激性丧失[5],达到减毒目的。报道认为,半夏中含有溶血磷脂酰胆碱类物质,可引起炎症反应及神经元髓鞘脱失和不同程度变性。可推测其可能与半夏的刺激性毒性相关[17],本实验结果表明,石灰制半夏和法半夏均无此成分,由此更确定半夏多物料多流程炮制中,加入石灰主要以解半夏毒为主。因此法半夏炮制石灰甘草共用达到减毒增效作用。
本研究通过UPLC-Q-TOF-MS/MS全面分析半夏化学成分为药效物质基础研究和质量控制奠定了一定的基础。分析不同物料不同流程对半夏成分的影响,可以为阐明半夏经炮制后功效发生变化的物质基础及其临床合理应用提供依据。
利益冲突 所有作者均声明不存在利益冲突
[1] 中国药典[S]. 一部. 2020: 123-124.
[2] 杨冰月, 李敏, 吴发明, 等. 基于止咳效价评价半夏及其炮制品品质的方法研究 [J]. 中草药, 2015, 46(17): 2586-2592.
[3] 苏彬, 李书渊, 陈艳芬, 等. 半夏及其炮制品镇咳祛痰作用的比较 [J]. 广东药学院学报, 2013, 29(2): 181-184.
[4] 游秋云, 王平. 生半夏、法半夏水提物对小鼠镇静催眠作用的比较研究 [J]. 湖北中医杂志, 2013, 35(3): 3-5.
[5] 翟兴英, 张凌, 李冰涛, 等. 采用UPLC-Q-TOF- MS/MS分析半夏药材中的化学成分 [J]. 中国实验方剂学杂志, 2019, 25(7): 173-183.
[6] 杨彬, 王媛, 田梦, 等. 基于UPLC-Q-TOF-MS/MS研究法半夏中甘草化学成分 [J]. 中国实验方剂学杂志, 2017, 23(3): 45-49.
[7] Liu Y M. Simultaneous determination of three β-carbolines al-kaloids and ephedrine in pinellia tuber by using LC/ESI(+)/MS/MS [D]., 2011: 20-26.
[8] 王佳月, 高广慧, 朱嘉琪, 等. UPLC-Q-TOF-MS/MS技术研究了哥王水提物中的化学成分 [J]. 中国中药杂志, 2019, 44(14): 3055-3063.
[9] 赵艳敏, 刘素香, 张晨曦, 等. 基于HPLC-Q-TOF-MS技术的甘草化学成分分析 [J]. 中草药, 2016, 47(12): 2061-2068.
[10] 冷晶, 朱云祥, 陈璐琳, 等. 甘草中2个新三萜皂苷 [J]. 中草药, 2015, 46(11): 1576-1582.
[11] 陶伟伟, 段金廒, 杨念云, 等. 乌拉尔甘草皂苷类成分研究 [J]. 中草药, 2013, 44(12): 1552-1557.
[12] 李文斌, 罗琳, 赵益丹, 等. 基于文献计量分析的3种药用甘草的研究现状[J]. 世界中医药, 2019, 14(3): 624-632.
[13] 俞腾飞, 田向东, 李仁, 等. 甘草黄酮、甘草浸膏及甘草次酸的镇咳祛痰作用 [J]. 中成药, 1993, 15(3): 32-33.
[14] 韩洁, 赵晶, 田维毅, 等. 肠菌群体外转化对甘草药用成分及镇咳作用的影响 [J]. 安徽医科大学学报, 2012, 47(4): 422-424.
[15] 张明发, 沈雅琴. 甘草及其提取物对呼吸系统的药理作用 [J]. 现代药物与临床, 2010, 25(4): 262-267.
[16] Kamei J, Nakamura R, Ichiki H,. Antitussive principles of, a main component of the Kampo preparations Bakumondo-to (Mai-men-Dong- Tang) [J]., 2003, 469(1/2/3): 159-163.
[17] 钟凌云. 半夏刺激性毒性成分、炮制减毒机理及工艺研究 [D]. 南京: 南京中医药大学, 2007.
Effect of multi-material and multi-process processing on chemical composition ofbased on UPLC-Q-TOF-MS/MS
CUI Mei-na1, ZHONG Ling-yun1, LAN Ze-lun2, ZHANG Da-yong2, YANG Ming1
1. Jiangxi University of Chinese Medicine, Nanchang 330004, China 2. Sichuan New Lotus Chinese Herbal Medicine Co., Ltd., Chengdu 611731, China
To analyze the chemical constituents of Banxia ()processed by multi-material and multi-process by ultra-high performance liquid chromatography tandem quadrupole time-of-flight mass spectrometry (UPLC-Q-TOF-MS/MS), and explore the effects of different materials and processes on its constituents. Through comparing the difference of components, to provide reference for elucidating the change rule of chemical components ofbefore and after processing.The varieties ofobtained by different materials and processing procedures were divided into four groups: soaked,made of lime,made ofetand Fabanxia ().was used as a control. The alcohol extracts of five samples were used as the donor solution, Waters Acquity BEH C18column (100 mm × 2.1 mm, 1.7 μm) was used, acetonitrile-0.1% formic acid water was used as the mobile phase for binary gradient elution, electrospray ionization source (ESI) was used for mass spectrometry, and the primary and secondary mass spectra information of positive and negative ion full scan was used.The components contained in the five groups of samples were identified by the first order exact mass to charge ratio, the second level fragment data, references or databases, and the law of mass spectrometry fragmentation. A total of 101 chemical constituents were preliminarily characterized, including seven alkaloids, five amino acids, five amides, 14 alcoholamines, 26 flavonoids, six lysophosphatidylcholines, 14 fatty acid glycerolipids, six organic acids, seven saponins, and 11 compounds of other types.UPLC-Q-TOF-MS/MS is used to analyze the chemical constituents of different processed varieties of, and it is found that there are significant differences in the chemical constituents before and after processing of.introduces licoflavone and triterpene saponins for, while lime has little effect on the introduction of components. It is speculated that the addition of lime is to reduce the toxicity ofwithout affecting the pharmacodynamic components. Compared with raw products, the components ofdecreased after soaking, and it was speculated that the components ofmay be lost during soaking., which is processed through multiple materials and multiple processes, reduces the irritating and toxic ingredients and increases the licoflavone. This method is rapid and accurate, providing a new strategy for exploring the multi-process processing mechanism of, which is of great significance for the in-depth study of its pharmacodynamic substances and quality control.
(Thunb.) Breit;; Ultra-high performance liquid chromatography tandem quadrupole time-of-flight mass spectrometry; multi-material multi-process; licoflavone
R284.1;R283.6
A
0253 - 2670(2021)24 - 7428 - 10
10.7501/j.issn.0253-2670.2021.24.004
2021-04-17
国家重点研发计划(2018YFC1707201)
崔美娜,在读硕士,主要从事中药炮制工艺及机理研究。Tel: 13699512559 E-mail: 13699512559@163.com
钟凌云,博士,教授,博士生导师,主要从事中药炮制研究。E-mail: ly1638163@163.com
杨 明,博士,教授,博士生导师,主要从事炮制制剂研究。E-mail: yangming16@126.com
[责任编辑 王文倩]

