忽略股浅动脉重建与普通球囊重建治疗股浅动脉狭窄/闭塞远期疗效对照研究
任洪成, 庄金满, 李 选, 李天润, 栾景源, 王昌明, 丁明超, 黄小勇
随着人口老龄化和饮食结构改变, 外周动脉疾病(peripheral arterial disease,PAD)发病率越来越高。 有文献报道国内 PAD 患者超过 3 000 万,5 年病死率约为30%, 每年因PAD 截肢患者为120~150 例/百万,严重影响患者生活质量[1]。 股浅动脉(superficial femoral artery,SFA)为 PAD 通常受累部位, 血管腔内重建术因创伤小、 恢复快逐渐成为治疗SFA 病变的主要方法,但存在术后再狭窄难题[2]。 为此,本中心提出忽略股浅动脉重建(superficial femoral artery nonrevascularization,nSFA)概念[3-4],即在保证PAD 患者髂动脉-股深动脉-膝下动脉(至少1 条流出道)通畅情况下,不予重建SFA,实施以药物治疗为基础的步行运动锻炼治疗方案。 该方案可降低围手术期远端血栓栓塞事件发生率,避免对SFA 内膜损伤,中期随访结果显示其治疗慢性PAD 患者的效果相仿于普通球囊扩张联合支架植入重建SFA 术[3-4]。本研究回顾性对比普通球囊扩张重建与nSFA 治疗SFA 狭窄/闭塞患者的远期效果、安全性、治疗费用及住院时间。 现将结果报道如下。
1 材料与方法
1.1 研究对象
收集 2014 年 1 月至 2016 年 4 月在北京大学第三医院和航天中心医院住院治疗的SFA 狭窄/闭塞患者电子病历资料。 入组标准:①年龄>40 岁;②Rutherford 分级2~5 级; ③可耐受血管腔内治疗; ④下肢彩色多普勒超声、CTA、MRA 或 DSA 检查证实SFA 重度狭窄或闭塞。 排除标准:①伴有严重心、脑血管病变,呼吸、肝、肾功能不全等无法耐受腔内治疗;②急性下肢动脉缺血;③半足以上坏疽需要截肢;④接受开放手术治疗;⑤凝血功能障碍,有出血倾向;⑥妊娠期或哺乳期;⑦对非离子对比剂过敏。 本研究已通过医学伦理委员会批准(IRB00006761-M202 0301)。
1.2 治疗方法
根据患者病变特点和病情决定治疗方法。
nSFA 组——①对于SFA 重度狭窄/闭塞且伴有髂动脉和/或股深动脉重度狭窄/闭塞患者, 腔内重建髂动脉和/或股深动脉:Seldinger 技术穿刺成功后,置入4 F 血管鞘和4 F 造影导管,高压注射器行造影明确靶血管病变部位,换入6 F/7 F 血管长鞘,经外周静脉给予肝素30~50 mg;路径图下导丝导管配合通过髂动脉和/或股深动脉狭窄、闭塞段,选择与靶血管直径相同或小于靶血管直径1 mm 普通球囊,以6~8 atm 压力扩张狭窄闭塞段2 min, 若残余狭窄仍>30%、病变出现弹性回缩或限流夹层,植入补救性支架;复查造影确认血管通畅后,拔除鞘管,血管缝合器缝合血管穿刺点。术后常规静脉泵入肝素抗凝治疗1 d,患者活化凝血酶原时间控制在70~90 s。 出院前及随访期间步行运动锻炼治疗:每次行走需达到下肢疼痛为止,每周至少3 次,每次行走时间由30 min逐渐增加至60 min(除外因疼痛休息时间),结合药物治疗。 ②对于SFA 重度狭窄/闭塞未伴有髂动脉和(或)股深动脉重度狭窄/闭塞患者,仅指导患者步行运动锻炼和药物治疗,以促进侧支循环建立。
经皮腔内血管成形术(PTA)组——①对于SFA重度狭窄/闭塞未伴有髂动脉和/或股深动脉重度狭窄/闭塞患者,以普通球囊扩张SFA,必要时植入补救性支架;②对于SFA 重度狭窄/闭塞且伴有髂动脉和/或股深动脉重度狭窄/闭塞患者, 同期腔内重建SFA和髂动脉,不处理股深动脉。 具体操作步骤同上述。
一般治疗:控制血压、控制血糖、降脂等,嘱患者戒烟。 扩张血管治疗:给予前列地尔等扩张血管药物。 术后医嘱:血管腔内介入术后6 个月内口服肠溶阿司匹林(100 mg/d)和西洛他唑(100 mg/12 h),6 个月后长期口服肠溶阿司匹林(100 mg/d)。
1.3 随访和疗效评价
门诊随访为主,必要时电话随访,截至2020 年7 月。 主要评价指标为Rutherford 分级、保肢率和生存率;次要评价指标为住院时间、治疗费用、主要不良事件发生率。
1.4 统计学方法
采用SPSS.24.0 软件进行统计学分析。服从正态分布数据以表示,组间比较用t 检验;非正态分布数据以M(P25,P75)表示,组间比较用 Mann-Whitney U 秩和检验。 计量资料以频数和率表示,组间比较用卡方检验,若理论数≤1,则用Fisher 精确检验。 Kaplan-Meier 生存曲线评估两组患者生存率和保肢率,Log-rank 检验比较两组间保肢率和生存率生存曲线差异。
2 结果
入组患者共 106 例(115 条患肢)。 其中 PTA 组59 例患者(60 条患肢),男 42 例(43 条患肢),女 17 例(17 条患肢);nSFA 组 47 例患者(55 条患肢),男 38例(45 条患肢),女 9 例(10 条患肢)。 两组患肢数均符合估计样本量。 两组患者基线资料和病变特征具可比性,差异无统计学意义(P>0.05),见表 1。 两组患者间基线Rutherford 分级差异无统计学意义(P>0.05),术后 1 年、2 年差异均无统计学意义(P>0.05);nSFA 组患者术后 3 年、4 年、5 年 Rutherford 分级改善均优于 PTA 组(P<0.05),见图 1。
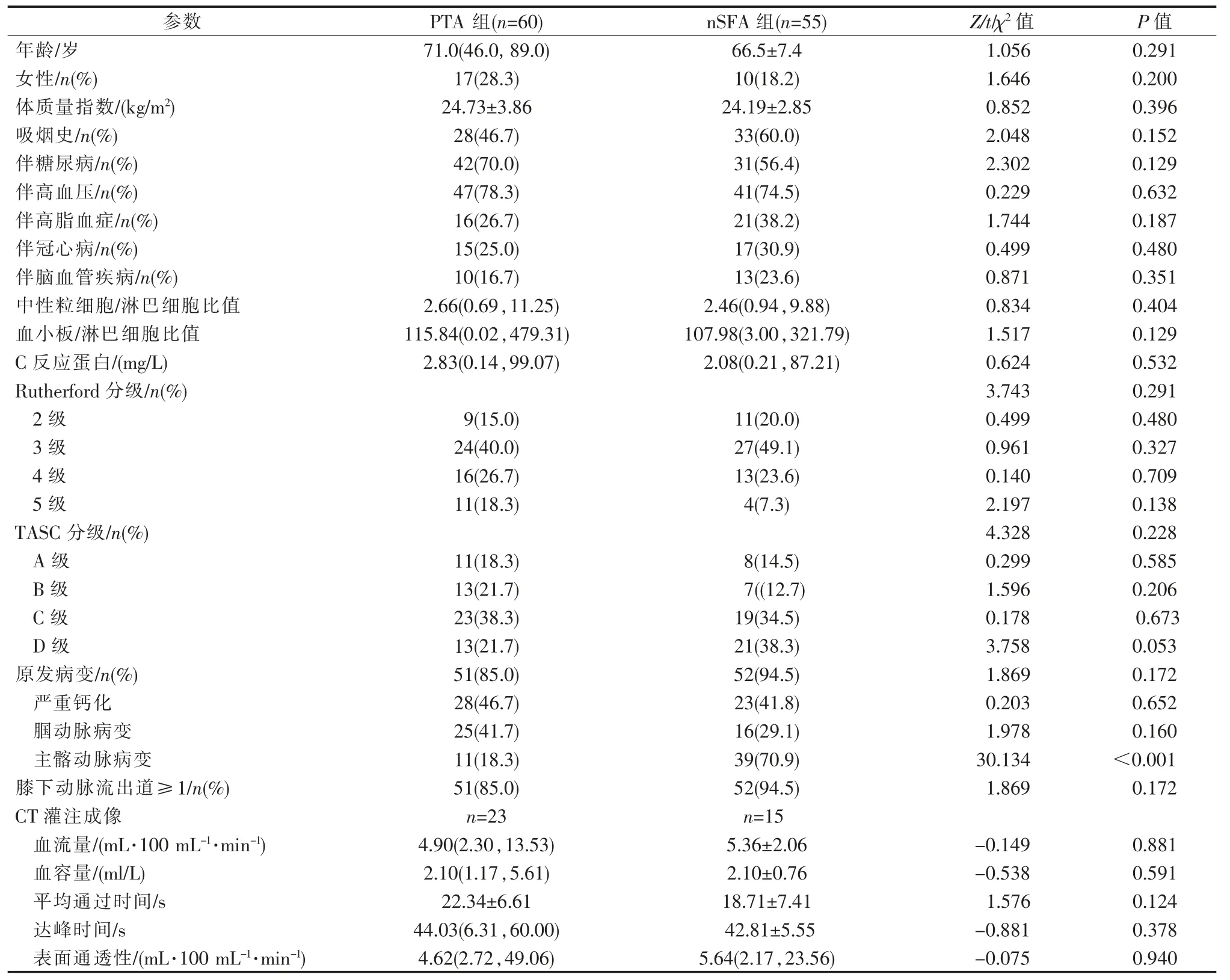
表1 两组患者基线资料和病变特征比较
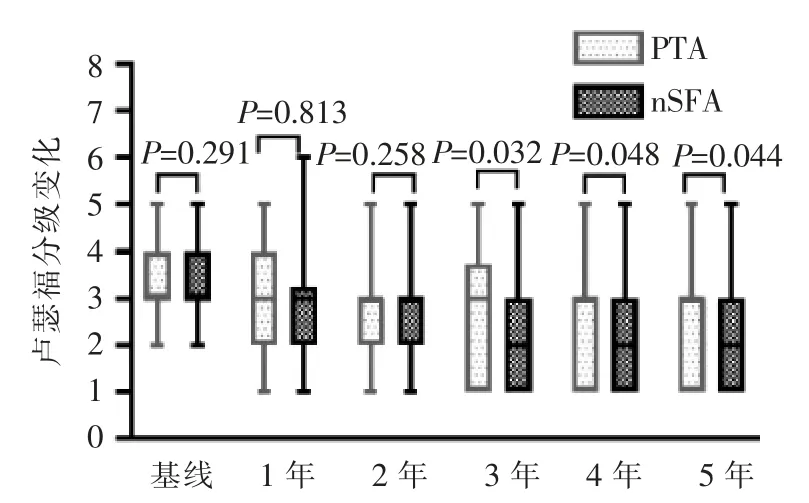
图1 两组患者Rutherford 分级比较
nSFA 组失访 1 例,随访时间为 60(22,77)个月,随访期46 例54 条患肢中截肢1 条;PTA 组均获随访,随访时间为 60(1,76)个月,随访期截肢 3 条。Log-rank 检验显示, 两组患者保肢率差异无统计学意义(P>0.05),见图 2。 nSFA 组随访期死亡 7 例,PTA 组随访期死亡18 例,nSFA 组患者总体生存率优于 PTA 组,但差异无统计学意义(P>0.05),见图 3。
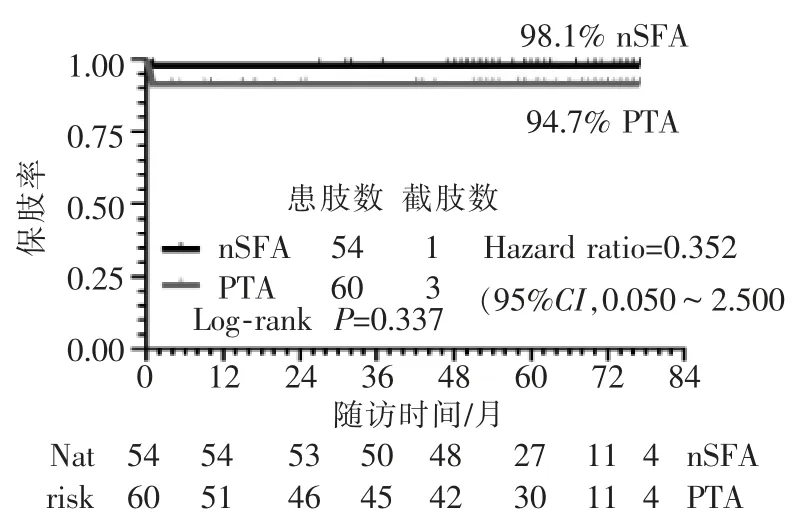
图2 两组患者保肢率比较
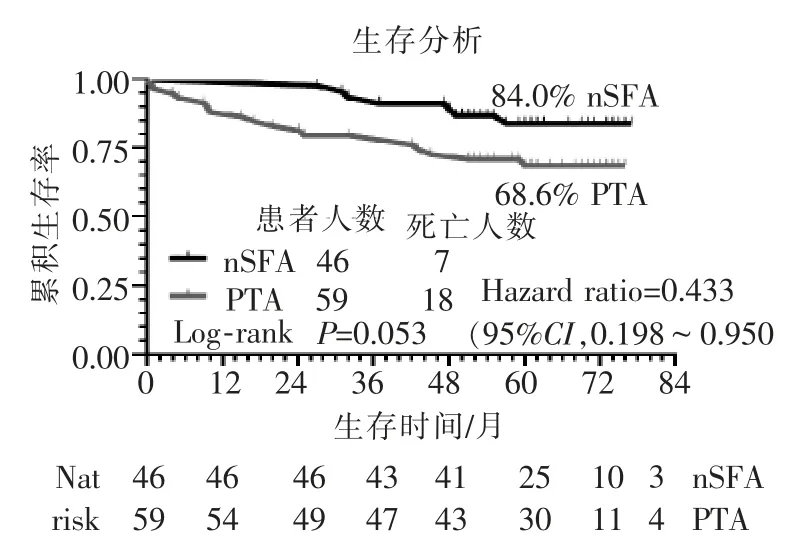
图3 两组患者生存率比较
nSFA 组患者平均住院时间、治疗费用、围手术期主要不良事件发生率、随访期间肢体相关主要不良事件发生率均低于PTA 组, 差异有统计学意义(均 P<0.05)。 见表 2。
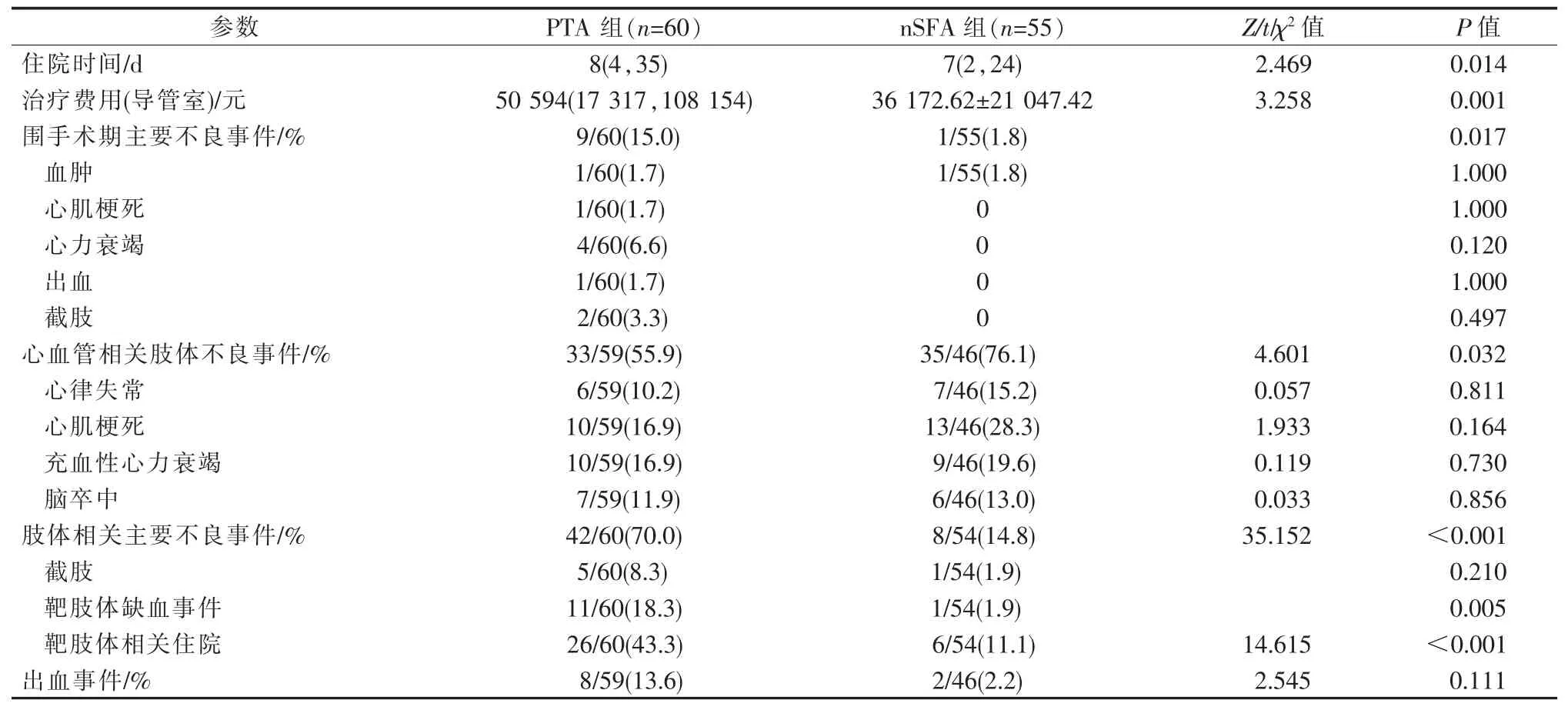
表2 两组患者住院时间、治疗费用、围手术期和随访期主要不良事件比较
3 讨论
PAD 血管腔内治疗中nSFA 治疗方案是基于以下3 点:①PAD 多表现为多节段病变,髂动脉-SFA-腘动脉段往往受累[5],SFA 受累尤为常见;股深动脉为短干多分支血管,较少受累及。 SFA 重度狭窄/闭塞时形成的髂动脉-股深动脉和膝下动脉侧支,对恢复下肢动脉血流灌注至关重要[6-7]。 ②髂动脉、股深动脉腔内治疗术后具有很好的远期通畅率[8]。SFA 因需承受弯曲、挤压、拉伸、扭转等多种复杂的生物力学作用,且富含平滑肌细胞,腔内治疗术后再狭窄发生率较高[9]。 ③步行运动锻炼可改善间歇性跛行患者跛行症状和生活质量[10]。 针对间歇性跛行保守治疗无效、肢体严重缺血的Rutherford 分级 2~5 级患者,血运重建具体策略尚无统一标准。 本研究发现对SFA 重度狭窄/闭塞、 膝下动脉至少有一条流出道患者行腔内血运重建时,仅重建髂动脉或股深动脉并忽略SFA,后期加强步行运动锻炼和药物治疗也是可行的。
本研究中两组患者间术后近期Rutherford 分级改善情况相仿,nSFA 组远期改善优于PTA 组。分析原因:①普通球囊重建SFA 虽可短期迅速改善下肢血供, 但腔内操作治疗时极易损伤非靶病变段血管; ②随着时间延长及原发病变进展,SFA 腔内重建术后可出现再狭窄; ③普通球囊重建髂动脉-股深动脉可改善下肢流入道血供,进一步促进侧支循环开放,提高远端血流灌注压,有助于患者临床症状缓解和后续步行运动锻炼开展。 步行锻炼虽起效慢,但侧支循环一旦形成,远期通畅率较高。 对于需要血运重建的Rutherford 分级5、6 级患者, 影像学准确评估和治疗方案制定非常重要[11]。 《下肢动脉硬化闭塞症诊治指南》[12]推荐腔内重建时应至少保证一条直达足部的膝下动脉流出道。 血管灌注区段(angiosome)和术中造影判定染色的靶病变血管(angiographsome)理论体系指导下膝下动脉重建术,是近年研究热点[13]。
本研究中nSFA 组患者围手术期主要不良事件发生率、随访期靶肢体相关不良事件发生率均低于PTA 组, 可能与 PTA 重建 SFA 重度狭窄/闭塞病变时,可引起远端血栓栓塞和SFA 闭塞段两端内膜损伤有关。 在对比两种治疗方法临床效果和安全性的同时,也需要考虑医疗成本和效价比问题。 本研究中nSFA 组患者平均治疗费用和住院时间均低于PTA 组,差异有统计学意义。
总之,SFA 重度狭窄/闭塞患者nSFA 重建方案与PTA 重建SFA 方案相比,远期疗效和安全性较好,治疗费用较低,尤其对于膝下动脉流出道较好的SFA 多节段闭塞患者,不失为腔内重建仍不理想情况下较好选择之一。 鉴于本研究为样本量较小的回顾性研究,尚需更高质量的随机对照研究进一步验证。

