从高砷铅阳极泥中回收As2O3试验研究
彭情亮,张旭泳
(江西铜业技术研究院有限公司,江西南昌 330096)
铅电解阳极泥中含有铅、锑、砷、铋、铜、金、银等有价元素,是重要的二次资源[1-2]。从铅阳极泥中综合回收有价金属时,杂质砷的存在会对操作环境造成污染,还会影响所回收产品质量[3],因此,在回收有价金属之前,有必要对铅阳极泥进行脱砷预处理。从铅阳极泥中预处理脱砷,目前现有工艺主要有火法工艺、湿法工艺和火法-湿法联合工艺[4-6]。火法脱砷主要有挥发焙烧法、还原焙烧法、熔炼法及水蒸气焙烧脱砷法。火法工艺较为成熟,适应性强,流程简单,但是存在脱砷率低、环境污染严重的缺点[7-8]。用湿法处理高砷铅阳极泥,砷能得到有效脱除。目前主要工艺有酸浸、碱浸、氯化等[9-13]。湿法工艺砷脱除率高,但会产生大量浸出液,且存在流程长、工序多、砷及其他有价元素回收复杂等缺点。火法-湿法联合工艺主要是苏打烧结—水浸脱砷,该工艺可以实现砷和其他有价金属的高效分离,但添加剂消耗量大,成本过高[14]。将砷从铅阳极泥中脱除只是处理砷的第一步,要彻底解决脱砷问题,就要将砷转化为可利用的产品或对环境无害的形态。试验研究了采用碱性加压浸出工艺将铅阳极泥中的砷浸出到溶液中,然后从浸出液中回收三氧化二砷,从而有效实现铅锌冶炼系统中砷的开路,也将砷转化为可利用的三氧化二砷。
1 试验部分
1.1 试验原料与试剂
试验原料:铅阳极泥取自某铅冶炼厂,自然堆存5~10 d,粉碎至粒径-100目,化学成分见表1,XRD物相分析结果如图1所示。铅阳极泥的XRD图谱中只出现Bi2O3和Ag3Sb的特征衍射峰,这可能是其他元素为非晶质形态的缘故。
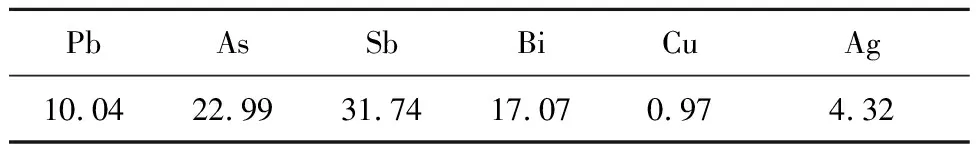
表1 铅阳极泥的化学组成 %
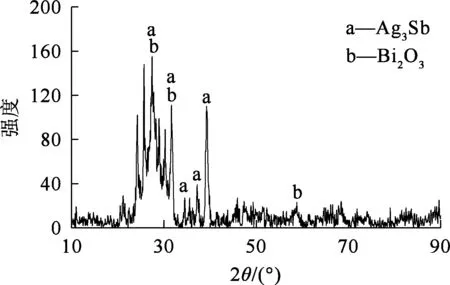
图1 铅阳极泥的XRD图谱
试验试剂:氢氧化钠、亚硫酸钠、硫酸,均为分析纯。
1.2 试验设备
GJ-4B型密封化验制样粉碎机,GS-5型加压釜(5 L),SHB-ⅢA型循环水式真空泵,KH-55A型电热鼓风干燥箱,万用电炉,PH-3S型酸度计。
1.3 试验原理与方法


式中,M表示Pb、Cu、Ag等金属离子。
As2O3还原沉淀:浸出液中加亚硫酸盐或二氧化硫进行还原,酸性条件下,五价砷被还原为三价砷;As2O3在酸性溶液中溶解度较低,通过蒸发浓缩即可结晶析出。涉及的主要反应如下:

试验步骤:1)称取一定量铅阳极泥、氢氧化钠放入烧杯,加水调浆后加入到反应釜中,拧紧螺母,打开升温开关、循环冷却水及机械搅拌桨,并通入压缩空气,控制出口气流以防止带出料浆;2)待釜内温度升至设定温度时开始计时,保温一定时间后停止加热,冷却至釜内温度为50 ℃后,关闭压缩空气;釜内压力归零后,打开,将料浆倒入烧杯并进行液固分离;3)量取500 mL滤液,置于电炉上加热,控制加热时间,待溶液体积减少为原来的1/3时停止加热,取下烧杯自然冷却至室温;4)对冷却后的溶液进行固液分离,固体即为砷酸钠;5)砷酸钠固体用水溶解,然后用硫酸调pH至一定范围,加入一定量还原剂亚硫酸钠,置于电炉上加热蒸发,待溶液体积减少至原来的1/4时停止加热,取下自然冷却并进行液固分离,固体烘干后,检测成分,分析物相。
2 试验结果与讨论
2.1 铅阳极泥的碱性加压浸出
铅阳极泥质量400 g,按试验设计的液固体积质量比与一定浓度NaOH溶液在加压釜中混合,搅拌升温,通压缩空气至1.20 MPa。反应一定时间后停止加热,釜体用冷却水冷却至70 ℃以下后出料并进行液固分离。
选定4因素3水平设计正交试验方案,考察液固体积质量比、NaOH质量浓度、反应温度、反应时间对砷浸出率的影响。正交试验因素、水平及结果见表2。
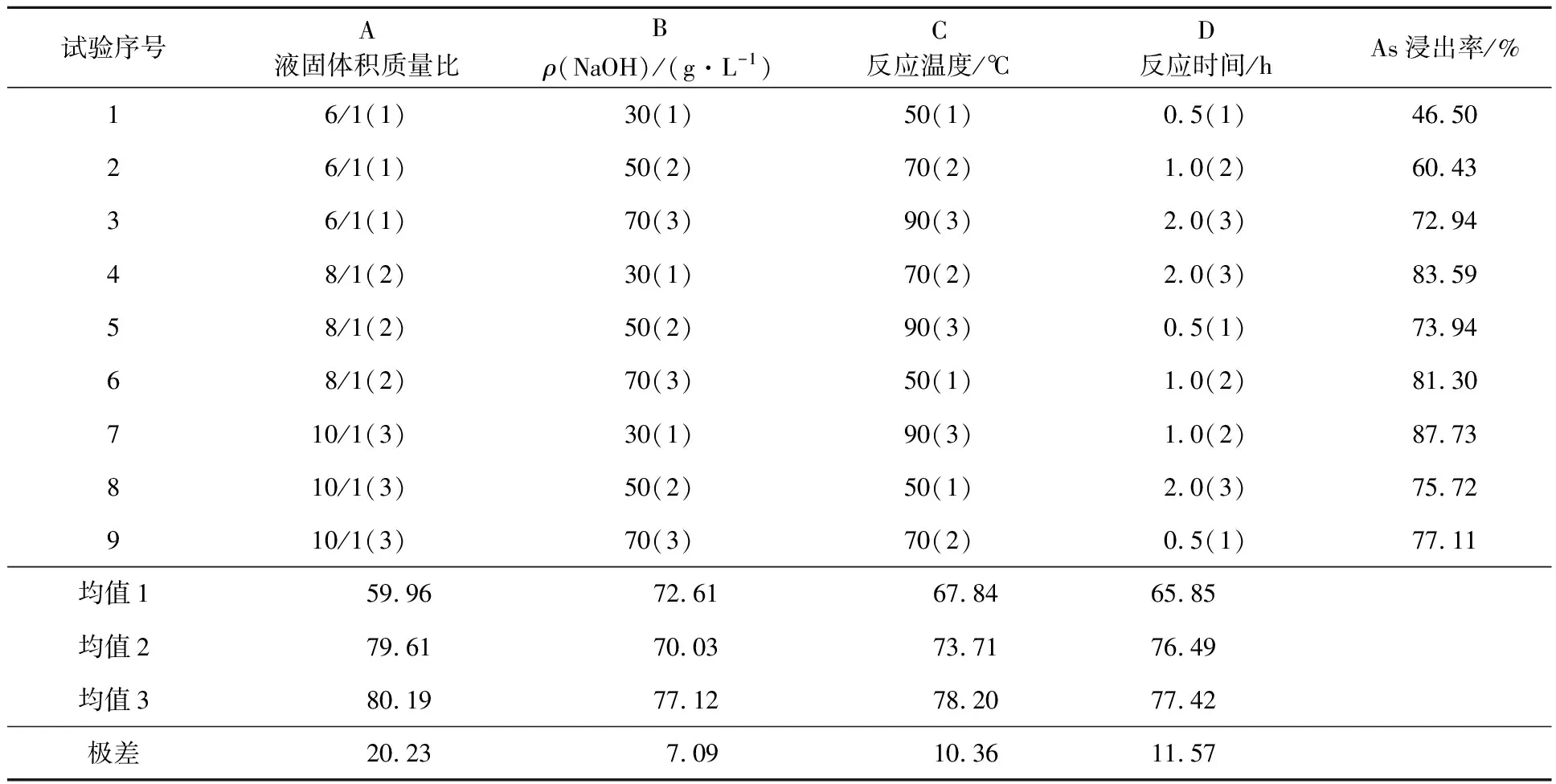
表2 正交试验因素、水平及结果
最优试验条件应为A3B3C3D3,但从成本角度考虑,不一定要选择最好水平。由表2看出:A3B1C3D2条件下,As浸出率最高。根据极差,各因素对试验结果的影响由大到小依次为A→D→C→B。
最优浸出条件为液固体积质量比10/1,NaOH质量浓度30 g/L,温度90 ℃,反应时间1.0 h。 最优条件下进行4组重复性试验,结果见表3。可以看出:采用加压氧化碱浸,砷浸出率在87%以上,其他金属几乎不被浸出或浸出率很低,有效实现了砷与其他有价金属的分离。
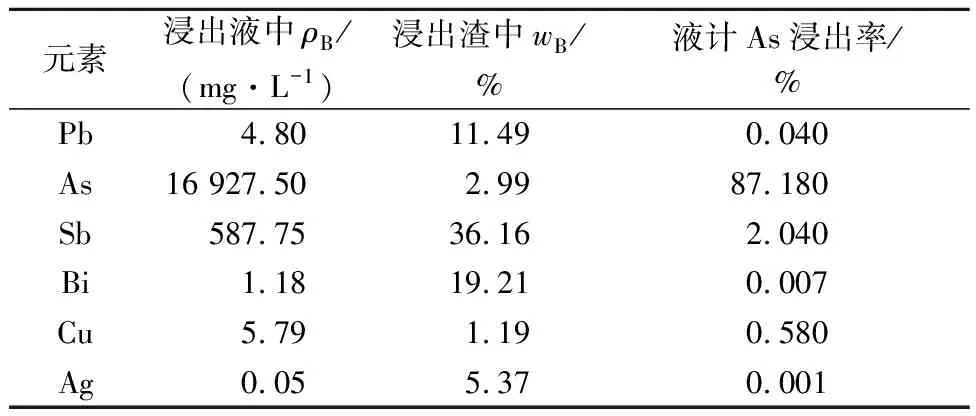
表3 最优条件下的综合试验结果
2.2 浸出液中砷酸钠的结晶
取表3浸出液500 mL,在电炉上加热蒸发,浓缩体积对砷酸钠结晶率的影响试验结果见表4。

表4 砷酸钠蒸发结晶试验结果
由表4看出:随溶液蒸发,砷结晶率逐渐升高。考虑到蒸发结晶成本,溶液体积蒸发至原体积的1/3即可,此时浸出液中89%的砷以砷酸钠形式结晶析出。砷酸钠成分见表5。结晶母液中砷质量浓度4.035 g/L,NaOH质量浓度23 g/L,补充水和NaOH后返回浸出。
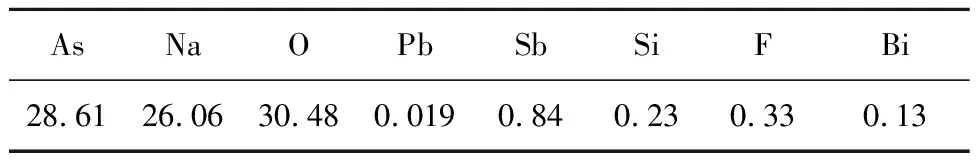
表5 结晶析出的砷酸钠成分 %
2.3 砷酸钠溶解还原制备三氧化二砷
取蒸发结晶所得砷酸钠50 g,用500 mL水溶解,调溶解液pH并加还原剂亚硫酸钠,再蒸发浓缩结晶三氧化二砷。
2.3.1 溶液初始pH的影响
控制还原剂亚硫酸钠加入量为理论加入量的1.5倍,常温下还原反应3.0 h,低温蒸发浓缩至原体积的1/4,再冷却至常温结晶4.0 h。溶液初始pH对产物中As2O3质量分数及As沉淀率的影响试验结果如图2所示。可以看出:产物中As2O3质量分数及As沉淀率随pH升高而降低;pH=0时,产物中As2O3质量分数及As沉淀率均达最大。但pH越低,所需硫酸的量就越大,综合考虑生产成本,控制溶液初始pH为1.0即可,此时产物中As2O3质量分数为88.24%,As沉淀率为80.34%。
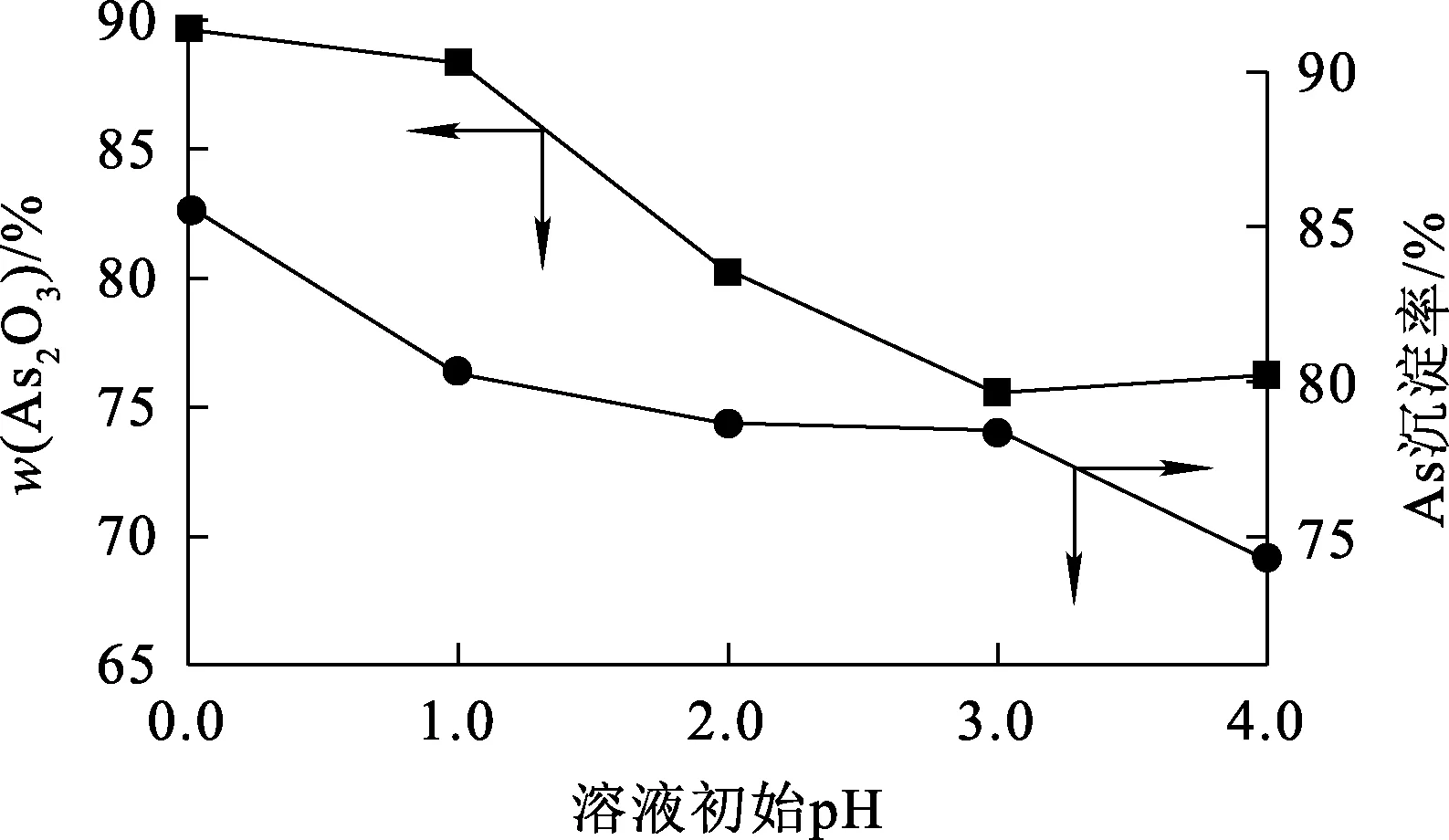
图2 溶液初始pH对产物中As2O3质量分数及As沉淀率的影响
2.3.2 还原剂加入量的影响
控制溶液初始pH=1.0,其他条件及操作方式不变,还原剂加入量(理论加入量倍数)对产物中As2O3质量分数及As沉淀率的影响试验结果如图3所示。可以看出:随还原剂亚硫酸钠加入量增加,产物中As2O3质量分数和As沉淀率均呈先升高后下降趋势。还原剂加入量过大,溶液中的其他杂质也会被还原并随As2O3一同沉淀,导致As2O3纯度下降。还原剂加入量为理论加入量的2.0倍时,产物中As2O3质量分数和As沉淀率都达到最大,分别为91.25%和81.14%。因此,确定适宜的还原剂加入量为理论加入量的2.0倍。
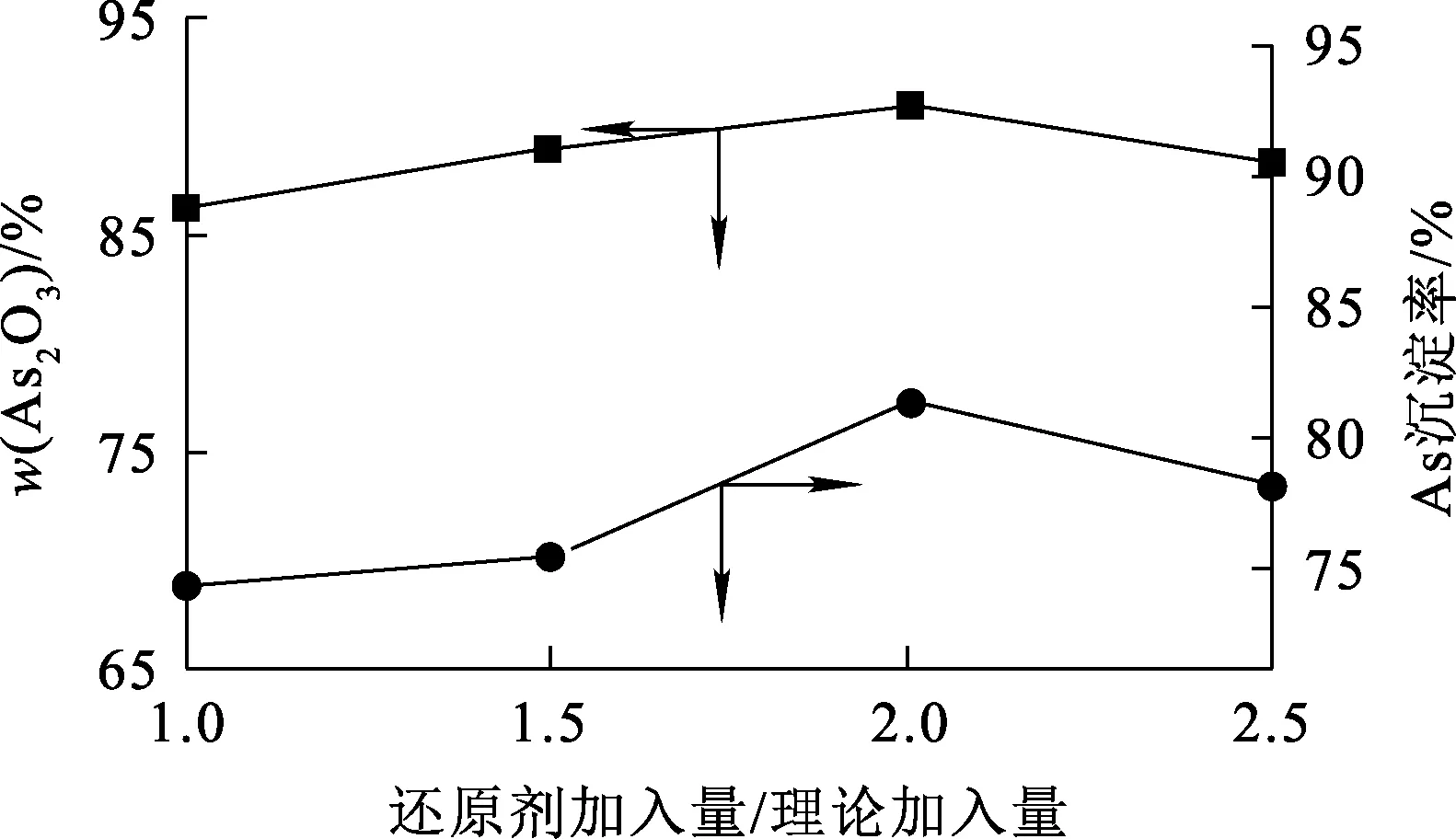
图3 还原剂加入量对产物中As2O3质量分数及As沉淀率的影响
2.3.3 反应时间的影响
控制溶液初始pH=1.0,亚硫酸钠加入量为理论加入量的2.0倍,其他条件及操作方式不变,反应时间对产物中As2O3质量分数及As沉淀率的影响试验结果如图4所示。
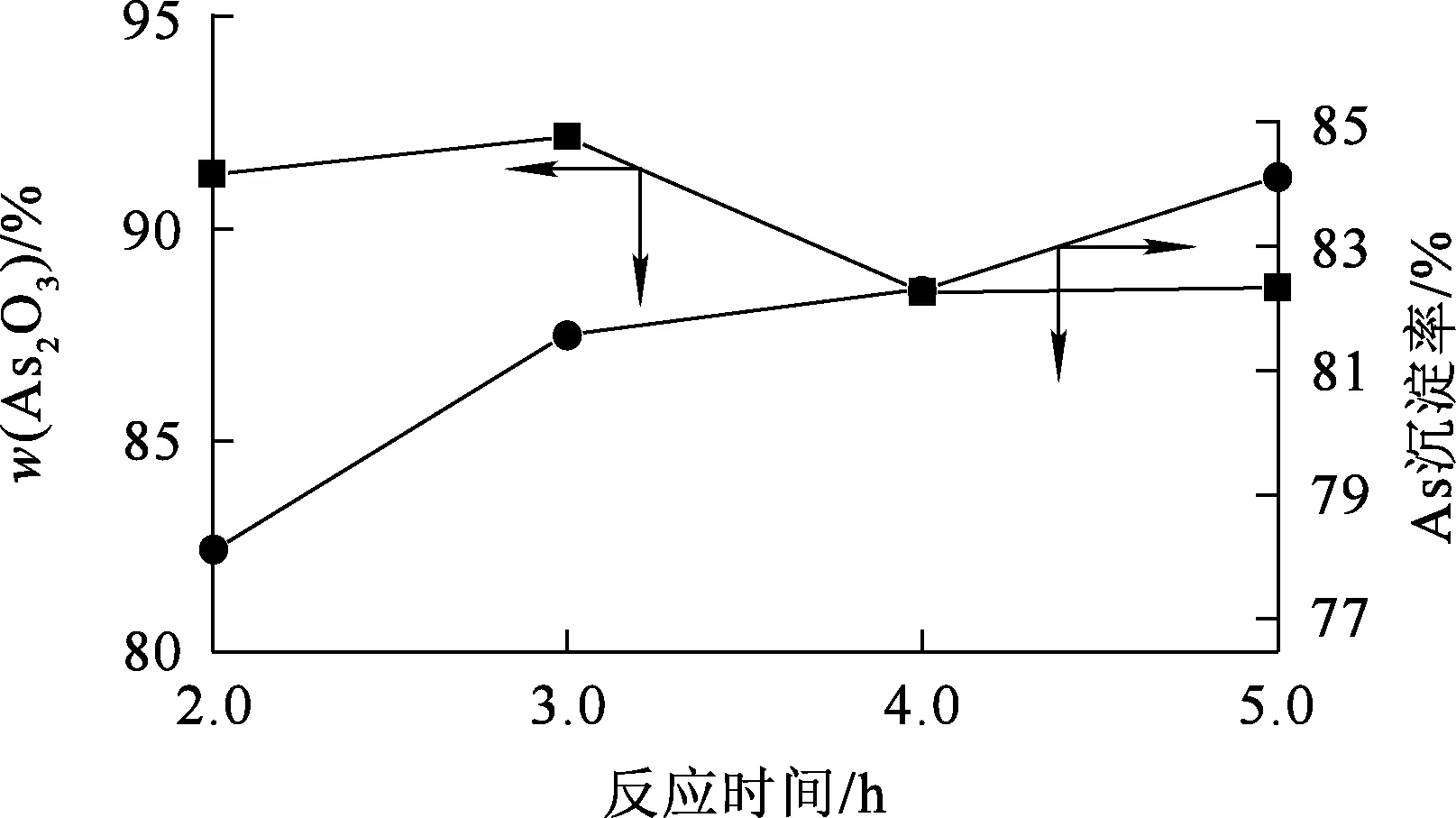
图4 反应时间对产物中As2O3质量分数及As沉淀率的影响
由图4看出:反应时间对产物中As2O3质量分数的影响呈先升高后下降趋势,而As沉淀率逐渐升高;反应3.0 h后,产物As2O3纯度及As沉淀率都趋于稳定,此时产物中As2O3质量分数为92.13%,As沉淀率为81.65%。
2.3.4 反应温度的影响
其他反应条件不变,反应温度对产物中As2O3质量分数及As沉淀率的影响试验结果如图5所示。可以看出:随反应温度升高,产物中As2O3质量分数及As沉淀率都下降。亚硫酸根还原五价砷的反应为放热反应,升高温度对产物生成不利,因此,还原反应以在常温下进行为宜。
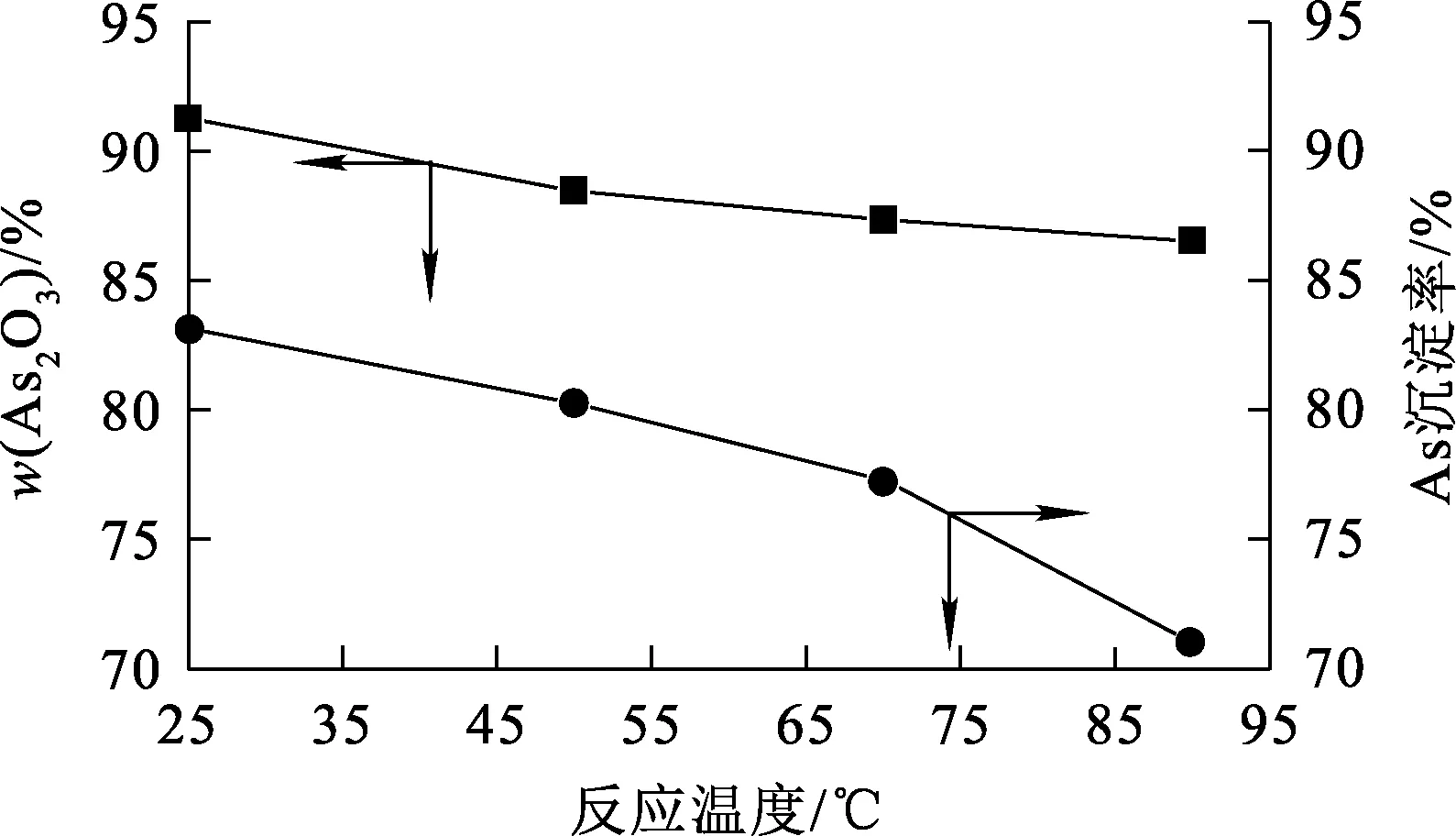
图5 反应温度对产物中As2O3质量分数及As沉淀率的影响
2.3.5 溶液浓缩后体积的影响
其他条件不变,溶液浓缩后体积对产物中As2O3质量分数及As沉淀率的影响试验结果见表6。
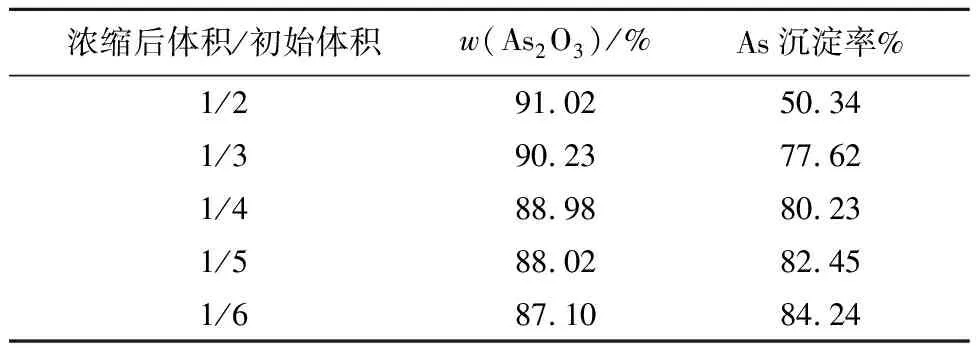
表6 溶液浓缩后体积对产物中As2O3质量分数及As沉淀率的影响
由表6看出:随浓缩后液体积减小,产物中As2O3质量分数逐渐降低,As沉淀率逐渐增大。浓缩后液体积过小,会导致溶液中其他杂质也随As2O3一同析出,从而降低产物纯度。综合考虑,溶液体积以浓缩至原来的1/4较为适宜。
2.3.6 冷却结晶时间的影响
其他条件不变,冷却结晶时间对产物中As2O3质量分数及As沉淀率的影响试验结果见表7。
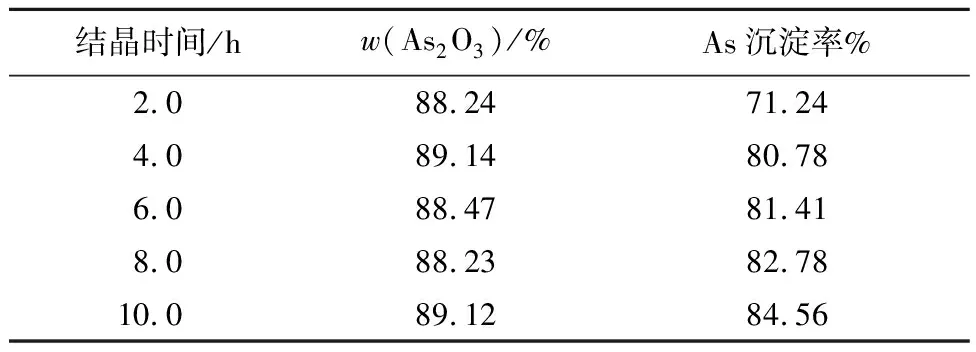
表7 冷却结晶时间对产物中As2O3质量分数及As沉淀率的影响
由表7看出:随结晶时间延长,产物中As2O3质量分数变化不大,但As沉淀率逐渐提高;结晶时间以4.0 h为宜。
2.3.7 综合试验
根据条件试验结果,在溶液初始pH=1.0、还原剂加入量为理论加入量的2.0倍、常温下反应3.0 h、溶液浓缩后体积为初始体积的1/4、常温下冷却结晶4.0 h条件下,进行放大试验。砷酸钠质量200 g,经还原、蒸发结晶、热水洗涤、干燥制备,得63.2 g As2O3,其成分见表8,As2O3纯度达99.16%,As沉淀率达83.58%。XRD衍射分析结果(图6)表明,产物中主要物相为As2O3,质量达到GB 26721—2011二级品标准要求。
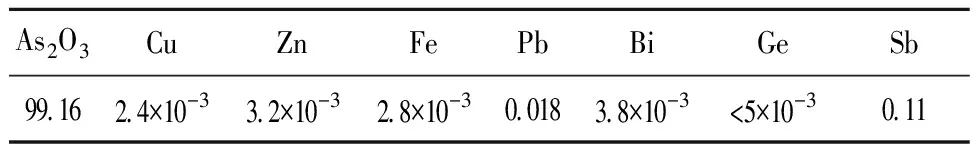
表8 As2O3产品的成分 %

图6 As2O3产品的XRD图谱
3 结论
采用碱性加压浸出工艺从铅阳极泥中脱除砷是可行的,适宜条件下,砷脱除率可达87.18%,铅及其他金属元素浸出率很低或不被浸出。碱性浸出液通过蒸发,可将89.51%的砷以砷酸钠形式结晶出来。结晶的砷酸钠用稀硫酸溶液重新溶解再结晶后可得高纯度As2O3,适宜条件下,As2O3纯度达99.16%,符合GB 26721—2011二级品标准要求。

