传染性脾肾坏死病毒、鳜鱼蛙病毒和鳜弹状病毒三重PCR检测方法的建立
梁红茹,马赛亚,付小哲,林 强,刘礼辉,牛银杰,黄志斌,林 蠡,李宁求
(1中国水产科学研究院珠江水产研究所,农业农村部渔用药物创制重点实验室,广东省水产动物免疫技术重点实验室,广东 广州 510380;2仲恺农业工程学院 动物科技学院,广东 广州 570228)
水产品中的名优鱼类如鳜、鲈、鳢等,由于肉质细嫩、味道鲜美、蛋白含量高等优点越来越受欢迎。目前名优鱼类养殖规模不断扩大,已成为我国一种重要的淡水养殖鱼类。然而,近年来我国鳜鱼、鲈鱼等主养区常发生暴发性死亡,研究发现主要是由3种病毒引起,分别是传染性脾肾坏死病毒(infectious spleen and kidney necrosis virus,ISKNV)、鳜鱼蛙病毒(Siniperca chuatsi ranairidovirus,SCRIV)及鳜弹状病毒(Siniperca chuatsi rhabdovirus,SCRV)。ISKNV是吴淑勤等[1]在病鳜体内发现,并证明了该病毒正是鳜鱼大规模暴发传染病的主要病原之一;而后何建国等[2]进一步对该病毒进行深入探究,将其命名为传染性脾肾坏死病毒;SCRIV属虹彩病毒科,近年来感染鳜鱼较为普遍,具有较高的致病率和致死率[3-5];SCRV具有极强的致病性,感染后的临床症状通常表现为内脏、皮肤和鱼鳍出血,死亡率高达90%[6]。这3种病毒是近些年引起鳜鱼发病的主要病毒病原体,一旦发病,就会导致极高的死亡率,且三者的临床症状经常难以区分且经常混合感染,目前尚未发现有效的治疗措施,严重威胁着鳜鱼养殖业的健康和产业经济发展。
虽然3种病毒常混合感染,但目前检测方法仅能针对单一病毒或2种病毒,费时费力;急需开发能同时检测3种病毒的鉴别诊断方法。为此,本试验尝试通过三重PCR检测方法,建立操作简单、灵敏度高、特异性强,且可同时检测ISKNV、SCRIV和SCRV 3种病原的方法,以期为鳜鱼等养殖品种流行病学调查提供方法支撑。
1 材料与方法
1.1 材 料
1.1.1 病 原 传染性脾肾坏死病毒(ISKNV)、鳜鱼蛙病毒(SCRIV)、鳜弹状病毒(SCRV)、传染性胰坏死病毒(IPNV)、草鱼呼肠孤病毒(GCRV)、锦鲤疱疹病毒(KHV)、神经坏死病毒(NNV)、罗非鱼湖病毒(TiLV)、鲤春病毒血症病毒(SVCV)和新加坡石斑鱼虹彩病毒(SGIV),均由中国水产科学研究院珠江水产研究所保存。
1.1.2 试剂与仪器 PCR仪(晶格,中国),核酸电泳仪(北京六一,中国),凝胶成像系统 VerSa Doc2000(Bio-Rad,美国),微量分光光度计(南京五义,中国)。
1.2 引物的设计与合成
根据GenBank中ISKNVMCP基因序列(HQ317460.1)、SCRIVMCP基因(MG941005.1)和SCRVN基因的(NC008514.1),针对ISKNVMCP基因及其保守区分别设计引物为:ISKNV-MCP-F/ISKNV-MCP-R和ISKNV-550-F/ISKNV-550-R;针对SCRIVMCP基因及其保守区分别设计引物为:SCRIV-MCP-F/SCRIV-MCP-R和SCRIV-400-F/SCRIV-400-R;针对SCRV的N基因及其保守区分别设计引物为:SCRV-N-F/SCRV-N-R和SCRV-780-F/SCRV-780-R。各引物均由广州艾基生物科技有限公司合成,引物信息见表1。

表1 本研究所用的引物信息Table 1 Information of primers used in this study
1.3 重组质粒的构建
分别以感染ISKNV、SCRIV、SCRV的临床样品为模板,以其对应引物ISKNV-MCP-F/ISKNV-MCP-R、SCRIV-MCP-F/SCRIV-MCP-R、SCRV-N-F/SCRV-N-R分别进行PCR 扩增。PCR反应总体系为25 μL:2×EasyTaq PCR SuperMix 12.5 μL,对应引物分别各1 μL,模板1 μL,用ddH2O补充至25 μL。同时以ddH2O代替模板作阴性对照。PCR 扩增反应参数为:94 ℃预变性5 min;94 ℃ 30 s,58 ℃ 30 s,72 ℃ 90 s,共30个循环;72 ℃终延伸 10 min。反应产物用1%琼脂糖凝胶电泳检测。PCR扩增产物纯化后,取4 μL PCR产物与1 μL pEASY-T1载体连接,并转入大肠杆菌Trans1-T1感受态细胞中,培养后提取质粒进行PCR鉴定,同时将质粒送广州艾基生物科技有限公司进行测序鉴定,构建重组质粒P-ISKNV、P-SCRIV、P-SCRV。
1.4 三重PCR检测方法的建立
分别进行单一PCR扩增和三重PCR扩增来验证引物的特异性,PCR反应总体系为25 μL:2×EasyTaq PCR SuperMix 12.5 μL,引物ISKNV-550-F/ISKNV-550-R或SCRIV-400-F/SCRIV-400-R或SCRV-780-F/SCRV-780-R,或ISKNV-550-F/ISK-NV-550-R+SCRIV-400-F/SCRIV-400-R+SCRV-780-F/SCRV-780-R各1 μL,模板P-ISKNV、P-SCRIV、P-SCRV或P-ISKNV+P-SCRIV+P-SCRV 1 μL,用ddH2O补充至25 μL。反应参数为:95 ℃预变性5 min;95 ℃ 30 s,58 ℃ 30 s,72 ℃ 30 s,共35个循环;72 ℃终延伸 7 min,同时用ddH2O代替模板作阴性对照,对所得扩增产物用1%琼脂糖凝胶电泳进行检测。
1.5 三重PCR反应体系的优化
为使3个片段均得到有效扩增,设定56~65 ℃ 10个退火温度,每个处理相差1 ℃,以及27种不同的引物用量,同时设立以ddH2O代替模板的处理为阴性对照,用1%琼脂糖凝胶电泳进行检测。确定最佳退火温度后进行引物用量的优化,(ISKNV-550-F/ISKNV-550-R)/(SCRIV-400-F/SCRIV-400-R)/(SCRV-780-F/SCRV-780-R)引物用量均设0.5,1,1.5 μL共3个剂量,分别交叉组合后共27个处理。同时设立以ddH2O代替模板作阴性对照,所得PCR扩增产物用1%琼脂糖凝胶进行电泳检测。
1.6 三重PCR检测方法的敏感性和特异性检测
1.6.1 敏感性检测 取10 ng/μL的3种质粒P-ISKNV、P-SCRIV和P-SCRV各1 μL,用ddH2O混匀后进行10倍梯度稀释。稀释后取10-1~10-8倍稀释的3种阳性模板,利用优化后的最佳PCR体系和条件进行扩增,同时用ddH2O代替模板作阴性对照,以确定三重PCR检测方法反应的敏感性。
1.6.2 特异性检测 分别取 IPNV、GCRV、KHV、SGIV、NNV、TiLV、SVCV的核酸产物1 μL作为模板,以ISKNV、SCRIV、SCRV、ISKNV+SCRIV+SCRV混合模板为阳性对照,用ddH2O代替模板作为阴性对照,在最佳条件下进行PCR扩增,验证此法的特异性。
1.7 三重PCR检测方法的应用
对中国水产科学研究院珠江水产研究所2019年采集并保存的22份疑似感染ISKNV、SCRIV和SCRV的样品(编号为1~22),分别进行单一PCR检测和三重PCR检测,设立以标准质粒P-ISKNV、P-SCRIV和P-SCRV代替模板的阳性对照组,用ddH2O代替模板作为阴性对照组。
2 结果与分析
2.1 ISKNV、SCRIV和SCRV重组质粒的构建
分别将ISKNV、SCRIV和SCRV对应的模板和引物进行PCR扩增,扩增片段大小分别约1 300,1 392和1 290 bp(图1),将这些片段分别与T1载体连接,经PCR及测序鉴定,证实片段与预期相符,证明已成功构建重组质粒P-ISKNV、P-SCRIV、P-SCRV。阴性对照均未扩增出条带。

M.DNA Marker DL2000;1.目标基因扩增产物;2.阴性对照组M.DNA Marker DL2000;1.Amplification products of target gene;2.Negative control
2.2 ISKNV、SCRIV和SCRV三重PCR检测方法的建立
ISKNV、SCRIV和SCRV三重PCR 引物特异性试验结果见图2。

M.DNA Marker DL2000;1.ISKNV MCP基因保守区单一PCR扩增;2.SCRIV MCP单一PCR扩增基因保守区;3.SCRV N基因保守区单一PCR扩增;4.扩增MCP、MCP和N基因保守区的三重PCR;5.阴性对照M.DNA Marker DL2000;1.Single PCR amplification conserved region of ISKNV MCP gene;2.Single PCR amplification conserved region of SCRIV MCP gene;3.Single PCR amplification conserved region of SCRV N gene;4.Multiplex PCR amplification conserved region of MCP,MCP and N gene;5.Negative control
通过单一PCR,能扩出ISKNVMCP基因保守区约550 bp的片段、SCRIVMCP基因保守区约400 bp的片段和SCRVN基因保守区约780 bp的片段;通过三重PCR,能同时扩出上述3个基因保守区;阴性对照组无扩增条带(图2)。
2.3 ISKNV、SCRIV和SCRV三重PCR检测方法反应条件的优化
2.3.1 最佳退火温度 在确定最佳退火温度试验的10个扩增结果中,可观察到56~65 ℃各梯度处理均可扩增出目的条带(图3),其中60 ℃下目的条带最亮,该温度下N基因和MCP基因的保守区扩增条带最清晰且特异,因此将60 ℃定为最佳退火温度。
2.3.2 最佳引物浓度 由图4可以看出,在27个引物处理中,当(ISKNV-550-F/ISKNV-550-R)/(SCRIV-400-F/SCRIV-400-R)/(SCRV-780-F/SC-RV-780-R)为1/1.5/0.5 μL扩增条带(16号条带)最亮,因此1/1.5/0.5 μL为最佳引物用量。
综合以上2个试验结果,可得优化后的三重PCR反应条件。反应体系组成为:2×EasyTaq PCR SuperMix 12.5 μL,引物ISKNV-550-F/ISKNV-550-R 1 μL、SCRIV-400-F/SCRIV-400-R 1.5 μL、SCRV-780-F/SCRV-780-R 0.5 μL,模板P-ISKNV、P-SCRIV和 P-SCRV各1 μL,用ddH2O补充至25 μL;扩增反应参数设置为:95 ℃ 5 min;95 ℃ 30 s,60 ℃ 30 s,72 ℃ 30 s,共30个循环;72 ℃ 7 min。

M.DNA Marker DL2000;1~10.分别为退火温度56~65 ℃的PCR产物,每处理相差1 ℃;11.阴性对照M.DNA Marker DL2000;1-10.PCR products at annealing temperatures from 56-65 ℃,the difference between each treatment is 1 ℃;11.Negative control图3 ISKNV、SCRIV和SCRV三重PCR检测方法退火温度的优化Fig.3 Optimization of annealing temperature for ISKNV,SCRIV and SCRV multiplex PCR detection

M.DNA Marker DL2000;1~23,25~28.(ISKNV-550-F/ISKNV-550-R)/(SCRIV-400-F/SCRIV-400-R)/(SCRV-780-F/SCRV-780-R)引物用量分别为0.5/0.5/0.5,0.5/0.5/1,0.5/0.5/1.5,0.5/1/0.5,0.5/1/1,0.5/1/1.5,0.5/1.5/0.5,0.5/1.5/1,0.5/1.5/1.5,1/0.5/0.5,1/0.5/1,1/0.5/1.5,1/1/0.5,1/1/1,1/1/1.5,1/1.5/0.5,1/1.5/1,1/1.5/1.5,1.5/0.5/0.5,1.5/0.5/1,1.5/0.5/1.5,1.5/1/0.5,1.5/1/1,1.5/1/1.5,1.5/1.5/0.5,1.5/1.5/1,1.5/1.5/1.5 μL;24,29.阴性对照M.DNA Marker DL2000;1-23,25-28.Ratio of primer dosage to (ISKNV-550-F/ISKNV-550-R)/(SCRIV-400-F/SCRIV-400-R)/(SCRV-780-F/SCRV-780-R) was 0.5/0.5/0.5,0.5/0.5/1,0.5/0.5/1.5,0.5/1/0.5,0.5/1/1,0.5/1/1.5,0.5/1.5/0.5,0.5/1.5/1,0.5/1.5/1.5,1/0.5/0.5,1/0.5/1,1/0.5/1.5,1/1/0.5,1/1/1,1/1/1.5,1/1.5/0.5,1/1.5/1,1/1.5/1.5,1.5/0.5/0.5,1.5/0.5/1,1.5/0.5/1.5,1.5/1/0.5,1.5/1/1,1.5/1/1.5,1.5/1.5/0.5,1.5/1.5/1,1.5/1.5/1.5 μL,respectively;24,29.Negative control图4 ISKNV、SCRIV和SCRV三重PCR检测方法引物用量的优化Fig.4 Optimization of primer proportion for ISKNV,SCRIV and SCRV multiplex PCR detection
2.4 ISKNV、SCRIV和SCRV三重PCR检测方法的敏感性
ISKNV、SCRIV和SCRV质粒分别10倍系列稀释,取10-1~10-8倍稀释的模板进行三重PCR扩增。结果(图5)显示,稀释倍数为10-3时仍能扩增出3条明显的目的条带,说明该方法对ISKNV、SCRIV和SCRV DNA的检测下限均为0.01 ng/μL。
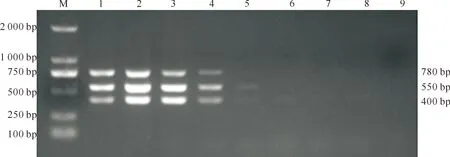
M.DNA Marker DL2000;1~8.分别为10-1~10-8倍稀释的ISKNV、SCRIV、SCRV扩增产物;9.阴性对照M. DNA Marker DL2000;1-8.10-1-10-8 times dilution of ISKNV,SCRIV and SCRV;9.Negative control图5 ISKNV、SCRIV和SCRV三重PCR检测方法的敏感性试验Fig.5 Sensitivity test of ISKNV,SCRIV and SCRV multiplex PCR detection
2.5 ISKNV、SCRIV和SCRV三重PCR检测方法的特异性
在最佳条件下进行PCR扩增,检测此方法的特异性,结果(图6)显示, 以IPNV、GCRV、KHV、SGIV、NNV、ISKNV、TiLV、SVCV核酸产物为模板均未扩出目的条带,以ISKMV、SCRIV、SCRV和ISKNV+SCRIV+SCRV混合模板分别成功扩增出目的条带。

M.DNA Marker DL2000;1.IPNV;2.GCRV;3.KHV;4.SGIV;5.NNV;6.ISKNV;7.TiLV;8.SVCV;9.ISKNV;10.SCRIV;11.SCRV;12.阴性对照;13.以ISKNV+SCRIV+SCRV为模板的阳性对照M.DNA Marker DL2000;1.IPNV;2.GCRV;3.KHV;4.SGIV;5.NNV;6.ISKNV;7.TiLV;8.SVCV;9.ISKNV;10.SCRIV;11.SCRV;12.Negative control;13.Positive control with ISKNV+SCRIV+SCRV template图6 ISKNV、SCRIV和SCRV三重PCR检测方法的特异性Fig.6 Specificity of ISKNV,SCRIV and SCRV multiplex PCR detection
2.6 ISKNV、SCRIV和SCRV临床样品的检测
图7~10表明,单一PCR检测与三重PCR检测的结果基本一致;在22份感染样品中,ISKNV阳性6份,阳性率为27%;SCRIV阳性9份,阳性率为41%;SCRV阳性样品有2份,阳性率为9%;其中ISKNV和SCRIV均为阳性的样品有2份,阳性率为9%;SCRIV和SCRV均为阳性的样品有2份,阳性率为9%;ISKNV、SCRIV和SCRV混合感染阳性率为0。

M.DNA Marker DL2000;1~22.分别对应 1~22号临床样品;23.阳性对照;24.阴性对照;下同M.DNA Marker DL2000;1-22.Corresponding to 1-22 clinical samples respectively;23.Positive control;24.Negative control;The same below图7 ISKNV、SCRIV和SCRV疑似临床样品的单一ISKNV PCR检测Fig.7 ISKNV single PCR test of ISKNV,SCRIV and SCRV suspected clinical samples

图8 ISKNV、SCRIV和SCRV疑似临床样品的单一SCRIV PCR检测Fig.8 SCRIV single PCR test of ISKNV,SCRIV and SCRV suspected clinical samples

图9 ISKNV、SCRIV和SCRV疑似临床样品的单一SCRV PCR检测Fig.9 SCRV single PCR test of ISKNV,SCRIV and SCRV suspected clinical samples
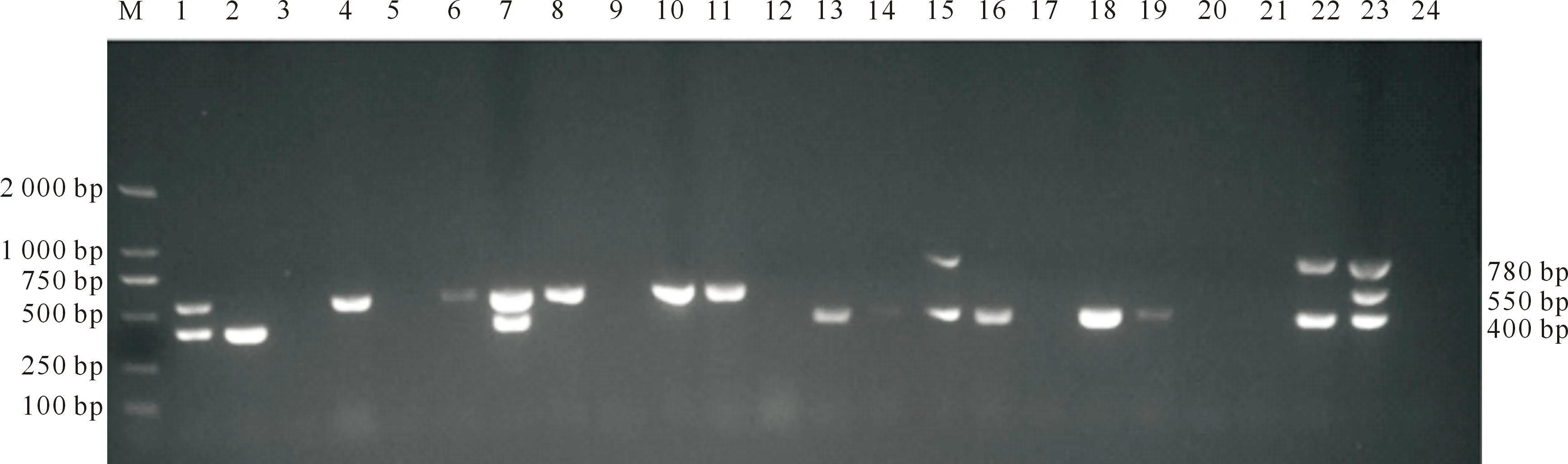
图10 ISKNV、SCRIV和SCRV疑似临床样品的三重PCR检测Fig.10 Multiplex PCR test of ISKNV,SCRIV and SCRV suspected clinical samples
3 讨 论
鳜鱼养殖历史悠久,是我国优质淡水鱼之一,其以产量高、肉嫩、刺少、味甜、蛋白质丰富等营养价值而被消费者喜爱。然而随着我国鳜鱼养殖技术、设备和饲料市场的迅速扩张和发展[7],传染性脾肾坏死病毒、鳜鱼蛙病毒和鳜弹状病毒等病毒病已成为制约鳜鱼养殖业可持续发展的主要因素[8-10]。这3种病毒具有毒力强、致死率高等特点,且鳜鱼常发生多种病毒的混合感染。因此在没有特效治疗药物的情况下,对病原的快速诊断具有更加重要的意义[11-13]。
本试验建立的三重PCR检测方法是在同一反应体系中加入3对引物,同时扩增出3条目的条带的技术,多重PCR成功建立的关键是引物设计以及反应条件的优化[14-16]。本次试验根据目前已报道的ISKNVMCP基因、SCRIVMCP基因和SCRVN基因序列信息中的保守区域[17-18],在综合考虑每对引物的特异性和引物之间可能发生的反应前提下,设计了3对引物,其中SCRVN基因最初扩增条带为280 bp,但其在试验过程中易因污染而造成假阳性,条件优化后ISKNV、SCRIV、SCRV三者扩增片段分别为550,400和780 bp,片段大小差异较明显,能在琼脂糖凝胶电泳中明显区分且无其他非特异性条带。
多重PCR扩增效率会受到扩增温度和各引物之间用量比例的影响,在反应条件的优化过程中,27组引物用量、10个连续退火温度处理中50%以上能得到3条清晰的目的条带,最终确定60 ℃为最佳退火温度,(ISKNV-550-F/ISKNV-550-R)/(SCRIV-400-F/SCRIV-400-R)/(SCRV-780-F/SCRV-780-R)3种引物最佳用量为1/1.5/0.5 μL。优化后的三重PCR反应体系可以特异性扩增不同病毒的特异性片段,且无非特异性扩增,说明此检测方法对不同病毒都能进行准确检测。
应用建立的三重PCR方法对22份疑似混合感染样品进行检测发现,ISKNV、SCRIV和SCRV阳性样品分别有6份,9份和2份,ISKNV、SCRIV和SCRV混合感染阳性率为0份,与单一PCR检测的结果吻合率高达100%,表明本研究所建立的三重PCR检测方法可适用于临床样品的检测和病原学调查。
目前尚无ISKNV、SCRIV和SCRV特效治疗药物,本研究建立的三重PCR方法可快速、特异性检测ISKNV、SCRIV和SCRV 3种感染鳜鱼的常见病毒,灵敏度高,且可一次性对以上3种病毒进行鉴定,提高了临床诊断的效率,可为流行病学调查提供便利。

