早期宫颈癌(Ⅰa2~Ⅰb2)复发相关因素分析
常建苗,王 静,刘晓娟
(河北北方学院附属第一医院,张家口 075000)
宫颈癌为女性常见的恶性肿瘤,发病率居生殖系统肿瘤之首。宫颈癌根治术最初于19世纪90年代由Wertheim描述,20世纪50年代由Meigs重新推广[1]。尽管放疗是一种治疗宫颈癌的方法,但是手术切除肿瘤可降低正常组织放射治疗相关的并发症。对于早期宫颈癌,手术一直是治疗早期宫颈癌的标准治疗方法。经腹根治性子宫切除+盆腔淋巴结切除术是早期宫颈癌治疗的首选方案,这被全世界的妇科肿瘤医生广泛认可并且执行,直到微创理论的提出。多项研究证实[2-4],腹腔镜宫颈癌根治术的切除范围,包括宫旁组织、阴道切除长度及淋巴结切除数等,能达到开腹手术的切除标准,并且与开腹手术相比,腹腔镜手术具有并发症少、出血少,住院时间更少及花费更少等优点。
2020年NCCN[5]指南提出,宫颈癌FIGO分期为早期(Ⅰa2~Ⅱa2)患者的手术路入方式由腹腔镜或经腹改为经腹广泛子宫+盆腔淋巴结切除术,这一修改引起了广泛关注。本研究通过研究影响Ⅰa2、Ⅰb1及Ⅰb2期宫颈癌患者的复发因素,比较两种手术路入方式对早期宫颈癌患者的预后影响,为临床工作提供更加可靠的依据。
1 病例资料
1.1 一般资料 回顾分析2015年1月至2018年12月于河北北方学院附属第一医院行手术治疗的Ⅰa2~Ⅰb2期宫颈癌病例171例,其中失访8例。163例病例中,根据妇科检查、影像学检查及病理资料,按照2018年FIGO分期标准重新进行分期。根据手术方式不同分为开腹手术组及腹腔镜组,开腹手术组70例,腹腔镜组患者93例。患者年龄29~65岁,中位年龄50.23岁,随访中位时间为31.72个月。
1.2 纳入与排除标准 纳入标准:(1)宫颈癌Ⅰa2~Ⅰb2期(2018年FIGO分期),行标准的宫颈癌根治术;(2)术后病理报告及影像学检查全面;(3)有完整的病历及随访资料;(4)术后按标准行辅助治疗。排除标准:(1)哺乳期和妊娠期宫颈癌;(2)有其他器官肿瘤病史;(3)术前已接受其他治疗方法,如放化疗或内分泌治疗。
1.3 统计学处理 采用SPSS22.0软件,定量资料不符合正态分布,采用秩和检验;定性资料用%表示,采用卡方检验;多因素分析采用logistic回归分析。P<0.05为差异有统计学意义。
2 结 果
2.1 开腹手术组与腹腔镜组的一般情况 开腹手术组及腹腔镜组患者的年龄、随访时间、FIGO分期、病理类型、深肌层浸润、脉管癌栓、复发情况等比较,差异均无统计学意义(P>0.05),见表1。
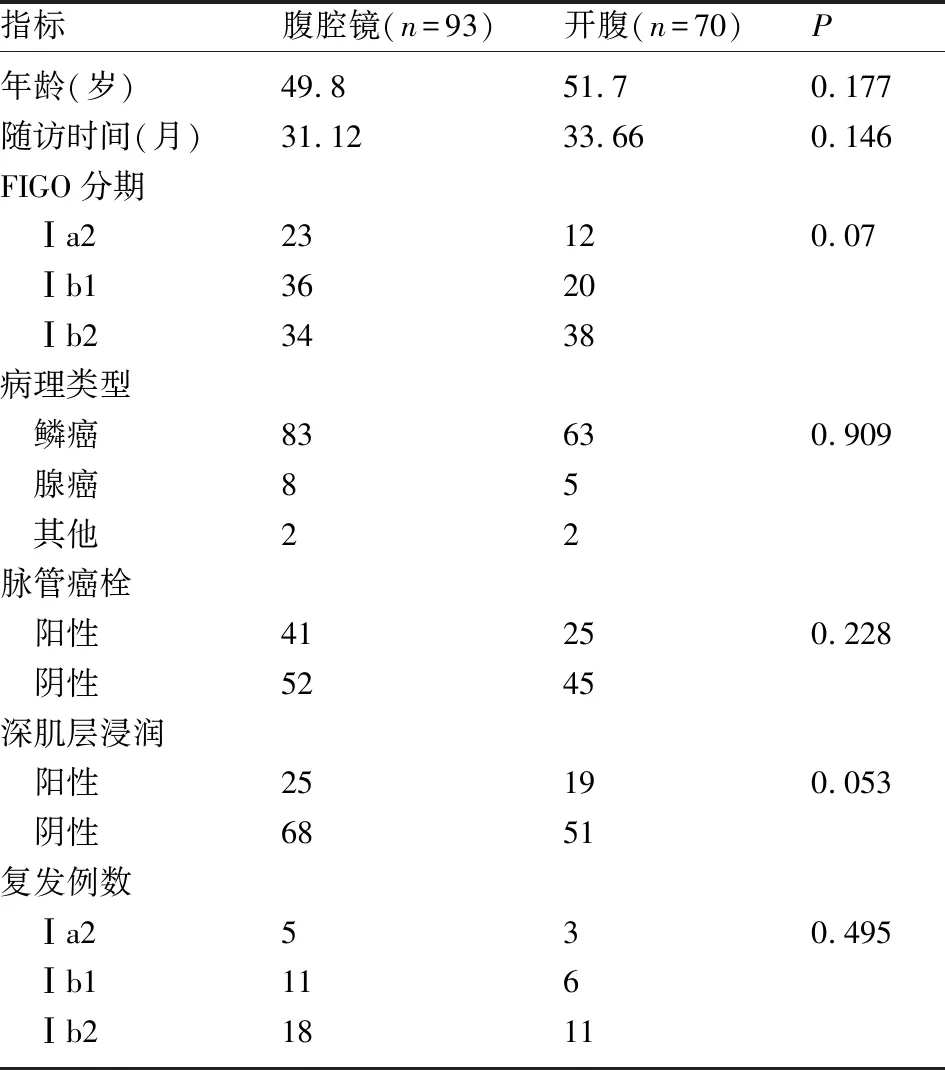
表1 开腹手术组及腹腔镜组患者的一般资料
2.2 影响患者复发率的单因素分析 截至随访日期2020年1月,复发患者共54例,复发率为33.12%,其中腹腔镜组34例(36.56%),开腹手术组20例(28.57%)。病理类型、脉管癌栓及手术方式等均不是影响Ⅰa2期患者复发的因素。对于Ⅰb1期患者,深肌层浸润的22例患者中,10例复发,复发率为45.45%,而无深肌层浸润患者的复发率20.59%(7/34),深肌层浸润为患者复发的高危因素,差异有统计学意义(P<0.05)。脉管癌栓、深肌层浸润以及腹腔镜手术是影响Ⅰb2期患者复发的因素。见表2。
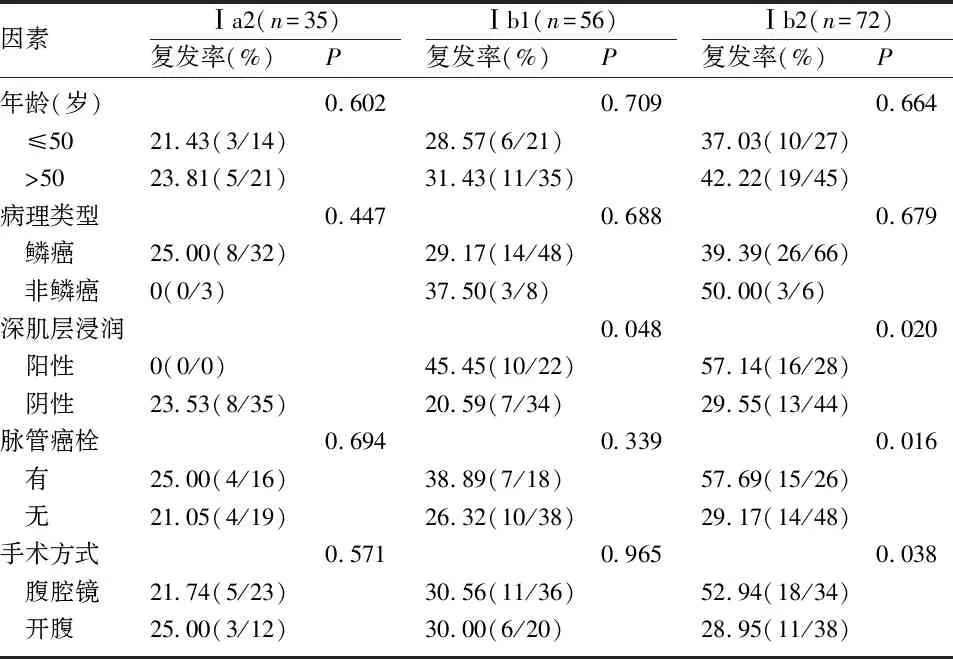
表2 影响早期宫颈癌患者复发率的单因素分析
2.3 影响Ⅰb2期宫颈癌患者复发率的多因素分析 将Ⅰb2期患者中经单因素分析后有统计学差异的因素纳入logistic回归模式进行多因素分析。结果显示,手术方式及深肌层浸润是影响患者复发的独立危险因素(OR值分别为3.693及4.481,P<0.05)(表3)。
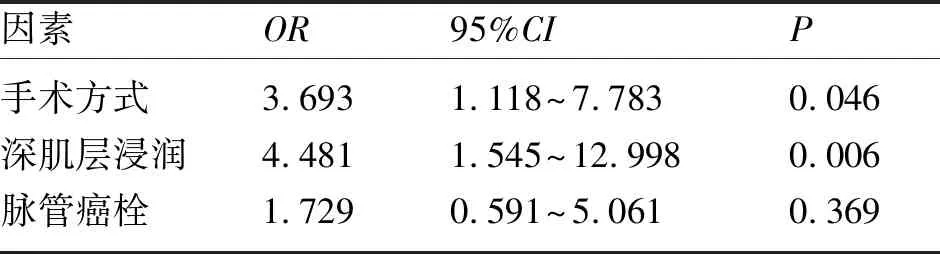
表3 影响Ⅰb2期宫颈癌患者复发率的多因素分析
3 讨 论
2018年NCCN指南中手术方式的更改主要依据2018年Melamed等[6]及Ramirez等[7]的研究结果。两项研究均表明,接受微创根治性子宫切除术患者与开腹相比,总生存期短。Cusimano等[8]回顾了2006~2017年行根治性子宫切除术的病例,微创手术组的5年无进展生存期及总生存期更差。NCCN指南更改的原因可能是行微创根治性子宫切除术患者的复发风险较高,总生存率较低。
但是随着宫颈癌新分期的提出,由原2009年的临床分期标准改为2018年临床-影响-病理分期,尤其对于Ib期宫颈癌患者,新分期指出Ⅰb1为浸润深度≥5.0mm而癌灶最大径线<2.0cm的浸润癌,Ⅰb2癌灶最大径线≥2.0cm而小于4.0cm的浸润癌,癌灶直径>4.0cm的浸润癌为Ⅰb3。Melamed等、Ramirez等[6-7]研究中分期均按2009年的FIGO分期。Melamed等[6]研究中,在肿瘤最大直径<2cm的亚组中,无法准确估计微创手术与开腹手术生存期的优劣性。Ramirez等[7]的结果并不能推广到“低风险”宫颈癌患者(肿瘤大小<2cm;无淋巴血管浸润;浸润深度<10mm;无淋巴结浸润),不能评估两种手术入路的肿瘤预后。但是在Uppal等[9]研究中,术前锥切的患者及最终病理学上没有可见肿瘤的患者有较低的复发风险。Kong等[10]评估了128例接受微创根治术的宫颈癌患者,其中接受经阴道内阴道断端切开的患者和接受腹腔镜下阴道断端切开的患者比较,腹腔转移的风险较高,表明CO2气腹下腹腔内切开阴道断端,可能增加转移复发风险,影响预后,这可能与腹腔镜手术时病灶中肿瘤细胞进入腹腔有关。而对于Ⅰa2患者,并无肉眼可见肿瘤,腹腔镜手术能够减少肿瘤暴露于腹腔,为接受微创手术提供可能。对于新分期下的宫颈癌患者,尚需要更详细的研究,为比较早期宫颈癌患者接受微创手术寻找可能性。
本文中,对于新分期中的Ⅰb2期患者,腹腔镜手术为影响其复发的独立危险因素,而对于Ⅰa1期及Ⅰb1期患者的复发率无影响。所以新分期的提出可能使宫颈癌患者的分期更加详细准确,需要更多的Ⅰ类证据及前瞻性多中心的随机实验来确定Ⅰa2及Ⅰb1期宫颈癌患者接受腹腔镜下宫颈癌根治术的无病生存期及总生存期的优劣性。
对于宫颈癌手术路入方式,NCCN指南的改变可能使大多数患者失去了接受微创根治性子宫切除术的可能,这可能会对妇科肿瘤工作者的手术技能提升训练和随后熟练掌握该手术特有的技能产生重大影响,而失去了微创手术的并发症少、出血少,住院时间短等优点。全面否定早期(Ⅰa2~Ⅱa1)宫颈癌患者的微创手术,可能是我们所有人的损失。随着宫颈癌新分期的提出,对于Ⅰa2至Ⅰb1期宫颈癌患者,尚需要足够有力的、前瞻性的、评估生存结果的随机试验,来进一步评估解腹腔镜手术的利弊。在未来,需要逐渐修改微创技术并证明其与开腹手术的等效性,并且对微创技术进行创新和进一步研究。

