全腹腔镜远端胃癌根治术中胃肠吻合共同开口关闭方式的对比研究
朱阿考,俞雪华,刘信春,单毓强,应荣超,张 健
(1.浙江大学医学院附属杭州市第一人民医院胃肠肛外科,浙江 杭州,310006;2.杭州市第一人民医院桐庐分院普通外科;3.浙江大学医学院附属第一医院胃肠外科)
胃癌在世界范围内具有很高的发病率与死亡率,外科治疗一直是治愈胃癌的主要手段。Kitano等[1]于1994年报道了一种新的腹腔镜辅助远端胃切除术,由此胃癌手术进入了微创手术时代。大样本研究已证实腹腔镜胃癌手术与开放手术具有相似的临床效益与预后,但在手术创伤、失血量、住院时间、术后并发症等方面具有明显优势[2],腹腔镜胃癌手术的适应证也逐渐由早期胃癌向进展期胃癌拓展[3]。近年,随着腹腔镜相关器械的研发、吻合方式的改良,全腹腔镜消化道重建得到了更大的发展与推广,全腹腔镜胃切除术是指在腹腔镜下完成主要操作的胃癌根治性手术。因绝大部分操作均在腔镜下完成,在暴露、层面解剖、视野等方面具有明显优势[4-5]。然而,全腹腔镜胃切除术仍存在较多难点,主要困难在于腹腔镜下的消化道重建[6]。随着腹腔镜下微创器械的发展,目前全腔镜远端胃切除术(totally laparoscopic distal gastrectomy,TLDG)消化道重建获得广泛开展,其主要吻合方式包括毕Ⅰ式(三角吻合或Delta吻合)、毕Ⅱ式(加或不加Braun吻合)、Roux-en-Y(或un-cut Roux-en-Y),大部分中心选择以线性闭合器为主的毕Ⅱ式+Braun消化道重建[7]。但切割闭合器胃肠吻合后会形成直径约2 cm的共同开口,如何安全可靠的关闭共同开口是目前讨论的重点。目前临床主要有直线切割闭合器直接闭合或以倒刺线连续缝合关闭两种方式,各有优缺点[8-9]。然而,目前尚缺乏对这两种闭合方式近期疗效与安全性的对比研究。因此,本研究收集了两种不同闭合方式的病例,对比分析两种闭合方式的便利性、安全性及经济性。
1 资料与方法
1.1 临床资料 本研究采用回顾性队列研究的方法,收集2016年1月至2020年12月本中心收治的331例接受完全腹腔镜远端胃癌根治+毕Ⅱ+Braun吻合患者的临床及手术视频资料。纳入标准:(1)术前胃镜、病理检查及CT明确诊断为胃癌;(2)术前检查示肿瘤无远处转移、周围器官浸润,可行TLDG;(3)术式为完全腹腔镜远端胃癌根治+毕Ⅱ加Braun吻合,胃肠吻合共同开口以切割闭合器闭合或免打结可吸收倒刺线(knotless barbed absorbable sutures,KBAS)连续缝合;(4)患者营养状况良好,心肺功能、肝肾功能良好,可耐受手术;(5)患者及家属均已签署相关知情同意书。排除标准:(1)术中探查显示肿瘤多发转移或浸润周边脏器,无法行根治性手术;(2)有上腹部大手术史(除腹腔镜胆囊切除术外);(3)肿瘤位置不宜行远端胃癌根治术;(4)合并全身性疾病,如严重肝硬化、严重慢性肺部疾病等,无法耐受手术;(5)病历或影像资料不完整,无法完整评价;(6)采取其他手术方式或中转开腹。术前评估可行TLDG并充分告知患者相关手术方式及风险,患者均同意施行手术并签署知情同意书。
1.2 手术方法 入组病例均由同一团队医师施行完全腹腔镜远端胃癌D2根治术及毕Ⅱ+Braun吻合方式行消化道重建。采用气管插管全身麻醉,患者取平卧分腿位或截石位,主刀立于患者左侧,助手立于右侧(吻合及缝合时主刀与助手站位互换),扶镜手立于患者两腿之间。建立气腹,压力维持在12~14 mmHg,于脐周做观察孔置入腹腔镜探查,确定无肉眼可见腹膜及远处转移后采用5孔法行腹腔镜手术。遵循日本胃癌处理规约行D2淋巴结清扫,采用先离断十二指肠、后清扫胰腺上区淋巴结的前入路清扫策略,完成淋巴结清扫后以直线切割闭合器离断胃体约2/3,将标本装袋后绕脐以3~4 cm小切口取出,并送切缘行快速病理检查,明确上、下切缘均为阴性后行消化道重建。同时在标本取出口处拖出、按输出襻对大弯侧环形摆放空肠并在预吻合部位标记,然后直视下以普通3-0可吸收线连续缝合行空肠侧侧吻合完成Braun吻合。主刀换到右侧站位,于残胃切割缘大弯侧角做1 cm切口,右下操作孔置入腔镜下切割闭合器,钉仓臂穿入空肠、金属臂穿入胃内,对齐后击发行残胃-空肠侧侧吻合,镜下通过共同开口检查腔内吻合口通畅性及有无出血。然后助手提起共同开口,倒刺线组以3-0 KBAS连续全层缝合共同开口;闭合器组助手、主刀提起共同开口各角,以腹腔镜切割闭合器1~2道横向进行闭合,交角、出血部位烧灼或缝合加强。腹腔常规留置引流管2根,一根位于右侧肝肾隐窝十二指肠旁,一根位于左侧吻合口旁,不常规留置空肠营养管或胃管。
1.3 观察指标 比较两组围手术期指标、手术费用及倾倒综合征、胆汁反流性胃炎、肠梗阻及吻合口相关并发症发生情况,计算两组术后并发症发生率。
2 结 果
2.1 手术情况 最终成功纳入331例患者,中位年龄63岁,均行TLDG,并采用毕Ⅱ+Braun吻合方法重建,无中转开腹。手术操作严格遵循肿瘤根治的无菌、无瘤原则,术中快速病理示上下切缘均阴性。其中179例采用KBAS连续缝合关闭共同开口(KBAS组),152例以腹腔镜直线切割闭合器闭合共同开口(闭合器组),其中58例需要2枚钉仓完成闭合,94例以1枚钉仓完成闭合,钉仓使用量平均(1.38±0.49)枚。两组患者性别、年龄、BMI、肿瘤大小与病理分期等临床资料差异无统计学意义(P>0.05),见表1。
表1 两组患者临床资料的比较
2.2 围手术期各项指标 术中出血量平均(57.3±17.8)mL,切口长度平均(3.8±0.6)cm,清扫淋巴结数量(25.3±6.5)枚,总体淋巴结阳性病例率为34.7%(115/331),按照美国癌症联合会第8版胃癌TNM临床分期:Ⅰ期63例、Ⅱ期227例、Ⅲ期41例,其中4例新辅助化疗3~4个周期后行根治手术。两组手术总时间、术后住院时间差异无统计学意义,但KBAS组共同开口关闭时间(P<0.001)、术后排气时间(P=0.018)长于闭合器组,耗材使用费低于闭合器组(P<0.001),见表2。

表2 两组患者围手术期指标的比较
2.3 术后并发症 两组均无术后吻合口出血病例。闭合器组术后1例患者发生腹腔出血,术后7 h二次腹腔镜探查发现为共同开口闭合缘出血,局部予以缝合后止血成功;KBAS组未发生术后腹腔内出血。闭合器组3例发生消化道瘘,1例考虑十二指肠残端漏,经双套管冲洗等保守治疗痊愈;2例考虑为胃肠吻合口漏,经双套管冲洗引流等治疗后,分别于术后第26天、第41天拔管痊愈;闭合器组吻合口漏发生率为2.0%(3/152)。KBAS组共发生3例术后消化道瘘,其中2例证实为十二指肠残端漏,经持续引流、清创等治疗后逐步痊愈,1例术后出现疑似吻合口漏的腹腔严重感染症状,因患者家属放弃进一步检查与治疗而自动出院并死亡,无法具体明确吻合口漏部位;KBAS组术后吻合口漏发生率为1.7%(3/179)。两组吻合口漏发生率差异无统计学意义(P=0.83)。闭合器组3例患者出现轻微的胃肠吻合口梗阻症状,经保守治疗7~12 d后自行缓解,考虑为吻合口水肿所致;KBAS组1例术后出现持续吻合口梗阻症状,考虑为胃肠吻合口成角所致,术后第8天在胃镜下输出襻放置空肠营养管,保守治疗21 d后拔管,恢复正常饮食。两组吻合口梗阻发生率差异无统计学意义(P=0.51)。余者均无其他围手术期相关并发症发生。两组总并发症发生率差异无统计学意义[4.6%(7/152) vs. 2.2%(4/179),P=0.25]。
3 讨 论
第4版日本《胃癌治疗指南》已将腹腔镜手术推荐为临床Ⅰ期远端胃癌手术的常规方式,我国CLASS-01 研究及韩国KLASS-02研究结论均证实,具备丰富经验的团队施行腹腔镜远端胃癌D2根治术治疗局部进展期胃癌安全、可行[9]。但对于远端胃大部切除术后的消化道重建方案存在较多争议,如何寻找简便且安全可靠的全腔镜下消化道重建方式是目前亟待解决的难点[4]。目前完全腹腔镜胃切除术后消化道重建主要应用直线切割闭合器完成,术式主要包括毕Ⅰ式重建、毕Ⅱ式重建(加Braun吻合)、Roux-en-Y(或Un-Cut Roux-en-Y),目前毕Ⅱ+Braun式重建选择最多,其在毕Ⅱ吻合术的基础上增加了小肠的Braun吻合,可保持空肠的不离断从而保持空肠原有蠕动波与电节律,充分发挥传统手术的优点,操作简便[10]。对于胃-空肠直线切割吻合器吻合后留下的共同开口的关闭目前主要有闭合器关闭与手工缝合两种,如采用输入襻对大弯的胃空肠吻合方式,共同开口段小肠会旷置,因此不需要保持足够的肠腔宽度,远端胃毕Ⅱ重建+Braun吻合可选择直线切割闭合器关闭共同开口,操作更加便捷高效。但共同开口闭合时需将不同组织厚度的胃壁与小肠壁用同一钉高的直线切割闭合器闭合,小肠端因闭合高度较高极易出现切割缘出血,往往需要额外的烧灼或缝合止血。而手工缝合关闭共同开口具有可节省耗材费用、吻合口不易狭窄等优势,其安全性也被证实[11],但用普通可吸收线连续缝合时,对主刀的缝合技能及团队的配合要求较高,学习曲线偏长。
倒刺缝线是一种具有与缝合方向相反的倒刺的单股缝线,因其特殊的结构优势近年逐渐在腹腔镜手术中得到应用。意大利学者对84例胃旁路手术以随机对照的方式进行研究,其中46例应用KBAS连续缝合进行胃肠旁路吻合,结果证实了KBAS连续缝合在胃肠吻合中的可靠性[12]。近年,越来越多的医疗中心报道使用KBAS连续缝合关闭胃肠吻合后形成的共同开口,但与切割闭合器直接关闭的优劣一直未进行相应的对比研究。本研究回顾性收集了近年我中心接受TLDG+毕Ⅱ式重建+Braun吻合术的病例资料,总结分析了KBAS连续缝合与直线切割闭合器关闭胃肠共同开口的操作便捷性、围手术期安全性及耗材费用等方面的数据,结果表明两种方法均能达到共同开口的满意闭合,术后吻合口漏、出血、吻合口狭窄及肠梗阻等相关并发症发生率均较低,但KBAS组关闭耗材费用更低,而闭合器组能更快完成关闭操作,具有较高的安全性与操作便捷性。
在全腹腔镜下行胃肠吻合采取右侧站位时,建议采取输出襻对大弯侧的方向,以保证输出襻的顺畅。选择切割闭合器关闭共同开口的技巧:(1)胃肠吻合时应尽量保持残胃与小肠对齐(图1),从而留下尽量小的共同开口以利于闭合(图2);(2)助手需要分别提起共同开口的前角与中心点(如提拉困难可分别缝合一针固定),然后以1~2道切割闭合器完成闭合(图3);(3)因胃壁明显厚于空肠壁,小肠交叠闭合端切割缘极易出现出血(图4箭头),需重视;如有切割缘出血,建议以高频电刀进行烧灼或直接缝合止血(图5),以避免术后出血。闭合器闭合后的视图见图6。以KBAS缝合共同开口时,缝合技巧为:(1)建议选择15~20 cm的3-0 KBAS,主刀立于右侧;(2)如共同开口肠壁不规则或组织条件差,可预先进行修剪;(3)第一针入针点、最后一针出针点均需越过闭合线0.5 cm以上(图7);(4)缝合第一层为胃-空肠壁全层缝合,第二层为浆肌层缝合包埋;(5)缝合完成KBAS留置1 cm左右剪断,无需打结或上夹;缝合完成后的吻合口见图8。
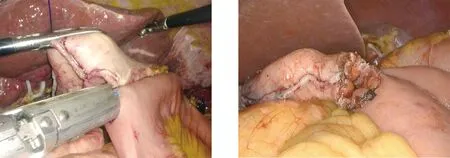
图1 胃肠侧侧吻合时,残胃壁与空肠壁尽量对齐后击发吻合 图2 对齐后吻合,形成的共同开口较小且整齐
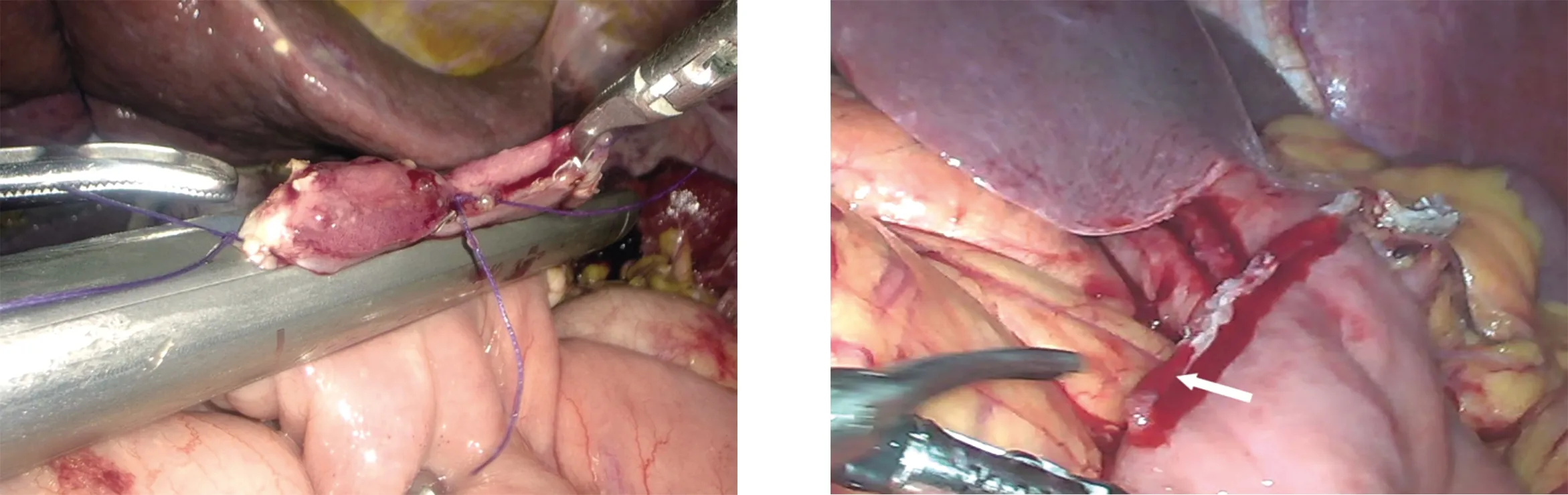
图3 提起共同开口近远端将残胃缘与空肠缘对齐后击发 图4 胃壁明显厚于空肠壁,小肠交叠闭合端切割缘极易出血(箭头)
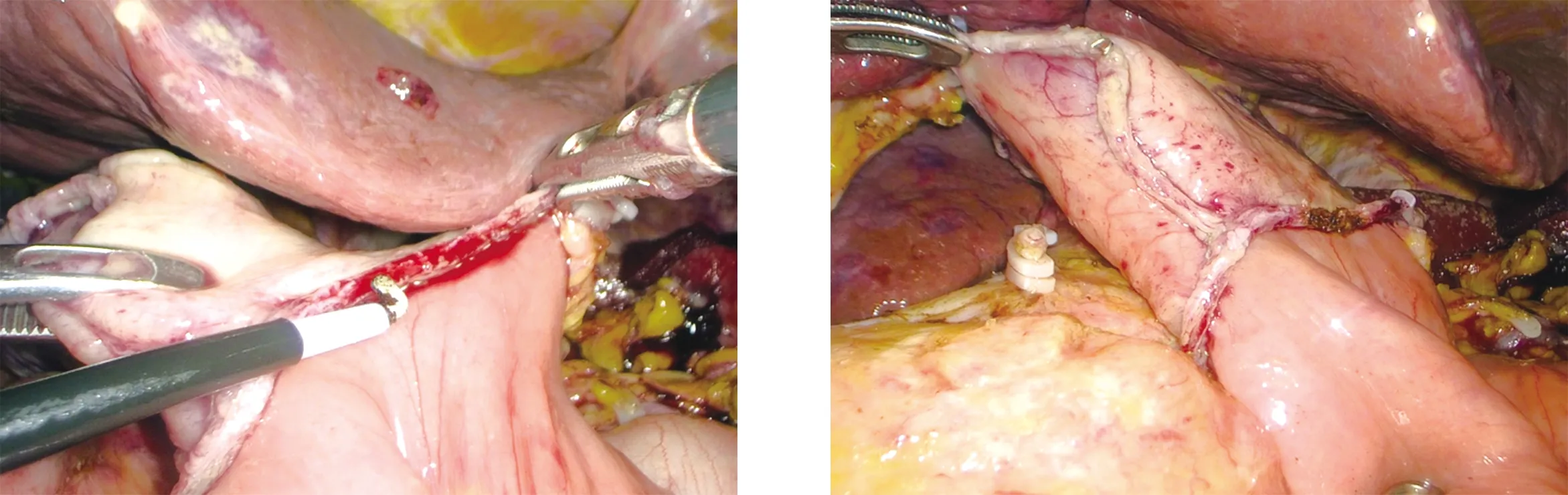
图5 切割缘出血需加强缝合或电刀烧灼妥善止血 图6 切割闭合器闭合共同开口后视图
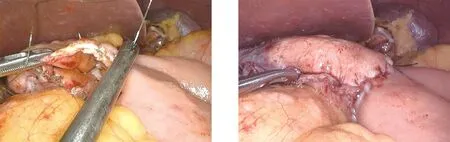
图7 KBAS连续缝合关闭共同开口第一针需越过闭合线0.5 cm以上 图8 KBAS连续缝合关闭共同开口后视图
综上所述,完全腹腔镜下行TLDG后毕Ⅱ+Braun吻合时,掌握正确方法与技巧,应用直线切割闭合器或KBAS连续缝合关闭共同开口均是安全且容易实施的,术者可根据自身情况选择合适的手术方式。但本研究目前仅为单中心回顾性队列研究,因手术总例数限制且并发症发生率较低,目前研究的数据尚未体现出两种闭合方式安全性方面的差异,下一步本中心计划进行前瞻性随机对照研究,进一步探索两种共同开口关闭方式的优劣。

