10种口服中成药联合化疗治疗乳腺癌的网状Meta分析
来保勇,吕灵艳,赵 静,楚爱景,王春晖,裴晓华, 3*
·循证医学与临床用药·
10种口服中成药联合化疗治疗乳腺癌的网状Meta分析
来保勇1,吕灵艳1,赵 静1,楚爱景1,王春晖2,裴晓华1, 3*
1. 北京中医药大学第三附属医院,北京 100029 2. 北京中医药大学房山医院,北京 102400 3. 北京中医药大学厦门医院,福建 厦门 361001
基于网状Meta分析方法比较10种口服中成药联合化疗治疗乳腺癌的疗效和安全性。检索CNKI、Wanfang、VIP、SinoMed、PubMed、EMbase、Web of Science、Cochrane Library数据库中相关口服中成药治疗乳腺癌的随机对照试验(randomized controlled trial,RCTs),检索时间为建库至2021年1月1日。2人独立对文献进行筛选、提取数据和质量评价。采用RevMan5.3、Stata14.0、Gemtc14.3软件进行数据分析。共纳入61项RCTs,涉及10种口服中成药。网状Meta分析结果显示,以化疗为共同干预措施,口服中成药改善乳腺癌I~III期患者客观缓解率(objective response rate,ORR)的疗效排序为参一胶囊>金龙胶囊>西黄丸/胶囊>平消胶囊>复方斑蝥胶囊>华蟾素胶囊>槐耳颗粒>小金片/丸;改善I~III期患者疾病控制率(disease control rate,DCR)的疗效排序为金龙胶囊>西黄丸/胶囊>华蟾素胶囊>平消胶囊>复方斑蝥胶囊>槐耳颗粒>小金片/丸;改善Ⅲ~Ⅳ期患者ORR的疗效排序为槐耳颗粒>西黄丸/胶囊>参一胶囊>华蟾素胶囊>平消胶囊>小金片/丸;改善III~IV期患者DCR的疗效排序为平消胶囊>参一胶囊>西黄丸/胶囊>华蟾素胶囊>槐耳颗粒>小金片/丸;生活质量(quality of life,QOL)改善率的疗效排序为西黄丸/胶囊>槐耳颗粒>参一胶囊>华蟾素胶囊>金龙胶囊>复方斑蝥胶囊>平消胶囊;西黄丸有益于提高乳腺癌患者的疾病无进展生存期(progression free survival,PFS)和患者总生存期(overall survival,OS),平消胶囊有益于提高OS;缓解白细胞减少发生率的疗效排序为参一胶囊>槐耳颗粒>华蟾素胶囊>西黄丸/胶囊>贞芪扶正颗粒>平消胶囊>复方斑蝥胶囊>小金片/丸;减少消化道反应发生率的疗效排序为贞芪扶正颗粒>西黄丸/胶囊>槐耳颗粒和参一胶囊>平消胶囊>华蟾素胶囊>小金片/丸>复方斑蝥胶囊。对于I~III期患者,参一胶囊联合化疗改善ORR的效果显著,金龙胶囊联合化疗改善DCR效果最明显;对于III~IV期患者,槐耳颗粒联合化疗改善ORR效果最明显,平消胶囊和参一胶囊联合化疗改善DCR方面有较好效果。西黄丸在改善患者生活质量方面更明显,参一胶囊有助于降低乳腺癌患者白细胞减少的发生率。贞芪扶正颗粒在降低乳腺癌患者消化道反应发生率方面更有优势。
中成药;中医药;乳腺癌;网状Meta;随机对照试验;参一胶囊;金龙胶囊;西黄丸/胶囊;平消胶囊;复方斑蝥胶囊;华蟾素胶囊;槐耳颗粒;小金片/丸;贞芪扶正颗粒;养正消积
乳腺癌是女性最常见的癌症之一,其发病率约占全身各种恶性肿瘤的7%~10%,是全球女性癌症相关死亡的首要原因[1-2]。2018年《全球癌症统计》对全球180多个国家36种癌症的发病和死亡人数进行了推算,结果显示2018年全球新发各种癌症病例中乳腺癌病例为210余万,约占11.6%[3]。世界卫生组织国际癌症研究机构发布了2020年全球最新癌症负担数据,结果显示2020年全球乳腺癌新增人数达226万,而肺癌为220万,乳腺癌正式取代肺癌,成为全球第一大癌症[4]。我国的相关肿瘤流行病学报告显示中国女性乳腺癌每年增加约30.4万例,发病率呈现逐渐上升的趋势,并且近年来其发病年龄日益年轻化,这给个人和整个社会带来巨大的疾病负担[5]。
目前乳腺癌的治疗主要有外科手术、化疗、放疗、靶向疗法及免疫治疗等[6-7]。然而,目前这些治疗虽然取得了一些疗效,但无论是手术、放化疗还是免疫治疗都存在一定的局限性,会导致不同程度的不良反应或副反应,不少患者因此而不能耐受或恐惧治疗,从而延迟甚至停止治疗计划,临床尚不能取得理想效果[8-9]。近年来,随着现代肿瘤治疗模式和理念的发展,中医药与乳腺癌的现代治疗也更加紧密,中医药与手术、化疗、靶向治疗等相辅相成[10-11]。中成药作为中医药的重要组成部分,目前其广泛用于乳腺癌的辅助治疗,既往研究显示口服中成药同样能给乳腺癌患者带来获益,如研究者系统评价了西黄丸和参一胶囊联合化疗能提高乳腺癌患者治疗的临床有效率、改善生存质量、降低相关不良反应发生等[12-13]。然而,市场上关于肿瘤治疗的口服中成药繁多,目前尚缺乏口服中成药干预乳腺癌直接比较的研究,其相对疗效和安全性尚不明确,不利于中成药治疗乳腺癌的临床实践及最佳方案的选择。本研究旨在采用贝叶斯网状Meta分析方法综合比较相关口服中成药治疗乳腺癌的有效性和安全性,以期为乳腺癌的口服中成药干预提供循证依据。
1 资料与方法
1.1 纳入标准
1.1.1 研究类型 随机对照试验(randomized controlled trial,RCT)。
1.1.2 研究对象 明确诊断为乳腺癌患者,对年龄、病程、疾病类型、疾病分期、并发症等不做限制。
1.1.3 干预类型 试验组以口服类相关中成药联合常规化疗为主要干预措施,药物的剂量及干预时机等不做限制。对照组为乳腺癌的常规化疗。试验组和对照组中除比较的措施外,其他共同干预措施应一致。对照若为同一种药物仅剂量不同,则参照相关方法将其数据合并为一组。
1.1.4 结局指标
(1)主要结局指标:①客观缓解率(objective response rate,ORR);②疾病控制率(disease control rate,DCR)。疾病控制情况(ORR和DCR)参照世界卫生组织(WHO)实体瘤客观疗效通用指标或RECIST1.0标准[14],其包括完全缓解(complete remission,CR)、部分缓解(partial remission,PR)、疾病稳定(stable disease,SD)、疾病进展(progressive disease,PD)4个方面;其中ORR包括CR和PR的总人数;DCR包括PR和SD总人数。③生活质量(quality of life,QOL)改善:基于Karnofsky(KPS)量表评分结果依次评估为生活质量提高(治疗后KPS评分增加>10分)、生活质量稳定(治疗后KPS评分增加或减少未超过10分)、生活质量下降(治疗后评分下降>10分)。④远期疗效情况:包括疾病无进展生存期(progression free survival,PFS)和患者总生存期(overall survival,OS)。
生活质量改善率=(提高+稳定)例数/总例数
(2)次要结局指标:①相关不良反应情况,包括白细胞减少发生率和消化道反应发生率;②免疫功能,治疗后患者T淋巴细胞亚群CD4/CD8情况。
1.2 排除标准
排除判断为数据重复的文献,数据资料存在明显错误或无法获取相关完整资料的研究及无符合结局指标或无法提取相关结局有效数据的文献。
1.3 文献检索
系统检索CNKI、CNKI、Wanfang、VIP、SinoMed、PubMed、EMbase、Web of Science、Cochrane Library等文献数据库中关于相关中成药治疗乳腺癌的RCTs,检索时限均为建库至2021年1月,中文检索词主要为乳腺癌、乳癌、乳腺肿瘤、中成药、中药、中医、片、丸、散、胶囊、颗粒、口服液等;英文检索词主要为breast cancer、Chinese patent medicine、traditional Chinese medicine、Chinese herbal medicine等。
1.4 文献筛选与资料提取
首先排除重复文献,然后对文献进行筛选,对不能通过文摘信息确定的文献进行全文阅读筛选,最终确定纳入分析的文献。资料提取包括文献基本信息、研究对象人口学资料、疾病信息、方法学质量信息、干预和对照信息、相关疗效和安全性结果等。以上过程由2名研究人员合作完成,在文献筛选及资料提取过程中如果遇到分歧,则通过互相讨论达成共识,若2人不能达成共识,则请第3方裁决。
1.5 纳入研究的方法学质量评价
采用Cochrane手册中“risk of bias”评价工具评价纳入文献的方法学质量[15],相关评价条目的偏倚风险根据文献报告情况依次评价为低偏倚风险(low risk)、高偏倚风险(high risk)或偏倚风险不清楚险(unclear risk)。由2名研究者单独对方法学关键要素信息进行评价并交叉核对结果,如遇到分歧与第3方讨论协商。
1.6 数据分析
采用Review manager 5.3绘制风险偏倚图,进行异质性检验。二分类变量采用比值比(odds ratio,OR)表示,连续型变量采用均数差(mean different,MD)表示,区间估计均采用95%置信区间(confidence interval,CI)。根据临床异质性以干预类型为依据进行亚组分析,通过检验和2指数分析统计学异质性,异质性较小时用固定效应模型分析数据(≥0.1且2≤50%),否则使用随机效应模型(<0.1或2值>50%)。采用Stata14.0软件中“network meta”命令绘制干预措施网络图。采用Gemtc14.3软件进行贝叶斯网状Meta分析,对纳入研究各干预措施进行直接证据和间接证据比较。采用马尔可夫链蒙特卡洛拟合一致性模型进行贝叶斯推断,在Gemtc14.3软件中对潜在的标尺缩减参数(potential scale reductionfactor,PSRF)进行评估,若PSRF值≥1.2说明目前的模拟次数不足以达到很好的收敛,增加模拟次数再评估;当PSRF值在1.00~1.05时说明迭代效果的收敛性良好,且越接近1表示数据收敛性良好,采用一致性模型进行网状Meta分析。当各干预措施间存在闭合环时需进行不一致性检验,采用点分法模型进行非一致性检验,若>0.05,采用一致性模型进行分析;否则,采用非一致性型进行分析。基于Gemtc14.3软件中贝叶斯分析模型计算各干预措施的疗效概率排序,推断每种措施成为最有效治疗的可能性大小情况。数据分析过程中基于疾病病理分期对相关主要结局指标进行亚组分析,同时根据纳入文献方法学质量及疾病分期报告情况进行敏感性分析以评估结果稳定性。最后用Stata14.0绘制比较-校正漏斗图,识别相关结果中是否存在小样本效应,以及评估发表偏倚情况。本研究参照网状Meta分析报告条目PRISMA扩展声明进行报告[16]。
2 结果与分析
2.1 文献筛选
系统检索相关数据库,共获得2916篇相关文献,去除重复文献后剩余1611篇,通过阅读文摘信息,初步筛选出76篇进行全文阅读筛选,最终纳入61篇文献进行数据分析。文献筛选结果见图1。
2.2 纳入文献基本特征
纳入61项RCTs,共计患者5162例,平均年龄(46.44±5.01)岁,样本量为30例至253例不等,发表年份为2004—2020年,均为双臂试验。涉及相关口服类中成药10种,分别包括西黄丸/胶囊16项研究[17-32]、平消胶囊6项研究[33-38]、槐耳颗粒11项研究[39-49]、参一胶囊7项研究[50-56]、复方斑蝥胶囊5项研究[57-61]、华蟾素胶囊7项研究[62-68]、金龙胶囊3项研究[69-71]、小金片/丸3项研究[72-74]、养正消积2项研究[75-76]、贞芪扶正胶囊1项研究[77]。纳入文献基本特征信息见表1。同时采用Stata14.0绘制各干预措施的网状关系图,见图2。

图1 文献筛选流程

表1 纳入研究的基本特征
续表1

纳入研究n/例年龄/岁TNM分期干预措施(试验组/对照组)治疗周期结局指标 TCTC 孔颖等[34]595952.7±4.851.9±4.5NR平消胶囊+化疗/化疗12~18周①②⑥⑧ 李红君等[35]494951.08±9.1251.23±9.72IV平消胶囊+化疗/化疗6周①②③④⑤⑦⑧ 李豫江等[36]303034~4834~48II~III平消胶囊+化疗/化疗8周①②⑦ 杨沁惠[37]424253.87±6.2355.42±6.78NR平消胶囊+化疗/化疗12~18周①②⑤ 张清媛等[38]44444245NR平消胶囊+化疗/化疗12周①②③⑥ 陈前军等[39]22164343II~III槐耳颗粒+化疗/化疗8周①②⑥⑦ 陈莹等[40]505061.50±5.1661.42±5.12I~IV槐耳颗粒+化疗/化疗6周①②③⑥ 代佑果等[41]34344242II~III槐耳颗粒+化疗/化疗8~12周⑧ 梁月琴等[42]485049.651.2IV槐耳颗粒+化疗/化疗24周⑥⑦⑧ 鲁明骞等[43]454548.248.2I~IV槐耳颗粒+化疗/化疗18周③⑧ 陆烨等[44]151551.7±7.851.7±7.8I~IV槐耳颗粒+化疗/化疗18周③⑥⑧ 屈淑贤等[45]353060~7960~79NR槐耳颗粒+化疗/化疗2年③⑧ 王伟等[46]484840.9±4.042.1±4.5I~III槐耳颗粒+化疗/化疗18周③⑥⑦ 杨震[47]303054.9±8.954.9±8.9I~II槐耳颗粒+化疗/化疗6周③ 张朦等[48]303053.58±5.5253.64±5.62IV槐耳颗粒+化疗/化疗24周①② 赵子伟等[49]313142.8±1.342.4±1.6III~IV槐耳颗粒+化疗/化疗12周①②③⑧ 焦东晓等[50]484856.2±7.356.8±6.9II~III参一胶囊+化疗/化疗9周①②⑥⑦ 寇小格等[51]2828NRNRIV参一胶囊+化疗/化疗NR①②③⑥⑦ 许鸿雁等[52]404054.7±9.556.6±8.2IV参一胶囊+化疗/化疗16周⑥ 张绪良等[53]696646.26±15.5246.13±14.3IV参一胶囊+化疗/化疗12周①② 赵华峰等[54]28285051IV参一胶囊+化疗/化疗16周①②⑥⑦ 赵曙等[55]4545NRNRI~III参一胶囊+化疗/化疗8周③⑥ 周航等[56]2424NRNRNR参一胶囊+化疗/化疗6~8周⑥ 孔秋梅等[57]434351.6±7.750.9±7.0I~IV复方斑蝥胶囊+化疗/化疗9周①②③⑥⑦⑧ 李莉等[58]4141NRNRII~III复方斑蝥胶囊+化疗/化疗18周①② 刘海舟等[59]393945.26±3.8244.95±3.47NR复方斑蝥胶囊+化疗/化疗6~9周①②③⑥⑦⑧ 徐洁等[60]22224146NR复方斑蝥胶囊+化疗/化疗12周①②④⑤⑥ 张军华等[61]3434NRNRII~III复方斑蝥胶囊+化疗/化疗6周⑧ 陈浩[62]464646.34±7.8845.67±7.91III~IV华蟾素胶囊+化疗/化疗6周④⑤⑥ 邓爽等[63]313150.27±6.2349.57±5.86IV华蟾素胶囊+化疗/化疗8周①②④⑤ 郭宁等[64]606045.37±7.6845.54±7.82II~III华蟾素胶囊+化疗/化疗8周①②⑥ 何林莉等[65]686843.7±1.944.33±2.10NR华蟾素胶囊+化疗/化疗8周①②⑥ 柯红等[66]202138.3±8.939.5±8.8NR华蟾素胶囊+化疗/化疗12周①②③⑥⑦ 李玲[67]303049.34±7.3448.36±8.52III~IV华蟾素胶囊+化疗/化疗12周期①②④⑤⑥⑦ 田柳[68]313150.27±6.2349.57±5.86IV华蟾素胶囊+化疗/化疗9~18周①②④⑤⑥⑦ 白俊文等[69]32324345II~III金龙胶囊+化疗/化疗6周①②③ 山院飞等[70]424228~6430~65II~III金龙胶囊+化疗/化疗8周⑧ 张绪良等[71]96964443II~III金龙胶囊+化疗/化疗12周①②③ 侯文宇等[72]393942.09±8.1441.58±7.91IV小金片+化疗/化疗12周①②⑥⑦⑧ 王逊等[73]545451.9±10.653.0±9.5I~III小金片+化疗/化疗12周③⑧ 张超等[74]515145.9±5.844.9±8.8III小金丸+化疗/化疗12周①②⑧ 徐宁等[75]474330.2±2.430.2±2.4NR养正消积胶囊+化疗/化疗18周①②⑧ 徐志宏等[76]4040NRNRNR养正消积胶囊+化疗/化疗18周①②⑧ 李勇[77]303046.32±6.2345.29±7.01NR贞芪扶正颗粒+化疗/化疗12周⑥
T-试验组 C-对照组 NR-未报道 TNM-肿瘤淋巴转移 ①疾病客观缓解率(ORR) ②疾病控制率(DCR) ③生存质量情况 ④疾病无进展生存期(PFS) ⑤总生存期(OS) ⑥白细胞减少发生率 ⑦消化道不良反应 ⑧相关免疫功能改变情况
T-treatment group C-control group NR-none reported TNM-tumor node metastasis ①objective response rate ②disease control rate ③quality of life ④progression free survival ⑤overall survival ⑥incidence of leucopenia ⑦digestive tract adverse reaction ⑧related changes in immune function
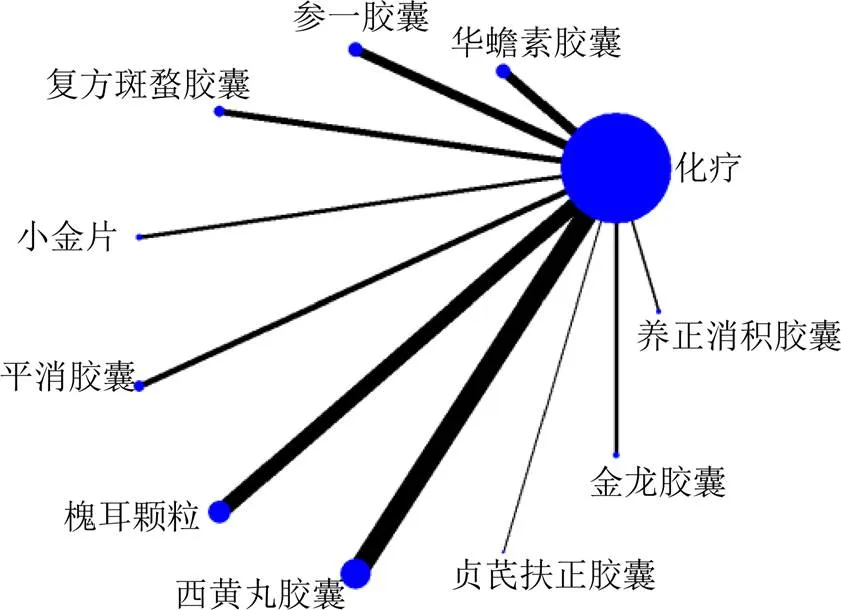
图2 纳入研究各干预措施比较的网络关系
2.3 纳入文献方法学质量
纳入文献有26项研究报道随机方法为随机数字表或简单随机法[19-23,26,28,30,34-35,38,48-50,53-54,57-58,60-61,65,67,70,73-74,76],评价其为低偏倚风险;有2项研究[18,68]报道按就诊顺序和奇偶数随机分组,评价其为高偏倚风险;其他研究仅报道“随机”分组,评价其偏倚风险为不清楚。有2篇[47,63]报道采用不透明信封进行序列隐藏,其他文献均未报道序列隐藏。考虑纳入文献的干预类型,无法对受试者和干预者实施盲法,评价为高偏倚风险。所有研究未报道结局评价人员盲法,其偏倚风险为不清楚。所有研究数据完整,未报道脱落失访数据。纳入各研究结局报道情况与方法部分内容一致。其他偏倚主要评估基线资料信息,纳入文献基线均可比。纳入文献的方法学质量情况见图3。
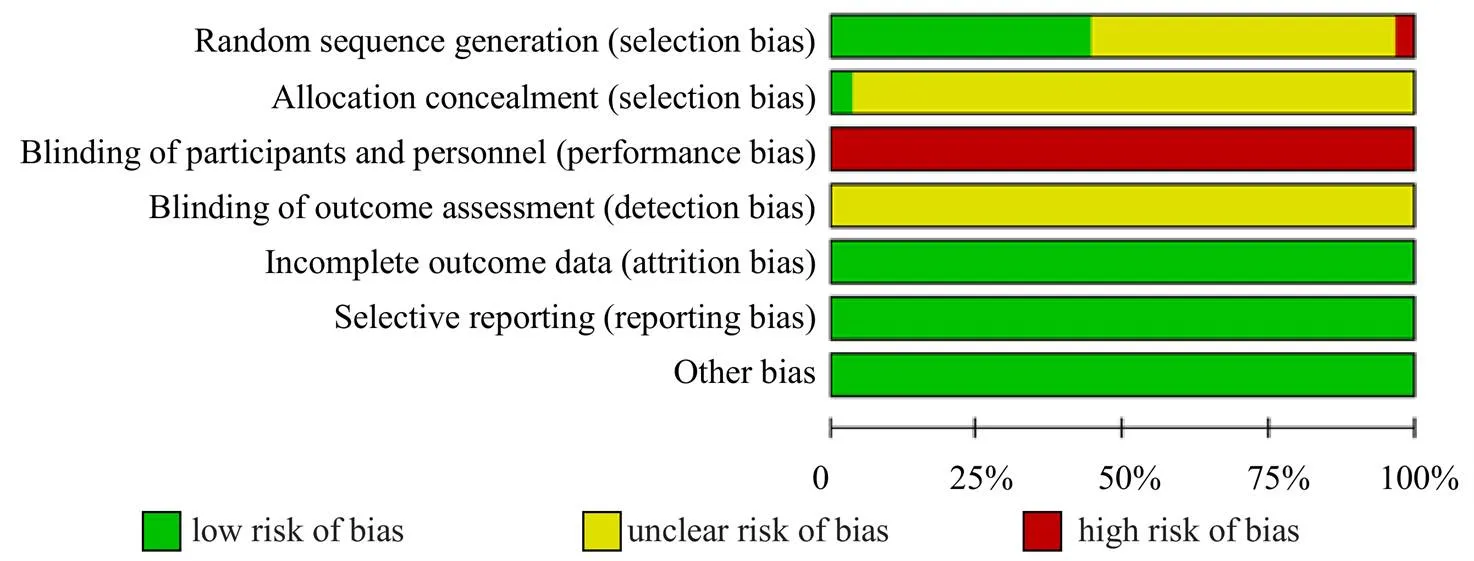
图3 纳入研究各偏倚风险项目的所占百分比
2.4 网状Meta分析结果
纳入各干预措施间不存在闭合环,即各干预措施间不存在直接比较,所有干预药物之间的两两比较均来自间接比较,因此不需要进行不一致性检验,其结果均可直接在一致性模型下进行统计分析。数据分析的基础设置如下:链(number of chains):4;退火(tuning iterations):20 000;迭代(simulation iterations):50 000;步长(thinning interval):10,初始值(initial values scaling):2.5。分析中根据实际情况调节初始值和迭代次数,其中ORR、DCR、PFS和OS分析中初始值设定为4;QOL分析中设置退火:60 000,迭代:100 000,初始值:6,其他结局指标的数据分析采用基础设置。
2.4.1 ORR 网状Meta分析结果显示与单纯化疗相比,复方斑蝥胶囊、华蟾素胶囊、槐耳颗粒、金龙胶囊、平消胶囊、参一胶囊、小金片/丸、西黄丸/ 胶囊及养正消积胶囊联合化疗治疗乳腺癌的ORR疗效优于单纯化疗,且差异具有统计学意义(<0.05)。而小金片/丸联合化疗在改善ORR方面较单独化疗,疗效差异无统计学意义。9种中成药间两两比较的ORR差异均无统计学意义,见表2。
2.4.2 DCR 网状Meta分析结果显示,复方斑蝥胶囊、华蟾素胶囊、槐耳颗粒、金龙胶囊、平消胶囊、参一胶囊、小金片和西黄丸/胶囊联合化疗治疗乳腺癌的ORR疗效优于单纯化疗,且差异具有统计学意义(<0.05)。而小金片/丸和养正消积胶囊联合化疗在改善DCR方面较单用化疗,疗效差异无统计学意义。9种中成药间两两比较的DCR差异均无统计学意义,见表3。
2.4.3 QOL改善率 网状Meta分析结果显示,复方斑蝥胶囊、华蟾素胶囊、槐耳颗粒、金龙胶囊、参一胶囊和西黄丸/胶囊联合化疗治疗乳腺癌的QOL改善率疗效优于单纯化疗,且差异具有统计学意义(<0.05)。而平消胶囊联合化疗在QOL改善率方面较单用化疗,疗效差异无统计学意义。7种中成药间两两比较的QOL改善率差异均无统计学意义,见表4。
2.4.4 PFS 网状Meta分析结果显示,在提高PFS 方面西黄丸/胶囊联合化疗治疗乳腺癌优于单纯化疗,且差异具有统计学意义(<0.05)。而复方斑蝥胶囊、华蟾素胶囊、平消胶囊联合化疗在改善PFS方面较单用化疗,疗效差异无统计学意义。4种中成药间两两比较的PFS差异均无统计学意义,见表5。
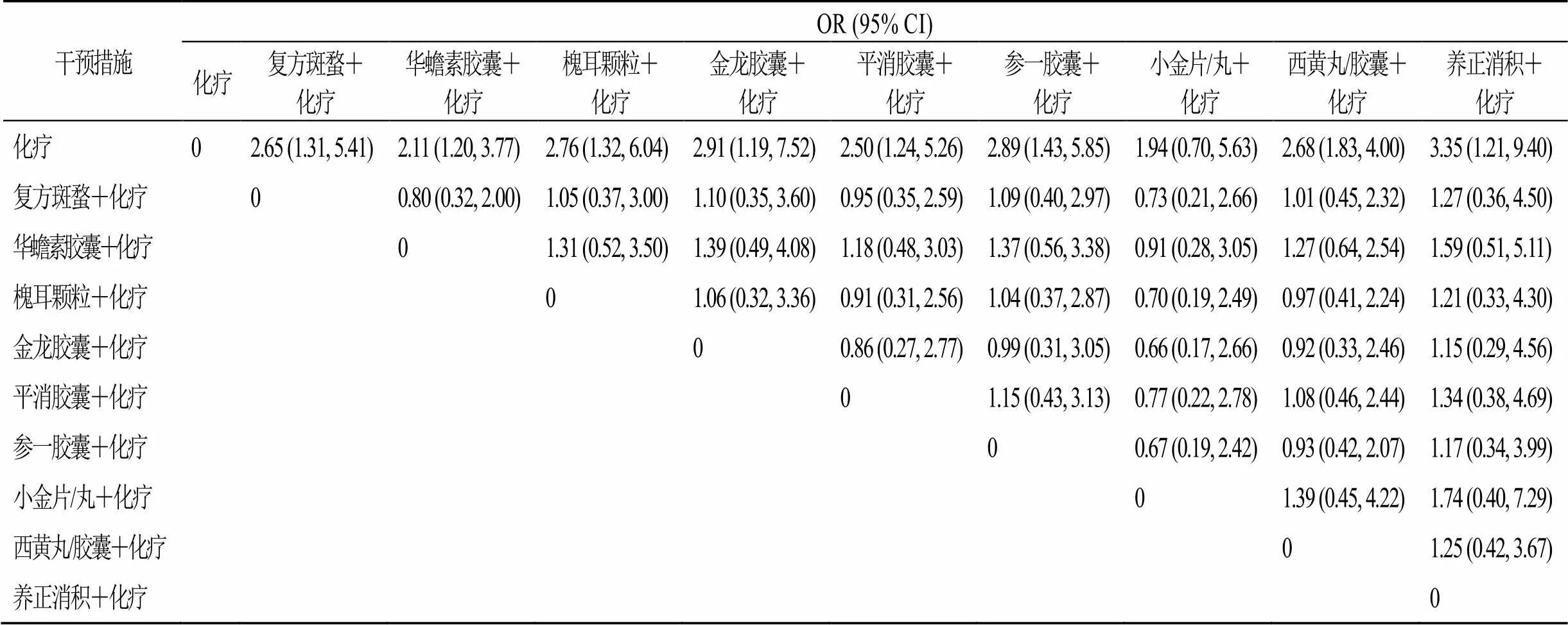
表2 ORR网状Meta分析结果
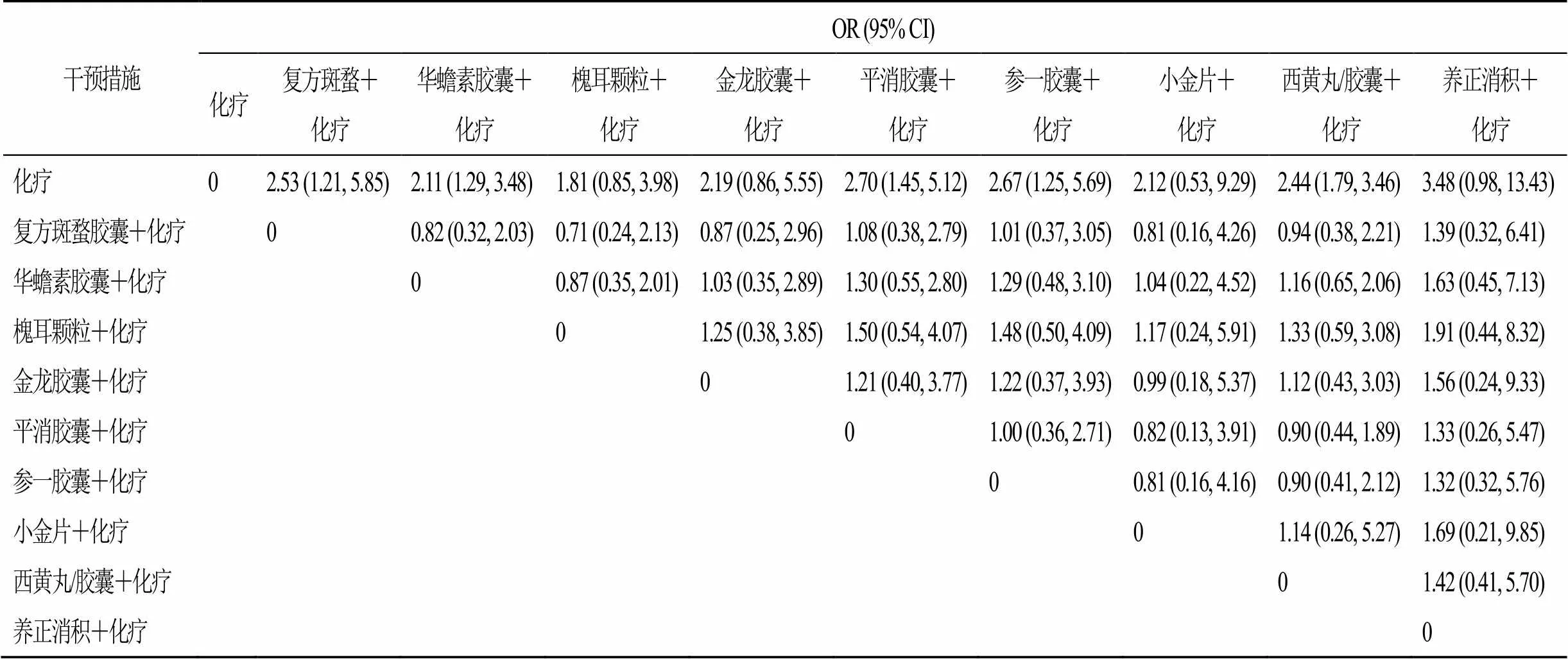
表3 DCR网状分析结果

表4 QOL改善率网状分析结果
2.4.5 OS 网状Meta分析结果显示,西黄丸/胶囊和平消胶囊联合化疗治疗乳腺癌在提高OS方面优于单纯化疗,且差异有统计学意义(<0.05)。而复方斑蝥胶囊、华蟾素胶囊联合化疗在OS改善方面较单用化疗,疗效差异无统计学意义。4种中成药间两两比较的OS差异均无统计学意义,见表6。
2.4.6 白细胞减少发生率 网状Meta分析结果显示,华蟾素胶囊、槐耳颗粒、参一胶囊、西黄丸/胶囊联合化疗治疗乳腺癌的白细胞减少发生率明显低于单纯化疗,且差异具有统计学意义(<0.05)。而复方斑蝥胶囊、平消胶囊、小金片/丸和贞芪扶正颗粒联合化疗治疗乳腺癌的白细胞减少发生率较单纯化疗,疗效差异无显著统计学意义。中成药间两两比较的疗效差异均无统计学意义,见表7。
2.4.7 消化道不良反应发生率 网状Meta分析结果显示,西黄丸/胶囊、贞芪扶正颗粒联合化疗治疗乳腺癌的消化道不良反应发生率明显低于单纯化疗,且差异具有统计学意义(<0.05)。而复方斑蝥胶囊、华蟾素胶囊、槐耳颗粒、平消胶囊、参一胶囊和小金片/丸联合化疗治疗乳腺癌的白细胞减少发生率较单纯化疗,疗效差异无显著统计学意义。中成药间两两比较结果显示槐耳颗粒、参一胶囊、西黄丸/胶囊及贞芪扶正颗粒联合化疗方案的消化道不良反应发生率低于复方斑蝥胶囊联合化疗方案,差异具有统计学意义(<0.05);其他中成药间两两比较差异均无统计学意义,见表8。

表5 PFS网状分析结果

表6 OS网状分析结果MD (95% CI)

表7 白细胞减少发生率网状分析结果
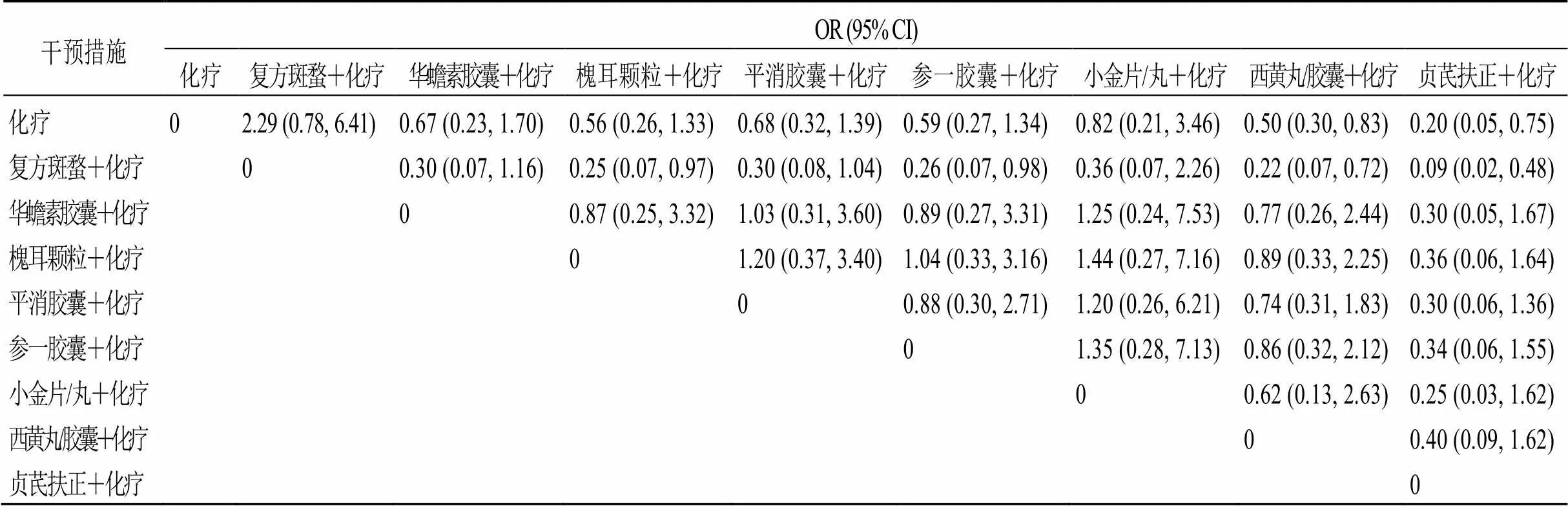
表8 消化道反应发生率网状分析结果
2.4.8 CD4+/CD8+变化程度 网状Meta分析结果显示,槐耳颗粒、平消胶囊、小金片/丸和养正消积胶囊联合化疗能提高乳腺癌患者血液中CD4+/CD8+值,且差异具有统计学意义(<0.05)。而复方斑蝥胶囊、金龙胶囊和西黄丸/胶囊联合化疗方案对乳腺癌患者血液中CD4+/CD8+值的影响较单纯化疗,疗效差异无统计学意义。中成药间两两比较结果显示平消胶囊联合化疗方案在提升乳腺癌患者血液中CD4+/CD8+值优于复方斑蝥胶囊联合化疗方案,差异具有统计学意义(<0.05);其余中成药间两两比较,疗效差异无统计学意义,见表9。
2.5 干预措施疗效排序
利用Gemtc14.3进行网状Meta分析时,并基于贝叶斯模型计算各干预措施疗效的优选排序概率,推断每种措施在不同结局指标下成为最有效治疗的可能性大小,评估相关药物的疗效优势情况。
2.5.1 ORR 网状Meta分析结果提示养正消积胶囊联合化疗成为最佳干预措施的可能性最大,其次为参一胶囊和西黄丸/胶囊联合化疗。相关口服中成药联合化疗及单纯化疗治疗乳腺癌患者ORR的贝叶斯疗效排序依次为养正消积胶囊(0.31)>金龙胶囊(0.15)>参一胶囊(0.16)>槐耳颗粒(0.12)>西黄丸/胶囊(0.19)>复方斑蝥胶囊(0.12)>华蟾素胶囊(0.19)>平消胶囊(0.14)>小金片/丸(0.27)>化疗(0.86)。虽然概率排序结果提示养正消积胶囊联合化疗成为最佳干预措施的可能性最大,而“2.4.2”项中DCR的网状Meta分析结果提示养正消积胶囊联合化疗在改善DCR方面较单用化疗的疗效差异无统计学意义。考虑养正消积胶囊只纳入2项研究,且均未报告疾病TNM分期,这可能会对结果造成一定偏倚,故排除这2项研究[75-76],对其他研究结果再次分析。ORR结果显示除小金片/丸以外,其他药物联合化疗治疗乳腺癌的ORR疗效优于单纯化疗,差异具有统计学意义(<0.05)。概率排序为金龙胶囊>参一胶囊>槐耳颗粒>西黄丸>复方斑蝥胶囊>平消胶囊>华蟾素胶囊>小金片/丸>化疗,见表10。
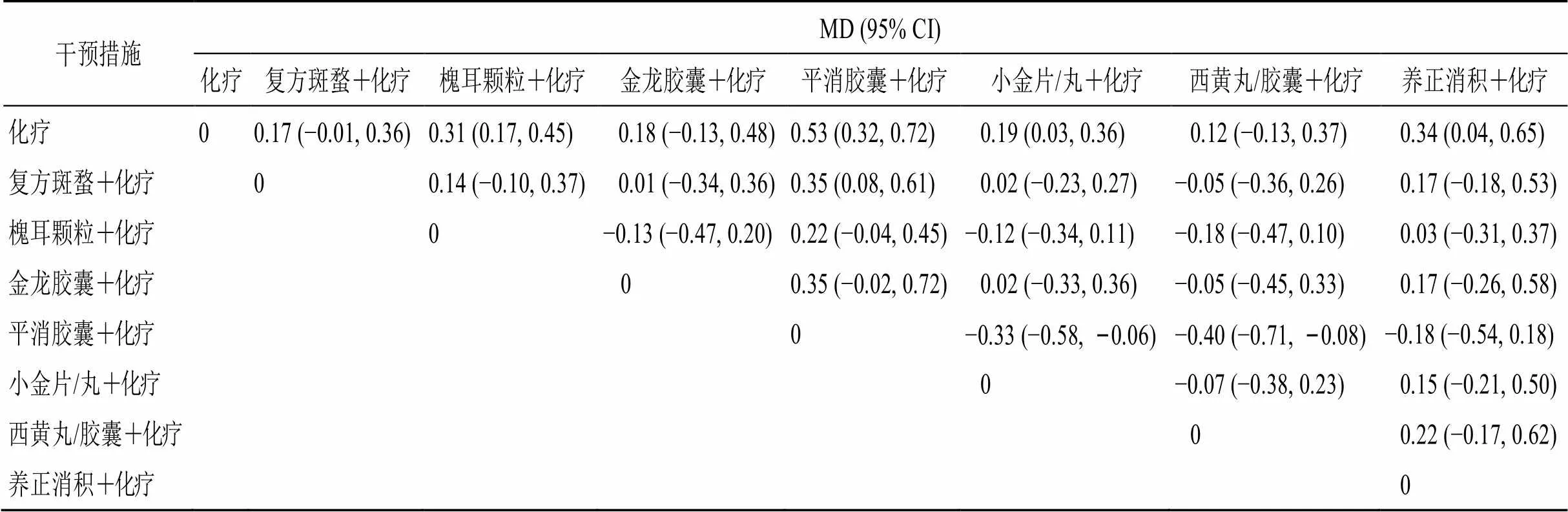
表9 CD4+/CD8+变化程度的网状分析结果

表10 干预措施疗效排序结果
*代表疗效概率排序相等
*means the probability of curative effect is equal
2.5.2 DCR 由网状Meta分析结果可知,养正消积胶囊联合化疗成为最佳干预措施的可能性最大,其次为参一胶囊和平消胶囊联合化疗。相关口服中成药联合化疗及单纯化疗治疗乳腺癌患者DCR的贝叶斯疗效排序依次为养正消积胶囊(0.41)>参一胶囊(0.17)>平消胶囊(0.17)>西黄丸/胶囊(0.21)>华蟾素胶囊(0.17)>复方斑蝥胶囊(0.12)>金龙胶囊(0.11)>槐耳颗粒(0.23)>小金片/丸(0.14)>化疗(0.73)。概率排序结果提示养正消积胶囊联合化疗成为最佳干预措施的可能性最大,而“2.4.2”项中DCR的网状Meta结果提示养正消积胶囊联合化疗在改善DCR方面较单用化疗的疗效差异无统计学意义。考虑养正消积胶囊仅2项研究,其结果可能会对结果造成一定偏倚,故排除这2项研究,对其他研究结果再次分析。DCR结果显示除小金片/丸、金龙胶囊和槐耳颗粒以外,其他药物联合化疗治疗乳腺癌的DCR疗效优于单纯化疗,差异具有统计学意义(<0.05)。概率排序为参一胶囊>平消胶囊>西黄丸>华蟾素胶囊>复方斑蝥胶囊>金龙胶囊>槐耳颗粒>小金片/丸>化疗,见表10。
2.5.3 QOL改善率 由网状Meta分析结果可知,西黄丸/胶囊联合化疗成为最佳干预措施的可能性最大,其次为槐耳颗粒和参一胶囊联合化疗方案。相关口服中成药联合化疗及单纯化疗治疗乳腺癌患者QOL的贝叶斯疗效排序依次为西黄丸/胶囊>槐耳颗粒>参一胶囊>华蟾素胶囊>金龙胶囊>复方斑蝥胶囊>平消胶囊>化疗。见表10。
2.5.4 PFS 由网状Meta分析结果可知,西黄丸联合化疗成为最佳干预措施的可能性最大,其次为平消胶囊联合化疗。相关口服中成药联合化疗及单纯化疗治疗乳腺癌患者PFS的贝叶斯疗效排序依次为西黄丸/胶囊>平消胶囊>复方斑蝥胶囊>华蟾素胶囊>化疗。见表10。
2.5.5 OS 由网状Meta分析结果可知,平消胶囊联合化疗成为最佳干预措施的可能性最大,其次为西黄丸联合化疗。相关口服中成药联合化疗及单纯化疗治疗乳腺癌患者OS的贝叶斯概率排序依次为平消胶囊>西黄丸/胶囊>华蟾素胶囊>复方斑蝥胶囊>化疗。见表10。
2.5.6 白细胞减少发生率 由网状Meta分析结果可知,参一胶囊联合化疗成为最佳干预措施的可能性最大,其次为槐耳颗粒联合化疗。相关口服中成药联合化疗及单纯化疗治疗乳腺癌患者白细胞减少发生率的贝叶斯疗效排序依次为参一胶囊>槐耳颗粒>华蟾素胶囊>西黄丸/胶囊>贞芪扶正颗粒>平消胶囊>复方斑蝥胶囊>小金片/丸>化疗。见表10。
2.5.7 消化道反应发生率 由网状Meta分析结果可知,贞芪扶正颗粒联合化疗成为最佳干预措施的可能性最大,其次为西黄丸/胶囊联合化疗。相关口服中成药联合化疗及单纯化疗治疗乳腺癌患者消化道反应发生率的贝叶斯疗效排序依次为贞芪扶正颗粒>西黄丸/胶囊>槐耳颗粒和参一胶囊>平消胶囊>华蟾素胶囊>小金片/丸>化疗>复方斑蝥胶囊。见表10。
2.5.8 CD4+/CD8+变化程度 由网状Meta分析结果可知,平消胶囊联合化疗成为最佳干预措施的可能性最大,其次为养正消积胶囊联合化疗。相关口服中成药联合化疗及单纯化疗治疗乳腺癌患者血液中CD4+/CD8+值变化的贝叶斯疗效排序依次为平消胶囊>养正消积胶囊>槐耳颗粒>小金片>金龙胶囊>西黄丸/胶囊>复方斑蝥胶囊>化疗。见表10。
2.6 亚组分析
考虑乳腺癌疾病TNM分期对结局指标的影响,基于乳腺癌不同疾病分期I~III期和III~IV期对主要结局中ORR和DCR分别进行亚组分析,进一步分析不同TNM分期对药物应用的影响情况。
2.6.1 ORR结果 对于I~III期患者[19-20,22,25,33,36,39,50,58,64,69,71,74],结果显示参一胶囊、金龙胶囊、西黄丸联合化疗干预乳腺癌的ORR效果优于单纯化疗,且差异有统计学意义,其他药物联合化疗较单用化疗差异无统计学意义;各干预措施疗效排序为参一胶囊(0.54)>金龙胶囊(0.24)>西黄丸/胶囊(0.15)>平消胶囊(0.2)>复方斑蝥胶囊(0.17)>华蟾素胶囊(0.14)>槐耳颗粒(0.06)>小金片/丸(0.21)>化疗(0.33)。对于III~IV期患者[22,29-32,35,48-49,51,53-54,63,67,72,74],结果显示槐耳颗粒和西黄丸联合化疗干预乳腺癌的ORR疗效分别优于单纯化疗,且差异有统计学意义,其他药物联合化疗较单用化疗差异无统计学意义;各干预措施疗效排序为槐耳颗粒(0.49)>西黄丸/胶囊(0.18)>参一胶囊(0.19)>华蟾素胶囊(0.14)>平消胶囊(0.08)>小金片/丸(0.18)>化疗(0.62)。
2.6.2 DCR结果 对于I~III期患者[20,22,25,33,36,39,50,58,64,69,71,74],结果显示金龙胶囊联合化疗干预乳腺癌的DCR效果优于单纯化疗,且差异有统计学意义,其他药物联合化疗较单用化疗差异无统计学意义;各干预措施疗效排序为金龙胶囊(0.6)>西黄丸/胶囊(0.22)>华蟾素胶囊(0.17)>平消胶囊(0.2)>复方斑蝥胶囊(0.15)>槐耳颗粒(0.07)>小金片/丸(0.21)>化疗(0.4)。对于III~IV期患者[22,29-32,35,48-49,51,53-54,63,67,72,74],结果显示平消胶囊、参一胶囊和西黄丸联合化疗干预乳腺癌的DCR疗效分别优于单纯化疗,且差异有统计学意义,其他药物联合化疗较单用化疗差异无统计学意义;各干预措施疗效排序为平消胶囊(0.41)>参一胶囊(0.24)>西黄丸/胶囊(0.23)>华蟾素胶囊(0.15)>槐耳颗粒(0.13)>小金片/丸(0.14)>化疗(0.69)。
2.7 敏感性分析
部分纳入研究未明确报告疾病TNM分期,考虑可能会对结果造成一定偏倚,故排除9篇未报告TNM分期的研究[18,34,38,59-60,65-66,75-76],对其他研究的ORR结果再次分析。结果显示除小金片/丸和华蟾素外,其他药物联合化疗治疗乳腺癌的ORR疗效优于单纯化疗,且差异具有统计学意义(<0.05)。概率排序为平消胶囊(0.39)>复方斑蝥胶囊(0.21)>参一胶囊(0.21)>金龙胶囊(0.16)>西黄丸(0.28)>槐耳颗粒(0.16)>华蟾素胶囊(0.26)>小金片/丸(0.19)>化疗(0.75)。另一方面,基于纳入文献的方法学质量评价,进一步剔除随机方法偏倚风险较高的2项研究[18,68],结果显示除小金片外,其他药物联合化疗治疗乳腺癌的ORR疗效优于单纯化疗,且差异具有统计学意义(<0.05)。概率排序为金龙胶囊(0.24)>参一胶囊(0.18)>西黄丸(0.16)>槐耳颗粒(0.12)>复方斑蝥胶囊(0.12)>平消胶囊(0.14)>华蟾素胶囊(0.16)>小金片/丸(0.29)>化疗(0.86)。敏感性分析结果与上述Meta结果整体趋势基本一致,仅部分药物疗效概率排序出现波动。
2.8 发表偏倚评估
本研究基于主要结局指标ORR和QOL改善率对其纳入的文献绘制比较-校正倒漏斗图评估发表偏倚和小样本效应情况。倒漏斗图提示ORR和QOL改善率所纳入研究大致对称分布在中线两侧,提示不存在明显的发表偏倚;另一方面也提示研究结果受小样本效应影响的可能性较小。见图4、5。
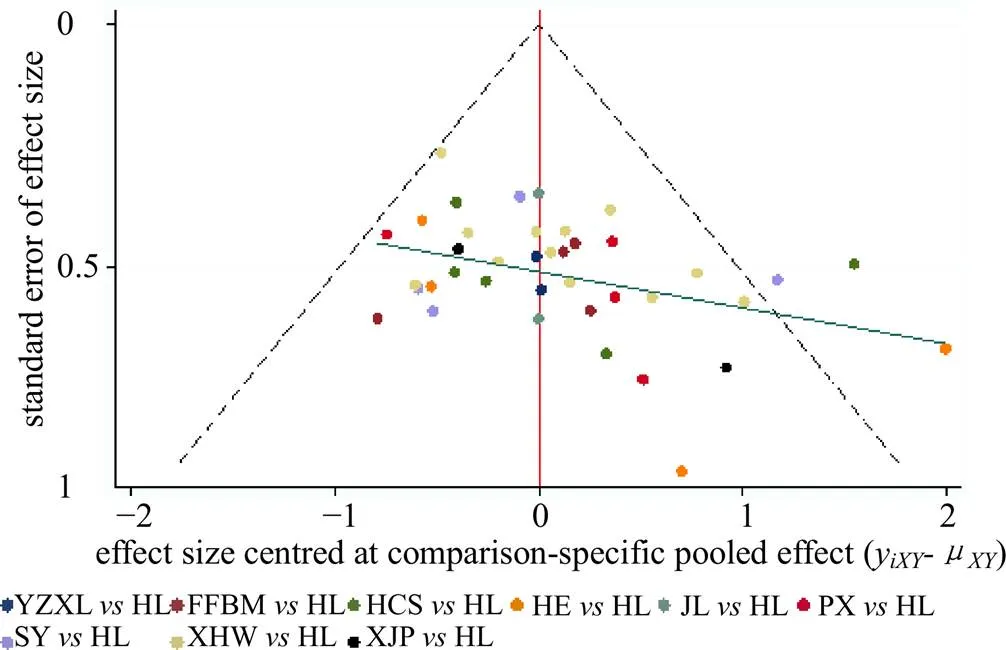
YZXL-养正消积胶囊 FFBM-复方斑蝥胶囊 HCS-华蟾素胶囊 HE-槐耳颗粒 JL-金龙胶囊 PX-平消胶囊 SY-参一胶囊 XHW-西黄丸 XJP-小金片/丸 HL-化疗,图5同
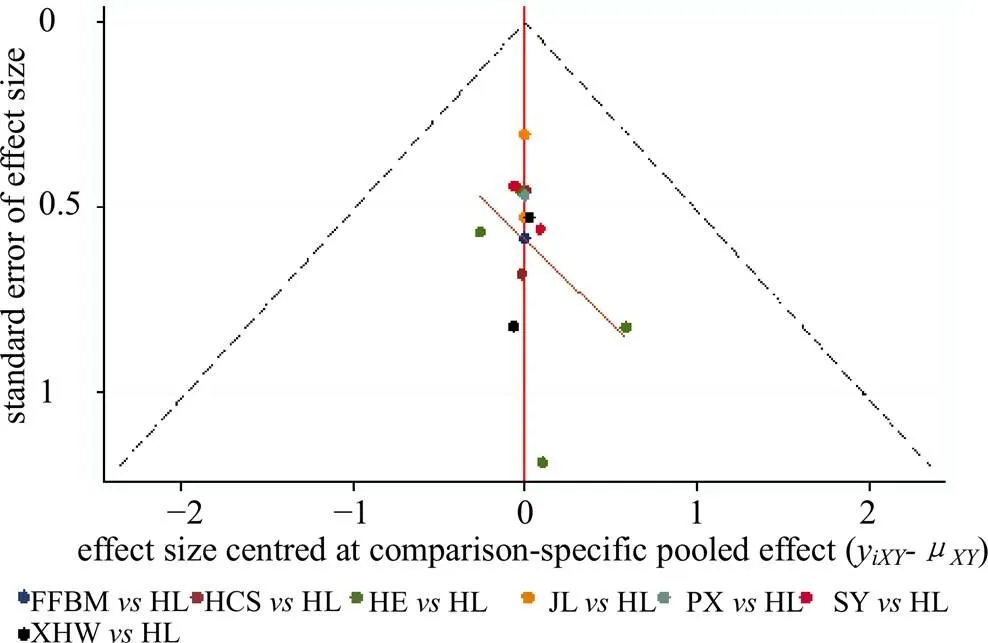
图5 QOL的校正-比较漏斗图
3 讨论
我国《中成药临床应用指导原则》中指出口服给药是目前临床应用最广泛的给药途径,考虑用药的安全性,临床应用中应首选口服剂型给药[78],同时既往调查显示某医院乳腺癌门诊应用相关中成药达27种,因此关于相关口服中药成在乳腺癌治疗中的应用具有较好前景[79]。本研究采用网状Meta分析方法系统评价相关口服类中成药联合化疗方案治疗乳腺癌的疗效,分别从近期疗效(ORR和DCR)、生活质量、远期疗效(PFS和OS)、降低相关不良反应等不同结局指标进行分析,梳理更具有疗效优势的药品信息,从而为乳腺癌患者选择口服类中成药提供的参考依据。本研究最终纳入61项RCTs进行数据分析,涉及西黄丸/胶囊、平消胶囊、槐耳颗粒、参一胶囊、复方斑蝥胶囊、华蟾素胶囊、金龙胶囊、小金片/丸、养正消积胶囊及贞芪扶正颗粒10种口服中成药。网状Meta分析疗效排序概率综合结果提示金龙胶囊、参一胶囊和槐耳颗粒改善ORR较明显,金龙胶囊联合化疗为最佳方案的可能性最大;参一胶囊、平消胶囊和西黄丸等联合化疗改善DCR更明显,参一胶囊联合化疗为最佳方案的可能性最大。值得注意的是亚组分析结果提示乳腺癌不同疾病分期患者适用药物存在不同,对于Ⅰ~Ⅲ期患者,参一胶囊联合化疗在改善ORR方面为最佳方案的可能性最大,金龙胶囊联合化疗在改善DCR方面为最佳方案的可能性最大。对于Ⅲ~Ⅳ期患者,槐耳颗粒联合化疗在改善ORR方面为最佳方案的可能性最大,平消胶囊和参一胶囊联合化疗在改善DCR方面疗效优势较明显。
在改善生活质量方面,西黄丸具有明显疗效优势,疗效排序概率提示西黄丸联合化疗为最佳方案的可能性最大;在提高远期疗效方面,结果显示西黄丸有益于提高乳腺癌患者的PFS和OS,平消胶囊有益于提高OS。在安全性方面,结果提示相对其他中成药,复方斑蝥胶囊联合化疗可能会增加患者消化道反应,因此,对于脾胃功能虚弱的患者或出现消化道反应的患者,应审慎选择复方斑蝥胶囊。其他中成药联合化疗尚不会增加不良反应,西黄丸/ 胶囊和贞芪扶正颗粒联合化疗在降低消化道不良反应方面较为明显。此外,结果提示参一胶囊、槐耳颗粒和华蟾素胶囊等联合化疗更有益于降低乳腺癌患者白细胞减少的发生率。本研究还分析了口服中成药对乳腺癌患者血液T淋巴细胞亚群含量的影响,结果提示平消胶囊、养正消积胶囊、槐耳颗粒等联合化疗在提高乳腺癌患者血液中CD4+/CD8+值方面较明显,从而有益于提高患者机体免疫功能,但报道该结果的研究数量有限,故中成药对患者血液中CD4+/CD8+值的影响情况有待进一步证实。数据分析过程中,发现临床异质性主要与疾病分期、口服中成药种类及用法、化疗种类及治疗疗程或周期等有关,方法学异质性主要与随机方法不清楚和盲法受限等相关,且亚组分析和敏感性分析提示不同疾病分期的用药存在一定不同选择,尤其是本研究关于报道生活质量改善率、PFS和OS的纳入研究数量有限,且一些研究未明确疾病分期情况,尚不能得出其指标下不同疾病分期的药物干预疗效排序信息,因此,基于以上临床结局的结果解释应审慎,实践用药应充分考虑患者实际情况。敏感性分析和发表偏倚分析提示研究结果整体尚稳定可靠。
乳腺癌在中医学中可归属于“乳岩”范畴,在古代文献中另有“乳石痈、乳癌、乳石、奶岩”等命名,历代医家认为乳腺癌多为虚实夹杂之证,病因方面正气亏虚、冲任失调为内因,情志不遂、饮食失调等为外因,内外病因相合致气滞而瘀血内生,瘀毒凝结于乳中,日久发为乳癌[80]。随着肿瘤学科的发展,医家们不断摸索和总结对乳腺癌疾病的认知,在临床实践中总结相关诊治的经验,对乳腺癌的中医药治疗起到了重要的指导作用。如林洪生[81]提出“固本清源”治疗恶性肿瘤的学术思想,“固本”即扶正固本,“清源”则从源头上控制肿瘤,祛除“毒、瘀”等病理因素,临床提倡攻补兼施的原则。刘尚义教授将疡科相关理法创新运用到肿瘤疾病的治疗中,最终总结和提出“引疡入瘤”的学术思想,其内涵包括“疡理诊瘤、疡法治瘤、疡药疗瘤”等内容[82],为临床防治肿瘤疾病提供了更多的思路与方法。本研究中药物西黄丸出自《外科证治全生集》,结果显示其在改善乳腺癌患者生活质量和提高远期疗效方面具有明显优势,这与引疡入瘤理论中疡法治瘤和疡药疗瘤的思想内涵相一致。裴晓华等[10]分别从扶正固本、增效减毒、抗癌抑瘤3个方面系统总结了中医药在恶性肿瘤治疗中的应用,并结合现代医学研究阐述了中医药治疗恶性肿瘤的相关作用机制。在各家中医肿瘤学说的指导下,肿瘤的中医治疗逐渐系统化和规范化,为进一步从中医角度探索本研究结果,根据纳入中成药说明书、中药物组成及功用等,将其大致归为以下几类:补益剂、攻补兼施剂、祛邪剂。贞芪扶正颗粒和参一胶囊培元固本、益气扶正,可归属于补益剂;养正消积胶囊具有健脾益肾、化瘀解毒的作用,槐耳颗粒具有扶正固本、活血消癥之功,此二药属攻补兼施剂;其他药物具有活血化瘀、散结消肿及解毒止痛等功效,属于祛邪剂。综合本研究结果,可以发现相关口服中成药分阶段、个性化地与乳腺癌化疗治疗相结合,其临床实践取得了丰富成果。需要指出的是养正消积胶囊和贞芪扶正颗粒在干预乳腺癌的临床疗效和较低消化道反应方面分别具有一定效果,尤其是本研究结果提示贞芪扶正颗粒联合化疗在减低消化道反应方面具有较好效果,但其相关研究较少,故结果可靠性尚待更多高质量研究加以验证。
本研究可能存在以下的局限性:(1)纳入的部分中成药相关原始研究数量有限(如养正消积胶囊2篇、贞芪扶正颗粒1篇),其样本量较少,导致检验效能偏低,其网状Meta分析的相关疗效结果存在不确定性。(2)纳入研究间缺乏与其他治疗方式之间的比较(如放疗、靶向治疗等),可能对部分结果的解读和推广造成潜在影响。(3)相关药物的临床试验在生活质量、远期疗效指标(如PFS和OS)及免疫相关等结局指标方面的报告不足或尚未能开展研究,这可能使得多角度疗效评价缺乏充分数据支持,尤其是有13项研究(21.3%)对疾病分期未明确,使得基于疾病分期的用药分析受到一定限制。
综上所述,当前证据提示口服中成药联合化疗治疗乳腺癌的疗效往往优于单纯化疗,一般不会增加相关不良反应的发生。对于I~III期患者,参一胶囊联合化疗改善ORR的效果显著,金龙胶囊联合化疗改善DCR效果最明显。对于Ⅲ~Ⅳ期患者,槐耳颗粒联合化疗改善ORR效果最明显,平消胶囊和参一胶囊联合化疗改善DCR方面有较好效果。西黄丸在改善患者生活质量方面更明显,参一胶囊和槐耳颗粒有助于降低乳腺癌患者白细胞减少的发生率。贞芪扶正颗粒在降低乳腺癌患者消化道反应发生率方面更有优势。受纳入研究质量和缺少中成药直接对比研究的限制,上述结论有待更多大样本、高质量和报告规范的研究进一步验证。
利益冲突 所有作者均声明不存在利益冲突
[1] Lewis D R, Chen H S, Cockburn M G,. Early estimates of cancer incidence for 2015: Expanding to include estimates for white and black races [J]., 2018; 124(10): 2192-204.
[2] Song M M, Fang S, Tanaka S,. Effects of arsenic disulfide on proliferation, cytokine production, and frequencies of CD4(+), CD8(+), and regulatory T cells in mitogen-activated human peripheral blood mononuclear cells [J]., 2015, 29(2): 832-838.
[3] Feng R M, Zong Y N, Cao S M,. Current cancer situation in China: Good or bad news from the 2018 Global Cancer Statistics? [J].(Lond), 2019, 39(1): 22.
[4] Trayes K P, Cokenakes S E H. Breast cancer treatment [J]., 2021, 104(2): 171-178.
[5] 何明艳, 朱碧琪, 钟媛, 等. 2005—2013年中国女性乳腺癌发病及死亡趋势分析 [J]. 中华疾病控制杂志, 2019, 23(1): 10-14.
[6] 中国抗癌协会乳腺癌专业委员会. 中国抗癌协会乳腺癌诊治指南与规范(2019年版) [J]. 中国癌症杂志, 2019, 29(8): 609-680.
[7] Harbeck N, Gnant M. Breast cancer [J]., 2017, 389(10074): 1134-1150.
[8] Denegri A, Moccetti T, Moccetti M,. Cardiac toxicity of trastuzumab in elderly patients with breast cancer [J]., 2016; 13(4): 355-363.
[9] Valachis A, Nilsson C. Cardiac risk in the treatment of breast cancer: Assessment and management [J]., 2015, 7: 21-35.
[10] 裴晓华, 彭艳梅. 中医药治疗恶性肿瘤70年 [J]. 中国肿瘤外科杂志, 2019, 11(5): 305-308.
[11] Qi F, Zhao L, Zhou A,. The advantages of using traditional Chinese medicine as an adjunctive therapy in the whole course of cancer treatment instead of only terminal stage of cancer [J]., 2015, 9(1): 16-34.
[12] Mao D, Feng L, Huang S Q,. Meta-analysis of xihuang pill efficacy when combined with chemotherapy for treatment of breast cancer [J]., 2019, 2019: 1-14.
[13] 王晓珊, 吴琦, 梁良. 参一胶囊联合化疗治疗乳腺癌的系统评价 [J]. 实用医院临床杂志, 2012, 9(6): 192-195.
[14] Park J O, Lee S I, Song S Y,. Measuring response in solid tumors: Comparison of RECIST and WHO response criteria [J]., 2003, 33(10): 533-537.
[15] Green S, Higgins J P. Preparing a cochrane review [A] //[M]. Chichester: John Wiley & Sons, Ltd.,2019:11-30.
[16] Hutton B, Salanti G, Caldwell D M,. The PRISMA extension statement for reporting of systematic reviews incorporating network meta-analyses of health care interventions: Checklist and explanations [J]., 2015, 162(11): 777-784.
[17] 陈漉. 西黄胶囊联合化疗治疗中晚期乳腺癌的疗效观察 [J]. 中国卫生标准管理, 2016, 7(13): 151-152.
[18] 周璇, 廖盼丽, 吴文英, 等. 西黄胶囊联合GP方案对中晚期乳腺癌患者血清TNF-α, VEGF, MMP-2, MMP-9水平的影响 [J]. 现代生物医学进展, 2017, 17(23): 4525-4528.
[19] 李江艳, 憨镔. 西黄胶囊辅助治疗对乳腺癌患者雌性激素受体、肿瘤标志物及雌性激素的影响研究 [J]. 中医药临床杂志, 2020, 32(7): 1307-1310.
[20] 毛丹, 黄立中, 周春花, 等. 西黄胶囊治疗术后化疗后三阴乳腺癌34例疗效观察 [J]. 新中医, 2014, 46(4): 155-157.
[21] 王黎. 西黄胶囊联合化疗治疗中晚期乳腺癌的疗效观察 [J]. 中医药学报, 2015, 43(6): 82-84.
[22] 吾建香, 王德华. 西黄胶囊联合TEC化疗方案治疗Ⅲ期乳腺癌临床研究及对免疫功能的影响 [J]. 新中医, 2020, 52(12): 117-119.
[23] 张杰, 张颖, 孟惠彦, 等. 西黄胶囊辅助乳腺癌患者全程化疗的临床研究 [J]. 环球中医药, 2015, 8(1): 9-12.
[24] 王千丹. 西黄胶囊在乳腺癌辅助治疗中的应用 [D]. 太原: 山西医科大学, 2017.
[25] 张晓宇, 李泽钊, 白杰, 等. 西黄胶囊联合白蛋白紫杉醇治疗晚期三阴性乳腺癌临床研究 [J]. 中草药, 2020, 51(24): 6324-6327.
[26] 洪日, 吴永强, 吴越. 西黄丸辅助治疗中晚期乳腺癌的疗效观察 [J]. 中国中药杂志, 2014, 39(6): 1120-1123.
[27] 金娟, 李志鸿. 西黄丸联合化疗治疗乳腺癌30例 [J]. 中华中医药杂志, 2010, 25(5): 715-716.
[28] 千维娜, 李治, 李仁廷, 等. 西黄丸联合TP方案治疗中晚期乳腺癌效果分析 [J]. 辽宁中医杂志, 2020, 47(6): 115-117.
[29] 王兵. 西黄丸联合TP方案治疗中晚期乳腺癌的临床研究 [J]. 现代药物与临床, 2018, 33(7): 1746-1750.
[30] 王鹏, 刘彩香, 诸华健, 等. 西黄丸联合CAF方案治疗晚期乳腺癌患者的增效减毒效果观察 [J]. 中药药理与临床, 2017, 33(5): 186-189.
[31] 徐国暑, 谢鑫灵, 孙大兴. 西黄丸联合TC化疗方案对晚期乳腺癌患者临床疗效及生活质量的影响研究 [J]. 中华中医药学刊, 2018, 36(1): 232-234.
[32] 徐炜, 丁少坤, 许宁宁, 等. 西黄丸联合GP方案治疗晚期乳腺癌的疗效观察 [J]. 河北医药, 2020, 42(9): 1358-1361.
[33] 金政男. CAF方案联合平消胶囊治疗乳腺癌术后临床观察 [J]. 辽宁中医杂志, 2012, 39(1): 98-99.
[34] 孔颖, 应佳可, 杨翀. CAF方案联合平消胶囊治疗乳腺癌的效果观察 [J]. 现代实用医学, 2020, 32(5): 492-493.
[35] 李红君, 陈光华, 李文东, 等. 平消胶囊联合卡培他滨治疗晚期乳腺癌的临床研究 [J]. 现代药物与临床, 2019, 34(7): 2151-2155.
[36] 李豫江, 李志刚, 吴涛. 乳腺癌术前行平消胶囊联合化疗疗效观察 [J]. 现代肿瘤医学, 2005, 13(2): 260-262.
[37] 杨沁惠. 平消胶囊治疗乳腺癌临床疗效研究 [J]. 甘肃科技, 2017, 33(1): 93-94.
[38] 张清媛, 赵文辉, 来玉娟, 等. 平消胶囊联合内分泌药物治疗或化疗对晚期乳腺癌的影响 [J]. 中国中西医结合杂志, 2005, 25(12): 1074-1076.
[39] 陈前军, 赖熙雯, 司徒红林, 等. 乳腺癌术前行槐耳颗粒联合化疗临床疗效 [J]. 中国肿瘤, 2004, 13(5):330-331.
[40] 陈莹, 刘津珠. 槐耳颗粒联合AP方案治疗乳腺癌的临床研究 [J]. 现代药物与临床, 2020, 35(1): 52-55.
[41] 代佑果, 寸英丽. 槐耳颗粒联合化疗对乳腺癌患者细胞免疫功能的影响 [J]. 现代肿瘤医学, 2007, 15(10): 1438-1439.
[42] 梁月琴, 尹文洁, 钱文, 等. 槐耳颗粒联合全身化疗对晚期乳腺癌患者免疫功能及预后的影响 [J]. 中国普外基础与临床杂志, 2015, 22(12): 1482-1486.
[43] 鲁明骞, 孔庆志, 卢宏达, 等. 槐耳颗粒联合化疗对乳腺癌患者术后机体免疫功能的影响 [J]. 辽宁中医杂志, 2017, 44(5): 966-969.
[44] 陆烨. 槐耳颗粒联合化疗治疗乳腺癌正虚血瘀证的临床研究 [D]. 南京: 南京中医药大学, 2006.
[45] 屈淑贤, 韩涛, 刘永明, 等. 槐耳颗粒对老年乳腺癌TC方案辅助化疗安全性及免疫功能的影响 [J]. 中国中医药现代远程教育, 2020, 18(3): 73-76.
[46] 王伟, 史立波, 张曼丽, 等. 乳腺癌术后化疗联合槐耳颗粒的疗效及对部分标志因子的影响 [J]. 西部医学, 2019, 31(1): 113-117.
[47] 杨震. 槐耳颗粒联合化疗对乳腺癌术后患者的临床疗效观察 [J]. 中国现代药物应用, 2017, 11(5): 93-95.
[48] 张朦, 张翠英, 陈速研. 槐耳颗粒联合化疗对晚期三阴性乳腺癌的抑制及肿瘤血管生成的影响 [J]. 内蒙古医学杂志, 2020, 52(10): 1169-1171.
[49] 赵子伟, 姚永强. 吡咯替尼联合槐耳颗粒治疗人表皮生长因子受体2阳性晚期乳腺癌患者化疗耐药效果观察 [J]. 临床军医杂志, 2020, 48(3): 284-286.
[50] 焦东晓, 孟玉新, 乔敏, 等. 人参皂甙Rg3联合新辅助化疗对晚期乳腺癌患者的疗效及VEGF水平的影响 [J]. 实用临床医学, 2017, 18(9): 27-29.
[51] 寇小格, 梁东良, 李小瑞. 参一胶囊联合卡培他滨治疗晚期乳腺癌临床观察 [J]. 肿瘤防治研究, 2011, 38(3): 319-321.
[52] 许鸿雁, 庄庆媛. 人参皂甙Rg3与化疗联合治疗晚期乳腺癌的临床观察 [J]. 中国热带医学, 2012, 12(3): 357-359.
[53] 张绪良, 王旭东, 唐东昕. 参一胶囊联合多西紫杉醇+顺铂治疗晚期乳腺癌患者的临床疗效观察及对患者生活质量的影响 [J]. 中国生化药物杂志, 2015, 35(11): 97-99.
[54] 赵华锋, 许菊萍, 冯凯祥, 等. 参一胶囊联合卡培他滨治疗复发转移耐多药乳腺癌效果分析 [J]. 临床医学, 2017, 37(12): 117-118.
[55] 赵曙, 马文杰, 李洪滨, 等. 参一胶囊联合化疗在乳腺癌术后辅助治疗中的作用 [J]. 第四军医大学学报, 2009, 30(22): 2536.
[56] 周航, 曾继泽, 石磊. 参一胶囊在乳腺癌术后辅助化疗中的临床疗效观察 [J]. 遵义医学院学报, 2006, 29(4): 364-365.
[57] 孔秋梅, 张文芳. 复方斑蝥胶囊联合化疗对三阴性乳腺癌患者肿瘤标志物、免疫指标、生命质量的影响及疗效评价 [J]. 河北医药, 2017, 39(14): 2128-2131.
[58] 李莉, 纳智明, 王建军. 复方斑蝥胶囊联合新辅助化疗对HER2阴性乳腺癌的疗效及其对Ki67、ER和PR表达的影响 [J]. 中国生化药物杂志, 2015, 35(11): 103-106.
[59] 刘海舟, 卢海跃, 张卫峰. 复方斑蝥胶囊对乳腺癌术后化疗患者免疫功能的影响 [J]. 中华中医药学刊, 2016, 34(1): 125-128.
[60] 徐洁, 郭卿. 复方斑蝥胶囊联合内分泌治疗、化疗对晚期乳腺癌的影响 [J]. 黑龙江医药, 2014, 27(5): 1049-1051.
[61] 张军华, 李中, 张刚, 等. 复方斑蝥胶囊配合乳腺癌新辅助化疗的临床观察 [J]. 中国肿瘤临床与康复, 2012, 19(2): 147-149.
[62] 陈浩. 华蟾素胶囊联合NX化疗方案对晚期乳腺癌患者血清肿瘤标志物及中位生存期的影响 [J]. 河北医学, 2019, 25(3): 533-537.
[63] 邓爽, 冯国斌, 徐久东. 华蟾素胶囊联合含卡培他滨基础方案治疗晚期乳腺癌疗效及耐受性观察 [J]. 药学与临床研究, 2017, 25(5): 439-443.
[64] 郭宁, 李彩霞, 朱德淼, 等. 华蟾素胶囊联合吡柔比星治疗晚期乳腺癌的临床研究 [J]. 现代药物与临床, 2019, 34(1): 200-204.
[65] 何林莉, 周波. 华蟾素胶囊联合全身化疗治疗中晚期乳腺癌的疗效及安全性 [J]. 中国医院用药评价与分析, 2018, 18(3): 334-336.
[66] 柯红, 崔洁, 金锦莲, 等. 华蟾素胶囊联合CAF方案治疗中晚期乳腺癌的临床效果分析 [J]. 世界中医药, 2017, 12(10): 2358-2361.
[67] 李玲. 华蟾素胶囊联合含卡培他滨基础方案治疗晚期乳腺癌疗效及对相关血清指标的影响 [J]. 当代医学, 2020, 26(1): 91-93.
[68] 田柳. 华蟾素胶囊辅助治疗晚期乳腺癌疗效及耐受性观察 [J]. 西南国防医药, 2017, 27(11): 1173-1175.
[69] 白俊文, 吴万敏. 金龙胶囊在乳腺癌新辅助化疗中的疗效分析 [J]. 中国肿瘤临床, 2014, 41(4): 246-249.
[70] 山院飞, 康鸿斌, 张瑞明, 等. 金龙胶囊对乳腺癌术后化疗患者免疫功能的影响 [J]. 肿瘤防治研究, 2014, 41(5): 456-459.
[71] 张绪良, 周俊伟, 毛哲玉, 等. 金龙胶囊联合TEC方案在乳腺癌新辅助化疗中的疗效及安全性观察 [J]. 现代中西医结合杂志, 2016, 25(12): 1299-1301.
[72] 侯文宇, 刘紫朦, 杨华夏. 小金片联合TEC方案化疗对晚期乳腺癌患者免疫功能及临床疗效的影响 [J]. 山东医药, 2018, 58(10): 89-91.
[73] 王逊, 孙桂芝. 小金片联合化疗对乳腺癌根治术患者外周血细胞免疫功能、VEGF水平及生活质量的影响 [J]. 山东医药, 2019, 59(32): 76-78.
[74] 张超, 冯秀芳, 王秀云, 等. 小金丸联合多西他赛、表柔比星、环磷酰胺治疗Ⅲ期乳腺癌的疗效及对患者免疫功能的影响 [J]. 中国药房, 2016, 27(15): 2059-2061.
[75] 徐宁, 王皓. 养正消积胶囊联合化疗对转移性乳腺癌的疗效及T淋巴细胞亚群水平的影响 [J]. 贵州医科大学学报, 2018, 43(3): 345-348.
[76] 徐志宏, 刘荣凤, 王晓翔, 等. 养正消积胶囊联合化疗治疗转移性乳腺癌的临床疗效及安全性 [J]. 山东大学学报: 医学版, 2016, 54(5): 79-83.
[77] 李勇. 贞芪扶正颗粒防治乳腺癌化疗不良反应的临床观察 [J]. 中国厂矿医学, 2008, 21(2): 225.
[78] 杨耀芳. 对执行中成药临床应用指导原则重要性的探讨 [J]. 中国临床药理学杂志, 2012, 28(8): 618-620.
[79] 郎万吉, 钱建琼, 郎枫. 三阴乳腺癌巩固期治疗的门诊中成药应用分析 [J]. 亚太传统医药, 2018, 14(5): 103-104.
[80] 王鹏波, 代云云, 董涵, 等. 中医药干预乳腺癌治疗的研究进展 [J]. 中国实验方剂学杂志, 2021, 27(7): 235-243.
[81] 周慧灵, 郑佳彬, 马雪娇, 等. 林洪生固本清源理论指导下的恶性肿瘤“五治”治疗经验 [J]. 中华中医药杂志, 2020, 35(1): 195-198.
[82] 邓茜, 杨柱, 龙奉玺, 等. 基于疡科理论与肿瘤关系探析刘尚义教授“引疡入瘤”学术思想 [J]. 南京中医药大学学报, 2018, 34(3): 236-238.
A network Meta-analysis of 10 kinds of oral Chinese patent medicine combined with chemotherapy in treatment of breast cancer
LAI Bao-yong1, LYU Ling-yan1, ZHAO Jing1, CHU Ai-jing1, WANG Chun-hui2, PEI Xiao-hua1, 3
1. The Third Affiliated Hospital of Beijing University of Chinese Medicine, Beijing 100029, China 2. The Fangshan Hospital of Beijing University of Chinese Medicine, Beijing 102400, China 3. The Xiamen Hospital of Beijing University of Chinese Medicine, Xiamen 361001, China
To compare the efficacy and safety of 10 kinds of oral Chinese patent medicine combined with chemotherapy in the treatment of breast cancer, a network Meta-analysis was performed.CNKI, Wanfang, VIP, SinoMed, PubMed, Embase, Web of Science and Cochrane Library database were searched from inception to January 1, 2021. The inclusion criteria were the randomized controlled trials (RCTs) of Chinese patent medicine plus chemotherapy for breast cancer. Literature screening, data extraction, the quality assessment was independently conducted by two authors. RevMan5.3, Stata14.0 and Gemtc14.3 were used for data analysis.A total of 61 RCTs were eventually included, involving 10 oral Chinese patent medicines. The results of network Meta-analysis showed that, combined with chemotherapy, in terms of improving ORR (I—III stage), the order of efficacy was Shenyi Capsule (参一胶囊) > Jinlong Capsule (金龙胶囊) > Xihuang Pill/Capsule (西黄丸/胶囊) > Pingxiao Capsule (平消胶囊) > Compound Cantharis Capsule (复方斑蝥胶囊) > Cinobufagin Capsule (华蟾素胶囊) > Huaier Granule (槐耳颗粒) > Xiaojin Tablet/ Pill (小金片/丸); In terms of improving DCR (I—III stage), the order of efficacy was Jinlong Capsule > Xihuang Pill/Capsule > Cinobufagin Capsule > Pingxiao Capsule > Compound Cantharis Capsule > Huaier Granule > Xiaojin Tablet/Pill; In terms of improving ORR (III—IV stage), the order of efficacy was Huaier Granule > Xihuang Pill/Capsule > Shenyi Capsule > Cinobufagin Capsule > Pingxiao Capsule > Xiaojin Tablet/Pill; In terms of improving DCR (III—IV stage), the order of efficacy was Pingxiao Capsule > Shenyi Capsule > Xihuang Pill/Capsule > Cinobufagin Capsule > Huaier Granule > Xiaojin Tablet/Pill; In terms of improving QOL, the order of efficacy was Xihuang Pill/Capsule > Huaier Granule > Shenyi Capsule > Cinobufagin Capsule > Jinlong Capsule > Compound Cantharis Capsule; Xihuang Pill/Capsule was beneficial in improving PFS and OS of breast cancer patients, Pingxiao Capsule was beneficial in improving OS of breast cancer patients; In terms of reducing the incidence rate of leukocyte decline, the order of efficacy was Shenyi Capsule > Huaier Granule > Cinobufagin Capsule > Xihuang Pill/Capsule > Zhenqifuzheng Granule (贞芪扶正颗粒) > Pingxiao Capsule > Compound Cantharis Capsule > Xiaojin Tablet/Pill; In terms of alleviating the incidence of gastrointestinal reactions, the order of efficacy was Zhenqifuzheng Granule > Xihuang Pill/Capsule > Huaier Granule and Shenyi Capsule > Pingxiao Capsule > Cinobufagin Capsule > Xiaojin Tablet/Pill > Compound Cantharis Capsule.Shenyi Capsule increased ORR more significantly than other Chinese patent medicines and Jinlong Capsule increased DCR more significantly than other Chinese patent medicines for I—III stage breast cancer. Huaier Granule increased ORR more significantly than other Chinese patent medicines and, Pingxiao Capsule and Shenyi Capsule increased DCR more significantly than other Chinese patent medicines for III—IV stage breast cancer patients. Xihuang Pill/Capsule can improve the QOL of patients with breast cancer more significantly than other Chinese patent medicines and. Shenyi Capsule can alleviate the incidence of leukocyte decline. Zhenqi Fuzheng Granule can alleviate the incidence of gastrointestinal reactions.
Chinese patent medicine; traditional Chinese medicine; breast cancer; network Meta-analysis; randomized controlled trial; Shenyi Capsule; Jinlong Capsule; Xihuang Pill/Capsule; Pingxiao Capsule; Compound Cantharis Capsule; Cinobufagin Capsule; Huaier Granule; Xiaojin Tablet/Pill; Zhenqifuzheng Granule; Yangzheng Xiaoji
R285.64
A
0253 - 2670(2021)21 - 6609 - 16
10.7501/j.issn.0253-2670.2021.21.019
2021-05-13
国家自然科学基金面上项目(817743191001982)
来保勇,博士研究生在读,研究方向为中医药防治乳腺疾病。Tel: (010)52075224 E-mail: by_lai@126.com
裴晓华,教授,博士生导师,研究方向为中医药防治乳腺疾病。Tel: (010)52075224 E-mail: pxh_127@163.com
[责任编辑 潘明佳]

