前列腺特异性膜抗原靶向近红外荧光手术导航技术在前列腺癌中的应用进展
冯科森,焦健华,,张景良,秦卫军
(1.中国人民解放军61035部队卫生队,北京昌平 102205;2.空军军医大学西京医院泌尿外科,陕西西安 710032)
前列腺癌是男性最常见恶性肿瘤之一,近年来其发病率在全球及国内均迅速上升[1-2]。目前,手术是治疗前列腺癌最有效的方法之一,而根治性前列腺癌切除术和盆部淋巴结清扫术是最常用术式[3]。根治性前列腺癌切除术中,术者确定切缘范围主要依靠术前影像学检查、术中肉眼所见及探查、术者自身经验和术中冰冻病理检查。手术切除范围过大会损伤正常组织,影响尿控等正常功能;而切除范围过小会导致阳性切缘,患者容易出现复发。在盆部淋巴结清扫术中,术者也很难在手术中实时分辨淋巴结是否已出现转移。目前,欧洲泌尿外科学会(European Association of Urology,EAU)和美国国立综合癌症网络(National Comprehensive Cancer Network,NCCN)指南均推荐对高风险患者进行扩大盆部淋巴结清扫术[3]。但淋巴结清扫范围越大,导致相关并发症发生的可能性也越高[4]。因此,如何在手术中尽可能保留正常组织和功能,同时对前列腺癌侵犯区域进行彻底切除是临床医生经常需要面对和解决的问题。靶向荧光术中导航技术正是解决这一问题的良方,本文就前列腺癌中前列腺特异性膜抗原(prostate membrane specific antigen,PSMA)靶向近红外荧光(near-infrared fluorescence,NIRF)手术导航技术的研究进展进行综述。
1 靶向NIRF手术导航技术的基本概念
1.1 光学分子影像学光学分子影像学源自1999年WEISSLEDER教授最早提出的分子影像学(mo-lecular imaging)技术[5],是利用生物体自发荧光对分子和分子作用途径检测的一种无创技术,成像依靠不同波长荧光[6]。该技术常用波长为400~1 000 nm,包括可见光波段(波长:400~650 nm)和NIRF波段(波长>650 nm)[6]。与可见光波段相比,NIRF具有波长较长、组织穿透力较强、散射较小等优点,更适合进行体内成像。
1.2 靶向光学分子影像手术导航靶向光学分子影像手术导航是一种基于光学分子影像学技术,对肿瘤进行细胞及分子层面靶向实时在体成像的技术[7]。在静脉注射肿瘤靶向NIRF染料后,肿瘤靶向荧光染料通过配体-受体结合作用实现体内自动寻靶。施术者利用高敏感度的荧光采集设备及快速图像融合计算,实现术中实时荧光成像以精准切除肿瘤组织及淋巴结转移[7]。
1.3 靶向NIRF染料靶向NIRF染料通过将NIRF染料与靶向恶性肿瘤特异性标志物的配体,如抗体、多肽、小分子化合物相结合从而实现荧光染料在手术中对恶性肿瘤的靶向成像。传统非靶向NIRF染料如吲哚菁绿(indocyanine green,ICG)等主要依靠实体恶性肿瘤的高通透性和滞留效应(enhanced permeability and retention,EPR)进行成像,不连接肿瘤靶向特异性配体,不具有针对恶性肿瘤特异靶向性,因而难以在手术中准确分辨前列腺癌和正常组织。与这些传统NIRF染料相比,靶向NIRF染料可通过配体-受体特异性结合作用,精准识别恶性肿瘤,因此具有靶向性更好、特异性更高、与恶性肿瘤结合时间更长等优点。靶向NIRF染料的使用与否也是靶向NIRF手术导航技术与非靶向NIRF手术导航技术的区别所在。
1.4 PSMAPSMA是一种具有叶酸水解酶和N-乙酰化α-键酸性二肽酶(N-acetylated a-linked acidic dipeptidase,NAALADase)活性的Ⅱ型跨膜糖蛋白,在前列腺癌细胞中显著高表达且其表达量为生理表达量的100倍以上[8]。有研究表明,PSMA可在绝大多数原发性前列腺癌和98%前列腺癌淋巴结转移中高表达[9],并且其表达量随Gleason分期升高而增加[10]。因此,PSMA作为一种前列腺癌特异性高表达膜蛋白,便于和靶向染料结合,是靶向NIRF染料的理想靶点。
2 常用设备
靶向NIRF手术导航技术所使用的设备一般是具有近红外波段荧光成像功能的荧光手术设备。国外研究中常用的设备包括Artemis、FDPM imager、FLARE、Fluobeam、HyperEye、荧光腹腔镜Karl Strorz/PINPOINT、Kit-FLARE、Mini-FLARE、Photodynamic Eye(PDE)、Munich/SurgOptix原型摄像系统、Goggle系统、加装NIRF成像模块的达芬奇手术机器人等设备[11-12]。目前国内报道的临床研究中所使用的设备有:杨晓峰等[13]在前列腺癌根治性切除术和扩大盆腔淋巴结清扫中使用的荧光腹腔镜系统。以上具有近红外波段成像功能的设备均可进行靶向NIRF手术导航,因此靶向NIRF染料的研发也就成为该研究领域的热点。与传统的非靶向NIRF成像相比,PSMA靶向NIRF染料是PSMA靶向NIRF手术的关键技术,能够极大提高前列腺癌病灶的信噪比,为减少阳性切缘和精准清除转移淋巴结提供重要保证。下面我们进一步对PSMA靶向NIRF染料研究进展进行综述。
3 靶向荧光染料
根据靶向PSMA的配体种类不同,可以将PSMA靶向NIRF染料分为抗体靶向染料、小分子靶向染料、可激活靶向染料和双模靶向染料(图1)。
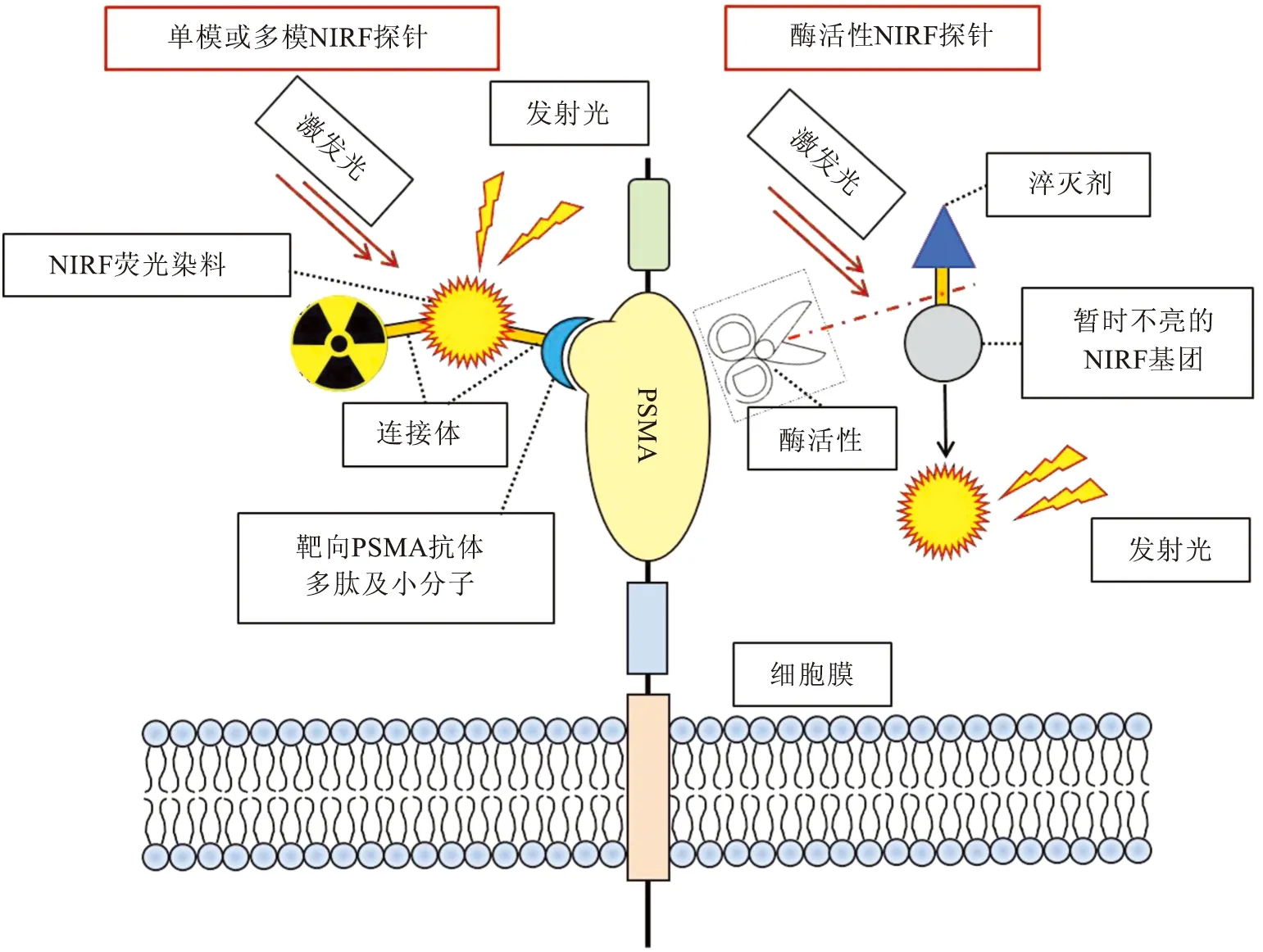
图1 PSMA靶向NIRF染料结构示意图
3.1 抗体PSMA靶向NIRF染料抗体PSMA靶向NIRF染料是指将全抗体或抗体片段偶联NIRF染料构成的PSMA靶向NIRF染料。J591是1种PSMA靶向人源化单克隆抗体,其以良好的特异性最早应用于PSMA抗体靶向染料的合成。2011年,NAKAJIMA等[15]首先将J591抗体连接吲哚菁绿(indocyanine green,ICG),构建首个PSMA抗体靶向NIRF染料。但在该染料中,ICG连接于J591抗体后便发生荧光淬灭,只有在与PSMA阳性前列腺癌细胞结合并内化后才能再次发出荧光[15]。这种连接配体后易发生荧光淬灭的缺点限制了ICG在合成靶向荧光染料中的应用,但这一缺点在商业化NIRF染料IRDye800CW中得以克服。2016年,约翰斯·霍普金斯大学医学院团队MUKHERJEE等[16]首次将J591抗体连接NIRF染料IRDye800CW构建J591-IRDye800CW(又名ProstaFluor),并且在PSMA+LMD前列腺癌细胞荷瘤裸鼠模型中证明该染料对PSMA+前列腺癌在注射后24~120 h具有良好的成像效果,且目前ProstaFluor已进入临床试验。同时,NAGAYA等[17]通过将PSMA单抗连接IR-700DX构建Anti-PSMA-IR700同时实现了NIRF成像和光热治疗的效果。
随着近年来抗体技术发展,单链抗体等新抗体的研发也进一步推进了抗体PSMA靶向NIRF染料的发展。2016年,MAZZOCCO等[18]将PSMA单链抗体ScFvD2B连接于近红外染料X770构建PSMA靶向NIRF染料X770-ScFvD2B,并顺利用该染料对PSMA阳性前列腺癌细胞(LNCaP细胞)荷瘤鼠在静脉注射后24~ 240 h进行体内成像。在另一项研究中,本课题组HAN等[19]从大型酵母展示单链抗体库中筛选出一株人源PSMA单链抗体gy1并连接近红外染料IRDye800CW构建首个人源PSMA单链抗体NIRF染料,并使用该靶向染料顺利对PSMA+PC3前列腺癌细胞荷瘤鼠进行体内成像且取得较好效果。在此工作基础上,研究人员进一步将单链抗体gy1构建为PSMA人源性全抗体PSMAb,将其连接至IRDye800CW上构建出PSMAb-IRDye800CW,它是首个靶向PSMA人源全抗体NIRF染料,同时该研究顺利对PSMA+PC3前列腺癌细胞荷瘤鼠进行了体内成像[20]。
目前,抗体偶联的NIRF探针在前列腺癌术中显像具有独特优势,一方面是由于抗体代谢相对较慢,可在3~7 d达到术中成像的最佳信噪比,为手术提供了较为充裕的时间;另一方面是由于抗体分子量相对较大,主要经肝脏代谢而非肾脏代谢,其荧光在尿液中含量较少,避免了术中尿液渗漏导致的手术视野荧光污染。与PSMA靶向小分子配体相比,PSMA靶向抗体临床试验的进度相对较慢,在临床试验方面仍需努力。
3.2 小分子PSMA靶向NIRF染料小分子PSMA靶向NIRF染料是通过化学合成PSMA小分子化合物配体或抑制剂后偶联NIRF染料构成的靶向染料。2005年,HUMBLET等[21]通过合成一种PSMA靶向小分子化合物GPI,并且连接四磺化七甲川吲哚菁绿类染料IRDye78构建首个小分子PSMA靶向近红外染料GPI-78并顺利将其用于PSMA+LNCaP前列腺癌细胞荷瘤鼠的体内成像。
Cy5.5和IRDye800CW等商业化NIRF染料的出现及使用促进了PSMA小分子靶向染料迅速发展。一项研究将PSMA小分子抑制剂CTT-54.2与NIRF染料Cy5.5连接构建成Cy5.5-CTT-54.2,其在体外实验中显示出对PSMA+前列腺癌细胞较强靶向性[22]。另一项研究通过合成一种PSMA靶向小分子抑制剂YC-27 3与IRDye800CW连接构建小分子PSMA靶向NIRF染料并且成功用于PSMA+前列腺癌PC3pip细胞荷瘤鼠模型体内成像[23]。此外,一项研究通过合成一种靶向PSMA小分子化合物PSMA-1,并将其分别与IRDye800CW和Cy5.5相连接,构建2种PSMA靶向近红外染料,PSMA-1-IRDye800CW和PSMA-1-Cy5.5[24]。2种PSMA靶向荧光染料均在注射4 h后在对PSMA+PC3pip前列腺癌细胞荷瘤鼠进行活体成像中达到较好的成像效果[24]。另一项研究通过化学合成PSMA小分子抑制剂SCE(一种尿素化合物)并连接IRDye800CW构建PSMA靶向近红外染料SCE-IRDye800CW,并用该染料顺利对PSMA+LNCaP细胞荷瘤鼠进行体内成像[25]。
除IRDye800CW和Cy5.5外,一些新的NIRF染料也进入临床前期研究。一项研究通过合成PSMA小分子抑制剂赖氨酸尿素谷氨酸盐(Lysine-urea-glutamate,KUE)连接一种含锌NIRF染料ZW800-1(zwitterionic fluorophores)并用KUE-ZW800-1成功对PSMA+前列腺癌LNCaP细胞荷瘤鼠进行体内成像[26]。同时,目前将PSMA靶向小分子配体KUE连接Cy5.5、Cy7、Cy7.5等陆续进入临床前研究阶段[26-27]。另一项研究设计PSMA靶向近红外染料OTL78,该染料包括一个PSMA小分子配体DUPA和一种NIRF染料S0456,应用于PSMA+前列腺癌22Rv1和LNCaP细胞荷瘤鼠的体内成像并获得信噪比5∶1的良好效果[28]。此外,还有研究将BODIPY荧光染料与PSMA小分子配体连接,构建PSMA靶向NIRF染料[29]。
近年来,小分子PSMA靶向NIRF染料的快速发展得益于以PSMA小分子配体为基础的PSMA正电子发射型计算机断层显像(positron emission computed tomography,PET)在临床中的快速应用和发展。但小分子配体分子量较小,主要经肾脏代谢,术中尿液渗漏可能导致的术野荧光污染问题有待进一步地研究。
3.3 可激活NIRF染料靶向染料具有“开关”效应,即平时保持关闭状态不发出荧光,只有在与靶分子结合时才发出荧光。该染料利用靶分子酶活性,可在降低背景荧光的同时增加与靶分子结合荧光信号,以显著提高信噪比[12]。由于PSMA具有叶酸水解酶和谷氨酸羧肽酶活性,因此可被设计为可激活NIRF染料的靶点。KAWATANI等[30]利用PSMA谷氨酸羧肽酶活性设计首个可激活PSMA靶向NIRF染料5GluAF-2MeTG。在5GluAF-2MeTG中,2MeTG是一种可以被PSMA的谷氨酸羧肽酶活性催化水解的底物,5GluAF是一种近红外染料。当二者结合时2MeTG可通过最低未被占据分子轨道使5GluAF发生荧光淬灭,从而实现“关闭”荧光;在与PSMA结合后,PSMA谷氨酸羧肽酶活性将2MeTG解离,5GluAF重新发出强荧光从而实现“打开”荧光,以实现对PSMA+前列腺癌的成像。同时,另一项研究将前列腺癌PSMA靶向和肿瘤位置相对缺氧结合,合成了PSMA靶向与缺氧协同的多功能探针,用于前列腺癌的精准成像[31]。
3.4 多模态染料多模态染料是指将NIRF染料、核素等同时连接同一个配体从而实现同一靶向染料在多种成像方式下均可成像。由于每种成像方式都具有其自身独特优势和缺陷,因此同时组合多种成像方式有望结合多种成像方式的优势,克服单一成像方式的缺陷。
有研究构建了可同时进行单光子发射计算机断层成像术(SPECT/CT)和NIRF成像的PSMA靶向双模态染料。一项研究通过合成一种PSMA靶向的新的化合物“1”并将其分别连接111In和IRDye800CW,构建了首个PSMA靶向的双模态染料并成功用于PSMA+LNCaP前列腺癌细胞荷瘤鼠模型的SPECT/CT和NIRF成像[32]。另一项研究将PSMA胞外段结合的抗体D2B与111In和IRDye800CW连接构建了PSMA靶向双模染料111In-DTPA-D2B-IRDye800CW,并将该染料成功用于PSMA+LNCaP前列腺癌细胞皮下荷瘤鼠模型和PSMA+LS174T前列腺癌细胞腹腔荷瘤鼠模型的SPECT/CT和NIRF成像[33]。在静脉注射111In-DTPA-D2B-IRDye800CW后48~168 h,NIRF成像可取得较高信噪比及较好成像效果[33]。同时,该课题组进一步尝试IRDye700DX构建111In-DTPA-D2B-IRDye700DX用于PSMA靶向成像和光热治疗[34]。
一些研究构建可同时进行PET和NIRF成像的PSMA靶向双模态染料。在已应用于前列腺癌患者诊断检查的68Ga-PSMA-11 PET的基础上,该研究分别将FITC、AlexaFluor488、DyLight800和IRDye800CW 4种荧光染料连接68Ga-PSMA-11,首次构建了4种可同时进行术前68Ga-PSMA PET和术中荧光手术导航的PSMA靶向双模态染料[35]。其中68Ga-PSMA-11-DyLight800和68Ga-PSMA-11-IRDye800CW 2种染料所使用荧光波段均为NIRF,更适合体内成像,且68Ga-PSMA-11-IRDye800CW在接种PSMA阳性LNCaP前列腺癌细胞荷瘤裸鼠中的信噪比更高,荧光成像效果更好[35]。因此该研究在大型动物实验中,将68Ga-PSMA-11-IRDye800CW 按照30 μg/kg注射给2只2~3月龄小猪,并在1 h后对它们顺利使用达芬奇手术机器人进行NIRF引导下前列腺切除术,进一步验证68Ga-PSMA-11-IRDye800CW应用于临床的可行性[35]。鉴于68Ga-PSMA-11 PET/CT已在临床中应用及IRDye800CW在临床试验中的广泛应用,68Ga-PSMA-11-IRDye800CW有望快速向临床应用进行转化。
3.5 纳米染料目前,随着纳米材料的快速发展,多个纳米材料相关的PSMA靶向染料正在进行临床前研究。一方面,有研究使用纳米材料包裹ICG后在材料表面修饰PSMA靶向短肽从而实现ICG的PSMA靶向前列腺癌成像[36];另一方面,有研究以聚乳酸-聚乙二醇纳米颗粒为载体,通过表面修饰PSMA靶向肽,从而构建111In和IRDye800CW标记的双模探针[37]。另外,研究人员还尝试使用量子点荧光染料进行PSMA靶向成像,将J591抗体连接量子点近红外染料Quantum dot 800并用该染料顺利对PSMA+前列腺癌C4-2细胞荷瘤鼠进行体内成像[38]。但目前纳米材料的潜在体内毒性等问题导致目前尚无PSMA靶向NIRF纳米染料进入临床试验。
4 临床试验
目前已申请进入临床试验的PSMA靶向荧光染料有2项,均为PSMA抗体NIRF染料。一项为ProstaFluor,即HuJ591-IRDye800CW,由Spectros公司申请开展一期、二期临床试验(NCT01173146)。另一项为美国希望之城医疗中心申请的PSMA单克隆抗体MDX1201连接荧光染料A488用于ⅡB/Ⅲ/Ⅳ期前列腺癌患者的荧光引导下腹腔镜前列腺癌根治术的临床试验(NCT02048150)。
5 挑战与展望
近年来,PSMA靶向NIRF手术导航技术发展迅速,正处在由临床前科研阶段向临床应用转化的关键阶段。随着更多PSMA靶向染料研发和更多大规模临床试验开展,今后在手术中实时精准辨别前列腺癌与正常组织、转移淋巴结和正常淋巴结将不再困难。可激活及多模态PSMA靶向近红外染料有望进一步降低染料信噪比并不断丰富靶向染料的功能。目前,近红外Ⅱ区染料也在迅速发展,有望为荧光手术注入新的动力。我们相信随着人们对靶向NIRF染料的不断研究,前列腺癌PSMA靶向荧光手术导航技术将取得新的突破。