遗传性血管神经性喉水肿1例
李燕萍,胡瑞利
(河北北方学院附属第一医院 耳鼻咽喉头颈外科,河北 张家口 075000)
遗传性血管神经性喉水肿(hereditary angioneurotic laryngeal edema,HALE)是遗传性血管性水肿的喉部表现,为一家族遗传性补体缺陷病,临床较为罕见,易误诊。我院近期收治HALE 1例,对其家系进行调查发现家族中有 3例同病患者,现报道如下。
1 临床资料
患者,女,71岁,因“咽痛、呼吸困难伴颈部肿胀半天”于凌晨入院。患者半天前拔牙后出现咽痛症状,吞咽时加重,伴颈部及咽喉肿胀,肿胀感短期内迅速加重,很快出现口唇及颜面部肿胀,并渐出现发音含糊,伴呼吸困难,为求诊治,急来我院,急诊查体后以“喉水肿”收住院。发病后无咳嗽、咳痰、鼻塞、流涕等,一般情况差,饮食睡眠差。患者既往多次(10余岁发病,发作频率1年数次至数年1次不等)无明显诱因喉水肿、颜面部水肿、四肢水肿病史,每于输液治疗2~3 d后症状明显改善,具体用药不详;脑梗病史17年,高血压病史5年,均规律药物治疗;曾于北京完善变应原检查,未发现明显致敏物质;否认“肝炎”“结核”等传染病史,否认自身免疫性疾病。家族中患者姐姐及母亲有反复多次无诱因咽喉水肿、四肢水肿病史,家系中其他人未出现类似症状,见图1。查体:神清,端坐呼吸,呼吸频率25~30次/min,颜面、口唇、口底、颈部明显肿胀,咽部水肿明显,悬雍垂及双侧腭舌弓水肿,软腭游离缘水肿明显,间接喉镜下见:会厌舌面水肿、双侧杓区水肿明显,表面发亮,双侧声带、室带黏膜光滑。入院后查血常规WBC 19.02×109/L,中性粒细胞百分比88.5%,中性粒细胞绝对值16.84×109/L,补体C3 0.89 g/L,补体C4<0.073 g/L,考虑遗传性血管神经性喉水肿可能性大,给予心电监护、持续低流量吸氧、抗炎、激素、肾上腺素雾化吸入等对症治疗,向家属交代病情危重,备床旁气管切开包。治疗12 h后症状减轻(图2、3),1 d后患者咽痛及呼吸困难症状明显改善,建议继续治疗,患者拒绝治疗要求出院。出院后随访,患者北京查补体 C1抑制物0.05 g/L,确诊为HALE,予达那唑 0.2 g/次,3次/d,口服,2个月后复查补体C4水平恢复正常。
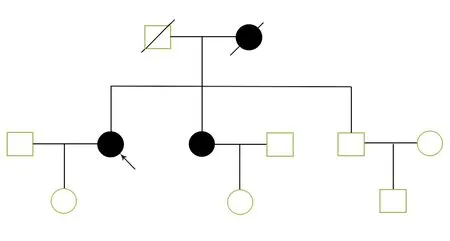
图1 遗传性血管神经性水肿患者家系图谱
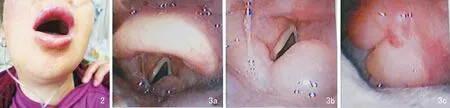
图2 治疗后12 h,患者口唇颜面及颈部肿胀较前明显减轻,但仍可以看到口唇肿胀发亮,口底及颈部肿胀 图3 治疗后12 h电子喉镜检查 3a:会厌舌面水肿; 3b:双侧杓区水肿; 3c:左侧悬雍垂、腭舌弓仍有明显水肿
2 讨论
HALE为常染色体显性遗传病,国外文献报道发病率约为1/50 000[1],国内多为个案报道,无大宗病例分析,缺乏流行病学数据。HALE病因为血清中C1-酯酶抑制剂(C1-inhibitor,C1-INH)含量低、功能不全或缺乏所致。C1-INH是一种血浆球蛋白,对纤维蛋白溶解、凝血、激肽、补体系统内的多种特异性蛋白裂解酶形成有重要的调节作用[2],如其含量低,可引起缓激肽等水平增多,血管扩张通透性增高,血浆外渗,最终引起局部水肿。临床上以反复发作,难以预测的皮肤和黏膜下水肿为特征,水肿的特点是发作性,自限性,水肿可累及身体任何部位,以四肢、颜面、呼吸道和胃肠道黏膜较为常见,其中最致命的是上呼吸道黏膜水肿,可因喉水肿迅速进展导致呼吸困难或窒息,与急性会厌炎、变态反应性水肿有相似的临床表现,然而糖皮质激素或抗组胺药均无效,如抢救不及时可窒息死亡,是HALE的主要死因之一[3-4]。典型的临床表现结合患者家族史、C1-INH及补体检查必要时进行相关基因检测,可以明确诊断[3]。该病可能的诱因有外伤、头颈部手术或操作、口腔操作、心理压力[5],本例患者本次发病即为拔牙后。该病一般数小时发病,72 h后逐渐消退。
治疗分为急性期治疗和缓解期预防治疗,对于急性发作,症状严重者国外选用C1-INH 浓缩制剂Berinert和重组人C1-INH Ruconet,或缓激肽受体拮抗剂Icatibant、血浆激肽释放酶抑制剂Ecallabtide[6],但这些药物我国目前尚缺乏,国内推荐静脉滴注新鲜冰冻血浆[7]处理紧急HALE症状。对于缓解期预防用药,国内主要是弱雄性激素达那唑和抗纤溶制剂,国外推荐C1酯酶抑制剂,美国FDA批准用于成人及青少年预防遗传性血管性水肿的药物有Haegarda和Cinryze,Cinryze是美国首个也是唯一一个用于年龄低至6岁儿童HALE患者预防血管性水肿发作的药物[8-10]。
遗传性血管神经性喉水肿为一种罕见疾病,具有潜在致死性,对于反复发作不明原因喉水肿患者临床医生应提前预判,警惕该病可能,尽早进行补体和C1-INH检测明确诊断,对于病情进展迅速,应随时做好气管切开准备,避免出现窒息死亡等严重并发症。

