术中冷冻消融和冷热复合消融治疗不可切除胰腺癌的临床研究
钱祝银,张 彬,陈奕秋,吴迎春,顾玉青,朱一超
1南京医科大学第二附属医院胰腺中心,江苏 南京 210003;2南京医科大学生理学系,江苏 南京 211166;3南京医科大学第二附属医院超声医学科,江苏 南京 210003
胰腺癌被称为“癌中之王”,是一种恶性程度很高的消化系统肿瘤[1-2]。胰腺癌发病隐匿,早期诊断困难,超过80%的胰腺癌患者初次诊断时已失去根治手术的机会。不可切除胰腺癌预后极差,中位生存时间仅3~6 个月[3]。目前,不可切除胰腺癌的传统治疗方法以全身化疗为主,患者往往难以耐受较强的化疗方案,且效果较差。因此,探索有效的不可切除胰腺癌综合治疗方法成为消化系统肿瘤防治领域的研究热点。
冷热复合消融(intraoperative combined cryoabla⁃tion and hyperthermia,ICCH)是本中心从2020 年起在原有单一冷冻消融(intraoperative cryoablation therapy,IOCT)基础上的改良升级,在国内外首次实现集深低温冷冻消融与高温热疗于一体的不可切除胰腺癌治疗的新方案。本技术创新性地在同一消融探针中实现了从-196 ℃至80 ℃的超宽温度范围,突破了以往单一冷冻治疗或高温热疗的局限,结合了两者优势。本研究对3 年来运用IOCT 和ICCH 治疗不可切除胰腺癌的临床实践经验进行总结,与同行分享。
1 对象和方法
1.1 对象
2018年6月—2021年3月在南京医科大学第二附属医院胰腺中心接受消融手术患者136 例,经快速冰冻切片及石蜡切片检查与影像诊断证实为胰腺癌。纳入标准:①影像学及病理结果证实的局部进展期胰腺癌;②术前影像学及术中超声探查明确的胰腺癌伴肝脏寡转移(转移灶≤3个);③患者和家属知情同意并签署知情同意书。排除标准:①胰腺癌伴肝脏或腹腔广泛转移,或远处转移;②胰腺囊性肿瘤伴恶变,或胰腺癌伴囊性变或坏死;③严重心肺、肝肾功能不全或其他基础疾病不能耐受全身麻醉及手术者。根据患者年龄、性别等因素进行倾向性评分匹配,将所有患者分为两组:IOCT组101例,年龄(62.68±8.67)岁,男56 例(55.4%),女45 例(44.6%);ICCH 组35 例,年龄(62.91±9.25)岁,男20 例(57.1%),女15 例(42.9%)。根据美国癌症联合委员会(AJCC)胰腺癌分期标准(8版),IOCT组病例中Ⅲ期60例,Ⅳ期41例;ICCH组Ⅲ期25例,Ⅳ期10例。两组患者肿瘤部位、肿瘤大小及术前合并症等比较,差异无统计学意义。本研究经南京医科大学第二附属医院医学伦理委员会批准(批准号:2018⁃KY⁃088)。
1.2 方法
两组均行开放手术,术中探查确认肿瘤无法手术切除后,再行肿瘤的超声检查。通过超声检查判断肿瘤大小及与周围脏器的毗邻关系[2],并在超声引导下行肿瘤穿刺活检。获取病理结果后,先进行IOCT 或ICCH 治疗,再解除肿瘤所致的胆道或肠道梗阻。
IOCT 组:术中超声引导下将直径为1.7 mm 的消融探针精准穿刺至瘤体的最远端,通过氩气制冷效应,15 s内将靶区组织冷冻至-150 ℃左右,冷冻时间8~15 min,同时用温盐水冲洗保护冰球周围器官,通过氦气的热效应,复温至30 ℃,视为1个周期;再重复一次上述治疗共2个周期,分段充分复温,拔出探针。
ICCH 组:术中超声引导下将直径为2.6 mm 的消融探针精准穿刺至瘤体的最远端,通过液氮制冷效应,将靶区组织冷冻至-196 ℃左右,冷冻时间6~10 min,通过酒精蒸气的热效应,复温至80 ℃,视为1个周期;再重复一次上述治疗共2个周期,分段充分复温8 min,超声监测冰球融化,拔出探针(图1、2)。
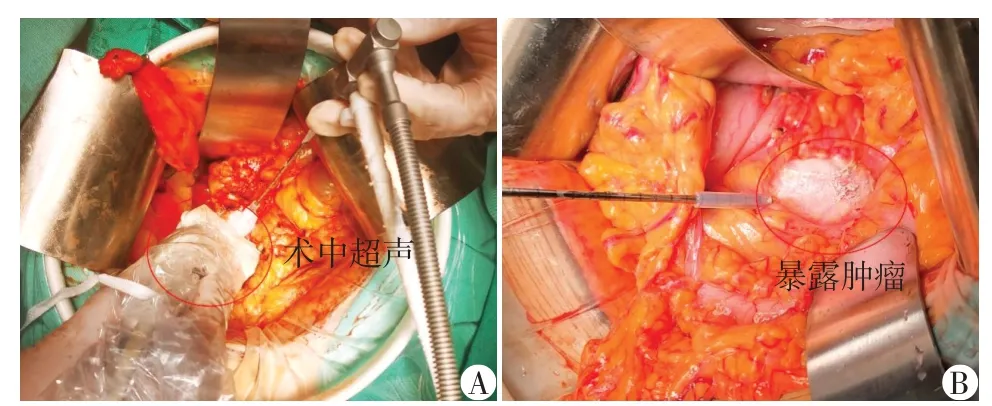
图1 开腹直视下不可切除胰腺癌ICCH技术Figure 1 Open abdomen of patients with unresectable pancreatic cancer in treatment of ICCH

图2 不可切除胰腺癌术中ICCH的温度曲线Figure 2 The temperature curve of ICCH for unresectable pancreatic cancer
两组手术过程中均全程通过超声监测冰球的形态、大小、是否完全覆盖肿瘤,以及冰球与周围器官的关系,实时调整,以免冻伤。术后胰瘘、胃排空延迟、术后出血等并发症的诊断和分级按国际胰腺外科小组(ISGPS)的定义[4-6]。手术前后分别进行相关指标如糖类抗原199(CA199)、总胆红素(TB)、白蛋白(ALB)、血糖检测,以及疼痛指数评分(VAS 评分)。所有患者术后均按常规方案化疗。体能状态评分(performance status,PS)0~1 分的患者采用AG方案(白蛋白紫杉醇+吉西他滨),PS 2 分的患者采用GS 方案(吉西他滨+氟尿嘧啶)或Gem 和S1 单药化疗,PS>2分的患者没有纳入本研究。
1.3 统计学方法
使用SPSS 22.0行统计学分析,正态分布的定量指标用均数±标准差()表示,组间比较采用方差分析;非正态分布的定量数据用中位数(四分位数)[M(Q25,Q75)]表示,组间比较采用Mann⁃WhitneyU检验;定性数据用例数和构成比表示,组间比较采用卡方检验或Fisher 精确概率法。使用GraphPad Prism 6 绘制生存曲线,纵坐标以百分比形式显示,组间比较采用Log⁃Rank(Mantel⁃Cox)检验。P<0.05为差异有统计学意义。
2 结果
2.1 手术资料
与IOCT 组相比,ICCH 组减少了术中出血量(P<0.05,表1),可大大提高胰腺癌消融的治疗效率,降低手术风险。IOCT组有12例(11.9%)患者术中输血;ICCH 组有2 例(5.7%)患者术中输血。ICCH 组的术后禁食时间较IOCT 组短,但术后住院时间略长于IOCT组(P<0.05,表1)。并发症方面,两组术后胰瘘发生率、胃排空延迟发生率差异无统计学意义,但ICCH 组未出现术后出血或肺部感染(P<0.05,表1)。
2.2 围术期疗效评价
手术前后分别进行血清肿瘤指标CA199、TB、ALB、血糖检测,VAS评分等用于对照研究。两组术后VAS 评分、CA199 较术前均下降明显,但组间差异较小,无统计学意义(P>0.05)。而在消融治疗后,ICCH组血糖低于IOCT组,差异具有统计学意义(P<0.05,表1)。
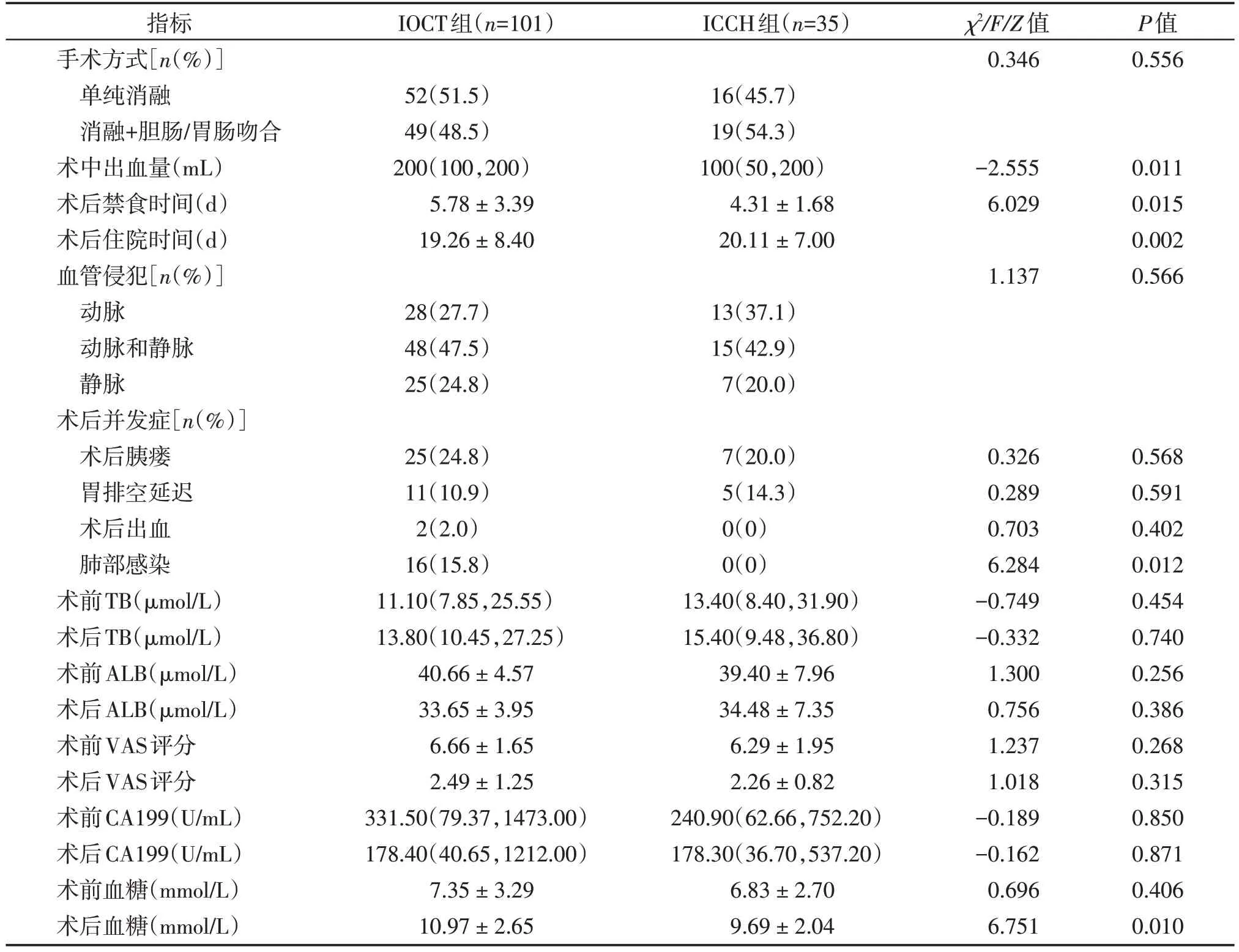
表1 两组不可切除胰腺癌患者手术相关指标分析Table 1 Operation indexes of patients with unresectable pancreatic cancer
2.3 胰头癌术后1年内的短期生存率评估
由于ICCH 技术开展时间较短,因此我们仅选取接受IOCT 或ICCH 术后1 年的胰头癌患者行生存期分析。两组病例分别为IOCT 组42 例,ICCH组11 例,2组患者肿瘤分期差异无统计学意义。比较两组胰头癌患者1年内生存率,ICCH组患者生存期>1 年6 例,>6 个月~1 年1 例,≤6 个月3 例,失访1 例;IOCT 组患者生存期>1 年6 例,>6 个月~1 年9 例,≤6 个月16 例,失访11 例。ICCH 组术后的生存率显著优于IOCT组(P=0.034,图3)。
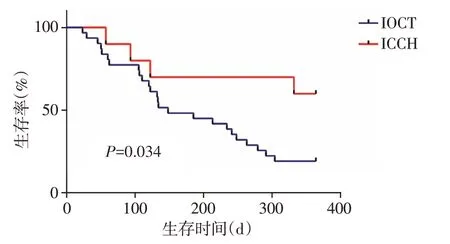
图3 胰头癌患者术后1年内的生存曲线Figure 3 The survival rate of patients with pancreatic head carcinoma within 1 year after surgery
3 讨论
胰腺癌仍然是最致命的恶性肿瘤之一,早期诊断困难,预后极差,5 年生存率仍仅为9%。手术切除是唯一可能治愈胰腺癌的治疗方法。但胰腺癌起病隐匿,确诊后只有不足20%的患者可以进行切除[7]。目前,不可切除胰腺癌的治疗以吉西他滨为基础的单药或联合化疗为主。研究证实FOLFIRI⁃NOX或纳米⁃紫杉醇与吉西他滨联合使用可提高生存率,但中位生存时间仍小于1 年[8]。尽管化疗方案和靶向疗法不断发展,但是胰腺癌仍对化学疗法表现出高度抵抗力。
近年来,高强度聚焦超声治疗、不可逆电穿孔[9]、冷冻消融[10-11]及射频消融等局部治疗在不可切除胰腺癌中逐步开展,表现出相对安全、高效、便捷的优势,在局部肿瘤控制和缓解疼痛方面疗效显著[12]。理想的联合治疗可在不增加并发症的前提下,改善患者的生活质量和提高存活率[13]。但目前尚无标准的联合治疗方案,需待临床上的进一步研究[14]。本课题组于2017 年1 月起开展不可切除胰腺癌的术中IOCT,取得了初步成果。术后肿瘤指标CA199和VAS 疼痛评分明显下降,肿瘤缩小,术后生存时间优于传统放化疗[10-11]。
单一热消融或冷消融都存在一定不足。单一热消融为防止高温扩散到周围健康组织,治疗中保留外围边缘“安全范围”,避免整个胰腺肿瘤消融,导致胰腺肿瘤清除不全,易复发,且常伴随十二指肠、主要血管损伤和胰瘘的并发症[15]。热疗常伴有肿瘤周围区域血液灌注的增加,导致热量流失而降低肿瘤边缘温度,减弱热疗效果。局部热疗引起的血流量增加也存在刺激胰腺肿瘤从原发部位转移的风险[16]。单纯冷冻消融的不足在于,肿瘤细胞细胞杀伤不彻底,胰腺肿瘤复发率较高。冷冻消融比射频消融或激光消融引起强烈的炎症和凝血反应,或导致更高的并发症发生率。并发症方面,本研究IOCT组发生术后出血2例,肺部感染16例;而ICCH组未发生以上并发症。冷冻消融有时可能引起全身性炎症反应综合征,即“冷休克”现象,威胁生命[15]。
ICCH是本中心在原有单一IOCT基础上的改良升级,在国内外首次实现集深低温冷冻消融与高温热疗于一体的不可切除胰腺癌治疗新方案[17]。在胰腺癌手术过程中,冷冻向加热的切换时,由于强烈快速的升温会在组织内产生剧烈的热应力及高温破坏作用,从而加强对胰腺癌的损毁。冷热复合消融可实现冷/热消融优势互补。热疗可加快冷冻后的复温,使肿瘤组织在短时间内经历温度剧烈变化,促使更多肿瘤细胞死亡;同时可缩短手术用时,降低手术风险。冷疗可预先减少血流灌注,使热疗过程中的热量散失降低,因而增强了热疗疗效。冷热复合消融术中的热疗作用局限于冰球范围内,只对靶区组织进行加热,结合超声实时监测,在冰球完全融化后停止,能有效避免热损伤的发生,确保热消融的安全性。冷疗与热疗均可灭活穿刺部位周围神经,冷热复合消融中效果叠加,可能更好地缓解疼痛。本研究中IOCT和ICCH两组的术前VAS疼痛评分比较差异没有统计学意义,术后比较差异也无统计学意义,说明对术后镇痛的影响尚待进一步研究。通过局部冷却和加热,肿瘤血管的通透性显著增强,脂质体外泄至肿瘤间质,同时热应力增大诱发机械组织损伤,引起较单纯冷/热消融更为严重的微血管破裂[18]。冷热复合消融可使蛋白质变性更彻底,消融范围更大。高温也可以有效地防止穿刺路径出血以及肿瘤转移。本研究ICCH 组术中出血量明显低于IOCT组。ICCH组术后血糖浓度显著低于IOCT组术后血糖,但由于两组数值均超出血糖的正常水平,其临床意义尚待进一步研究。
目前,不可切除胰腺癌缺乏切实有效的治疗方案。冷热复合消融技术较单纯冷冻消融技术,在手术效率、肿瘤控制、并发症发生率方面疗效更佳,尤其对于胰头癌患者,在ICCH治疗的同时,解除肿瘤所致的胆道、胃肠道梗阻,并获得病理诊断,配合术后化疗或免疫等治疗,进一步提高生活质量和延长生存时间,值得临床推广。

