基于网络药理学研究加味柴芍六君汤治疗慢性萎缩性胃炎的作用机制
林泽豪,傅 颐,陈静怡,庄芬妮,黄安闻,连雄瀚,朱景茹,涂文玲,甘慧娟
(福建中医药大学中医学院,福建 福州350122)
慢性萎缩性胃炎(chronic atrophic gastritis,CAG)是临床常见的消化性疾病,为胃癌发生发展过程中的关键始动环节,以胃黏膜固有腺体萎缩为主要病理特点,甚至伴见肠化或上皮内瘤变,被世界卫生组织定义为癌前状态。该病症状易反复发作,严重影响患者的生活质量,其发病率和检出率随年龄增长而增加[1-2]。现代医学治疗CAG主要采取根除幽门螺杆菌(Hp)、胃黏膜保护、抗氧化治疗、促进胃黏膜再生、内镜微创技术等治疗方法[3],临床取得一定疗效,但多以对症治疗为主,远期疗效较差。因此,迫切需要一种替代疗法用以防治CAG。中医药治疗消化疾病具有独特的优势和广阔前景,且因其疗效安全,不良反应小的特点而备受关注,临床上有诸多医家运用加味柴芍六君汤治疗CAG取得了良好的疗效[4-6],然而其治疗CAG的作用机制尚未得到充分揭示。网络药理学是从系统生物学和生物网络平衡的角度阐释疾病的发生发展过程、从改善或恢复生物网络平衡的整体观角度认识药物与机体的相互作用并指导新药发现[7],近年来,越来越多科研工作者从系统的角度探讨中药复方多成分多靶点与疾病的关系,为现代中医药的研究提供了新的方向。因此,本文以网络药理学为切入点,对加味柴芍六君汤治疗CAG的靶点作用网络进行分析,预测其治疗CAG的可能作用机制。
1 方 法
1.1 加味柴芍六君汤有效活性成分与作用靶点搜集与筛选 通过中药系统药理学平台(简称TCMSP,http://tcmspw.com/tcmsp.php),分别以“白 芍”“白术”“半夏”“柴胡”“陈皮”“丹参”“莪术”“茯苓”“甘草”“人参”为检索词进行检索,设置口服生物利用度(OB)≥30%和类药性(DL)≥0.18为筛选条件,搜集加味柴芍六君汤的有效活性成分信息。然后对筛选出的有效活性成分进行蛋白靶标查找,将获取的蛋白靶标进行基因名称转换,获取加味柴芍六君汤的作用靶点信息。
1.2 CAG的疾病作用靶点获取 用GeneCards数据库对“Chronic at-rophic gastritis”进行检索,获取CAG的疾病作用靶点。通过Venny 2.1.0在线工具,获得CAG与加味柴芍六君汤共同作用靶点,即加味柴芍六君汤治疗CAG的作用靶点。
1.3 蛋白互作网络的可视化构建与分析 将加味柴芍六君汤的有效活性成分-作用靶点信息、单味药-有效活性成分信息和CAG-作用靶点信息导入C-ytoscape3.7.2软件,分别绘制出三者之间的蛋白互作网络,再利用“Merge”功能将其合并成加味柴芍六君汤治疗CAG的有效活性成分-作用靶点网络。将共同作用靶点导入到String数据库“Multiple proteins”检索框中,以互动得分≥0.900为筛选条件,构建加味柴芍六君汤与CAG之间的相互作用网络(PPI网络),并对PPI网络进行分析。
1.4 GO生物学过程和KEGG信号通路富集分析利用String数据库分析后的核心靶点进行GO生物学过程和KEGG信号通路富集分析;利用Bioconductor生物信息软件包,对所预测的化学成分靶点进行富集分析,以P<0.05为筛选条件进行可视化处理,再将加味柴芍六君汤对应的靶蛋白直接映射到通路上,选取既包含药物靶点又包含疾病靶点的通路做出KEGG信号通路富集分析柱状图。
1.5 分子对接 利用PubChem数据库得到加味柴芍六君汤活性成分的结构信息,在PDB数据库检索得到核心靶点的结构信息,最后利用Vina1.1.2软件完成加味柴芍六君汤活性成分与靶点受体的分子对接。
2 结 果
2.1 加味柴芍六君汤靶点信息获取 共筛选出加味柴芍六君汤有效活性成分195个(其中白芍13个、白术7个、半夏13个、柴胡17个、陈皮5个、丹参65个、莪术3个、茯苓15个、甘草92个、人参22个),药物靶点265个。文中只保留OB值排名第1的有效活性成分,见表1。将经过筛选转化的单味中药主要活性成分及作用靶点导入Cytoscape 3.7.2软件构建加味柴芍六君汤治疗CAG的有效活性成分-作用靶点网络,见图1。

表1 加味柴芍六君汤有效活性成分
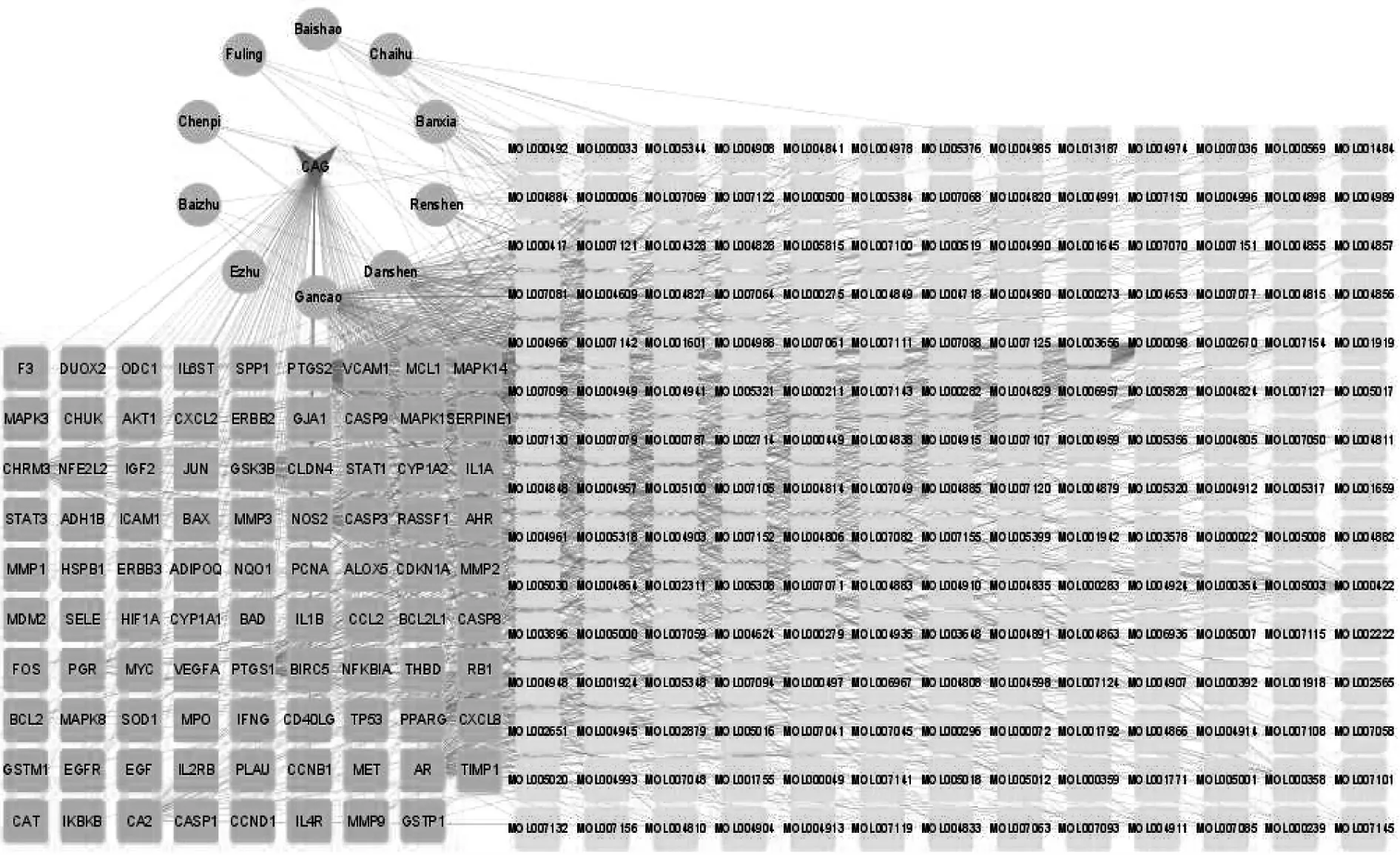
图1 加味柴芍六君汤治疗CAG的有效活性成分-作用靶点网络
2.2 加味柴芍六君子汤治疗CAG的作用靶点获取 通过GeneCards数据库检索得到CAG作用靶点613个,将加味柴芍六君子汤的作用靶点和CAG的作用靶点分别输入Venny 2.1.0在线工具分析,得到共同靶点89个。见图2。

图2 疾病-药物-靶点(DDT)韦恩图
2.3 相互作用网络构建与分析 将89个共同作用靶点输入到String数据库,构建出这89个共同作用靶点的相互作用网络模型。见图3。该网络包含89个共同作用靶点,336条连接线,平均度值为35.8,其中NFKBIA、SPP1、CASP9、TIMP1、MMP1、MCL1、CDKN1A、HIF1A、SERPINE1、STAT1、MPO、VCAM1、PPARG、AR、CASP8、IFNG、ERBB2、ICAM1、BCL2L1、MMP2、CAT、MAPK14、FOS、CCL2、IL1B、CCND1、EGFR、MYC、MAPK1、CXCLB、MMP9、EGF、STAT3、MAPK3、CASP3、VEGFA、MAPK8、PTGS2、JUN、TP53、AKT1的度值高于平均度值即为相对核心靶点。见图3。
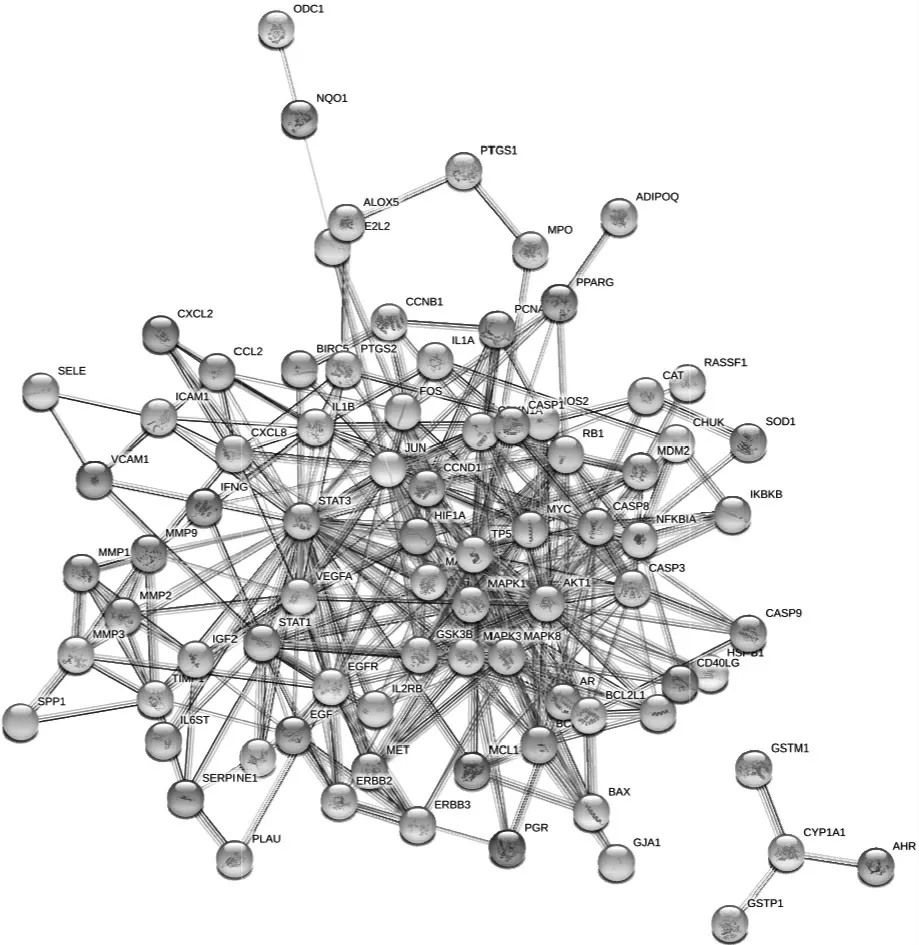
图3 共同作用靶点互作(PPI)网络图
2.4 GO生物学过程富集分析 通过R软件运行脚本对89个共同作用靶点进行GO生物学过程富集分析,获得P<0.05的GO条目117个,结果表明加味柴芍六君汤治疗CAG过程主要涉及磷酸酶结合、泛素样蛋白连接酶结合、细胞因子受体结合、受体配体活性、蛋白磷酸酶结合等生物学过程,文中共列出排名前20的GO富集气泡图。见图4。

图4 前20名GO富集气泡图
2.5 KEGG信号通路富集分析 通过R软件运行脚本对89个共同作用靶点进行KEGG信号通路富集分析,根据P<0.05筛选到152条信号通路,涉及到的信号通路类型主要有病毒感染(卡波氏肉瘤相关疱疹病毒感染、乙型肝炎病毒感染、丙型肝炎病毒感染、人类巨细胞病毒感染等)、癌症(前列腺癌、膀胱癌、胰腺癌、结直肠癌等)、信号传导(PI3K-Akt信号、AGE-RAGE信号、MAPK信号、HIF-1信号、JAK-STAT信号、RIG-I样受体信号、B细胞受体信号、幽门螺杆菌感染中的上皮细胞信号等)、流体剪切应力和动脉粥样硬化、麻疹等。见图5。

图5 KEGG信号通路富集分析柱状图
2.6分子对接 为了进一步验证“有效活性成分-作用靶点”网络的预测结果,将前5位核心靶点AKT1、TP53、JUN、PTGS2、MAPK8与其对应的主要活性成分kaempferol、baicalein、beta-sitosterol、Cavidine、nobiletin进行分子对接,获得的相关对接参数以及相应的计算结果,见表2。一般认为配体与受体结合的自由能越低,结合构象越稳定,发生作用的可能性越大,加味柴芍六君汤的主要活性成分与核心靶点结合自由能均<-5 kcal/mol,提示筛选出的核心靶点与其对应的活性成分具有良好的亲和力,证明结果具有一定的可信度。前5位核心靶点与其对应的活性成分对接结果,见图6。
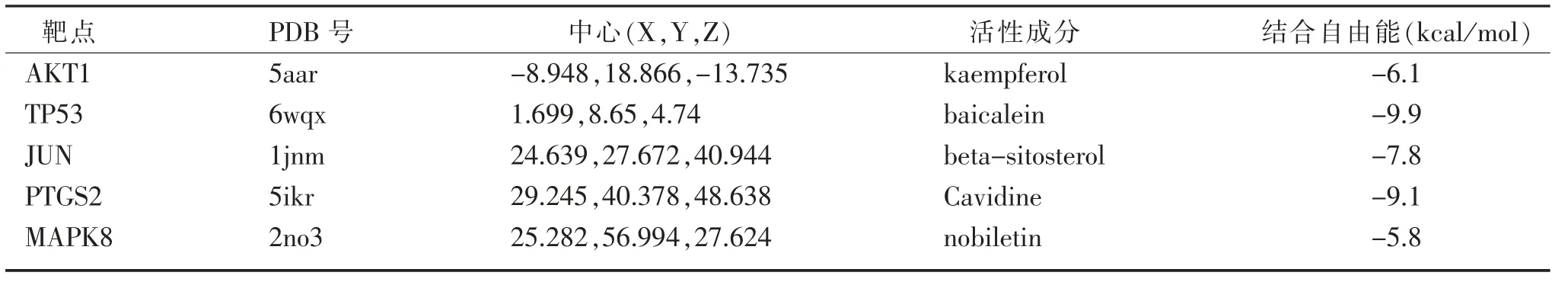
表2 活性成分与核心靶点对接参数及计算结果
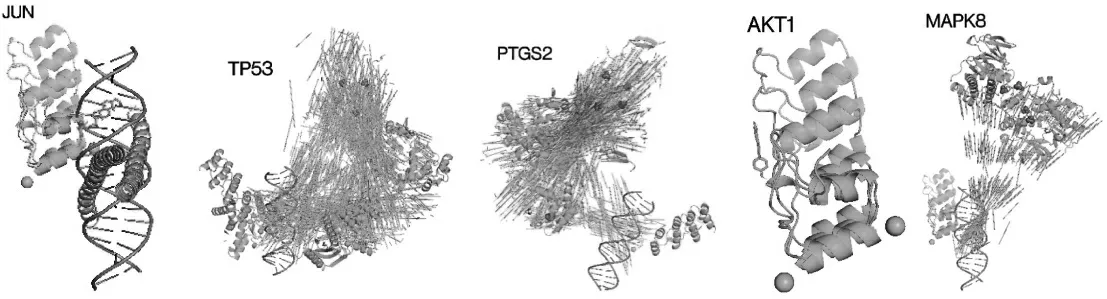
图6 对接结果图
3 讨 论
近年来,CAG的发病率呈明显上升趋势,且逐渐趋于年轻化,发病机制尚未明确,由于内外多重因素刺激导致胃黏膜腺体遭受破坏,从而出现萎缩、肠上皮化生甚至异型增生等难以逆转的病理学改变,长期反复发作容易诱发癌变,是许多科研工作者广泛关注的热点问题之一[8]。课题组前期研究证实,肝郁脾虚是CAG重要病理特点,肝郁、脾虚常相互影响,气郁、脾虚导致水液代谢障碍,产生痰湿,痰湿反过来影响了肝、脾功能,加重病情[9]。加味柴芍六君汤方中柴胡疏肝行气;白芍养血柔肝;人参、茯苓、白术健脾益气;半夏、陈皮理气燥湿化痰,和胃降逆;丹参活血祛瘀,通经止痛;莪术辛温,破血止痛;甘草调和诸药。全方共奏健脾和胃、活血祛瘀、疏肝理气之功。现代药理研究表明,白术能双向调节胃肠道,保护胃黏膜,提高免疫功能;白芍具有调节免疫,解除平滑肌痉挛作用,其中芍药甙能抗炎、保护胃黏膜;甘草具有抗溃疡、抗痉挛、调节免疫、抗肿瘤及解毒功效[10]。
本研究通过网络药理学的方法探讨加味柴芍六君汤治疗CAG的可能作用机制。通过对加味柴芍六君汤有效活性成分、作用靶点搜集与筛选,获取195个有效活性成分,包含槲皮素、常春藤皂苷元、甘草甜素、荜澄茄素、米橘素等。槲皮素能逆转DKK3启动子甲基化恢复其表达将有助于抑制胃癌的恶性转化。槲皮素逆转MSX1基因的甲基化状态后,恢复MSX1基因的功能则可诱导DKK3等基因的表达,理论上也可间接抑制胃癌的发生[11]。常春藤皂苷元能抑制胃癌MGC803增殖,对胃癌细胞侵袭、黏附、迁移能力有着明显的影响,是一种良好的抗肿瘤药物[12]。在对炎症趋化因子和促炎症因子的表达方面,甘草甜素能够抑制结肠髓过氧化物酶,减少活性氧化物质导致的脂质蛋白变性和器官损伤,改善炎症症状[13]。
将加味柴芍六君汤的作用靶点和CAG的作用靶点分别输入Venny2.1.0在线工具分析,得到共同作用靶点89个。通过构建共同作用靶点互作网络,分析得出IL1B、AKT1、TP53、JUN、MAPK8、VEGFA、MAPK3、STAT3、MAPK1等41个相对核心靶点。其中IL-1β是典型的促炎性细胞因子,炎性信号可通过激活炎症小体而刺激分泌IL-1β,过量分泌的IL-1β会引起广泛的炎症反应,导致炎性损伤[14]。IL-1β还是目前发现的最强的胃酸分泌抑制剂,持续的低酸分泌会促进萎缩的发生发展,增加胃癌的发生危险[15-16]。IL-6是一种具有多种生物学效应的细胞因子,是发动炎症反应的关键性因子,可以诱导内皮发生细胞活化,刺激中性粒细胞产生趋化作用,并产生大量的炎症介质[17]。有研究表明,IL-6在胃黏膜炎症反应过程中具有极其明显的指示作用,但是达到了一定的范围就可能会对胃黏膜产生损伤作用[18]。
通过GO生物学过程富集分析可知,加味柴芍六君汤对CAG的治疗作用主要通过参与以下生物学过程而发挥疗效:磷酸酶结合、泛素样蛋白连接酶结合、细胞因子受体结合、受体配体活性、蛋白磷酸酶结合等生物学过程。进一步的KEGG信号通路富集分析提示,加味柴芍六君汤主要通过调控HIF-1、PI3K-Akt、MAPK等多种信号通路而达到治疗CAG的作用。HIF-1α与慢性炎性反应的关系密切,是广泛存在于机体细胞中的一种转录调节因子,该基因由低氧诱导并介导细胞对缺氧微环境进行适性反应,缺氧时HIF-1α表达显著上调,由此启动60余种下游因子的转录以使细胞逐渐适应有氧到缺氧的转变[19]。PI3K/Akt途径信号传导与异常细胞增殖和凋亡有关,这两者都与肿瘤发生直接相关,PI3K/Akt通路在胃癌细胞增殖和存活中发挥着重要作用[20]。MAP-K途径可以将细胞表面信号转导至细胞核,对多数细胞的增生和程序化死亡等的调节起到重要意义[21]。分子对接结果显示,加味柴芍六君汤活性成分与相应核心靶点对接亲和力良好,对接体系稳定,进一步证明了本研究关于加味柴芍六君汤治疗CAG机制的有效性与可靠性。
本文采用网络药理学方法,从整体和系统的角度初步预测了加味柴芍六君汤治疗CAG的作用机制,其可能是通过抗炎,降低炎性因子IL-1β、IL-6的水平来减轻CAG黏膜细胞的缺氧状态,调节HIF-1α等细胞转录因子和蛋白的表达,或通过调控HIF-1、PI3K-Akt、MAPK等信号转导通路,从而改善胃黏膜瘀血状态,起到抗胃黏膜萎缩的作用,具有一定的研究价值。为进一步验证网络药理学结果的可靠性,后期有必要开展相应的基础实验进一步阐述加味柴芍六君汤治疗CAG的作用机制。

