锁骨下动脉闭塞血管内再通治疗的可行性分析
孙勇,杨波,康开江,高峰,莫大鹏,缪中荣,马宁
锁骨下动脉的狭窄和闭塞是常见的颅外段脑血管阻塞性疾病,常见的病因为动脉粥样硬化,其他病因还包括大动脉炎、主动脉夹层、创伤及其他内科疾病等[1]。锁骨下动脉起始段的完全闭塞不仅可以引起上肢缺血的症状,还常因动脉之间的压力差导致锁骨下动脉盗血综合征(subclavian steal syndrome,SSS)。传统的治疗方式多采用外科血管转流术,随着介入技术和材料的发展,近年来采用血管内再通治疗的方式逐渐增多,但针对此类患者治疗策略的选择及疗效随访报道较少[2-3]。本研究对近年来在首都医科大学附属北京天坛医院神经介入中心进行慢性锁骨下动脉闭塞血管内再通治疗的患者进行回顾性分析,现将结果汇报如下。
1 对象与方法
1.1 研究对象 回顾性连续收集2014年1月-2018年6月北京天坛医院神经介入中心收治的锁骨下动脉近端完全闭塞并存在上肢缺血症状或明确诊断为SSS的患者为研究对象。
纳入标准:①经DSA确诊为锁骨下动脉完全闭塞(前向血流消失);②存在病变侧上肢远端肢体乏力等缺血症状或明确诊断为SSS;③至少存在1项动脉粥样硬化的危险因素(高血压、糖尿病、高脂血症、肥胖、长期吸烟及饮酒);④患者从发病到接受血管内治疗的时间>30 d;⑤患者治疗前签署血管造影和血管内治疗同意书。
排除标准:①考虑为非动脉粥样硬化病变导致的锁骨下动脉闭塞;②虽影像学证实锁骨下动脉近端完全闭塞,但术前无椎-基底动脉缺血或病变侧上肢乏力等症状;③伴有颅内血管畸形、动脉瘤,近半年内有颅内出血性疾病、颅内手术病史或存在抗凝及抗血小板治疗禁忌证;④存在其他恶性疾病,预期生存时间<2年;⑤合并严重的肝肾功能不全或对造影剂过敏。
1.2 手术方法及围手术期处理 患者术前至少接受阿司匹林(100 mg/d)和氯吡格雷(75 mg/d)双联抗血小板治疗5 d以上。手术当日给予补液水化治疗稀释血液,降低术中血栓形成风险及对比剂对脏器的损伤。
所有患者均由经验丰富的神经介入医师(年手术量>100台)进行手术操作,手术穿刺入路一般选择右侧股动脉,局部麻醉成功后采用改良Seldinger穿刺技术穿刺股总动脉并置入8F动脉鞘,进行全身肝素化,使用猪尾导管进行主动脉弓造影,明确主动脉弓形态、锁骨下动脉闭塞情况及主动脉分支的走行及变异,造影延续至静脉后期,观察闭塞病变远端椎动脉盗血情况及锁骨下动脉闭塞病变的长度及角度,使用0.035英寸泥鳅导丝配合多功能导管及8F导引导管同轴经动脉鞘送至锁骨下动脉近端,一旦导丝通过,导管跟进确定远端为真腔后更换0.018英寸或0.014英寸导丝,参照病变相邻正常血管管径大小,使用导丝输送直径4~6 mm球囊进行预扩张,随后使用交换技术置入支架,对位准确后释放支架,除非闭塞段紧邻椎动脉或胸廓内动脉选用球扩式支架,否则一般选择自膨式支架,支架释放完毕后造影明确支架位置情况,包括展开是否良好、有无残留狭窄需要处理、椎动脉血流方向是否恢复及远端腋动脉血流情况,如残余狭窄率>30%可使用球囊进行后扩张。部分病例顺行再通困难时可同时采用桡动脉穿刺配合进行双向开通,桡动脉穿刺成功后经6F导管鞘置入5F单弯导管放置在闭塞段远端,逆行送入0.018英寸导丝至闭塞段血管远端后将导丝选入股动脉入路的8F导引导管,引导8F导引导管到达闭塞病变远端血管真腔,随后进行球囊扩张或支架释放。残余狭窄率参照北美症状性颈动脉内膜切除术试验(North American Symptomatic Carotid Endarterectomy Trial,NASCET)标准法计算,公式为:(闭塞近端正常直径-再通后最窄直径)/闭塞近端正常直径×100%。
术后3 d内患者收缩压维持在140 mm Hg(1 mm Hg=0.133 kPa)以下,以防止发生高灌注综合征。所有患者在术后复查平扫头颅CT以排除颅内出血及梗死,并继续给予补液治疗,促进造影剂排出体外。口服阿司匹林(100 mg/d)和氯吡格雷(75 mg/d)至少90 d,其后继续使用单一抗血小板药物。病情发生变化及时复查头颅CT或MRI。围手术期并发症定义为术后30 d内的缺血性卒中、心肌梗死和血管性死亡。
1.3 随访 对血管内治疗患者进行常规的随访,分别在血管内治疗术后1个月、3个月、6个月和12个月对患者进行随访,随访形式为门诊或住院复查及电话随访一般情况。本研究收集患者随访的影像学检查结果,根据CTA或DSA计算手术锁骨下动脉的再狭窄情况,术后再狭窄定义为随访时病变血管管径/术后即刻病变血管管径<50%。
1.4 分组和数据比较 依据术后锁骨下动脉是否成功再通将患者分为成功再通组及再通失败组,两组之间进行一般资料和临床特点的比较,包括性别、年龄、既往史、BMI、病变侧别、首次症状发作到治疗的时间。根据成功再通组患者所用支架类型分为自膨式支架组和球扩式支架组,比较两组术后锁骨下动脉残余狭窄率的差异。对成功再通的患者依据随访时是否发生锁骨下动脉再狭窄分为术后再狭窄组及无术后再狭窄组,两组之间进行一般资料和临床特点的比较。
1.5 统计学方法 采用SPSS 25.0软件对数据进行统计学分析。分类变量表示为例数(%),正态分布的连续变量表示为偏态分布的连续变量表示为M(P25~P75)。在统计检验中,分类变量采用χ2检验,正态分布的连续变量采用t检验,偏态分布的连续变量采用非参数检验(Mann-WhitneyU检验)。所有分析采用双侧检验,P<0.05认为差异有统计学意义。
2 结果
2.1 一般资料和临床特点 本研究共纳入106例患者,其中男性87例(82.1%),女性19例(17.9%),中位年龄61.0(56.8~67.0)岁;53例(50.0%)合并高血压,27例(25.5%)合并糖尿病,68例(64.2%)合并高脂血症,15例(14.2%)合并冠心病,79例(74.5%)有长期吸烟史,61例(57.5%)有饮酒史;99例(93.4%)为左侧锁骨下动脉闭塞,7例(6.6%)为右侧锁骨下动脉闭塞;平均BMI为24.5±2.8 kg/m2;首次症状发作到治疗的中位时间为5.0(1.4~18.0)个月。
2.2 手术结果 106例患者中有91例(85.8%)成功血管再通,15例(14.2%)血管开通失败,其中14例(13.2%)为反复尝试后导丝仍无法通过病变部位而放弃,1例为术中患者配合度较差,造影完成后未再进行开通操作(表1)。
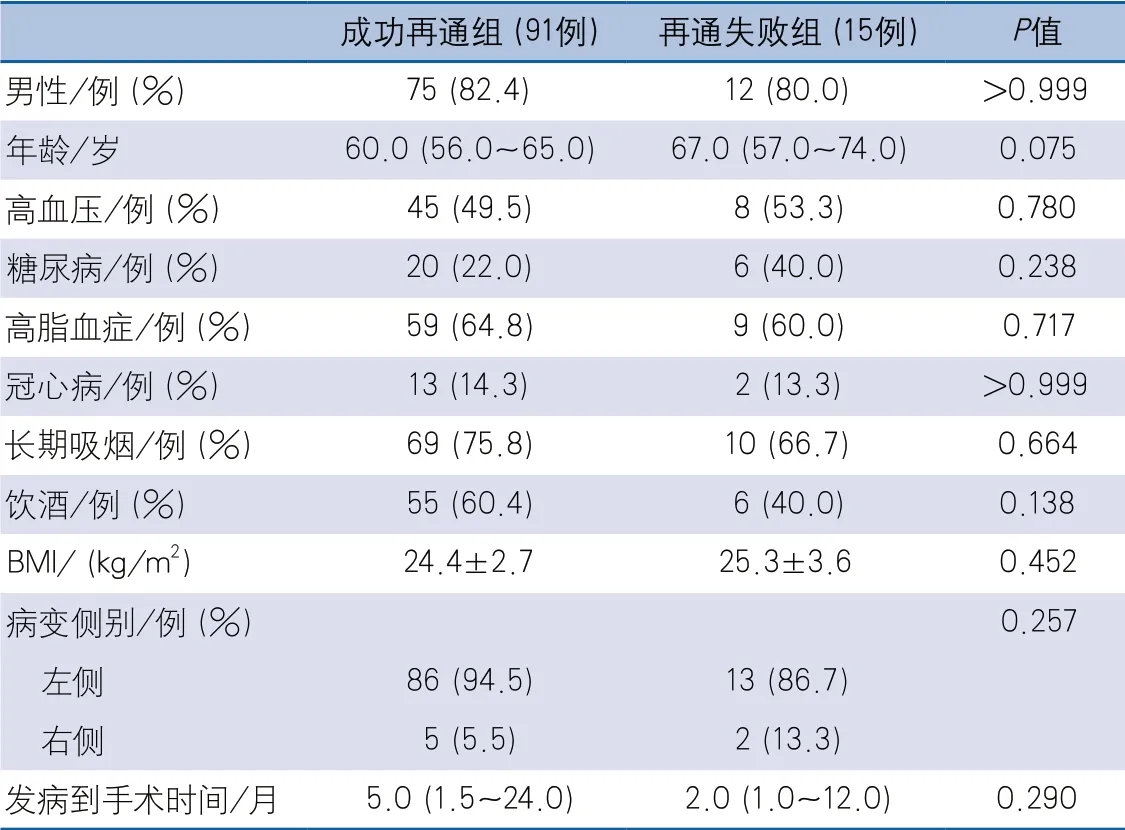
表1 成功再通组和再通失败组临床特点比较
成功再通组男性75例(82.4%),女性16例(17.6%),中位年龄60.0(56.0~65.0)岁,86例(94.5%)为左侧锁骨下动脉闭塞,5例(5.5%)为右侧锁骨下动脉闭塞;再通失败组男性12例(80%),女性3例(20%),中位年龄67.0(57.0~74.0)岁,13例(86.7%)为左侧锁骨下动脉闭塞,2例(13.3%)为右侧锁骨下动脉闭塞。两组患者性别、年龄、既往史、BMI、病变侧别、首次症状发作到治疗的时间等指标差异无统计学意义。
91例血管成功再通的患者中共有83例(91.2%)采用经股动脉入路顺行开通,8例(8.8%)采用双向开通;35例(38.5%)采用自膨式支架,56例(61.5%)采用球扩式支架;使用自膨式支架的术后残余狭窄率为10.0%(10.0%~16.3%),使用球扩式支架的术后残余狭窄率为10.0%(5.0%~10.0%),两者之间的差异无统计学意义(P=0.081)。
成功进行血管内再通治疗的患者术后椎-基底动脉供血不足及患侧上肢远端缺血情况均得到明显改善或消失,患侧桡动脉搏动较术前明显增强,锁骨下动脉盗血现象消失。
2.3 随访结果 106例接受血管再通治疗的患者均无围手术期并发症发生。成功再通组中85例(93.4%)患者完成了影像随访,随访的中位时间为13.0(6.0~15.0)个月,术后再狭窄5例(5.9%),无术后再狭窄80例(94.1%)。术后再狭窄组较无术后再狭窄组的中位年龄更高,差异有统计学意义,两组其他临床特点差异无统计学意义(表2)。本研究所有患者随访中无血管完全再闭塞者,无再发椎-基底动脉及上肢远端缺血症状,随访期内无缺血性卒中、血管性死亡等不良事件。15例再通失败的患者中有12例(80.0%)进行了临床随访,随访时间中位时间为14.5(8.0~19.0)个月,其中10例(83.3%)患者症状无明显好转,2例(16.7%)患者经长期规范药物治疗,头晕症状有所缓解。

表2 术后再狭窄组和无术后再狭窄组临床特点比较
3 讨论
锁骨下动脉闭塞的病因主要是动脉粥样硬化,患者中男性多于女性,年龄分布主要在40~80岁[1,4]。既往研究数据显示,左侧锁骨下动脉闭塞的发病率显著高于右侧,占总发病率的60%~70%,这可能与左侧锁骨下动脉起始部与主动脉弓之间的角度较锐,血流通过时产生涡流,更利于动脉粥样硬化斑块的形成,进而导致血管狭窄及闭塞有关[5],本研究的结果也证实了这一点。当血流动力学改变较小,颅内侧支循环代偿较好的情况下,锁骨下动脉闭塞的症状可能不明显,但当病变远端的椎动脉出现持续的逆向血流或远端腋动脉血流严重不足时,可能会有明显的椎-基底动脉供血不足的症状,包括头晕、视物不清、共济失调等,同时可能伴有患侧上肢的乏力、冷感及疼痛等[6]。既往治疗锁骨下动脉闭塞主要以外科血管手术为主,包括腋-腋动脉搭桥术、锁骨下动脉-锁骨下动脉搭桥术、颈动脉-锁骨下动脉搭桥术及锁骨下动脉剥脱术等,疗效尚可,但传统手术存在需要全身麻醉、创伤较大,并发症发生率较高且术后恢复时间长等不足[7]。随着介入技术及材料的发展,目前血管内再通治疗已成为治疗此类疾病的重要手段之一[8]。
在本研究中,经血管内再通治疗的106例锁骨下动脉闭塞患者中,闭塞再通成功率为85.8%,与既往文献报道的46%~100%相比处于较高水平[5,9-12]。该结果表明,使用目前的血管内介入治疗技术及材料对锁骨下动脉闭塞患者进行血管内再通治疗是可行的。
既往国内相关研究报道,慢性锁骨下动脉闭塞血管内再通术围手术期并发症的发生率为0~15.6%不等,本研究中患者术后30 d内均未出现缺血性卒中、心肌梗死和血管性死亡等并发症,发生率低于既往研究报道[5,9-10,13]。早期研究报道慢性锁骨下动脉闭塞血管内再通术围手术期并发症的发生率相对较高,近年来随着介入材料的发展以及技术的逐渐成熟而逐步降低,目前条件下在成熟的血管介入中心进行此项手术是相对安全的。此外,部分中心应用阻断同侧椎动脉血流以及使用脑保护装置来进一步降低并发症发生率,使得锁骨下动脉闭塞的血管内再通治疗更加安全[14-16]。
在成功进行血管再通的91例患者中,85例患者完成了临床随访,其中5例(5.9%)在随访期间发生了术后再狭窄,与谢建平等[5]、万跃等[17]的报道接近,低于张曦彤等[9]、王伟明等[11]、梁双超等[12]、俞恒锡等[18]报道的再狭窄率。本研究中术后血管再狭窄的患者中无血管完全闭塞患者,且所有患者均未再出现相关临床症状。结果提示血管内再通治疗可以显著改善锁骨下动脉闭塞患者的临床症状且术后血管再狭窄率较低。同时本研究提示,随着年龄的增加,锁骨下动脉闭塞血管内再通后再狭窄的风险也逐渐增加,这提示对于高龄的患者,术前应进行谨慎地评估以保证疗效。
本研究是回顾性研究,手术方式的选择依赖于医师对患者病情的判断;本研究样本量偏少,仍需大样本量的临床研究对血管内治疗锁骨下动脉闭塞的安全性和有效性进一步验证。
【点睛】本研究旨在分析血管内介入治疗在慢性锁骨下动脉完全闭塞患者中的安全性和有效性。研究结果表明,血管内介入治疗可作为该类疾病的治疗方式选择,具有成功率高、并发症少、疗效佳的优点。

