超声剪切波频散成像用于肝脏弥漫性病变研究进展
孙晓慧,崔立刚
(北京大学第三医院超声科,北京 100191)
近年来,超声剪切波弹性成像技术日益成熟,具有无创、简便及定量评估肝硬度等优势,可评估弥漫性病变肝脏的纤维化程度、指导慢性肝病治疗并监测预后[1]。目前大部分商用超声弹性成像仅将肝脏视为纯弹性体;但本质上大部分器官及组织为黏弹性体,兼具弹性固体性质和黏性流体性质[2],黏性亦为表征肝组织病理变化的重要参数[3],反映组织的抗形变能力。超声剪切波频散(shear wave dispersion, SWD)成像可同时获得肝脏黏性和弹性相关参数,定量评估其黏弹性。本文就SWD成像在肝脏弥漫性病变中的研究进展进行综述。
1 超声SWD成像原理
超声剪切波弹性成像杨氏模量或弹性模量计算公式为E=3ρC2;其基本原理为介质接受超声波激励后产生的剪切波速度与介质弹性呈正相关,然而黏弹性体接受超声波激励后产生的剪切波传播情况却并非如此简单。根据经典Voigt模型[2,4-5]可推导出反映剪切波速度与剪切波角频率、介质弹性及黏性之间关系的公式(1):
(1)
式中C(ω)为剪切波速度,ω为剪切波角频率,μ为介质弹性,η为介质黏性,ρ为介质密度。由该公式可知,黏弹性介质中,剪切波速度不仅与介质黏性和弹性有关,还与剪切波角频率有关;剪切波在某种黏弹性介质中传播时,其速度随频率变化而改变,此为剪切波的频散特性,其所致频散现象与介质黏性有关,纯弹性介质黏性为0,公式(1)可简化为公式(2),即剪切波速度与剪切波角频率无关,故不存在频散现象:
(2)
式中C(ω)为剪切波速度,μ为介质弹性,ρ为介质密度。采用超声剪切波弹性成像需假设黏弹性体为纯弹性体,即忽略剪切波的频散特性,直接利用剪切波速度估算介质弹性,故所得黏弹性组织弹性值与真实弹性值之间存在偏差,且无法准确评估组织黏性。超声SWD成像可在一定程度上弥补上述不足。
1.1 剪切波频散超声振动(shear wave dispersion ultrasound vibrometry, SDUV)成像 SDUV成像技术[2-3,5]通过声辐射力激励组织产生谐波振动,并测量不同谐波频率的剪切波速度,以观察组织的频散特性,可定量检测组织黏性和弹性。SDUV成像的理论基础为采用Voigt模型描述组织力学特征时,将不同频率剪切波速度代入公式(1),可拟合得到组织黏性和弹性系数[2-3]。目前 SDUV成像多用于离体研究[5]。已有的剪切波成像技术,如快速剪切波成像(supersonic shear imaging, SSI)[6],为在体生物组织黏弹性的定量检测提供了可能,其测量原理与SDUV成像类似。多数研究采用Voigt模型描述生物组织的黏弹性特征,但由于生物组织的复杂性,难以适当选择力学模型。
1.2 超声SWD成像 Canon Aplio i系列超声仪可利用剪切波的频散特性实现SWD成像,定量测量剪切波传播速度和剪切波频散斜率(shear wave dispersion slope, SWDS),其中前者用于计算组织弹性,后者则间接反映组织黏性,且无需依赖力学模型[7-8]。超声SWD成像通过检测不同频率的剪切波传播速度获得剪切波速度-频率曲线(图1),其斜率为剪切波频散值,与介质黏性呈正相关;即剪切波频散效应随介质黏性增加而加强,故剪切波频散值可间接反映组织黏性[8-9]。因此,Canon Aplio i系列超声SWD成像本质上为SWDS成像。
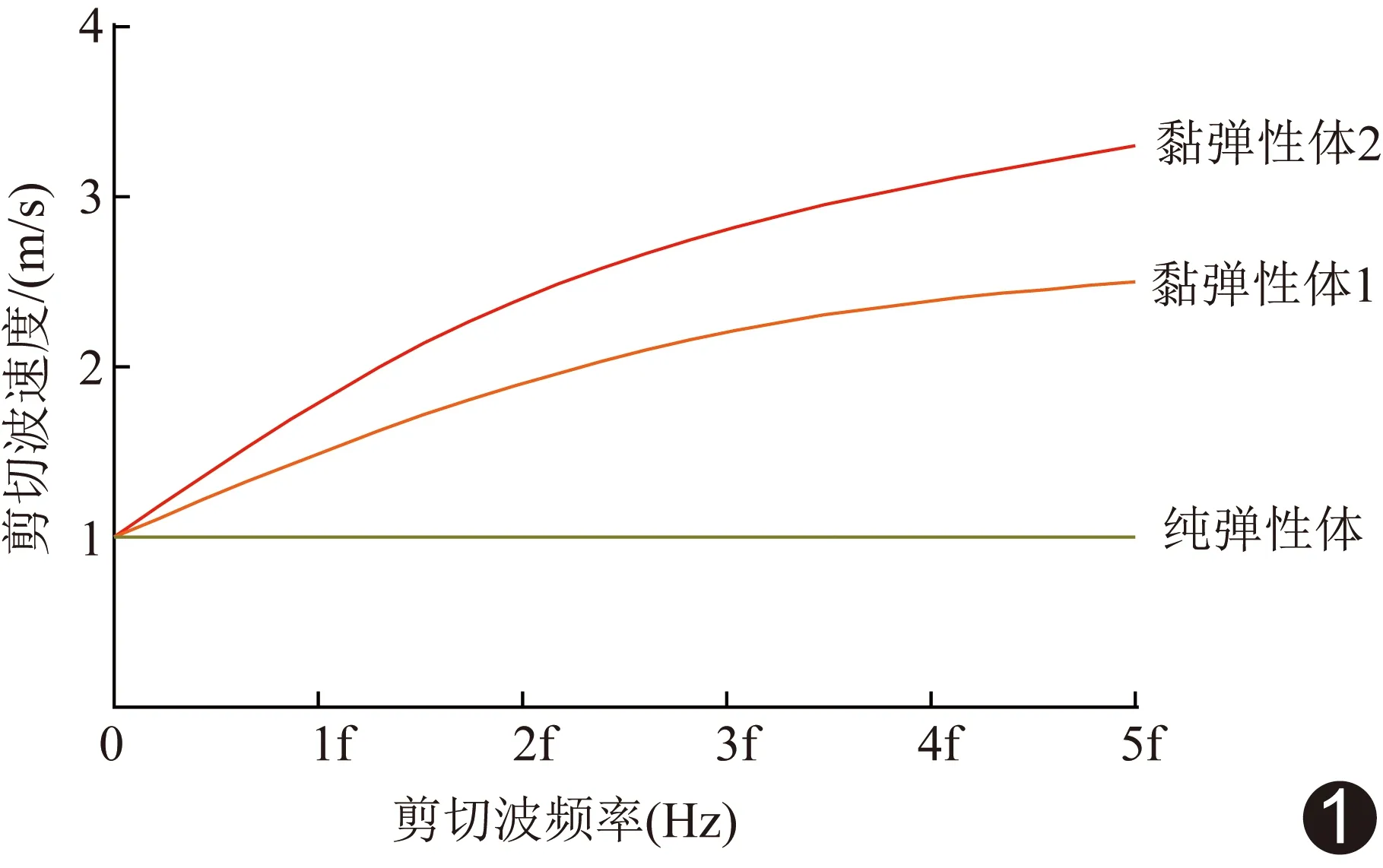
图1 Voigt黏弹性模型中剪切波速度与频率关系曲线图 纯弹性组织中剪切波速度恒定,与频率无关;而黏弹性组织中剪切波速度随频率变化而改变
1.2.1 操作方法 检查前患者至少禁食4 h。检查时嘱患者仰卧、右臂上抬置于头顶,将探头置于其右上腹,避开肋骨声影、血管、韧带、胆囊及囊肿等局灶性病变而获得最佳灰阶图像;之后嘱患者于平静呼吸状态下屏气,设置取样框3 cm×3 cm、上缘距肝被膜至少1 cm,通过“Multi模式”获取实时连续剪切波图像后冻结回放,亦可通过“1 shot模式”于图像稳定时采集单帧图像后冻结;随后采用四屏同步模式(图2),于图像上距探头5 cm范围、剪切波传播图相对规则平行区域内勾画直径10 mm的圆形ROI,测量剪切波弹性值和频散值,重复10次,取中位数,评估肝脏弹性和黏性。测量结果满足四分位数间距/中位数<0.30时为可靠数据。

图2 肝脏Canon Aplio i900超声SWD成像 A.剪切波弹性图; B.剪切波传播图; C.二维灰阶图; D.剪切波频散图
1.2.2 参考值 TROUT等[10]采用Canon Aplio i800超声仪检测无肝病史的128名儿童与32名成人肝脏剪切波频散值,发现儿童和成人肝脏剪切波频散值范围分别为(11.43±1.75)m/(s·kHz)和(10.24±1.65)m/(s·kHz)。由于该研究未能排除患有潜在肝脏疾病的受试者,且样本量较小,所得参考值代表性不佳。
1.2.3 可重复性 YOO等[11]发现Canon Aplio i系列超声SWD成像检测非酒精性脂肪性肝病患者与正常人肝脏剪切波频散值具有良好的观察者内(ICC=0.955)和观察者间一致性(ICC=0.800)。
2 超声SWD成像用于肝脏弥漫性病变
肝脏弥漫性病变指各种原因所致肝实质、纤维结构及脉管系统变性或损害,包括各型肝炎、脂肪肝、肝纤维化、肝硬化、肝淤血、肝寄生虫病及其他罕见肝脏疾病等[12]。目前超声SWD成像评估肝纤维化、脂肪变性及炎性坏死等尚处于初步探索阶段。
2.1 评估肝纤维化 大量临床研究已证实可根据肝脏弹性对肝纤维化进行有效分期,而肝脏黏性能否用于评估肝纤维化程度目前尚不明确。有学者[13]采用MR弹性成像(MR elastography, MRE)检测肝纤维化大鼠模型,发现其肝脏黏性和弹性参数均与肝纤维化程度有关,这意味着除肝脏弹性外,肝脏黏性亦可为肝纤维化分期提供有效信息。CHEN等[13]采用SDUV成像观察大鼠肝脏黏弹性与肝纤维化的相关性,发现肝脏黏性和弹性均随肝纤维化程度加重而增加,且肝脏弹性诊断不同分期肝纤维化的曲线下面积(area under curve, AUC)均高于黏性,即采用肝脏弹性对肝纤维化进行分期的准确性高于黏性。在此基础上,CHEN等[14]采用SDUV成像检测各种病因慢性肝病患者,并评估其肝脏黏弹性对肝纤维化分期的价值,结果显示肝脏弹性和黏性诊断≥F2期肝纤维化的AUC分别为0.98和0.86,表明肝脏弹性诊断≥F2期肝纤维化的准确性高于黏性,且多因素分析发现肝脏黏性与肝纤维化分期无显著相关性,与上述研究[13-14]结果基本相符。
2.2 评估肝脂肪变性 BARRY等[15]基于SDUV成像技术,利用剪切波的频散特性观察小鼠和大鼠肝脏力学特征,发现肝脂肪含量增加可导致剪切波频散增加,提示肝脏黏性有望成为评估肝脂肪变性程度的新指标。DEFFIEUX等[16]以病理结果为金标准,观察以肝脏黏性预测120例慢性肝病患者肝纤维化、脂肪变性和炎性坏死程度的准确性,发现肝脏黏性虽与肝纤维化程度有关,但与脂肪变性和炎性坏死程度无关。NIGHTINGALE等[17]纳入135例非酒精性脂肪性肝病患者,分析肝脏SWDS即剪切波频散值对脂肪性肝病的诊断价值,发现其诊断≥S2期肝脂肪变性的AUC仅为0.47,即肝脏黏性与其脂肪变性程度无明显相关性,无法用于评估非酒精性脂肪性肝病脂肪变性程度。上述临床研究结论与动物实验结果相悖的原因可能在于动物模型基本条件一致、病理改变相对单一,而肝病患者病因、病程、疾病管理及干预等方面均不相同;还可能与检查方法不同有关。目前仍未确知肝脏黏性能否用于评估肝脂肪变性程度。
2.3 评估肝炎性坏死 SUGIMOTO等[18]建立肝炎性坏死和纤维化大鼠模型,以Canon Aplioi系列超声SWD成像技术进行观察,发现大鼠肝纤维化程度与肝脏弹性相关,而炎性坏死程度与SWDS即肝脏黏性显著相关,提示根据肝脏弹性可有效预测其纤维化程度,黏性则能有效预测炎性坏死程度。LEE等[7]将这种SWD成像技术用于肝移植术后患者,发现移植术后肝损伤组患者肝脏弹性和黏性均高于无损伤组;仅肝纤维化程度可影响肝脏弹性,而肝纤维化和炎性坏死程度均能影响肝脏黏性;肝脏黏性和弹性诊断肝损伤的AUC分别为0.86和0.75,即肝脏黏性诊断肝移植术后肝损伤效能较佳。SUGIMOTO等[19-20]发现肝脏黏性评估非酒精性肝病炎性坏死分级具有较高准确性。de ARAUJO NETO[21]指出,肝纤维化可能为影响其炎性坏死程度与黏性之间相关性的混杂因素。对于肝脏黏性与其炎性坏死和纤维化程度的相关性及其评估肝移植术后肝炎复发和排斥性反应等的潜在应用价值尚需进一步观察。
3 小结
超声SWD成像为评估肝脏弥漫性病变提供了新视角。黏性可能为反映肝脏不同病理状态的有效参数,其在评估肝纤维化分期、脂肪变性及炎性坏死程度等方面的价值值得期待。开展大样本、多中心临床研究探索超声SWD成像的应用价值可为后续推广奠定基础。

