D-二聚体和胱抑素C对脑血管介入术后再狭窄的预测价值
王 娜,刘春丽,邓爰平,徐圣康
缺血性脑血管病(ICVD)主要病理生理基础是动脉粥样硬化(AS),采用介入治疗可有效解除病变脑血管狭窄或梗阻,已成为现阶段头颈部血管狭窄的重要治疗方法,但介入术后再狭窄是难以处理的医学难题,虽然临床对其发生机制的认识已明确,诊断时仍主要依赖于血管造影等影像学检查结果[1-2]。有报道显示,D-二聚体(D-D)是纤维蛋白单体经水解后形成的特异性纤溶过程标志物,可反映因动脉粥样硬化斑块不稳定所致凝血纤溶系统紊乱状态,现已广泛用于心肌细胞损伤评估[3]。汪冰等[4]研究发现,血清胱抑素C(CysC)水平与颅内外动脉粥样硬化性狭窄程度密切相关,是脑血管病变的主要危险因素。可见D-D及CysC在头颈部血管狭窄发生发展过程中可能占有重要地位。本研究分析脑血管介入术后病人D-D和CysC水平变化,探讨其对脑血管介入术后再狭窄的预测价值。
1 资料与方法
1.1 一般资料 选取2013年8月—2016年8月于我院介入治疗的缺血性脑血管病病人107例, 脑血管病变类型:短暂性脑缺血发作(TIA)69例,脑梗死38例;狭窄部位:大脑前动脉17例,大脑中动脉29例,大脑后动脉13例,椎动脉16例,基底动脉32例。纳入标准:①符合脑梗死和TIA相关临床诊断标准[5];②因脑梗死或TIA成功接受支架置入治疗,术后残余狭窄<20%,且围术期未见严重并发症;③年龄18~80岁;④病人及家属知晓本研究,并签署知情同意书。排除标准:①伴有恶性肿瘤或严重感染等基础疾病;②伴心、肝、肾等器官功能不全;③伴凝血功能障碍;④妊娠期或哺乳期病人;⑤介入治疗后未完成2年随访。
1.2 治疗方法 入选病人均根据《中国缺血性脑血管病血管内介入诊疗指南2015》[6]中相关操作规范和方法,实施脑血管狭窄部位支架置入,术后给予阿司匹林、氯吡格雷等药物抗凝,并针对基础疾病进行治疗;嘱病人术后定期门诊复查,随访2年内头颈部病变血管再狭窄发生情况。根据北美症状性颈内动脉膜切除协作研究组(NASCET)评估标准,再狭窄判断标准为CT血管造影(CTA)显示病变脑血管狭窄≥30%[7]。
1.3 研究方法 收集病人临床资料,根据随访2年内有无再狭窄发生将病人分为再狭窄组与对照组,比较两组手术时基线资料及术后1个月时血清D-D及CysC水平,绘制血清D-D及CysC水平受试者工作特征曲线(ROC),计算ROC曲线下面积(AUC),分析其对病变脑血管再狭窄的预测价值;根据Youden指数选择D-D及CysC最佳临界值。
血清D-D测量采用双抗体夹心法,试剂盒由上海捷门生物技术有限公司生产;CysC测量采用双抗体夹心法,试剂盒由上海佑隆生物科技有限公司提供。所有操作均严格按照试剂盒说明书执行。
2 结 果
2.1 两组基线资料比较 随访2年内,107例中出现再狭窄病人28例(26.17%)为再狭窄组,未发现再狭窄79例为对照组,两组基线资料比较差异均无统计学意义(P>0.05)。详见表1。

表1 两组基线资料比较
2.2 两组血清D-D及CysC水平比较 再狭窄组术后1个月时血清D-D及CysC水平高于对照组,差异均有统计学意义(P<0.01)。详见表2。
表2 两组血清D-D及CysC水平比较(±s) 单位:mg/L
2.3 D-D及CysC对脑血管介入术后再狭窄的预测价值 根据脑血管介入术后再狭窄发生情况和血清D-D、CysC水平绘制预测诊断ROC曲线,结果显示AUC分别为0.948和0.884,其血清D-D最佳临界值为0.77 mg/L,诊断灵敏度和特异度分别为92.86%和81.01%;血清CysC最佳临界值为1.55 mg/L,诊断灵敏度和特异度分别为82.14%和83.54%,两者诊断价值比较差异无统计学意义(Z=1.309,P>0.05)。详见表3、图1。

表3 血清D-D及CysC对脑血管介入术后再狭窄的预测价值
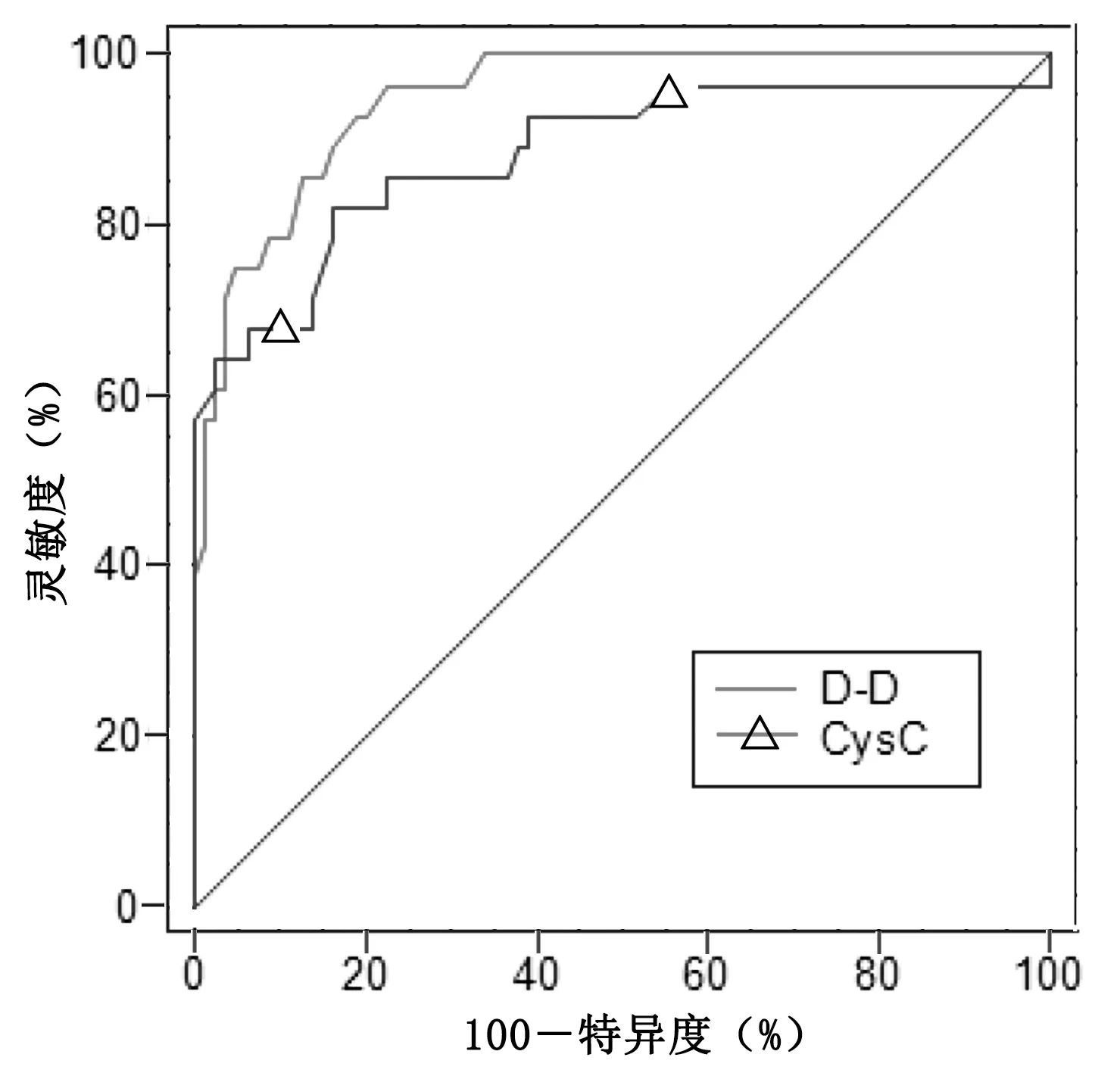
图1 D-D及CysC预测脑血管介入术后再狭窄的ROC曲线
3 讨 论
脑血管病是中老年人群常见疾病,据统计显示,我国每年约150万人因脑血管病死亡,且幸存病人中丧失劳动力者占75%[8]。缺血脑血管病在全部脑血管病中占65%~85%,是因供血动脉狭窄、梗阻或闭塞导致相应部位脑组织血流灌注减少,进而引起脑组织缺血坏死和神经功能障碍[9]。近年来,随着神经介入技术发展和材料改进,脑血管支架置入治疗发展迅速,但如何预防、诊断和治疗脑血管介入术后再狭窄,从而减少脑卒中再发生,仍是现阶段临床面临的主要难题。
研究显示,糖尿病等基础疾病及支架内再狭窄病史、支架类型和病人病程长短等均为脑血管再狭窄发生的危险因素[10-11]。Langwieser等[12]对35例椎动脉支架置入病人进行研究显示再狭窄发生率为23%。崔涛[13]回顾性分析145例因大脑中动脉狭窄行支架置入术病人临床资料,26例术后出现明显再狭窄,发生率为17.9%。表明介入术后再狭窄发生率较高,且不同地区或医院发生率差异较小。本研究随访结果发现,再狭窄发生率为26.17%,稍高于既往文献报道,其原因可能与研究对象自身病情、不同地区医疗水平及术后康复条件等因素相关[13]。本研究结果显示,再狭窄组病人中伴糖尿病、冠心病、高脂血症及吸烟史病人所占比例高于对照组病人,但两组比较差异无统计学意义,可能因本研究样本量偏小所致,提示糖尿病、冠心病、高脂血症及吸烟等也可能是增加缺血性脑血管病病人介入术后再狭窄发生的影响因素,有待进一步研究验证。
血栓形成是脑血管介入术后再狭窄发生的重要环节,血管内皮细胞损伤是动脉粥样硬化发病的早期关键环节,缺血性脑血管病病人中广泛存在动脉粥样硬化,而支架置入治疗可导致损伤加重,促使损伤标志物血友病因子大量释放进入血浆,与血小板糖蛋白Ⅰb-Ⅸ结合或连同纤维连接蛋白与血小板糖蛋白Ⅱb/Ⅲa结合,诱导血小板向受损内皮细胞表面聚集并释放颗粒物质,启动凝血反应,并造成继发性纤溶系统亢进,导致纤维蛋白降解产物D-D表达水平升高,因此,D-D作为机体高凝状态和纤溶亢进的重要标志物,对预测微小血栓形成具有重要指导意义[14-15]。血管内皮细胞损伤还可引起血管壁舒张功能异常和血管平滑肌细胞增殖、迁移,从而可加快动脉粥样硬化病程进展,CysC则可通过抑制组织蛋白酶B活性发挥保护内皮细胞作用。CysC与组织蛋白酶保持动态平衡还有利于减少细胞外基质成分细胞外基质(ECM)重塑,从而维持动脉壁正常结构和功能。此外,有研究表明,CysC可抑制氧化型低密度脂蛋白(ox-LDL)诱导的血管内皮细胞损伤,同时可有效减少活性氧(ROS)生成,发挥抗细胞凋亡效果[16-17]。可见CysC可通过多种机制延缓动脉粥样硬化病情进展,防止动脉血管狭窄。本研究结果显示,脑血管介入术后再狭窄病人术后1个月时血清D-D及CysC水平高于非狭窄病人,经ROC曲线分析发现,D-D和CysC对脑血管介入术后再狭窄发生均具有较高的预测价值,AUC分别为0.948和0.884,其中D-D以0.77 mg/L为临界值时,灵敏度和特异度分别为92.86%和81.01%;CysC以1.55 mg/L为临界值时,灵敏度和特异度分别为82.14%和83.54%,提示D-D预测脑血管介入术后再狭窄发生具有较高的灵敏度,而CysC则具有较高的特异度。
血清D-D和CysC水平与缺血性脑血管病病人介入治疗后再狭窄发生有关,再狭窄病人血清D-D和CysC水平明显升高,二者对介入术后再狭窄发生均具有较高预测价值。

