全氟及多氟化合物在土壤中的污染现状及环境行为研究进展
陈雷,戴玙芽,陈晓婷,周顺怡,林洁颖,刘韵,林庆祺,3*,晁元卿,2,汤叶涛,2,仇荣亮,2,3,王诗忠,2*
(1.中山大学环境科学与工程学院,广州 510006;2.广东省环境污染控制与修复技术重点实验室,广州 510006;3.华南农业大学资源环境学院,广州 510642)
全氟及多氟化合物(Per-and polyfluoroalkyl substances,PFASs)是碳链上的氢原子全部或部分被氟原子取代的一类持久性有机污染物,其分类见图1。常见PFASs 的种类、名称、结构式和离子类型等如附表1(扫描文章首页OSID 码浏览)所示。其中,全氟烷基酸类(Perfluorinated alkyl acids,PFAAs)按末端基团差异可分为全氟烷基羧酸(Perfluoroalkyl carboxylic acid,PFCAs,带有羧酸基团)与全氟烷基磺酸(Perfluorooctyl sulfonic acid,PFSAs,带有磺酸基团)。长碳链PFAAs(也称为传统型PFAAs,即碳原子数大于等于7 的PFCAs 和大于等于6 的PFSAs)因其稳定的化学性质而在全球范围内被广泛使用,但其对植物、动物甚至是人体的毒性也被不断证实[1-2]。因此全球许多国家和地区对PFAAs 进行了严格的管控,例如全氟辛烷羧酸(Perfluorooctanoic acid,PFOA)和全氟辛烷磺酸(Perfluorooctane sulfonate,PFOS)已分别在2017 年和2009 年被列入斯德哥尔摩公约,并在全球范围内限制使用[1]。由于市场发展需求,新型PFASs,即短链PFAAs(碳原子数小于7 的PFCAs 和小于6 的PFSAs)与新型多氟化合物,逐渐被用作长链PFAAs替代物而被大量生产并投入使用。短链PFAAs 不具备生物累积与生物放大潜力,且在生物体内半衰期比长链PFAAs更短[3]。
多氟化合物主要类型包括氯代或氢代多氟类、氟调醇类及全氟聚醚类。氯代或氢代多氟化合物即利用氯、氢原子取代碳链上的1 个或多个氟原子,例如6∶2氯代多氟醚基磺酸盐(6∶2 chlorine substituted perfluoroalkyl ether sulfonates,6∶2 Cl-PFESA,商业名F-53B)和6∶2 氟调聚磺酸(6∶2 fluorotelomer sulfonic acid,6∶2 FTSA)等[1-4]。而全氟聚醚类则是在分子骨架中引入醚键,如全氟聚醚基羧酸盐(Perfluoroethercarboxylic acids,PFECAs),主要种类有六氟丙烯氧化二聚酸(Hexafluoropropylene oxide dimer acid,HFPODA,其盐类物质商业名为GenX)、六氟丙烯氧化三聚酸(Hexafluoropropylene oxide trimer acid,HFPO-TA)、六氟丙烯氧化四聚酸(Hexafluoropropylene oxide tetramer acid,HFPO-TeA)和4,8-二氧-3H-全氟壬酸铵(Ammonium 4,8 -dioxa -3H -perfluorononanoate,ADONA),其中GenX 与ADONA 最为常用[5-6]。插入醚键使得新型多氟化合物在保持碳原子数和官能团不变的情况下,又被赋予一定的可降解性[7],然而,对于此类新型多氟化合物的降解特性研究仍较为缺乏。
PFASs 既含有疏水性C—F 键(键能接近485.5 kJ·mol-1),又含有羧酸根、磺酸根等亲水性官能团,同时结构中较弱的分子间作用力使PFASs 本身表面张力很低,从而显著降低目标溶液的表面张力,因此PFASs 被广泛用于表面活性剂、乳化剂、消防泡沫灭火剂、纺织以及食品包装等产品的生产中[8-9]。PFASs的使用导致其大量进入环境中,而由于其不易被降解,在环境中会长期存在。PFASs 通过多种途径进入土壤介质,如工厂污水排放、大气干湿沉降、含PFASs污水/污泥农用等[10]。某些PFASs(如短链的PFAAs)进入土壤后易被农作物吸收积累,通过食物链富集危害人体健康[11](图2)。PFASs 在土壤/沉积物-水中的分配、吸附/解吸作用是影响其在环境中的残留浓度、迁移、转化及生物可利用性、毒性等的重要因素之一,而环境中PFASs的迁移转化规律决定了其环境效应,是进行环境和健康风险评价的基础[12]。因此,PFASs在土壤中的吸附、解吸、迁移等过程会对其环境污染水平,乃至对植物或人体的毒性效应产生重要影响,明确PFASs 在土壤介质中的分布及归趋对人体的健康风险评估具有重要意义[13-16]。本文概述了土壤系统中PFASs的污染现状、吸附-解吸、迁移行为与影响因素以及对植物和人体的毒性作用,并对未来的研究方向进行了讨论与展望。
2 PFASs在土壤中的污染现状
近年来,国内外研究学者在土壤[17]、沉积物[18]、水体[19]甚至饮用水源[20]等多种介质中均检测到PFASs。其中PFOA、PFOS 是PFAAs 中检出率最高的两种全氟化合物[21],而新型多氟化合物如氯代多氟醚基磺酸盐(Cl-PFESAs)的检出也逐年增多[22-23]。土壤作为环境的重要载体,PFASs 在其中的污染特征和迁移行为不容忽视。世界许多国家和地区对土壤中PFASs 的污染现状进行了调查研究,通过对比部分国家及地区土壤中PFASs 的浓度分布(表1),发现其污染水平与工业化程度密切相关,污染物仍以传统的全氟化合物为主。新型多氟化合物随着使用量的增长在土壤中已有不同程度的检出,其环境问题需进一步关注。
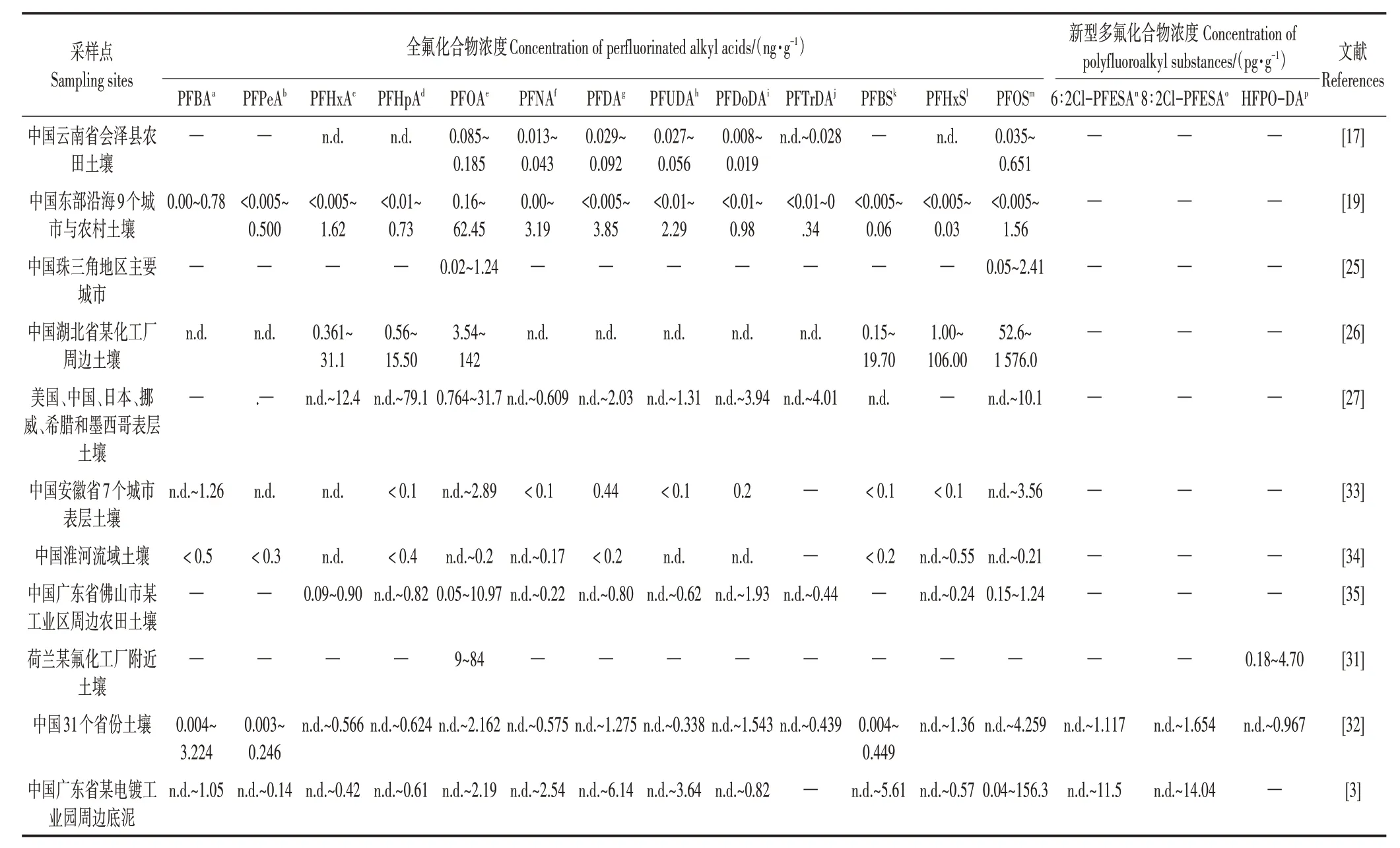
表1 部分国家及地区土壤中PFASs的浓度分布Table1 Concentration distribution of PFASs in soils in some countries and regions
2.1 土壤中全氟化合物的污染现状
目前国内外对全氟化合物在土壤环境中的分布已有大量报道。土壤中PFAAs 的污染程度和空间分布一般与当地工业化和城市化程度密切相关[24],工业发达地区的土壤PFAAs 污染更为严重。胡国成等[25]发现珠三角地区土壤中PFOA 与PFOS 总量在0.02~2.41 ng·g-1,其中东莞和深圳是全国主要的纺织、化工、电子等生产基地,大量产品生产以及工业废水的排放使土壤中的PFOA 和PFOS 平均浓度高于广州和珠海。值得注意的是,在氟化工厂及周边土壤中PFAAs 污染往往更严重。有研究发现[26]湖北某化工厂周边土壤中PFAAs 的总浓度为58.22~2 075.6 ng·g-1,主要污染物为PFOS,其次是PFOA 和全氟己烷磺酸(Perfluorohexanesulfonate,PFHxS),PFAAs 含量与距厂区距离呈显著负相关。相比之下,在工业发展程度较低的地区,土壤PFAAs 浓度则相对较低,与工业化城市土壤中PFAAs浓度最大可相差4~5个数量级。黄楚珊等[17]在云南省会泽县农田土壤中检出多种PFAAs,其中PFOA 和PFOS 作为主要的PFAAs,浓度范围分别只有0.085~0.185 ng·g-1和0.035~0.651 ng·g-1,远低于氟化工厂周边土壤的污染水平。此外,在全球范围内的表层土壤中,PFAAs 检出含量也较低,均值与国内土壤含量值相当,如STRYNAR 等[27]基于美国、中国、日本、挪威、希腊和墨西哥6 个国家的60个表层土壤样本分析,发现出现最频繁的PFAAs 依次为PFOS、PFOA、全氟十二烷羧酸(Perfluorododecanoic acid,PFDoDA)、全氟庚烷羧酸(Perfluoroheptanoic acid,PFHpA)和全氟己烷羧酸(Perfluorohexanoic acid,PFHxA),其中PFOA 与PFOS 最高浓度分别为31.7 ng·g-1与10.1 ng·g-1。综合来讲[28],羧酸类氟化物在土壤环境中的数量与浓度均大于磺酸类。不同地区土壤中各类PFAAs 组成比例存在差异,这与当地环境条件、经济发展和生产结构息息相关。
2.2 土壤中新型多氟化合物的污染现状
多氟类化合物种类繁多,使用量也在与日俱增。国内外学者目前更倾向于关注新型多氟化合物在水体环境[29]与生物体内[30]的相关研究,对土壤环境中多氟类物质相对关注较少。尽管如此,近年来国内外对于土壤的调查分析研究也渐渐涌现。总体而言,大部分新型多氟化合物在土壤中的赋存浓度不足传统型PFAAs的千分之一,其分布规律在空间上并未有太大差异。在荷兰某城市表层土壤中GenX 浓度在180~4 700 pg·g-1,处于较低水平,虽然GenX已被用来替代PFOA,但其检测浓度和频率还远不及PFOA[31]。在国内31 个省份的土壤中检测出更低水平的新型多氟化合物[32],其中6∶2 Cl-PFESA、HPFO-DA和全氟环己烷磺酸盐(Perfluoroethylcyclohexane sulfonate,PFECHS)的检出率分别为98.9%、40.5%和27.0%;6∶2 Cl-PFESA 的平均浓度最高(156 pg·g-1,与PFOS 浓度相近),占所检测到的新型PFASs 总量的65.5%,而8∶2 Cl-PFESA 的浓度不到前者一半(60.5 pg·g-1),HFPO-DA和PFECHs 的平均浓度分别为19.1 pg·g-1和2.31 pg·g-1,仅占新型PFASs总量的极少部分。我国多氟类化合物的低检测含量可能与还未完全限制使用PFOA、PFOS 有关,因此短时间内多氟替代物浓度并未提高。但目前6∶2 Cl-PFESA 为主的新型PFASs 的高检出率表明目前国内地区已开始使用这种替代品[29]。较全氟化合物而言,新型多氟化合物在远离氟化工厂的土壤介质中的含量更低,甚至可以忽略不计。随着现代化生产与使用的大幅增加,新型多氟替代物在土壤环境的赋存浓度总体呈上升趋势。近年来关于土壤中新型多氟替代物污染水平、分布特征研究仍处于初始阶段,相关研究仍占少数,后续可有针对性地加强探究。
3 PFASs在土壤中的环境行为及其影响因素
3.1 PFASs在土壤中的吸附机理
PFASs 进入环境后,首先会被吸附在环境介质上。PFASs 在土壤介质中的迁移行为以及生物有效性很大程度上取决于其在土壤中的吸附-解吸过程,进而对其在环境中的归趋产生重要影响。
PFASs 在土壤中的吸附是一个复杂的过程,且因PFASs 具体种类而存在差异。吸附机理[12]一般包括以下4 种(图3):(1)疏水作用。CHEN 等[36]和MILINOVIC 等[37]认为对于PFAAs 而言,疏水作用在其土壤吸附过程中占主导作用,而这主要源于土壤中有机质的贡献,天然有机质的组成和结构差异对PFASs在土壤中的分配及迁移有巨大影响。同时PFAAs 又含疏水性C—F 链,这使得它们更易与土壤有机质结合产生疏水作用而被吸附。(2)静电作用。对于PFAAs,例如全氟壬酸(Perfluorononanoic acid,PFNA),可与带负电荷的土壤颗粒产生静电斥力,从而减少土壤对其的吸附量[38]。尤其是对某些阳离子新型多氟化合物而言,如全氟辛酰胺铵盐(Perfluorooctaneamido ammonium salt,PFOAAmS)和全氟辛烷酰胺基甜菜碱(Perfluorooctane amidoalkyl betaine,PFOAB),因其Koc值(土壤有机碳标准化分配系数,指化合物在水和沉积物-土壤两相中的平衡浓度关系)较大,静电作用较强,疏水作用的影响并不明显[38]。而新型多氟化合物的吸附机理也与静电作用有关,CHEN 等[39]发现与PFOS相比,F-53B 更容易与酸性土壤中带正电荷的位点发生静电吸附作用,因此更容易被土壤吸附。(3)离子交换作用。胡桂林等[40]通过探究K+浓度对腐植酸(Humic acid,HA)吸附PFOA 的影响,发现大量K+可聚集形成外层复合物和压缩双电层并占据HA 表面的吸附位点,导致PFOA 的吸附量下降,这说明离子交换作用也是影响吸附过程的重要因素。(4)表面络合、配体交换作用。GAO 等[41]发现PFOA 可能通过配体交换作用取代铁铝氧化物上的羟基而发生吸附。另一方面,铁/铝氧化物还可为PFOA 吸附提供正活化位点,达到静电吸附效果。与之类似,XIAO 等[38]发现PFOAB 和PFOA 均含一个羧基基团,可与土壤中铁/铝氧化物形成络合物;PFOS 的替代物F-53B 在土壤中的吸附量也被证实与土壤中Al2O3和Fe2O3等金属氧化物和土壤有机碳含量呈正相关,这表明配体交换和表面络合作用也可促进F-53B 在土壤中的吸附过程[42]。
基于目前国内外已有研究,在上述4 类吸附机理中,疏水作用和静电作用是土壤吸附PFAAs 的主导机理,其他作用的贡献则较少[36-37,41-43]。目前,针对传统PFASs 在土壤中的吸附-解吸的研究相对关注较多,也取得了一些进展,但随着新型PFASs(如一些新兴替代物)的不断出现,因结构改变,其在土壤中的吸附-解吸行为仍需进一步探索。
3.2 PFASs在土壤中的迁移行为
污染物在土壤中的迁移,主要体现在其进入土壤表层下的包气带后发生一系列作用,一部分被吸附截留在土壤中,一部分则通过化学反应转化或降解,且相关性质发生变化。因此,充分了解PFASs在土壤介质中的迁移行为对于评估其环境影响和潜在风险至关重要。
PFASs 在土壤中的吸附截留对其在土壤中的迁移转化具有重要影响。近年来许多研究表明,有机质与土壤矿物对土壤吸附PFASs的影响明显,尤其是土壤矿物的多孔介质固相吸附对PFASs 起到主要截留作用。在PFASs的实验室模拟迁移试验中,由于土壤成分的复杂性,石英砂或石灰石常被用作主要的多孔固相介质来模拟土壤矿物对PFASs 迁移的影响。LV等[44]研究了PFOA在饱和石英砂和石灰石多孔介质中的截留和迁移情况,发现在相同溶液化学条件下,PFOA 在石灰石柱中的截留率(28.7%~48.4%)高于石英砂柱(几乎无PFOA 截留),原因在于PFOA 阴离子与带负电荷的SiO2砂粒之间存在静电斥力,导致SiO2表面几乎无法吸附PFOA,且石灰石比石英砂具有更小的负zeta 电位和更大的比表面积,可吸附更多的化合物。由于土壤是一个复杂的系统,单纯使用石灰石或石英砂来模拟PFASs在土壤介质中的迁移,无法厘清土壤中有机质及复杂矿物组分的影响,因此近年来针对实际土壤中PFASs 的迁移研究成为热点。XING等[45]通过饱和砂柱试验探究了PFOA 和PFOS 在饱和多孔介质中的不同传输行为和机理,发现PFOA 比PFOS具有更高的迁移率,这是由于PFOS的分子体积较大且含有磺酸基团,因此表现出更强的疏水性,更易于被吸附。在LYU 等[46]对PFOA 在3类土壤中迁移的研究中,黑土的有机质含量(2.57%)远高于沙漠土壤(0.05%),可通过疏水作用在土壤有机质表面吸附大量PFOA,从而使得PFOA 在黑土中的截留量提高,迁移率降低。而红壤中铝含量(26.90%)和铁含量(6.57%)又远高于沙漠土壤(铝:12.21%,铁:3.19%),因此红壤中PFOA 的截留率同样高于沙漠土壤。针对多氟类化合物如GenX在不同地区土壤介质中的截留与迁移行为的研究发现[47],固相吸附相较于空气-水界面吸附对GenX 截留贡献小,总体来看GenX 在土壤中依然具有显著的迁移能力。整体而言,天然土壤中的有机物和矿物等成分比石英砂和石灰石要复杂得多,导致不同类型土壤中PFASs的迁移行为和控制机制存在差异,因此应开展更多的研究工作,以了解PFASs在自然土壤系统中的迁移机制。
3.3 PFASs在土壤中吸附-迁移相关的影响因素
土壤吸附是影响PFASs 迁移的主要过程,并受PFASs 自身的结构、性质特点以及周围介质的物理化学(如土壤有机质含量和矿物组成等)、溶液化学(如pH、离子强度等)性质的影响(图3)。
3.3.1 PFASs分子结构
PFASs 分子结构(即碳链长度与官能团的差异)是影响它们在土壤中吸附-解吸特性的重要因素。全氟化碳链长度(一般在5~10)是影响PFASs 吸附的主要结构特性[48-50],且吸附量随着碳链长度的增加而增加。在链长为6~8 的全氟或多氟烷基同系物如PFOA 与PFDA、6∶2 FTSA 与8∶2 氟调聚磺酸(8∶2 fluorotelomer sulfonic acid,8∶2 FTSA)中也观察到类似的现象[51]。除全氟碳链长度外,MILINOVIC 等[37]发现PFOA、PFOS 二者的吸附量差异(PFOS>PFOA)还可归因于不同的功能性亲水基团。HIGGINS 等[52]也得出类似的结论,即磺酸基相对于羧基体积更大、疏水性更强,因此含有磺酸根的PFAAs 较含羧酸根的PFAAs 更易被吸附,且吸附效果更好。对于PFOA、PFOS 与其前驱体全氟辛烷酰胺基甜菜碱(Perfluorooctane amidoalkyl betaine,PFOAB)、全氟辛烷磺酰胺基甜菜碱(Perfluorooctane sulfonamidoalkyl betaine,PFOSB)、6∶2 氟调聚磺酰胺基甜菜碱(6∶2 fluorotelomer sulfonamidoalkyl betaine,6∶2 FTAB)、6∶2 FTSA而言,上述PFOSB 的固液分配系数(Soil-water distribution coefficient,Kd)最高,PFOAB 最低[51],这是由于PFOAB 比PFOS 或6∶2 FTAB 少一个脂肪族碳原子(PFOAB 含7 个),导致PFOAB 疏水效应较小或范德华力相互作用较弱,而且PFOAB 结构式中与全氟烷基链相邻的羰基占据的体积比磺酸基小,这种空间结构的差异可能是PFOAB疏水性较弱的主要原因。
3.3.2 土壤理化性质
土壤理化性质,例如表面电荷、pH、离子强度、阴/阳离子交换量(Anion/cation exchange capacity,AEC/CEC)和土壤组成等,也会影响PFASs 的吸附-解吸行为。大多数土壤是含有可变和恒定电荷胶体的混合物,它们的比例控制着土壤的净表面电荷特性。对于PFAAs(阴离子型PFASs)如PFOS、PFOA 和PFHxS 而言,当土壤pH 下降时,土壤净表面负电荷随之减少,吸附量增加[53],这是由于高表面负电荷会排斥PFASs带负电荷的核心官能团,进而减弱其与带正电荷的土壤颗粒表面之间的静电吸引。而且部分有机物的Kd值也会受pH 值影响,从而影响土壤吸附,如BARZEN-HANSON 等[54]发现8∶2 FTSA 的Kd值会随pH 的增加而降低。此外,阴/阳离子交换量对土壤吸附PFASs 的影响也与污染物的特性有关,如于路伟等[55]研究发现短链PFCAs 较强的离子特性可以使其与土壤中部分阴离子产生离子交换作用,从而增加土壤的吸附量,因此,土壤CEC 对短链PFCAs(C1~C6)的吸附无显著性影响,但土壤AEC 却与其吸附量呈显著正相关。另一方面,污染物在不同粒径土壤上的吸附能力变化趋势较为相似,即比表面积和孔径越大吸附容量越大。同时,较大的孔径结构能提供足够的空间来容纳PFASs 分子聚集[36,55]。如CHEN 等[36]系统地研究了土壤不同粒径组分对PFOA 的吸附。结果表明不同土壤粒径组分因有机质含量、阳离子交换量、孔体积等理化性质的差异而对PFOA 表现出不同的吸附能力(吸附量的大小关系为:腐殖质>黏粒>细粉粒>粗粉粒>细砂粒>粗砂粒)。其中,有机质和阳离子交换量是决定各土壤粒径组分吸附贡献的关键理化因素。PFAAs在土壤中的吸附量不仅受pH值的影响,也与离子强度成反比[40],说明土壤对PFAAs 的吸附受多种理化性质调节。总体而言,影响土壤吸附PFASs的主要因素包括有机质、AEC/CEC、pH、铁氧化物和黏粒含量等[55-56]。
3.3.3 土壤有机质与土壤矿物
土壤中有机质(OM)和金属矿物被认为是影响土壤吸附PFASs的两个极其重要的成分,其中有机质中的腐植酸(HA)是影响土壤吸附长链PFASs 的重要因素,而矿物则在极性有机化学物质的迁移中起着重要作用。腐植酸因含有酚羟基、醇羟基、羧基和羟基等大量活性基团,可以为污染物的吸附提供更多结合位点,因而对环境中污染物的迁移转化有着至关重要的影响[57]。JIA等[58]和UWAYEZU 等[59]均证实了PFOS可以大量吸附于沉积物中的腐植酸上,这表明腐植酸对PFOS 具有较强的吸附作用,而且,UWAYEZU 等[59]还发现腐植酸可与铁氧化物形成配合物并通过静电和疏水作用对PFOS 产生较强的吸附效果[60]。此外,土壤中的溶解性有机质(DOC)可以促进PFASs解吸,从而使其转化成更易迁移的脱附态[46,59]。XIANG 等[61]研究发现,土壤中小分子有机酸(草酸)可有效溶出土壤有机矿物配合物和金属离子,并形成草酸金属复合物,从而降低PFOA 在土壤吸附过程中的疏水作用力、配体交换作用和阳离子桥作用,进而促进PFOA解吸。在矿物对PFASs的吸附方面,矿物表面主要是通过静电作用、氢键、离子络合作用、配体交换作用对PFASs 进行吸附[62]。ZHAO 等[63]发现由于具有相似的矿物表面电荷特性,蒙脱石、高岭石与赤铁矿3 种矿物对同一PFASs 具有相似的吸附能力,一般而言,如果吸附剂具有相似的表面性质,吸附剂的吸附容量与其比表面积成正比。而有研究[63-64]表明,在中性pH环境下蒙脱石基本层带负电、层间带正电,高岭石与赤铁矿带负电,因此静电吸引只存在于蒙脱石与PFASs 之间,而PFASs 则通过氢键与赤铁矿发生吸附[41]。另外,某些矿物(例如Al2O3)也可能含有负电荷从而与PFASs产生静电排斥作用,但研究表明部分具有硅氧烷表面的矿物(如石英)可以克服上述作用而吸附PFASs[64]。此外,金属络合特性也会对矿物吸附PFASs的能力产生影响,羟基化金属阳离子的表面络合能力顺序为:Fe3+>Al3+>Pb2+>Ca2+>Mn2+>Mg2+[65],可较好解释赤铁矿(含铁)对PFAAs 的吸附亲和性高于蒙脱石和高岭石(含铝和锰)的现象,尤其是对PFSAs 的吸附亲和性相对高于PFCAs。而对于新型多氟化合物,金属氧化物在吸附过程中也发挥重要作用。例如WEI等[42]探究了金属氧化物对PFOS的替代物F-53B在土壤中的吸附影响,发现F-53B可通过配体交换取代铁/铝氧化物上的羟基,从而通过络合反应发生吸附,其吸附量与Fe2O3和Al2O3含量呈正相关关系。此外,磺酸基团也可以与矿物表面的金属离子络合,促进土壤对F-53B 的吸附,从而减少迁移。目前对PFASs(尤其是新型替代品)在环境中的迁移特性依然知之甚少,后续需深入了解PFASs在土壤环境中迁移的潜在危害及其对地下水的影响。
4 作物累积与健康风险
土壤-作物系统中PFASs污染主要来源于田间污水灌溉或污泥农用,由此通过农作物根系进入可食部位,经食物链进入人体,危害人体健康(图2)。
4.1 PFASs在作物中的累积与生态风险
近年来有不少关于植物吸收累积PFASs 机理的研究。PFASs 可以通过空气或颗粒在地表的沉积进而被植物叶片吸收[66]。然而,在大多数情况下,根系吸收是大多数PFASs进入植物体内的途径,同时将其转移至地上部分和可食用部位[67]。ZHAO 等[68]发现新型PFASs 如1H,1H,2H,2H-氟聚磺酸(6∶2 fluorotelomer sulfonate,6∶2 FTS)和6∶2 Cl-PFESA 在植物根系中蓄积的浓度远高于地上部分,这种根系蓄积取决于物质本身在土壤中的生物可利用性,疏水性越强的物质,生物可利用性越低。PFASs 在农作物中的累积还与其碳链长度有关。MCLACHLAN 等[69]认为碳链较短的PFCA 和PFBS 易通过植物的蒸腾作用向上运输,而其他碳链较长的PFCAs 则被土壤大量吸附。KRIPPNER 等[70]研究了10 种PFASs(C4~C10)在玉米幼苗中的累积情况,发现幼苗倾向于在地上部中积累C4~C7的PFCAs与全氟丁烷磺酸(Perfluorobutane sulfonate,PFBS)等短碳链PFASs,而碳链较长的PFASs则倾向于在根中被截留。LIU等[71]发现小麦和玉米籽粒中主要富集短链PFCAs(特别是PFBA),PFASs 在两种谷物中的生物富集系数(Bioaccumulation factor,BAF)随碳链长度的增加而降低;与玉米籽粒相比,小麦籽粒表现出较高的BAF 值,可能与其较高的蛋白质含量有关。STAHL 等[72]对生长在PFOA 和PFOS 污染土壤(0~50 mg·kg-1)上的春小麦、燕麦、土豆、玉米和多年生黑麦草进行调查,发现PFOA 和PFOS 在所有受试植物中均有累积,且PFOA 浓度普遍高于PFOS,说明相对于PFSAs,PFCAs 更易被植物吸收累积(PFCAs 的BAF 值一般高于PFSAs)[73]。PFASs 可通过不同的跨膜运输方式进入植物体内,分子量小的不带电荷和非极性物质,容易通过扩散作用跨过细胞膜进入植物体内,而含有极性基团的物质,其跨膜运输需要蛋白质作为载体。WEN 等[74]探究了玉米吸收PFOA和PFOS的载体介导过程,结果显示PFASs的跨膜运输主要涉及蛋白质载体的主动或被动运输过程。ZHANG 等[75]认为小麦吸收PFAAs 的主要机制是以蛋白质为载体的需要耗能的主动吸收运输过程,而TFAA和PFPrA的吸收分别受到某些阴离子通道阻滞剂和水通道蛋白抑制剂的抑制,这表明超短链PFAAs的吸收也与这两个通道有关。此外,大量研究表明植物吸收累积PFASs 与其碳链长度有关[66,72-75],其中长碳链PFASs 容易在根中富集,难以向茎叶运输,而短碳链PFASs容易向地上部迁移转运,并可以在蒸腾作用下通过韧皮部运输并贮存在叶片中。
作物体内积聚一定量的PFASs 便会产生毒害作用。例如LI 等[76]研究了PFOA 和PFOS 在代谢水平上对生菜的毒害效应,发现生菜生物量受PFOA 和PFOS影响甚微,但叶片氨基酸代谢相关途径(如苯丙氨酸代谢、酪氨酸代谢和苯丙氨酸、酪氨酸和色氨酸的生物合成等)却受到PFOA 的干扰。酪氨酸和苯丙氨酸可产生大量抗氧化剂(如黄酮类、酚类和木质素类)清除活性氧自由基,若酪氨酸和苯丙氨酸的合成受阻,则无法去除由PFOA 或PFOS 引起的活性氧自由基的累积而导致抗氧化防御系统受损。相比于被逐渐限制使用的传统PFAAs,新型PFASs的出现虽然缓解了需求,但是否会产生更大的毒害效应仍未可知。目前关于新型PFASs 对农作物毒害机理研究只有零星的报道。LIN 等[77]比较了PFOS 与其替代产品F-53B 对小麦幼苗的生理影响,发现低浓度(1~25 mg·L-1)的F-53B 处理组可轻微促进根系生长,但在高浓度(250 mg·L-1)时,相对于PFOS 处理组,小麦生物量和叶片光合色素含量分别降低了24%~30%和0.4%~18.0%,这是由于F-53B 诱导会产生更高的根膜通透性、活性氧和丙二醛含量,并降低抗氧化酶活性和谷胱甘肽含量,从而使小麦细胞抗氧化防御系统受到损伤和破坏。由此可见,F-53B 作为PFOS 替代品,长期暴露可能会对环境构成更高的生态风险。
4.2 PFASs暴露与健康风险
大量的研究表明,通过农作物摄入已成为人体暴露PFASs的主要途径[66,78],而在荷兰、比利时、捷克、意大利、挪威和中国等地,食用蔬菜已成为人体暴露PFOA/PFOS 的主要途径[79-80],KLENOW 等[81]的研究也表明食用蔬菜不仅成为人体暴露PFOA 的首要途径,亦是PFHxA 的首要暴露途径,其暴露量最高可达人体总暴露量的69%。此外,通过食用以被PFASs污染的作物为食的牲畜产品,从而间接摄入PFASs,也是人体暴露PFASs 的重要途径[70,82]。可见土壤-作物系统中PFASs的污染与健康风险较为严峻。一般而言,大多数PFASs在进入人体后较难去除,PFOA 和PFOS的人血清半衰期分别为3.8 a 和5.4 a,PFHxS 预测为8.8 a[83],含有醚键的Cl-PFESA 是人类已知的最具生物持久性的PFASs,总消除半衰期长达15.3 a[84]。毒理学研究表明PFASs累积会对人体器官、系统等产生极大的毒性效应[63,73,82]。而且大量研究表明PFASs 已成为人体多种疾病甚至癌症的潜在诱因。如STANIFER 等[85]观察到PFASs 暴露会导致肾功能降低,甚至引起与肾脏疾病相关的代谢途径失调现象。同时PFASs 还会对机体的免疫系统产生毒害作用,导致溃疡性结肠炎、儿童哮喘等相关疾病的发生[86]。此外,有研究发现,相较于传统的PFASs,一些新型PFASs表现出更强的毒性效应,如SHENG 等[87]研究发现HFPO-DA 的肝脏毒性强于PFOA,此外,与PFOA、PFOS 相比,6∶2 FTSA、HFPO-TA 及6∶2 Cl-PFESA 等新型PFASs 可对人胚胎干细胞系(HL7702)产生更强的细胞毒性,还可能导致生殖和发育异常[4]。SØRLI等[88]发现PFBS、PFHxS 等短链替代物与PFOA、PFOS等传统PFAAs 一样,均对人体呼吸系统表现出一定的毒性效应。近年来,欧洲食品安全局(EFSA)和美国环保署(EPA)先后降低了人体对PFOA 和PFOS 的日可耐受剂量的参考值,与之前的参考值相比下降了4~1 800 倍[82,89-90],由此可见PFASs 的健康风险问题日趋严峻。
5 结论与展望
本文综述了近年来土壤环境中PFASs 的污染现状、吸附迁移行为与毒性效应等方面的研究进展,为科学有效评估PFASs 在土壤中的环境行为与生物有效性提供参考。目前PFASs 在土壤环境与生命体内的污染仍然以PFOA、PFOS 为主,新型多氟化合物的污染问题也逐渐显现。不同种类、结构的PFASs在土壤介质中的环境行为具有差异性,其吸附-解吸行为受到疏水作用、静电相互作用、配体交换等多种机理控制。受土壤环境与土壤组分等多种因素影响的PFASs 吸附过程同时决定了其在土壤中的迁移和归趋。PFASs 通过生物富集和生物放大作用蓄积于生物体内。
多氟化合物尤其是一些新型替代物的不断涌现逐渐受到研究者的关注,相关研究主要集中在水体环境中的污染现状和毒理效应,其在土壤中的吸附、迁移等行为及相关机制的研究相对较为薄弱。未来本领域的探索可从以下几方面着手:
(1)目前对于土壤中的PFASs迁移研究大多介于两相界面,土壤作为固-液-气三相的系统,需加大力度深入开展PFASs(尤其是新型多氟化合物)在实际土壤三相界面上的迁移转化规律研究;
(2)虽然土壤环境介质中PFASs 的浓度水平较低,但由于PFASs 的难降解特性,会在土壤中长期赋存,进而通过作物富集在人体,因此,有必要考虑低浓度长期暴露条件下PFASs对生物体的毒性影响;
(3)PFASs 在实际土壤环境中通常以复合污染的形式存在,因此需深入研究不同种类、结构的PFASs在土壤中的交互效应与作用机制,进而深入探究植物对这些PFASs 吸收累积差异。厘清这些更有利于探究环境中共存的污染物的潜在风险,为PFASs的生态风险评估提供更准确的参考。