二代测序在Meckel综合征植入前遗传学检测的应用
何天文 区惠红 卢建 陈创奇 刘顿 丁红珂 刘玲 杜丽 尹爱华★
Meckel 综合征(meckel syndrome,MS)是由德国解剖学家Meckel 等在1822年首次报道的一种罕见的致死性常染色体隐性遗传病,临床上以枕部脑膨出、严重的多囊肾和轴后多指(趾)畸形等为主要特征[1-2]。Meckel 综合征预后差,胎儿常发生宫内死亡,出生的胎儿大多仅能存活数天至数周,且目前还无根治的方法,植入前遗传学检测和产前诊断是预防Meckel 综合征患儿出生的有效方法。近年来,二代测序(next generation sequencing,NGS)技术飞速发展,已经成为胚胎植入前遗传学检测(preimplataion genetic testing,PGT)的主要检测手段之一[3]。NGS 能检测染色体非整倍性、染色体结构异常和单基因遗传病,准确性好且精度高[4-5]。本研究运用NGS 对胚胎MKS1基因突变直接测序和构建胚胎单核苷酸多态性(single nucleotide polymorphisms,SNP)单倍型进行PGT,以期避免妊娠Meckel 综合征和非整倍体胎儿。现报道如下。
1 资料与方法
1.1 研究对象
男方(Ⅱ:1),35 岁,表型正常,既往体健。男方父母(Ⅰ:1 和Ⅰ:2)表型正常,既往体健。女方(Ⅱ:2),34 岁,表型正常,既往体健,怀孕2 次,生产0 次,流产2 次,2014年孕25 周时超声发现羊水过少行引产术,未进一步进行相关基因检测;2016年孕19 周时超声提示胎儿(Ⅲ:1)枕骨缺如、脑膨出、心包积液、三尖瓣反流、肝回声增粗、双侧多囊肾、左侧胫骨骨折、双足轴前多趾等多种畸形,在外院行引产术,外院芯片捕获高通量测序结果显示胎儿MKS1基因c.472C>T 纯合突变,该突变在数据库中有疾病相关性报道[6]。女方父母(Ⅰ∶3 和Ⅰ∶4)表型正常,既往体健(图1)。为了再次避免妊娠患儿,该夫妇于2017年5月在广东省妇幼保健院就诊咨询要求行PGT。该夫妇充分了解PGT 过程及相关风险后,签署知情同意书接受PGT。本研究经广东省妇幼保健院生殖医学伦理委员会批准。

图1 Meckel 综合征家系图Figure 1 Pedigree of Meckel syndrome
1.2 主要试剂与仪器
磁珠法血液基因组提取试剂盒(天根生化科技有限公司),微量样本全基因组扩增(MDA 法)试剂盒(北京中仪康卫医疗器械有限公司),胚胎植入前单基因病检测建库试剂盒(北京中仪康卫医疗器械有限公司),测序反应通用试剂盒、胚胎植入前单基因病检测标签接头试剂盒(北京中仪康卫医疗器械有限公司),胚胎植入前染色体非整倍体检测试剂盒(北京中仪康卫医疗器械有限公司),QUBIT 1X 双链DNA 高灵敏度分析试剂盒(北京中仪康卫医疗器械有限公司),核酸定量计Qubit Fluorometer(Invitrogen 公司,美国),verity 梯度PCR 仪、ABI3730 测序仪(ABI 公司,美国),MiSeq 高通量测序仪(Illumina 公司,美国)。
1.3 方法
1.3.1 标本采集及基因组DNA 提取
分别抽取夫妇(Ⅱ:1 和Ⅱ:2)及双方父母(Ⅰ:1、Ⅰ:2、Ⅰ:3 和Ⅰ:4)外周血各2 mL,EDTA 抗凝。Ⅱ:2 孕18~24 周时在超声引导下行羊膜腔穿刺术抽取胎儿羊水5~10 mL。磁珠法血液基因组提取试剂盒提取外周血基因组DNA,Qiamp DNA Blood Mini Kit 提取试剂盒提取羊水基因组DNA,均按试剂盒说明书进行操作。
1.3.2 Sanger 测序调查家系成员MKS1基因突变情况
用Oligo6 设计针对MKS1基因c.472C>T 突变位点的特异性PCR扩增引物(F:5′-TCTACCAAGCACACTAACCC-3′,R:5′-TCCCTCTCTCTGAGGCAC-3′,扩增片段位于chr17:56291905-56292495,扩增片段长度为591 bp),PCR 扩增产物用ABI3730 遗传分析仪进行序列测定。用SeqMan软件对ABI3730 遗传分析仪生成的ab1 测序结果文件进行分析,调查家系成员携带MKS1基因c.472C>T 突变情况。
1.3.3 家系成员单倍型的构建
以MKS1基因(NM_017777.3 chr17:56282797-56296966)反向转录编码区为目标,在该基因上下游2 M 区域内(chr17:54576882-58218653)选择200 个SNP 位点作为遗传连锁标记,利用ION AMPLISEQTM DESIGNER 网站设计多重PCR 引物,对提取的家系成员的基因组DNA 进行多重PCR,多重PCR 产物经纯化和建库后行NGS,选择有效SNP 位点进行构建家系成员的SNP 单倍型进行连锁分析,确定携带MKS1基因c.472C>T 突变的风险染色体。
1.3.4 胚胎活检
根据常规体外培养方法[6],首先采用卵细胞浆内单精子注射(intracytoplasmic sperm injection,ICSI)方式进行授精,待胚胎培养至第5/6 天,活检囊胚滋养层细胞2~9 个进行遗传学检测。
1.3.5 植入前遗传学检测
对活检获得的滋养层细胞进行基于等温多重置换扩增(multiple displacement amplification,MDA)技术的全基因组扩增(Whole genome amplification,WGA)。利用WGA 产物通过多重PCR 扩增胚胎MKS1基因编码区和高密度紧密连锁的SNP 位点,多重PCR 产物经纯化和建库后进行NGS。通过NGS 对胚胎MKS1基因突变位点直接测序和构建胚胎SNP 位点单倍型连锁分析。通过Sanger 测序检测MKS1基因c.472C>T 突变验证二代测序结果。针对正常和杂合携带致病突变的胚胎进行了低深度的染色体非整倍性筛查,以排除有携带染色体拷贝数异常的胚胎。
1.3.6 产前诊断
于孕18~24 周时行羊膜腔穿刺进行胎儿染色体核型G 显带分析和Sanger 测序检测胎儿MKS1基因c.472C>T 突变,验证PGT 结果。
2 结果
2.1 家系成员携带MKS1 基因c.472C>T 突变情况
通过Sanger 测序分析,发现该家系成员中男方(Ⅱ:1)、女方(Ⅱ:2)、男方父亲(Ⅰ:1)和女方母亲(Ⅰ:4)携带MKS1基因c.472C>T 的致病性突变(图2)。引产胎儿(Ⅲ:1)外院结果显示MKS1基因c.472C>T 纯合突变,分别遗传自父亲和母亲(图1)。
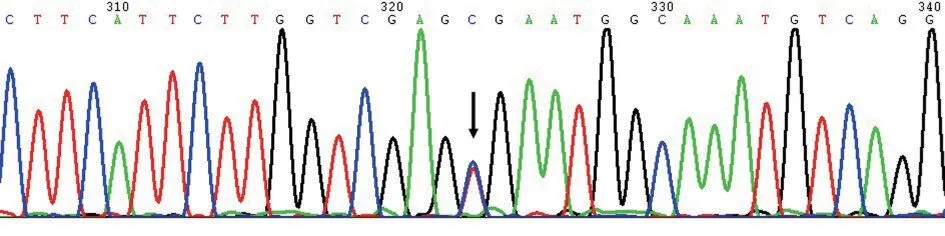
图2 MKS1 基因c.472C>T 突变Sanger 测序图Figure 2 Sanger sequencing of c.472C >T mutation in MKS1 gene
2.2 家系成员SNP 单倍型构建
经过多重PCR 和NGS 后,选择了74 个有效SNP 位点成功构建家系成员SNP 单倍型,成功确定夫妇的携带MKS1基因c.472C>T 突变的风险染色体。见表1、图3。

表1 夫妇有效SNP 位点数和分布Table 1 Number and distribution of effective SNPs in couples
2.3 植入前遗传学检测
第6 天活检6 个囊胚滋养层细胞分别标记为D601、D602、D603、D604、D605 和D606。胚胎 的MKS1基因c.472C>T 突变的NGS 结果、SNP 单倍型连锁分析结果和Sanger 测序结果提示6 个胚胎中D601、D602 和D603 为未检测到突变胚胎,D605 和D606 为杂合携带胚胎,D604为致病胚胎。D601、D602、D603、D605 和D606低深度的染色体非整倍体筛查结果显示D601为非平衡的整倍体胚胎,其它为平衡的整倍体。见图4、表2。

图4 胚胎SNP 单倍型分析结果Figure 4 SNP haplotype analysis results of embryos

表2 胚胎MKS1基因c.472C>T突变植入前遗传学检测结果Table 2 PGT results of c.472C>T mutation in MKS1 gene
2.4 产前诊断
选择正常且发育良好的整倍体胚胎(D602)进行移植,孕19 周经羊膜腔穿刺产前诊断结果显示胎儿染色体核型G 显带分析未发现异常,Sanger测序未检测到胎儿MKS1基因c.472C>T 突变,与PGT 结果一致,见图5。孕38 周顺产分娩一正常婴儿,体重2 690 g,健康状况良好。
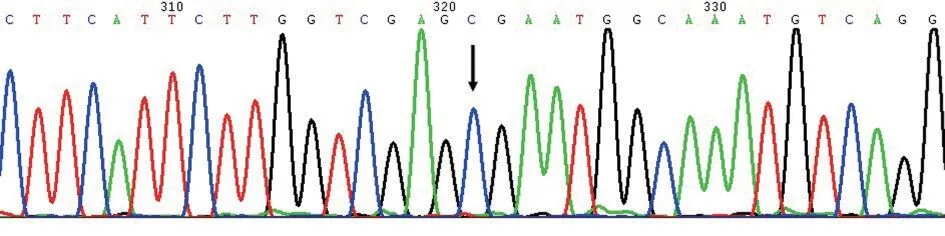
图5 胎儿MKS1 基因c.472C>T 突变的Sanger 测序图Figure 5 Sanger sequencing map of c.472C>T mutation in fetal MKS1 gene
3 讨论
Meckel 综合征是一种致死性常染色体隐性遗传病[7],发病率各国报道不一,以芬兰最高,约1/9 000 活产婴[8],我国仅见散发病例报道[9-10]。Meckel 综合征的临床表现比较一致,但是具有遗传异质性[11]。与Meekel 综合征相关的基因有多个,按基因定位发现的时间顺序分别称之为Meckel 综合征1~6 基因。2006年Kyttälä 等[12]利用基因克隆技术确定了MKS1基因定位于17q23,基因长13 869 bp,包含18 个外显子。本研究家系中引产胎儿为MKS1基因c.472C>T 纯合突变导致的Meckel 综合征,通过PGT 治疗后该夫妇分娩一正常婴儿,也再次验证了MKS1基因c.472C>T 突变的致病性。
日前,Meckel 综合征尚无有效的根治方法,植入前遗传学检测和产前诊断是预防Meckel 综合征患儿出生的主要手段。绒毛活检、羊水穿刺、脐带血穿刺传统的介入性产前诊断术具有创性,还具有一定流产风险[13]。Meckel 综合征携带者夫妇经产前诊断后确诊胎儿为Meckel 综合征后,需要选择终止妊娠,给孕妇带来一定的身体伤害和心理负担。对Meckel 综合征携带者夫妇进行胚胎植入前遗传学检测,在胚胎植入前进行遗传学分析后选择正常胚胎进行移植,可以避免异常胚胎妊娠的发生,阻断Meckel 综合征在家系中的再发风险。胚胎植入前遗传学检测将遗传病的预防提前到胚胎阶段,与传统的产前诊断相比具有明显的优势,可以避免可能的治疗性引产给母体带来身体和心理的创伤[6]。
随着基于MDA 技术的WGA 技术的发明,该技术克服了单细胞水平基因检测DNA 模板量过少的问题,极大地提高了检测结果的准确性和可靠性,但是WGA 有扩增不均匀和等位基因脱扣(allele drop-out,ADO)的风险[14]。NGS 技术的发明,实现了一次性对上百万条DNA 进行测序,不仅缩短了耗费时间,也将单碱基测序成本降至了最低,遗传性疾病的诊断率和分辨率迈入新的高度,给PGT 技术带来了革命性的改变[6]。NGS 具有高通量、高并行性和高分辨率等特性,二代测序技术可以提供高深度的多位点多基因分析,结合SNP 单倍型连锁分析,可以避免由ADO 带来的检测错误[15]。NGS 已经成为PGT 的主要的检测手段,其不但能检测染色体非整倍性、染色体结构异常和单基因遗传病,而且准确性好和精度高,与如荧光原位杂交和比较基因组杂交等传统的PGT 技术相比具有明显的优势。
本研究成功应用二代测序技术对遗传性Meckel 综合征家系进行植入前遗传学检测,可以阻断该单基因病在该家系中的再发风险,还可以避免选择非整倍体胚胎而导致的流产问题,是Meckel 综合征出生缺陷的有效预防手段。

