硫酸阿米卡星注射液上市后安全性及临床应用真实世界研究*
柯 英
四川绵阳四〇四医院 临床药学部,四川绵阳621000
阿米卡星(amikacin,AK)又名丁胺卡那霉素,是第三代半合成氨基糖苷类抗生素。用于需氧G-杆菌引起的感染性疾病的治疗,对许多肠道G-杆菌所产生的氨基糖苷类钝化酶稳定,不会因此类酶钝化而失去抗菌活性,作用于细菌核糖体的30S 亚单位,抑制细菌合成蛋白质[1]。该药抗菌谱较广,敏感性高,属于国家基本药物品种,临床应用广泛;但肾毒性是其限制性不良反应。为了解阿米卡星在真实世界中使用情况及其安全性,本研究纳入2017 年3月至2020 年12 月医院信息管理系统(HIS)中医嘱内容有关“阿米卡星”的共1103 例患者,分析其基本信息、给药剂量、合并用药以及不良反应等,了解阿米卡星临床使用和不良反应发生情况,从而进一步指导临床安全合理的使用。
1 资料与方法
1.1 研究对象
在医院信息系统(HIS)中,把医嘱内容包含“阿米卡星”的作为纳入条件,统计出2017 年3 月~2020 年12 月间共1103 例住院患者,收集其基本信息、诊断信息、医嘱信息、合并用药以及不良反应等内容。
1.2 分析方法
参照硫酸阿米卡星注射液说明书、《2012 年中国鲍曼不动杆菌感染诊治与防控专家共识》和《2014 中国产超广谱β-内酰胺酶肠杆菌科细菌感染应对策略专家共识》以及《铜绿假单胞菌专家共识》。采用频数分析法描述使用阿米卡星患者的年龄、性别、入院诊断、住院科室等基本情况。使用Clementine12.0 统计软件;采用Apriori 算法分析数据,它是一种挖掘关联规则的频繁项集算法,可对数据进行高效筛选、优化、整合。以支持度(A 和B这2 个项集在事务集中同时出现的概率)为主要参数,通过关联规则挖掘、发现大量数据中项集(药物)之间的关联或相关联系。同时将出现在数据库中的2 种进行分析合并,记录其支持度,筛选出所有支持度大于最小支持度的项集,统称为频繁项集,然后由频繁项集产生强关联规则,进而挖掘使用频率较高的合并用药方案[2]。
2 结果
2.1 患者基本信息
1103 例患者年龄跨度较大,从9 岁至98 岁不等,男性多于女性,见表1。
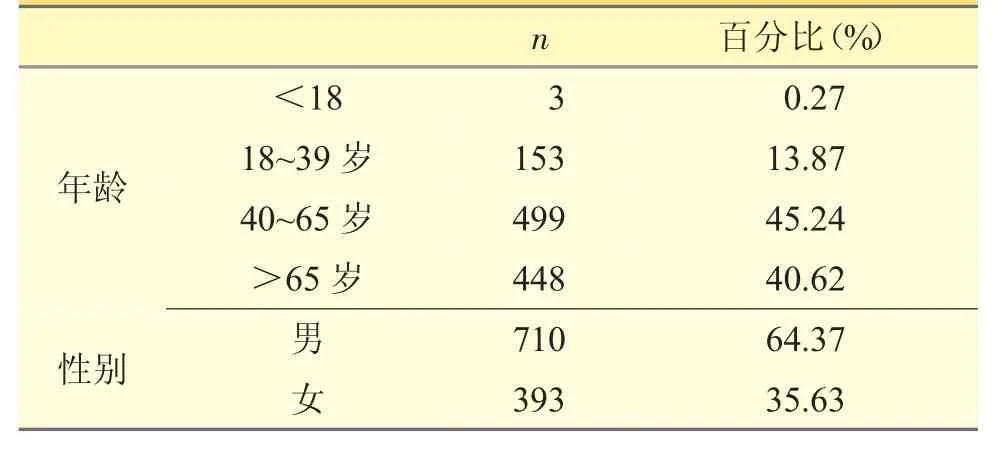
表1 使用阿米卡星的年龄、性别分布
2.2 科室分布情况
1103 例住院患者所在科室以感染科、呼吸科、ICU 为多,科室分布情况见表2。
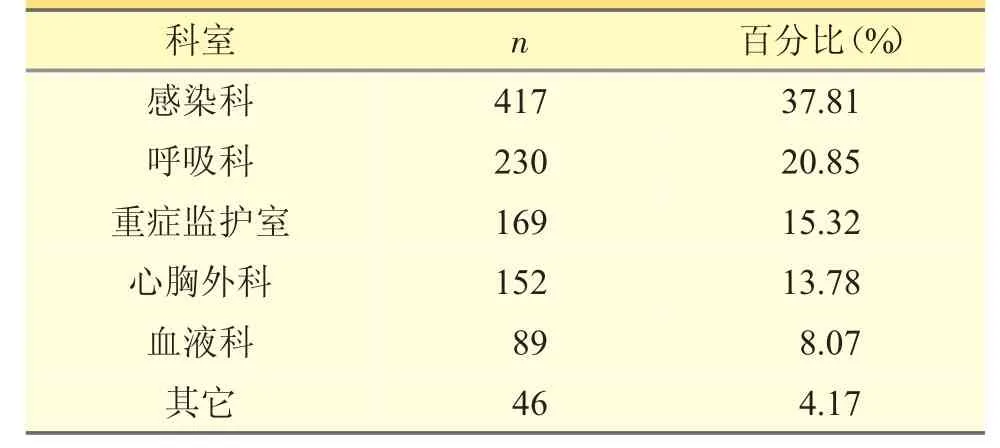
表2 使用阿米卡星的主要科室分布
2.3 阿米卡星用法用量及疗程
在统计数据中,阿米卡星用法包括全身给药1043 例(占94.56%)和局部给药60 例(占5.44%)。其中全身用药中包括静脉滴注1033 例和肌肉注射10 例;局部用药主要为纤维支气管镜下冲洗、结膜下注射和腹膜透析液中注射。
用药频次包括2 例q12h 给药,其余1101 例均为qd 给药。
溶媒选择以100~250 mL 0.9%NS 稀释的有800例(占72.53%);100~250 mL 5%GS 稀释的有204 例(占18.50%);5%GNS 稀释的有29 例(占2.63%)。
给药剂量有0.8、0.6、0.4、0.3、0.2、0.1 g 不等,其中用量为0.4 g 者最多、有838 例(占75.97%);其次为0.6 g 者有85 例(占7.71%);用量为0.8g 者有62例(占5.62%)。
用药疗程从1~79d 不等,其中1~10 d 有748 例(占67.82%);11~20 d 有242 例(占21.94%);21~30d有75 例(占6.80%);31~40 d 有25 例(占2.27%);41~50 d 有6 例;51~60 d 有3 例;61~70 d 有3 例,71~80 d 有1 例。疗程最长者79 天,为1 例45 岁耐药肺结核伴脑膜炎结核患者。
2.4 阿米卡星用量与年龄分布相关性
见表3。

表3 阿米卡星用量与年龄分布相关性
2.5 主要感染性诊断
根据HIS 系统诊断统计,共获得西医感染性诊断1103 条,排名前10 的诊断分别是:肺结核、肺部感染、慢性阻塞性肺疾病、感染性心内膜炎、支气管扩张伴感染、HIV、腹腔感染、肾盂肾炎、髋关节感染、肺脓肿。
2.6 合并用药
将合并用药定义如下:每例患者对应一个ID号,在每个ID 号中寻找阿米卡星的开始使用时间和停止使用时间,如果相同ID 号下,某种药物的开始使用时间在阿米卡星的使用时间范围内,则定义该药物属于阿米卡星的合并用药(溶媒、滴眼药、软膏不纳入合并用药分析)。
采用Clementine 建立阿米卡星与其他药物的关联分析模型,将与阿米卡星合并使用的药物定义为“前项”,合并用药数量可能是一种或多种,将阿米卡星定义为“后项”,支持度是在使用阿米卡星的人群中,使用“前项”的百分比越大,支持度越高,说明该合并用药或合并用药组合出现频次越高。与阿米卡星合并使用频率前5 位的药物分别是:左氧氟沙星、哌拉西林他唑巴坦钠、头孢哌酮他唑巴坦、替卡西林克拉维酸、美洛西林舒巴坦。见表4。

表4 使用阿米卡星的合并用药情况(n=例)
2.7 不良反应
在1103 例使用阿米卡星患者中,有41 例出现不同程度血肌酐进行性升高、尿量减少和血尿,排除10 例既往有肾功能不全的病例,有31 例可能与阿米卡星使用有相关性,其发生率为2.81%。
在31 例出现血肌酐升高、尿量减少和血尿患者中,男性有21 例,女性有10 例,年龄在62 岁~80岁;其中出现血肌酐升高的有15 例,出现尿量减少的有8 例,同时合并出现血肌酐升高和尿量减少的有5 例,出现血尿的有3 例;使用剂量0.4 g 有19例,0.6 g 有8 例,0.8 g 有4 例;用药疗程5~14 d 不等,最长者14 天。
3 讨论
3.1 阿米卡星的适应症分析
阿米卡星是一种氨基糖苷类抗生素,适用于铜绿假单胞菌及其他假单胞菌、大肠埃希菌、变形杆菌属、克雷伯菌属、肠杆菌属、沙雷菌属、不动杆菌属等敏感革兰阴性杆菌与葡萄球菌属(甲氧西林敏感株)所致严重感染,如菌血症或败血症、细菌性心内膜炎、下呼吸道感染、骨关节感染、胆道感染、腹腔感染、复杂性尿路感染、皮肤软组织感染等[3]。
本统计数据显示,重症感染、脓毒症休克、血液疾病合并感染以及免疫力低下患者容易感染耐药菌。《2012 年中国鲍曼不动杆菌感染诊治与防控专家共识》和《2014 中国产超广谱β-内酰胺酶肠杆菌科细菌感染应对策略专家共识》以及《铜绿假单胞菌专家共识》均提及联合氨基糖苷类有明显的协同效应,尤其对CRE 的治疗。本院是绵阳市传染病治疗中心,结核患者比较集中,近年来耐药结核越来越多,关于耐药结核菌,《2016 年WHO 耐药结核病治疗指南》明确规定,阿米卡星、氟喹诺酮类等为二线抗结核替代药物。在本次统计数据中,有267 例诊断有结核患者使用阿米卡星,包括不耐受HRZE 标准化疗方案选择阿米卡星替代治疗和耐药结核患者,其治疗符合诊疗规范;但该类患者因使用疗程较长,使用过程中应进行血药浓度监测,以保证其用药安全性和有效性。
3.2 阿米卡星的用法用量分析
硫酸阿米卡星注射液说明书要求成人肌内注射或静脉滴注。本次统计数据有60 例局部给药,在局部用药中,纤维支气管镜下冲洗、结膜下注射均为超说明书用药,需加强宣教和管理,减少不合理用药和规避医疗风险。
硫酸阿米卡星注射液的用量用于全身感染每12 h 7.5 mg·kg-1,或每24 h 15 mg·kg-1。成人一日不超过1.5 g,疗程不超过10 天。本统计数据显示,93.11%患者未在说明书规定的剂量范围内使用,存在剂量偏低。该药为浓度依赖性抗菌药物,根据PK/PD 理论,主流观点均建议1 日1 次给药,一方面提高疗效,另一方面可降低不良反应。本次研究中发现,有个别病例每日多次给药情况,而且给药剂量均未按说明书推荐剂量用药,估计与临床顾虑其肾毒性相关。但目前未见研究阿米卡星肾毒性发生与剂量、疗程及基因的相关性的有关文献,这方面需要深入研究。
硫酸阿米卡星注射液的配制要求每500 mg 加入氯化钠注射液或5%葡萄糖注射液或其他灭菌稀释液100~200 mL。成人应在30~60 min 将上述溶液缓慢滴入,应给予患者足够的水分,以减少肾小管损害[4,5]。本统计数据显示,少部分患者存在溶媒量偏低现象,应引起临床重视。
3.3 阿米卡星的合并用药分析
本统计数据显示,阿米卡星临床多与哌拉西林他唑巴坦、头孢哌酮舒巴坦、头孢哌酮他唑巴坦、美洛西林钠舒巴坦、左氧氟沙星等药物联用。相关研究证明,阿米卡星与抗菌药物等联用能起到协同作用,从不同环节有效抑制或杀灭细菌生长,提高临床疗效。在临床使用中,阿米卡星联用药物较多,应密切关注其疗效,注重合并用药带来的收益与风险。需注意氨基糖苷类与β-内酰胺类(头孢菌素类与青霉素类)混合时可导致相互失活,与上述抗生素联用时必须分瓶滴注。阿米卡星也不宜与其他药物同瓶滴注。
3.4 阿米卡星的不良反应分析
阿米卡星注射后可在肾脏皮质细胞和内耳液中蓄积,而且主要经过肾小球滤过排出,有一定耳肾毒性。本研究中主要通过监测肾功能变化,尿量监测,间接反映阿米卡星在使用过程中肾毒性等不良反应。在1103 例使用阿米卡星患者中,有41 例出现不同程度血肌酐进行性升高、尿量减少和血尿,排除10 例既往有肾功能不全的病例,有31 例考虑与阿米卡星使用有相关性。相比已报道的阿米卡星所致不良反应中,最多的为肾毒性,患者出现血尿,排尿次数减少或尿量减少,血尿素氮、血肌酐值增高等,这些症状基本一致。其大多可逆,停药后即见减轻,但亦有个别出现肾功能衰竭的报道[6,7]。其他不良反应,患者可发生听力减退、耳鸣或耳部胀满感;少数患者亦可发生眩晕、步履不稳等症状。关于听力减退,一般于停药后症状不再加重,但个别在停药后可能继续发展至耳聋,更应强调血药浓度监测的重要性和必要性。
在阿米卡星用药过程中,应注意进行下列检查:①尿常规和肾功能测定,以防止出现严重肾毒性反应;②需作听力检查或听电图检查,尤其注意高频听力损害,这对老年患者尤为重要;③疗程中有条件时应监测血药浓度,尤其新生儿、老年和肾功能减退患者。一日一次给药15 mg·kg-1者血药峰浓度应维持在56~64 mg·kg-1,谷浓度应为5~10 mg·kg-1。
4 结论
通过上述分析看出,本院硫酸阿米卡星注射液应用涉及很多科室,覆盖临床常见感染性疾病;但不合理应用现象较为普遍。针对在使用阿米卡星过程中存在的实际问题,提出以下改进意见:提升临床医生的用药知识水平,加大培训宣传力度;强化和推进临床药师参与合理用药指导;增强医嘱点评审核力度,对不合理用药及时与临床沟通反馈;积极推进血药浓度监测工作,保证临床安全、有效、合理的用药。
本研究结果表明,阿米卡星肾毒性发生率2.81%,总体安全性高,而且主要发生在老年患者、尤其是合并基础疾病多者,临床应重点监测此部分患者的使用剂量和疗程,或避免使用;阿米卡星肾毒性与剂量暴露大小有一定相关性,但本次研究发现,有使用长达1 个多月患者并未出现肾功能损害,所以是否还存在其他制约机制,比如基因等方面因素,值得进一步探索。在用药过程中,监测肾功能和保证液体量,以及进行血药浓度监测是重点;另外,探究预防或减轻阿米卡星肾毒性的方法似可成为医药研究的热点,如阿米卡星脂质体的研制、使用阿米卡星的同时,加用有效减轻肾毒性的药物等[8]。

