复合无机盐相变蓄冷材料的制备与改性研究
李梦欣 陈 鹏 吕钟灵 陈振乾
(1 东南大学能源与环境学院 南京 210096;2 华设设计集团股份有限公司 南京 210014)
随着经济社会的快速发展,我国用电量激增,电力系统峰谷差加大,峰谷用电量比高于发达国家[1],威胁电网的安全和稳定。截至2020年,我国建筑物能耗预计将占全国能源消耗的35%以上,其中供暖、通风和空调系统将占能源消耗的65%以上[2]。在夏季高峰期,空调制冷能耗可达总能耗的85%[3]。夏季空调负荷主要集中于白天,夜间制冷需求量较低,利用相变材料蓄冷技术,在夜间负荷低谷点利用谷电价制冷并储存,在白天负荷高峰时段将储存的冷量释放出来,能够克服能源需求与供应之间的不匹配,节约空调运行费用,降低空调设备安装容量,促进电力负荷削峰填谷,是缓解能源供需矛盾的有效途径。
无机水合盐是常见的蓄冷材料之一,具有价格低廉、高单位体积熔化潜热和高储热密度等优点[4],广泛应用于建筑节能、食品储存、温室节能、太阳能储存等领域[5-7]。但大多数水合盐存在过冷和相分离现象[8],以及由于多次热循环导致的相变材料热稳定性问题仍有待验证[9]。H.W.Ryu等[10]研究了成核剂对水合盐过冷现象的改善,硼砂、粉末碳、铜、氧化钛、硫酸钾对3种水合盐有良好的成核效果。相分离现象可以通过淀粉或各种类型的纤维素衍生物等增稠剂改善。M.Telkes[11]研究发现在水合盐中加入比表面积为125~210 m2/g的触变性材料(凹凸棒黏土),溶液在低浓度下也具有高黏度,并且在多次熔融-凝固循环也具有稳定的热性能。L.F.Cabeza等[12]通过4种不同的增稠材料对相变材料NaCH3COO·3H2O的影响进行研究,加入质量分数为20%的淀粉或50%膨润土时,相分离基本消失,样品热性能基本不变。T.P.Teng等[13]通过直接合成方法制备了纳米复合增强相变材料(NEPCM),向石蜡中添加不同质量浓度的Al2O3、TiO2、SiO2和ZnO纳米粒子,结果表明,加入TiO2能够更有效地降低石蜡熔化起始温度,提高凝固起始温度,从而提升导热性能。
针对建筑空调蓄冷温度需求,6~7 ℃为最合适的蓄冷材料相变温度。本文以目前建筑空调领域的温度要求6~7 ℃为目标温度,寻求合适的复合无机盐相变蓄冷材料,采用步冷曲线法对不同的降温剂、成核剂、增稠剂进行实验研究,分析不同添加量对蓄冷体系相变温度、过冷度、相分离程度的影响,改善水合盐本身的缺点,并添加导热剂提升其导热系数,缩短蓄冷释冷时间。本文制备出一种性能优良的复合无机盐相变材料,并对其相变温度、相变潜热、导热系数、充放冷循环稳定性等物性参数进行测试。
1 实验材料和方法
1.1 实验材料
实验采用十水硫酸钠(Na2SO4·10H2O)、十二水磷酸氢二钠(Na2HPO4·12H2O)、氯化铵(NH4Cl)、氯化钾(KCl)、硼砂、氧化铝(Al2O3)、聚丙烯酸钠(PAAS)、聚丙烯酰胺(PAM)、羧甲基纤维素(CMC)、纳米二氧化钛(TiO2)等化学试剂,以上化学试剂均由国药集团化学试剂有限公司生产提供,纯度为分析纯。
1.2 实验方法
1)凝固-冷却实验
称取不同配比的Na2SO4·10H2O和Na2HPO4·12H2O共20 g放进试管中,置于40 ℃热水浴中升温至融化,加入一定量的降温剂(NH4Cl、KCl)、成核剂(硼砂、Al2O3)、增稠剂(PAAS、PAM、CMC)、导热剂纳米TiO2,并充分搅拌。搅拌均匀后,向试管中插入带密封的热电偶,迅速将试管放入2 ℃恒温水浴仪(ZX—20B型)中冷却至凝固,凝固过程中观察样品状况,采用数据采集仪(Agilent 34970A型)每5 s扫描一次温度数据,绘制样品随时间变化的步冷曲线并进行分析,初步测试样品相变性能。
2)相变潜热测量实验
采用DSC差示扫描量热仪(Q2000型,温度精度±0.01 ℃、量热精确度±0.05%)打开设备保护气阀,将盛放适量样品的坩埚和标准样放入样品池,设置初始温度为-20 ℃、截止温度为40 ℃,升温速率为5 ℃/min,再将初始温度设为40 ℃、截止温度为-20 ℃,降温速率为5 ℃/min,得到样品DSC曲线,从而测得样品的相变温度和相变潜热。
3)导热系数测量实验
采用Hot Disk导热系数仪(TPS2500S型,精度<3%),将Hot Disk探头放置于测试样品中间,测试样品液态(12 ℃)及固态(2 ℃)条件下的导热系数。
2 实验结果与讨论
2.1 Na2SO4·10H2O和Na2HPO4·12H2O基底材料配比实验
在无机盐相变材料中,Na2SO4·10H2O和Na2HPO4·12H2O均具有相变潜热较高、平均相变温度较低等优点,两者热物性参数如表1所示。其中,Na2SO4·10H2O过冷度相对较低,但熔化后有较多未溶解的Na2SO4由于重力作用沉于底部,产生相分离现象[14];Na2HPO4·12H2O溶解时过冷度可达20~26 ℃[11],而溶解度较高,相分离不明显。因此,将两者组成复合相变材料体系,减弱纯无机盐材料的过冷及相分离现象。
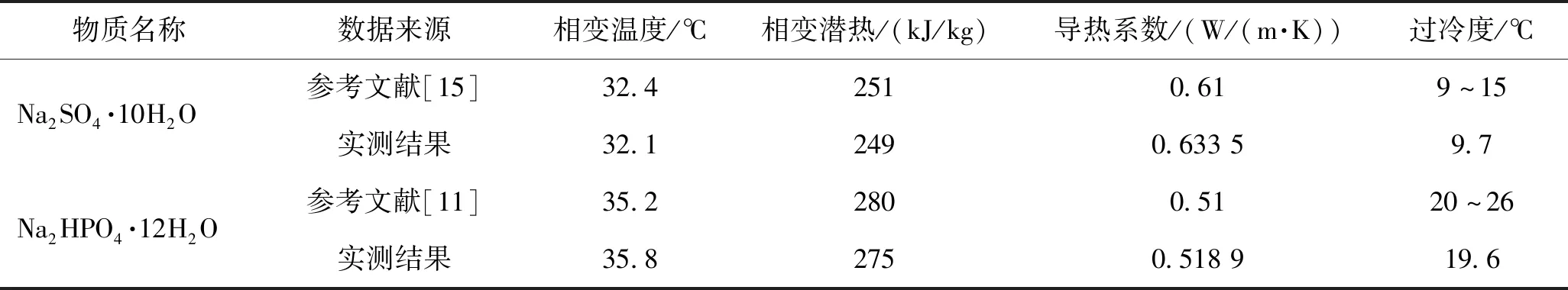
表1 Na2SO4·10H2O和Na2HPO4·12H2O的物性参数Tab.1 Physical parameters of Na2SO4·10H2O and Na2HPO4·12H2O
取Na2SO4·10H2O/Na2HPO4·12H2O配比分别为2∶8、4∶6、6∶4、8∶2以及两种纯物质的样品20 g,将这6组样品加热熔化,稳定一段时间后,分层情况如图1所示。再将样品放入低温恒温水浴中冷却,凝固情况及步冷曲线如图2和图3所示。

图1 不同Na2SO4·10H2O/Na2HPO4·12H2O配比静置后分层情况Fig.1 Stratification after standing at different Na2SO4·10H2O/Na2HPO4·12H2O

图2 不同Na2SO4·10H2O/Na2HPO4·12H2O配比冷却凝固后分层情况Fig.2 Stratification after cooling and solidification at different Na2SO4·10H2O/Na2HPO4·12H2O

图3 不同Na2SO4·10H2O/Na2HPO4·12H2O配比冷却过程步冷曲线Fig.3 Cooling curves of different Na2SO4·10H2O/Na2HPO4·12H2O in cooling process
由图1可知,6组不同配比的样品均存在显著的分层现象,其中Na2SO4·10H2O含量越高,相分离越明显。经冷却凝固后,如图2所示,6组样品依然存在上下层不均匀现象,体系始终存在相分离现象。
由图3可知,当Na2SO4·10H2O和Na2HPO4·12H2O两组分按一定配比混合时,相变温度相比于纯物质显著下降,各组分共晶温度均低于30 ℃。在4组不同复合体系中,Na2SO4·10H2O/Na2HPO4·12H2O配比为4∶6、6∶4、8∶2时,相变温度较低,约为24 ℃。这是由于在Na2SO4·10H2O中加入其它水合盐时,溶于水的其它无机盐离子会削弱原Na2SO4·10H2O分子与结晶水分子间的吸引力,因此,两水合盐复合体系的共晶温度低于任一种水合盐的相变温度。
另一方面,4组不同配比复合水合盐体系的过冷度也低于两种纯物质,Na2SO4·10H2O/Na2HPO4·12H2O配比为4∶6时,过冷度最小,为3.4 ℃,配比为2∶8时过冷度最大为9.3 ℃。过冷度的降低是由于复合无机盐体系中两种无机盐互相作为成核剂,使得整体更易结晶,但过冷度仍然较高,需后续实验进行改善。
综合相分离情况及步冷曲线,Na2SO4·10H2O/Na2HPO4·12H2O配比为4∶6时,分层现象相对纯Na2SO4·10H2O有明显改善,相变温度及过冷度均较低,有利于后续用于空调蓄冷的复合相变材料改性,且存在明显放热平台,因此选定为复合相变材料基底配比。
2.2 不同降温剂对体系相变温度的影响
为解决复合无机盐材料相变温度高于空调蓄冷温度要求的问题,需向体系中加入相变点调节剂。盐离子能够削弱水分子之间氢键的吸引力,使溶液的凝固点降低,因此NaCl、NH4Cl、KCl、NaNO3等能有效降低无机盐相变材料的凝固温度,实验证明,NH4Cl、KCl对于降低Na2SO4·10H2O相变温度具有较好效果[16]。随着无机盐降温剂的加入,体系相变潜热将持续下降,在Na2SO4·10H2O体系中加入6%的NaCl,相变潜热下降27.2%[17]。因此,当降温幅度一致时,应选择添加量较少、降温效率高的降温剂,以维持相对较高的相变潜热。
本文选择NH4Cl和KCl作为熔点降温剂,分析研究其对基底材料的相变温度的影响。为确保体系温度能达到约6 ℃,向8 g Na2SO4·10H2O+12 g Na2HPO4·12H2O体系中分别添加5 g的NH4Cl和KCl,经融化-凝固实验后,体系的步冷曲线如图4所示,两组样品的相变温度均降至10 ℃以下。在上一步基底材料实验中,也存在相变温度降低现象,但在两种物质掺杂比例高于两种降温剂的前提下,相变温度均高于20 ℃,相变温度降幅远小于添加降温剂时的降幅,这一现象侧面验证了两种降温剂的降温效果。由图4可知,添加NH4Cl的样品比添加KCl的样品相变温度低4.4 ℃,因此,NH4Cl降低复合无机盐体系相变温度效果更好。

图4 添加NH4Cl、KCl样品的步冷曲线Fig.4 Cooling curves of samples with NH4Cl and KCl
选择NH4Cl作为降温剂,进一步确定其添加量。分别向8 g Na2SO4·10H2O+12 g Na2HPO4·12H2O体系中添加1、2、3、4、5 g的NH4Cl,经融化-凝固实验后,体系的步冷曲线如图5所示。当NH4Cl添加量逐渐增加时,体系相变温度持续下降,NH4Cl降温效果显著。最初加入少量NH4Cl时,体系相变温度降幅较大,NH4Cl每增加1 g,体系相变温度降低5 ℃以上。后续NH4Cl添加量逐步增多后,对体系相变温度降低效果不显著,降温效果存在边际递减效应。

图5 添加不同质量NH4Cl样品的步冷曲线Fig.5 Cooling curves of samples with different mass NH4Cl
根据步冷曲线结果,当NH4Cl添加量为4 g时,体系相变温度为5.5 ℃,过冷度为1.5 ℃,相变过程较为平稳,满足空调领域蓄冷性能要求,因此添加4 g NH4Cl为复合相变材料降温剂。
2.3 不同成核剂对体系过冷现象的影响
过冷现象是指大多数水合盐冷却到理论相变点并不立即凝固,要继续冷却至相变温度以下几度甚至十几度才开始凝固的现象。根据热力学第二定律,在等温等压下,水合盐过冷度存在时,相变前后的自由能变化ΔG<0,相变过程才会自发进行[18]。
(1)
式中:ΔG为自由能变化量,kJ/mol;H为相变潜热,kJ/mol;Te为相平衡温度,℃;ΔT为过冷度,℃。
当ΔT>0时,相变过程发生,因此过冷度是凝固相变的推动力[19]。而在空调蓄冷过程中,过冷度会使主机能效下降,因此应设法降低过冷度。
目前,降低水合盐过冷度的主要方法是添加成核剂。成核剂能够降低以界面能为主要障碍的成核位垒。晶核在成核剂上形成,成核剂作为结晶生成中心的微粒,有可能使界面能降低,因此成核所需的推动力减小,即成核可以在较小的过冷度下发生。晶核与成核剂之间的接触角越小,对成核越有利,因此晶核与成核剂界面上原子排列相似时,将有更好的成核作用。一般而言,当成核剂与水合盐两者的晶格参数相差在15%以内时,成核剂更为有效。
目前,复合无机盐蓄冷材料存在过冷度1.5 ℃,因此需要添加成核剂加以改善。选择硼砂、Al2O3为体系成核剂,晶格参数如表2所示,分别向8 g Na2SO4·10H2O+12 g Na2HPO4·12H2O+4 g NH4Cl体系中添加0.2、0.4、0.6、0.8 g的硼砂和Al2O3,经融化-凝固实验后,体系的步冷曲线如图6和图7所示。

表2 物质的晶格参数Tab.2 Lattice parameters of materials
由图6可知,当体系中加入不同质量的硼砂,体系过冷度明显降低,当加入硼砂的量达到0.4 g时,过冷度几乎消失,且对体系相变温度无显著影响。此时继续增加硼砂的添加量,步冷曲线变陡,无明显相变平台。硼砂作为成核剂,对于相变体系具有良好效果。图7所示为添加不同质量Al2O3时体系的步冷曲线,体系过冷度维持在2~3 ℃。随着Al2O3添加量的增加,体系过冷度无明显下降趋势,因此Al2O3无法有效降低体系的过冷度。

图6 添加不同质量硼砂时体系的步冷曲线Fig.6 Cooling curves of systems with borax of different quality

图7 添加不同质量Al2O3时体系的步冷曲线Fig.7 Cooling curves of systems with Al2O3 of different quality
由表2可知,硼砂与Na2SO4·10H2O晶格类型相同,参数相近,能够有效降低Na2SO4·10H2O的过冷度,这与M.Telkes等[20-21]的研究结果一致。而硼砂与Na2HPO4·12H2O晶格类型一致,但晶格参数相差大于15%,对Na2HPO4·12H2O有一定成核效果,但无法消除其过冷度,盛青青等[22-23]的实验研究结果也表明,硼砂能够一定程度地降低Na2HPO4·12H2O的过冷度。Al2O3为三角晶格,与单斜晶格的Na2SO4·10H2O和Na2HPO4·12H2O不同,但实验证明,添加Al2O3可有效降低Na2HPO4·12H2O的过冷度[24-25],分析认为,Al2O3与Na2HPO4·12H2O晶体表面有较大的亲和力,属于取向附生成核剂,在Na2HPO4·12H2O结晶过程中,能提供优先沉积的位置,降低成核自由能。在本文实验中,硼砂较Al2O3能更有效促进体系成核,这可能是因为硼砂对Na2SO4·10H2O和Na2HPO4·12H2O两种基底材料均有显著成核作用,而Al2O3,与Na2SO4·10H2O晶格参数差异较大,无明显成核效果,仅对Na2HPO4·12H2O作用较好,因此Al2O3无法对体系产生良好成核作用。
根据步冷曲线结果,当硼砂添加量为0.4 g时,体系相变温度相比添加前无显著变化,过冷度基本消失,因此添加0.4 g硼砂为复合相变材料成核剂。
2.4 不同增稠剂对体系相分离现象的影响
复合体系中基底材料Na2SO4·10H2O和Na2HPO4·12H2O、降温剂NH4Cl不溶于结晶水而沉于底部,形成分层现象。当凝固开始时,晶体会首先在饱和溶液和固体沉积物的交界面生长形成一层屏障,阻碍底部无机盐与溶液中的游离水接触,无法充分结晶,在多次融化-凝固循环后,相变潜热大幅降低,蓄冷容量下降,使用周期缩短。防止相分离现象的主要方法是加入增稠剂,作用是形成黏度较大的凝胶体,将相变体系分散成一系列小的空间,形成弥散的小颗粒晶体,阻止大晶体的生长,减少未溶解无机盐的沉淀,使其能够在多次循环期间得到充分结晶。
聚丙烯酰胺(PAM)、羧甲基纤维素(CMC)、聚丙烯酸钠(PAAS)等增稠剂均能对无机盐溶液起到良好的增稠作用[26]。PAM是水溶性线性高分子聚合物,溶于水后溶液可视为网状结构,链间机械的缠结和氢键共同形成网状节点,使黏度增加。CMC中大量羧基极性基团,遇水时与水分子以氢键结合,使分子的运动受到限制,宏观上表现为黏度增大形成凝胶状液体。PAAS是具有亲水基团的高分子化合物,溶于水后由于羧酸根的离子现象使分子链增长,表观黏度增大而形成高黏性溶液。
向8 g Na2SO4·10H2O+12 g Na2HPO4·12H2O+4 g NH4Cl+0.4 g硼砂体系中分别添加0.6 g的PAAS、CMC、PAM,配置结束后静置一晚,并进行融化-凝固实验循环10次。
图8所示分别为添加3种增稠剂配置结束后、静置一晚后、循环10次后的相分离情况,从配置结束至静置一晚后,3组增稠剂体系均无分层现象,且均有一定削弱相分离的效果。经过融化-冷却循环实验10次后,添加PAAS的体系有显著分层,PAM体系有一定程度分层,而CMC体系无分层。图9所示为添加3种增稠剂循环1次和循环10次的步冷曲线对比,添加PAAS的体系出现过冷度显著增加的现象,这可能与该组溶液多次循环后重新出现相分离现象有关,该现象与鄢瑛等[27]的实验结论相符,PAAS均匀分散水盐体系能力较弱,剩余的无机盐难以再次结晶,导致该体系热稳定性较差。添加CMC的体系过冷度轻微增加。PAM体系无明显过冷度,但相变平台消失。综合考虑增稠效果、循环热物性特征,选定CMC为复合相变体系增稠剂。

图8 添加3种增稠剂后体系相分离情况Fig.8 Phase separation of systems with three thickeners

图9 添加3种增稠剂后体系第1、10次循环步冷曲线Fig.9 Cooling curves of the first cycle and the tenth cycle of systems with three thickeners
复合体系中添加增稠剂的量过少,则改善相分离效果不佳,在循环过程中产生沉淀;添加增稠剂的量过多,则体系会形成稳定的凝胶体,占用过多的结晶水,导致再次结晶的无机盐量减少。为确定增稠剂CMC下限添加量,向原有体系中添加0.2 g、0.4 g CMC,循环10次后,加入0.2 g CMC体系出现分层,0.4 g CMC体系均匀无分层,因此选定增稠剂CMC添加量为0.4 g,循环1次和循环10次后的步冷曲线如图10所示,其相变温度为6.2 ℃,过冷度为0.4 ℃。

图10 添加增稠剂0.4 g CMC体系第1、10次循环步冷曲线Fig.10 Cooling curves of the first cycle and the tenth cycle of system with 0.4 g CMC
2.5 不同添加量导热剂对体系导热性的影响
在空调蓄冷槽中,金属换热管及空调冷水导热系数较高,主要热阻存在于蓄冷介质部分,提高无机盐蓄冷材料的导热系数能够有效提升蓄冷槽整体的导热效果。纳米TiO2具有粒径小、比表面积大、表面活性大、热导性好、分散性好和所制悬浮液稳定等优点[28]。在蓄冷体系中添加纳米粒子,可以显著增加其导热系数。另外,纳米TiO2还可以改善蓄冷材料过冷度、比热容及相变潜热,质量分数为0.3%的纳米可提升复合水合盐相变材料固相比热容83.5%,液相比热容15.1%,提升相变潜热6.4%[29]。
采用瞬态平面热源法(Hot Disk法)测量体系内添加不同质量纳米TiO2的体系导热系数,测量固相导热系数时温度取2 ℃,测量液相导热系数时温度取12 ℃,测量结果如表1所示。添加纳米TiO2后,相对于基底材料Na2SO4·10H2O和Na2HPO4·12H2O纯物质0.5~0.6 W/(m·K)的导热系数,纳米TiO2作为导热剂有显著效果,纳米TiO2添加量越高,体系导热系数越高。考虑导热系数增加程度与成本,选定复合材料体系中纳米TiO2添加量为0.2 g。

表3 不同质量纳米TiO2体系导热系数Tab.3 Thermal conductivity of systems with nano-TiO2 of different mass
2.6 复合无机盐相变蓄冷材料热物性测试
根据上述实验确定的相变材料基底配比、降温剂、成核剂、增稠剂及导热剂,确定复合无机盐相变蓄冷体系配比为:32%Na2SO4·10H2O+48% Na2HPO4·12H2O+16%NH4Cl+1.6%硼砂+1.6%CMC +0.8%纳米TiO2。利用差示扫描量热仪DSC对配制好的复合无机盐相变材料进行相变温度和相变潜热的测试,DSC曲线如图11所示,其相变温度为6.1~6.3 ℃,相变潜热为130~139 J/g,液相导热系数为0.798 9 W/(m·K),pH值为7.62。在同一相变温度区间内的相变材料中,Calor Group Ltd公司生产的转熔温度为7.5 ℃的Na2SO4·10H2O+NH4Cl+KCl复合相变材料潜热为121 J/g[30-31],转熔温度为18 ℃的Na2SO4·10H2O+NaCl复合相变材料潜热为146 J/g[30-31],美国加州发明的“41”型相变温度为5 ℃的无机相变材料潜热为123.3 J/g,“47”型相变温度为8 ℃的无机相变材料潜热为95.4 J/g[32],与本文相变潜热相当。该体系相变潜热相对于Na2SO4·10H2O的251 J/g和Na2HPO4·12H2O的281 J/g有明显下降,推测主要是由于体系降温剂的引入。

图11 复合无机盐相变蓄冷材料DSC曲线Fig.11 DSC curve of composite inorganic salt phase change cool storage material
对复合相变材料进行融化-冷却循环实验,循环1次的相变材料基本无过冷度,相变平台明显,完成相变过程时间约为1 000 s。继续进行循环实验50次,步冷曲线、放冷曲线及相变温度变化如图12~图14所示。由实验结果可知,本文制备的复合无机盐相变材料步冷曲线有明显相变平台,相变温度能够基本保持在约6 ℃,过冷度无明显增加;融化曲线无明显相变平台,融化过程均匀平稳进行。复合无机盐相变材料凝固、融化过程曲线、相变温度随循环次数增加无显著变化,符合本文对相变温度的区间要求,材料具有良好的稳定性,可以作为低温蓄冷材料应用于建筑空调领域。
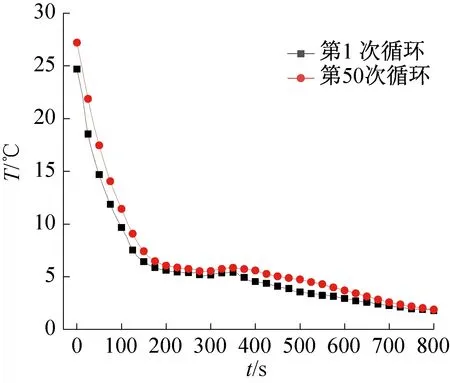
图12 体系第1、第50次循环步冷曲线Fig.12 Cooling curves of the first and the 50th cycle of the system

图13 体系第1、第50次循环放冷曲线Fig.13 Heating curves of the first and the 50th cycle of the system

图14 体系50次循环相变温度变化Fig.14 Phase transition temperatures of the system in 50 cycles
3 结论
1)Na2SO4·10H2O/Na2HPO4·12H2O质量配比为4∶6的混合体系,可以克服两种纯物质各自的缺点,其分层现象相比于纯Na2SO4·10H2O减轻,过冷度及相变温度均低于单一纯物质,得到相变性能良好的复合无机盐蓄冷材料。
2)在8 g Na2SO4·10H2O+12 g Na2HPO4·12H2O复合体系中加入降温剂、成核剂、增稠剂、导热剂4种添加剂,对复合体系影响如下:
(a)NH4Cl和KCl均能降低复合体系的相变温度,其中NH4Cl降温效果更好,加入4 g NH4Cl即可将体系相变温度降至约6 ℃;
(b)硼砂可有效降低复合体系的过冷度,添加0.4 g以上的硼砂能够基本消除过冷度,添加量越高对相变平台影响越大,Al2O3无明显成核作用;
(c)CMC和PAM能显著提高体系黏度,消除体系多次循环后相分离问题,其中添加0.4 g CMC可获得较优的相变性能,PAAS增稠效果相对较差;
(d)添加少量纳米TiO2即可提高体系导热系数,考虑其增加率与成本,取导热剂添加量为0.2 g。
3)配置的复合无机盐蓄冷材料体系最终配比为32%Na2SO4·10H2O+48%Na2HPO4·12H2O+ 16%NH4Cl+1.6%硼砂+1.6%CMC+0.8%纳米TiO2,其相变温度为6.1~6.3 ℃,相变潜热为130~139 J/g,液相导热系数为0.798 9 W/(m·K),pH为7.62,经过50次循环后,相变温度和过冷度变化较小,体系均匀无分层,具有良好的热稳定性,适用于建筑空调蓄冷。
——化工原料、农副产品

