我国12岁女性接种双价人乳头瘤病毒疫苗的成本-效用分析
周大创 罗孟捷 唐文熙


中圖分类号 R956 文献标志码 A 文章编号 1001-0408(2021)13-1602-05
DOI 10.6039/j.issn.1001-0408.2021.13.11
摘 要 目的:评价我国12岁女性接种双价人乳头瘤病毒(HPV)疫苗的成本-效用,为卫生服务决策者提供经济学证据。方法:采用CERVIVAC模型对我国12岁女性进行长期模拟至全部人群均进入死亡状态(循环周期为1年),分别计算接种双价HPV疫苗的试验组人群与未接种该疫苗的对照组人群的成本与健康产出,结合意愿支付阈值[WTP,1倍2019年我国人均国内生产总值(GDP)]判断其经济性。结果:在模拟期限内,试验组相较于对照组的增量成本-效果比(ICER)为28 660.56元/质量调整生命年(QALY),小于WTP,具有药物经济学优势。单因素敏感性分析结果显示,对ICER影响较大的5个参数依次为贴现率、HPV-16/HPV-18所引起的宫颈癌占比、疫苗有效率、每年早期/原位癌直接经济负担和每年晚期/转移癌直接经济负担。概率敏感性分析结果显示,在以1倍2019年我国人均GDP作为WTP的情况下,试验组较对照组具有更大的可接受性(概率为74%);当WTP高于25 876元/QALY时,试验组具有更大的成本-效用优势。结论:针对宫颈癌的预防,我国12岁女性接种双价HPV疫苗较不接种该疫苗更具有成本-效用优势。
关键词 宫颈癌;人乳头瘤病毒;双价疫苗;CERVIVAC模型;成本-效用分析
Cost-utility Analysis of 12-year-old Girls Vaccinated with Bivalent Human Papilloma Virus Vaccine in China
ZHOU Dachuang1,2,LUO Mengjie1,TANG Wenxi1(1. School of International Pharmaceutical Business,China Pharmaceutical University,Nanjing 211198,China; 2. Pharmacoeconomic Evaluation Research Center,China Pharmaceutical University,Nanjing 211198,China)
ABSTRACT OBJECTIVE: To evaluate the cost-utility of bivalent human papilloma virus (HPV) vaccine for 12-year-old girls in China and provide economic evidence for health service decision makers. METHODS: The CERVIVAC model was used to simulate the population of 12-year-old girls in China for a long time until all the population entered a state of death (1 year as a cycle). The cost and health output of the people in experimental group who received the bivalent HPV vaccine and the control group who did not receive the vaccine were calculated separately, and the economics was judged combined with willingness to pay threshold [WTP, 1 time of Chinas per capita gross domestic product (GDP) in 2019]. RESULTS: During the simulation period, the incremental cost-effectiveness ratio (ICER) of the experimental group compared with the control group was 28 660.56 yuan/QALY, which was less than WTP and had pharmacoeconomic advantages. The results of single-factor sensitivity analysis showed that the five parameters that had a greater impact on ICER were discount rate, the proportion of HPV-16/HPV-18-induced cervical cancer, vaccine effective rate, direct economic burden of early/in situ cancer each year and the direct economic burden of advanced/metastatic cancer each year. The results of probabilistic sensitivity analysis showed that the experimental group was more acceptable (74%) than the control group when using 1 time of Chinas per capita GDP in 2019 as WTP; the experimental group had a greater cost-utility advantage when WTP was higher than 25 876 yuan/QALY. CONCLUSIONS: For the prevention of cervical cancer, the bivalent HPV vaccine for 12-year-old girls in China has more cost-utility advantages than no vaccine intervention.
KEYWORDS Cervical cancer; HPV; Bivalent vaccine; CERVIVAC model; Cost-utility analysis
宫颈癌是威胁全球女性生命健康的主要恶性肿瘤之一。据统计,2018年全球新发宫颈癌病例将近60万例、死亡病例超过30万例[1]。在我国,宫颈癌的发病率和病死率均居于妇科恶性肿瘤第2位;患者发病年龄趋于年轻化,而且大多数发病时已到中晚期,严重影响了其生命健康[2-3]。人乳头瘤病毒(human papilloma virus,HPV)感染与宫颈上皮内瘤变以及宫颈癌的发生密切相关。研究表明,HPV容易感染受损的宫颈上皮,不利于宫颈上皮的自我修复,从而导致宫颈上皮癌变[4]。根据致病力或致癌危险性大小的不同,HPV分为高危型(如HPV-16、HPV-18、HPV-31、HPV-33、HPV-39、HPV-45等)和低危型(如HPV-6、HPV-11、HPV-42、HPV-43、HPV-44等)两大类,其中高危型HPV的持续感染是宫颈癌的独立危险因素,90%以上的宫颈癌患者均被检测出为高危型HPV感染者[5-6]。
宫颈癌的早期筛查和HPV疫苗接种均可有效预防宫颈癌的发生。我国于2009年7月7日启动了全国农村妇女“两癌”检查项目,但由于各地区经济发展不平衡以及医疗资源贫乏等原因,致使目前宫颈癌的筛查率仍然较低[7]。HPV疫苗接种可使机体产生抗体,从而有效预防宫颈癌的发生[8]。2008-2011年在我国江苏省开展的Ⅱ/Ⅲ期随机双盲试验显示,双价HPV疫苗具有有效性和临床可接受的安全性[9]。自2016年起,进口双价(可预防HPV-16、HPV-18)、四价(可预防HPV-6、HPV-11、HPV-16、HPV-18)和九价(可预防HPV-6、HPV-11、HPV-16、HPV-18、HPV-31、HPV-33、HPV-45、HPV-52、HPV-58)HPV疫苗先后在我国获批上市,但因疫苗价格与可及性等问题导致其接种率偏低。2019年底,国产双价HPV疫苗(大肠杆菌)获批上市,意味着未来国内疫苗供应不足的问题将不再成为疫苗接种的掣肘[8]。截至2019年,全球已有92个国家和地区将HPV疫苗纳入国家免疫计划[10],但我国目前暂未实施HPV疫苗免疫计划。
卫生经济学评估是疫苗免疫规划决策的重要科学依据之一,世界卫生组织(WHO)建议公共卫生服务决策者应当在充分考虑成本获益的基础上进行科学决策[11]。目前我国已有多项关于HPV疫苗接种的经济性研究,研究方法多以马尔可夫(Markov)模型开展模拟,结果显示,用HPV疫苗结合筛查来预防宫颈癌较单独筛查更具有有效性和经济性[12-16]。CERVIVAC模型采用真实年龄组发病率和病死率進行模拟,其长期模拟结果相较于Markov模型更加贴近真实情况。目前我国尚未有以CERVIVAC模型开展的HPV疫苗经济学评价研究,故本研究基于上述随机双盲试验结果构建CERVIVAC模型,对我国12岁女性接种双价HPV疫苗的成本-效用进行分析,为相关政策的落实提供经济学证据。
1 资料与方法
1.1 目标人群
HPV的主要传播途径为性传播、密切接触、间接接触、医源性感染和母婴传播[17]。WHO推荐的HPV疫苗接种人群为9~12岁女性,美国疾病预防控制中心推荐11岁或12岁女性进行疫苗接种[16]。我国绝大多数女性的初次性行为晚于12岁,9~14岁接种者仅需接种2剂次疫苗,参照其他HPV疫苗经济学评价目标人群[16],最终确定本研究的目标人群为我国12岁女性。
1.2 对照方案
尽管临床已大力推广HPV DNA检测技术,但由于成本与覆盖率等问题,目前我国宫颈癌的筛查技术仍以细胞学检查中的巴氏涂片法为主[12]。因当前宫颈癌的筛查率和HPV疫苗的接种率均处于较低水平,故本研究暂不考虑筛查成本。本研究假设宫颈癌的筛查方法和筛查规模不发生明显变化,将接种双价HPV疫苗(大肠杆菌)的人群作为试验组、未接种该疫苗的人群作为对照组进行比较分析。
1.3 模型结构
CERVIVAC模型是由泛美卫生组织(Pan American Health Organization,PAHO)的ProVac研究开发的、基于Microsoft Office Excel软件操作的、专门用于进行HPV疫苗经济学评价的静态模型[18-19]。此模型将所研究地区宫颈癌的发病率与病死率数据代入模型原始模板进行操作,研究者仅需输入相关参数即可进行经济学评价,操作方便、快捷且结果科学、可靠。但目前国内不太容易获得该模型的原始模板,故本研究基于已发表的CERVIVAC模型相关研究[17-18],以Microsoft Office Excel软件构建原始模型,将模型设为3个健康状态:健康、宫颈癌、死亡。假设目标人群入组时均为健康无感染状态,模拟研究队列从12岁直至全部人群均进入吸收态(死亡状态),循环周期为1年;宫颈癌病例数和病死数分别由存活女性人数与宫颈癌发病率和病死率相乘得出;以研究队列中需要接受治疗的宫颈癌病例数与平均治疗成本相乘得出总成本,并对成本与健康产出进行贴现,比较对照方案的终身成本和健康产出,以此得出药物经济学评价结果。
假设模型模拟第1年(12岁)的研究队列人群均为完全健康,第2年(13岁)直至全部人群均进入吸收态(死亡状态),健康状态间转移情况均符合下列公式(式中,H表示健康,C表示宫颈癌,D表示死亡,t表示周期数,ν表示宫颈癌发病率,δ表示自然死亡率,λ表示早期/原位癌比例,τ表示早期/原位癌治疗率,ε表示早期/原位癌治愈率,υ表示晚期/转移癌治疗率,ι表示晚期/转移癌治愈率,γ表示宫颈癌额外病死率,μ表示疫苗覆盖率,φ表示疫苗有效率,θ表示HPV-16/HPV-18所引起的宫颈癌占比):
对照组:H(t+1)=H(t)×(1-ν-δ)+{C(t)×[λ×τ×ε+(1-λ)×υ×ι]};C(t+1)=C(t)×{1-{γ+δ+[λ×τ×ε+(1-λ)×υ×ι]}}+H(t)×ν;D(t+1)=D(t)+[H(t)+C(t)]×δ+C(t)×γ。
试验组:H(t+1)=H(t)×[1-δ+(1-μ×φ×θ)×ν]+ C(t)×[λ×τ×ε+(1-λ)×υ×ι];C(t+1)=C(t)×{1-{γ+δ+[λ×τ×ε+(1-λ)×υ×ι]}}+ H(t)×[(1-μ×φ×θ)×ν];D(t+1)=D(t)+[H(t)+C(t)]×δ+C(t)×γ。
宫颈癌治愈率公式依据文献[14],即:宫颈癌治愈率=[√[1-(1-5年生存率)]] [5]。因疫苗有效率并非恒定,会随着接种时间延长而降低,故模拟开始的某年的疫苗有效率=疫苗有效率×[1-NORMDIST(接种后的年数,疫苗平均保护年限,保护年限标准差,1)][20]。参考双价HPV疫苗说明书,12岁女性仅需接种2剂次疫苗[8]。参照国内其他HPV疫苗药物经济学评价研究[15-16],假定覆盖率为70%。CERVIVAC模型参数及其分布如表1所示。
1.4 成本和效用值数据
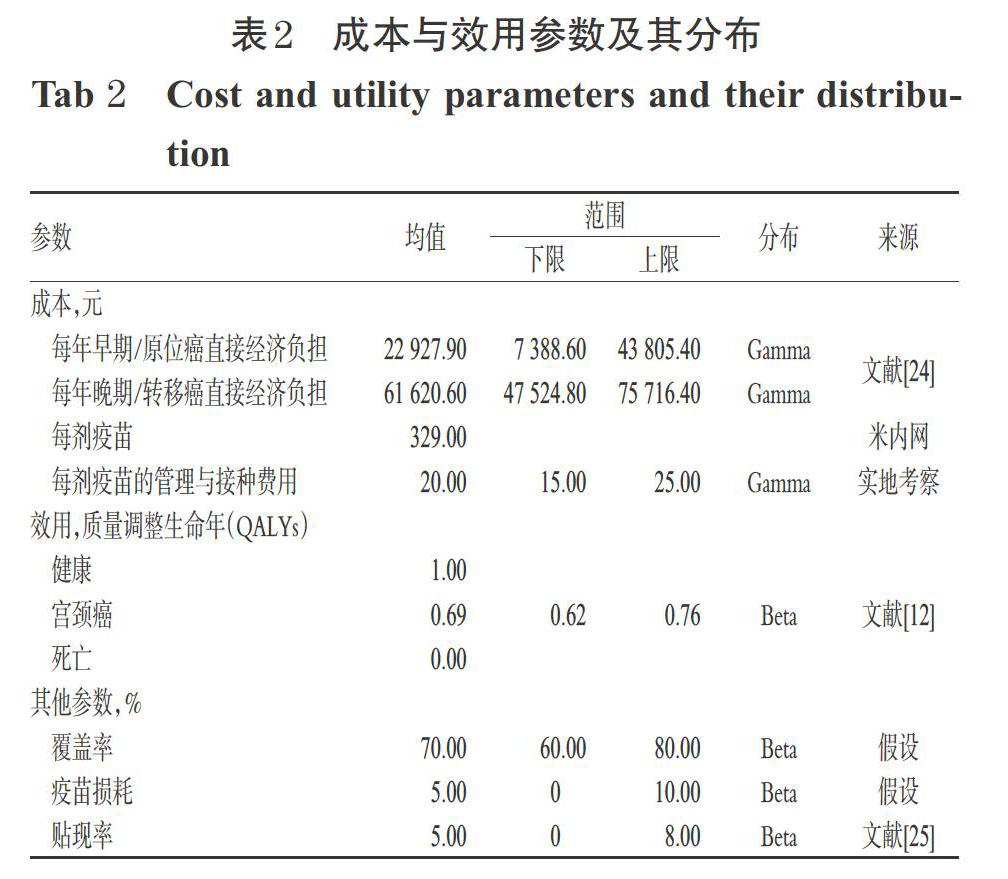
本研究基于全社会角度,成本考虑患者的直接经济负担,即直接医疗费用和直接非医疗费用。其中,直接医疗费用是指患者为了治疗疾病在卫生保健部门所花费的费用,如门诊费、药费、诊疗费、检查费、手术费和康复费等;直接非医疗费用是指患者在救治期间在非卫生保健部门所花费的费用,如住宿费、交通费、伙食费、营养费和陪护费等。本研究中的直接经济负担来源于2015年子宫颈癌筛查国家专项所抽取的14个省/直辖市23所医院的3 246例患者的费用数据,其早期癌治疗主要以子宫切除和放化疗为主,中晚期癌治疗主要以放化疗为主[24];疫苗成本来源于米内网(https://3g.menet.com.cn);疫苗接种与管理等额外成本来源于已接种疫苗的患者的费用单据与实地考察数据。随机双盲试验显示,HPV疫苗接种后可能会出现局部症状(疼痛、肿胀和发红等)或全身症状(乏力、发热、胃肠道症状、头痛、关节痛、肌痛、皮疹和荨麻疹),但大多为轻微、持续时间较短的自限性症状[9],因此暂不考虑不良反应的治疗成本。本研究设置健康状态人群效用值为1、死亡状态为0,并对存在不确定性或假设的成本与效用进行不确定性分析。根据《中国药物经济学评价指南(2020)》,本研究对成本和健康产出以5%的贴现率进行贴现[25],并选用1倍2019年我国人均国内生产总值(GDP,70 892元,数据来源于国家统计局官方网站)作为意愿支付阈值(WTP)。成本与效用参数及其分布如表2所示。
2 结果
2.1 成本-效用分析结果
在研究期限内,试验组(接种疫苗)的人均成本为338.89元,效用为19.114 503 QALYs;對照组(未接种疫苗)的人均成本为152.83元,效用为19.108 012 QALYs;两组间的增量成本-效果比(ICER)为28 660.56元/QALY,低于WTP,说明试验组(接种疫苗)更具有有效性和经济性。
2.2 敏感性分析结果
2.2.1 单因素敏感性分析结果 根据表1和表2中各参数的范围对存在不确定性的15个参数(即表1、表2中标注了上下限的参数,下同)进行单因素敏感性分析。结果显示,对ICER影响最大的5个参数依次为贴现率、HPV-16/HPV-18所引起的宫颈癌占比、疫苗有效率、每年早期/原位癌直接经济负担和每年晚期/转移癌直接经济负担。单因素敏感性分析飓风图如图1所示。
2.2.2 概率敏感性分析 根据表1和表2中各参数的范围与分布对存在不确定性的15个参数进行概率敏感性分析,依据1 000次蒙特卡洛模拟结果绘制成本-效果散点图(图2)和成本-效果可接受曲线(图3)。由图2可见,在以1倍2019年我国人均GDP作为WTP的情况下,试验组(接种疫苗)较对照组(未接种疫苗)具有更大的可接受性(概率为74%)。由图3可见,当WTP大于25 876元/QALY(50%可接受概率)时,试验组具有更大的成本-效用优势。
3 讨论
宫颈癌的发病率较高,大多数患者发病时已到了中晚期,而且治愈的患者仍有可能出现病情进展或复发。研究表明,早期宫颈癌患者治愈后的复发率为11%~22%,晚期宫颈癌患者治愈后的复发率为28%~46%;一旦出现复发或转移,患者的总体治疗效果差、生存时间短[26]。但宫颈癌是一种可防可治的恶性肿瘤,其疾病进展周期较长,并存在较长的可逆转的癌前病变期,经过宫颈癌筛查可有效发现其癌前病变,预防其发生。然而,目前常用的宫颈癌筛查方式的敏感性和特异度均不高[27],难以准确发现癌前病变;同时,因教育水平、接受程度等原因致使公众对“两癌筛查”的配合度不高、筛查进展情况不佳,癌颈癌防治形势仍然严峻[28]。而接种HPV疫苗相较于筛查可以更为有效地规避宫颈癌的发生,而且一次接种即可获得接近终身的免疫效果[8]。
目前国外已有较多关于HPV疫苗的经济学评价研究,主要研究方法以静态比例模型、Markov模型和传播动力学模型为主;WHO与PAHO还开发了PRIME模型和CERVIVAC模型,可以更方便、快捷地进行地区适应性调整的HPV疫苗经济学评价。我国也有多篇关于HPV疫苗的经济性评价研究,但研究方法较为单一,大多以Markov模型为主[12-14,16],仅有1篇以动态传染模型进行模拟[15]。因受限于模型原始模板的获取,国内学者以PRIME模型和CERVIVAC模型开展研究较为困难。不同模型的模拟结果存在差异,加之我国药物经济学发展起步较晚、方法学亟需完善,综合考虑不同模型的经济学评价结果可以使卫生决策者作出更为科学、可靠的决策。因此,本研究构建CERVIVAC模型对我国12岁女性接种双价HPV疫苗的成本-效用进行分析,为HPV疫苗的经济性评价提供更多的理论证据。CERVIVAC模型依靠地区发病率与病死率进行模拟,不同于其他静态比例模型,其还考虑到了队列时间与患者年龄变化的因素,而且较为方便、快捷,具有外推性和方法学借鉴意义;该模型还可以通过参数的改变用于研究HPV诱发的疾病。
WHO关于药物经济学评价的推荐意见为:当ICER小于1倍当地人均GDP时,可认为增加的成本是完全可以接受的,具有药物经济学优势[29]。本研究结果显示,试验组(接种疫苗)较对照组(未接种疫苗)的ICER为28 660.56元/QALY,小于1倍2019年我国人均GDP(70 892元),具有药物经济学优势。单因素敏感性分析结果显示,对ICER影响较大的5个参数依次为贴现率、HPV-16/HPV-18所引起的宫颈癌占比、疫苗有效率、每年早期/原位癌直接经济负担和每年晚期/转移癌直接经济负担。概率敏感性分析结果显示,在以1倍2019年我国人均GDP作为WTP的情况下,试验组(接种疫苗)较对照组(未接种疫苗)具有较大的可接受性(概率为74%);当WTP高于25 876元/QALY时,试验组具有更大的成本-效用优势。
本研究也存在一定的局限性:(1)数据大多来自参考文献,若参考文献数据不全或参数取自国外研究,则较难进行本土适应性调整;且参数来自不同的研究对象,代表性欠佳。(2)未将人类性行为等因素纳入考虑,也并未对干预后避免进一步感染的群体免疫进行考虑。(3)未考虑HPV诱发的除宫颈癌以外的其他疾病。(4)研究假设(如假设宫颈癌的筛查方法和筛查规模不发生明显变化)在一定程度上限制了本文结论的可推广性。
综上,通过接种HPV疫苗预防HPV感染可有效预防宫颈癌和其他HPV诱发疾病(如尖锐湿疣、头颈癌和肛门癌等)的发生,减少HPV对我国女性生命健康的威胁,同时降低了卫生体系在宫颈癌筛查与治疗方面的支出。目前我国的双价HPV疫苗供应量较为充裕,且价格相对低廉,女性接种意识和接种率也逐渐提高,这对开展HPV疫苗的药物经济学评价工作具有较为重要的现实意义。在未来的研究中,可以考虑开展更为广泛的真实世界研究,并将人类性行为、群体免疫等因素纳入研究方案,以便为卫生服务决策者提供更加全面的经济学参考证据。
参考文献
[ 1 ] BRAY F,FERLAY J,SOERJOMATARAM I,et al. Glo- bal cancer statistics 2018:GLOBOCAN estimates of incidence and mortality worldwide for 36 cancers in 185 countries[J]. CA Cancer J Clin,2018,68(6):394-424.
[ 2 ] 佐志刚,汤继英,蔡晓军,等.华蟾素胶囊联合紫杉醇、顺铂治疗中晚期宫颈癌的临床观察[J].中国药房,2017,28(24):3350-3353.
[ 3 ] 苏小玉,蒙莉萍,邹聪聪,等.重组人干扰素凝胶联合保妇康栓治疗宫颈高危型HPV感染的临床观察[J].中国药房,2020,31(8):984-988.
[ 4 ] 李璐. HPV E6/E7通过IFI16/p53通路调控宫颈上皮细胞生物学功能的机制研究[D].济南:山东大学,2019.
[ 5 ] TORRES-POVEDA K,BURGUETE-GARC?A A I, BAHENA-ROM?N M,et al. Risk allelic load in Th2 and Th3 cytokines genes as biomarker of susceptibility to HPV-16 positive cervical cancer:a case control study[J]. BMC Cancer,2016,16:330.
[ 6 ] 方芳,李芳,段燕康,等.宫颈病变患者人乳头瘤病毒感染分型研究[J].中国药房,2013,24(34):3241-3243.
[ 7 ] 赵超,魏丽惠.提高中国宫颈癌筛查率的新思考[J].中国计划生育和妇产科,2020,12(11):3-4.
[ 8 ] 李双,李明珠,丛青,等.人乳头瘤病毒疫苗临床应用中国专家共识[J].现代妇产科进展,2021,30(2):81-91.
[ 9 ] ZHU F C,HU S Y,HONG Y,et al. Efficacy,immunogenicity,and safety of the HPV-16/18 AS04-adjuvanted vaccine in Chinese women aged 18-25 years:event-triggered analysis of a randomized controlled trial[J]. Cancer Med,2017,6(1):12-25.
[10] 张师前,王凯,张远丽,等. HPV疫苗在中国的应用现状[J].中国实用妇科与产科杂志,2019,35(10):1090- 1095.
[11] ORGANIZATION W H. Human papillomavirus vaccines:WHO position paper,May 2017-recommendations[J]. Vaccine,2017,35(43):5753-5755.
[12] 孫雨欣,刘永军,刘通,等.宫颈癌疫苗用于18~25岁中国女性预防宫颈癌的药物经济学评价[J].中国循证医学杂志,2017,17(1):102-107.
[13] 刘怡君. HPV-16/18预防性疫苗的接种年龄对其预防子宫颈癌作用的卫生经济学研究[D].大连:大连医科大学,2015.
[14] 张倩.子宫颈癌筛查的风险分流及疫苗的卫生经济学评价研究[D].北京:北京协和医学院,2017.
[15] 宋晓彬,赵勤俭,周鼒,等.二价HPV疫苗接种策略的卫生经济学评估:基于动态模型[J].中华预防医学杂志,2017,51(9):814-820.
[16] 莫秀婷.我国宫颈癌预防策略的经济学评价[D].济南:山东大学,2015.
[17] 黄嘉元.人乳头瘤病毒及其引起的疾病[J].中国医药科学,2013,3(13):32-34.
[18] AGUILAR I B,MENDOZA L O,GARC?A O,et al. Cost- effectiveness analysis of the introduction of the human papillomavirus vaccine in Honduras[J]. Vaccine,2015,33 (Suppl 1):A167-A173.
[19] NOVAES H M,DE SO?REZ P C,SILVA G A,et al. Cost-effectiveness analysis of introducing universal human papillomavirus vaccination of girls aged 11 years into the National Immunization Program in Brazil[J]. Vaccine,2015,33(Suppl 1):A135-A142.
[20] WALWYN L,JANUSZ C B,CLARK A D,et al. Cost-effectiveness of HPV vaccination in Belize[J]. Vaccine,2015,33(Suppl 1):A174-A181.
[21] 国家癌症中心. 2018中国肿瘤登记年报[M].北京:人民卫生出版社,2019:196-215.
[22] 国务院人口普查办公室,国家统计局人口和就业统计司. 中国2010年人口普查资料[EB/OL].[2021-06-09]. http://www.stats.gov.cn/tjsj/pcsj/rkpc/6rp/indexch.htm.
[23] 王静,许可葵,史百高,等. 4 374例宫颈癌患者预后及其影响因素分析[J].中国肿瘤,2014,23(4):281-288.
[24] 陶思源,彭介入,王英,等.子宫颈癌及癌前病变患者直接经济负担及其影响因素研究[J].中华预防医学杂志,2018,52(12):1281-1286.
[25] 刘国恩.中国药物经济学评价指南:2020[M].北京:中国市场出版社,2020:27-28.
[26] 钟林,王冬.两种方案治疗56例宫颈癌骨转移的回顾性分析[J].中国药房,2015,26(26):3681-3683.
[27] 马艳,丁香平.阴道镜在宫颈病变筛查中的临床应用[J].江西醫药,2017,52(11):1182-1183.
[28] 向群英.宫颈癌筛查意愿的影响因素分析[J].实用妇科内分泌电子杂志,2019,6(20):10-11.
[29] 李轲,马爱霞.我国应用阿司匹林进行心血管疾病一级预防的药物经济学评价[J].中国药房,2018,29(24):3411- 3416.
(收稿日期:2020-12-23 修回日期:2021-06-10)
(编辑:胡晓霖)

