葡萄糖酸钠与二甲氨基丙基甲基丙烯酰胺复配对碳钢缓蚀性能的影响
常佳宇 陆 原 赵景茂*
(1.北京化工大学 材料科学与工程学院, 北京 100029; 2.中海油(天津)油田化工有限公司, 天津 300450)
引 言
随着全球工业化的快速发展,工业用水量、特别是占总用水量80%的循环冷却水的消耗量正在逐渐增加[1-4]。在循环冷却水系统中碳钢设备的结垢、腐蚀等问题给企业带来了巨大的损失[5-6],针对这一问题,可以采用添加缓蚀剂、进行涂层和表面钝化等方法对碳钢进行腐蚀防护。有机缓蚀剂由于成本低、添加量少等特点而被广泛应用,有机缓蚀剂分子中的O、N、P和S等含有孤对电子的杂原子可以向Fe原子的空d轨道提供电子,从而与Fe原子形成配位键[7-8]。目前主要使用有机磷酸酯以及无机磷酸盐和锌盐复配的缓蚀剂来控制循环冷却水的腐蚀程度[9-10],但磷的排放会导致水体富营养化以及赤潮现象,因此绿色环保缓蚀剂的研究日益受到人们的关注。
葡萄糖酸钠(sodium gluconate,SG)是一种工业中常用的有机物,被认为是冷却水系统中对铁和低碳钢有效的无毒缓蚀剂[11-12]。二甲氨基丙基甲基丙烯酰胺(DMAPMA)是一种化学反应单体,无毒,分子中含有N原子,可以向Fe原子的空d轨道提供电子,有可能具有一定的缓蚀作用。SG与DMAPMA的复配物既不含磷原子,也不含重金属锌,如果该复配物具有良好的缓蚀作用,那么在碳钢防腐领域将会有良好的研究价值和应用前景。
本文采用失重法、电化学法和表面分析技术,分别测试了SG、DMAPMA单独使用和复配使用对碳钢的缓蚀性能和协同效应,通过分子动力学模拟计算缓蚀剂分子在Fe表面的吸附能,使用协同参数S衡量复配缓蚀剂的协同效应强弱,并对协同缓蚀机理进行了探讨,以期得到一种效果良好且绿色环保的复配缓蚀剂。
1 实验方法
1.1 实验材料
采用20#钢标准试片,尺寸为50 mm×10 mm×3 mm;腐蚀溶液为自来水,其中Cl-的质量浓度为178.136 mg/L,pH值为7.53;葡萄糖酸钠、二甲氨基丙基甲基丙烯酰胺,分析纯,阿拉丁科技(中国)有限公司;石油醚,分析纯,北京伊诺凯科技有限公司;无水乙醇,分析纯,国药集团化学试剂北京有限公司。
1.2 缓蚀剂溶液的配制
将SG、DMAPMA分别加入到自来水中,配制成质量浓度为50、100、200 mg/L的单一缓蚀剂溶液。将SG和DMAPMA分别以1∶4、1∶1和4∶1的质量浓度比加入自来水中,体系的总质量浓度为100 mg/L,制得复配缓蚀剂溶液。以未添加缓蚀剂的自来水作为空白对照。
1.3 失重测试
用脱脂棉擦拭腐蚀试片表面的防锈油,依次经石油醚、无水乙醇清洗,然后冷风吹干进行称重。将试片悬挂在装有自来水或缓蚀剂溶液的玻璃瓶中,每组挂片做3个平行样,试验温度为60 ℃,时间为72 h。试验结束后,将试片取出,浸泡在酸洗液中3~5 min,用去污粉洗去试片上的腐蚀产物,然后用乙醇脱水,吹干后称重。
腐蚀速率(深度指标)按照公式(1)计算得到。
(1)
式中,V为腐蚀速率,mm/a;Δm为试片腐蚀前后的质量差,g;ρ为碳钢密度,7.8 g/cm3;S为试片的表面积,m2;t为试片的试验时间,h。
失重法的缓蚀率按照公式(2)计算得到。
(2)
式中,ηw为由失重法计算得到的缓蚀率;V0为空白对照组的腐蚀速率,mm/a;Vint为缓蚀剂溶液的腐蚀速率,mm/a。
1.4 电化学测试
电化学测试采用Interface 1000型电化学工作站(美国Gamry公司)完成。在60 ℃恒温水浴下采用三电极体系进行测试,以20#钢样品为工作电极,有效接触面积为1 cm2,铂为辅助电极,饱和甘汞电极为参比电极。试验溶液为自来水或缓蚀剂溶液。电化学阻抗(EIS)的频率测试范围为105~10-2Hz,振幅10 mV。动电位极化曲线测量的扫描范围为-250~+250 mV(相对于开路电位),扫描速率为0.167 mV/s。
电化学法的缓蚀率按照公式(3)计算得到。
(3)
式中,ηe为由电化学结果计算得到的缓蚀率;I为空白对照组的腐蚀电流密度,μA/cm2;Icorr为缓蚀剂溶液的腐蚀电流密度,μA/cm2。
表面覆盖率Θ按照公式(4)计算得到。
Θ=ηe/100%
(4)
1.5 表面分析
采用光学显微镜(JT- 1600B型,深圳市精拓优诚科技有限公司)和场发射环境扫描电子显微镜(FESEM)(Quanta 200F型,美国FEI公司)进行表面形貌观察。采用X射线光电子能谱仪(XPS)(ESCALAB 250Xi型,美国赛默飞世尔科技公司)分析表面成键情况。
1.6 分子动力学模拟
运用Material Studio 软件进行建模模拟,模拟过程采用Compass力场,在NVT系综下进行300 ps的计算,步长为1 fs,温度为333 K。计算得到缓蚀剂分子在金属表面的吸附形态、吸附能,探究缓蚀剂的缓蚀机理。
2 结果与讨论
2.1 失重分析结果
表1为采用失重法测得的单一缓蚀剂和复配缓蚀剂的腐蚀速率和缓蚀率。从表1中可以看出,单一SG的缓蚀率随着其质量浓度的增大而增加,在200 mg/L时缓蚀率最大,为69.97%;单一DMAPMA的缓蚀率也随着其质量浓度的增大而增加,在200 mg/L时缓蚀率最大,为63.34%。在SG和DMAPMA的复配体系中,1∶4、1∶1和4∶1这3种配比的复配缓蚀剂的缓蚀率均达到95%以上,其中1∶1配比的复配缓蚀剂的缓蚀率最高,为98.01%。在总质量浓度(100 mg/L)相同的条件下,1∶1配比的复配缓蚀剂的缓蚀率相对于单一SG和单一DMAPMA分别提高了53.09%和64.03%。
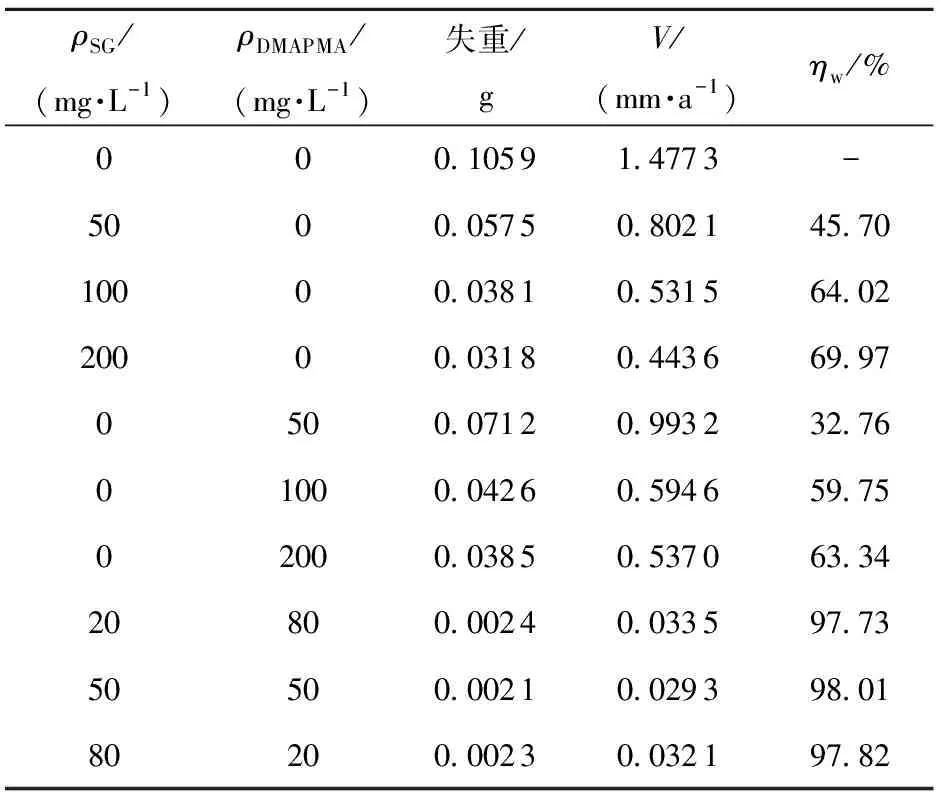
表1 采用失重法测得的单一缓蚀剂和复配缓蚀剂的腐蚀速率和缓蚀率
2.2 动电位极化曲线分析
图1为单一缓蚀剂和复配缓蚀剂的动电位极化曲线,表2为对动电位极化曲线拟合得到的电化学参数。

图1 单一缓蚀剂和复配缓蚀剂的动电位极化曲线Fig.1 Potentiodynamic polarization curves of the single and compound corrosion inhibitors

表2 动电位极化曲线的拟合参数、缓蚀率和表面覆盖率
由结果可知,SG和DMAPMA都属于阳极型缓蚀剂。与空白对照组相比,单一SG的自腐蚀电位E均正移,但是SG的质量浓度变化对E的影响不大。对于单一DMAPMA,50 mg/L的质量浓度对钢片的腐蚀没有抑制作用,继续增加质量浓度,溶液表现出一定的缓蚀效果,当质量浓度达到200 mg/L时,缓蚀率为72.16%。复配缓蚀剂与空白组相比,自腐蚀电位正移,曲线明显向左移动,并且缓蚀率都达到了95%以上,表明其缓蚀效果明显提高。当复配缓蚀剂中含有50 mg/L SG 和50 mg/L DMAPMA时,腐蚀电流密度最小,缓蚀率为97.20%,缓蚀效果最好。当SG和DMAPMA复配时,缓蚀效果明显要比单一使用时好很多,这说明二者之间存在着缓蚀协同效应。
2.3 电化学阻抗分析结果
图2为单一缓蚀剂和复配缓蚀剂的电化学阻抗谱图。图2(a)中,中高频区域阻抗弧全为半圆形,其中50 mg/L SG+50 mg/L DMAPMA配方的阻抗弧半径最大,缓蚀性能最好;图2(b)中,由低频区域的阻抗弧值大小可以看出,50 mg/L SG+50 mg/L DMAPMA配方的阻抗值最大,缓蚀效果最好,其次是80 mg/L SG+20 mg/L DMAPMA配方,其缓蚀效果较好。

图2 单一缓蚀剂和复配缓蚀剂的EIS谱图Fig.2 EIS of the single and compound corrosion inhibitors
由于在复配缓蚀剂的作用下,相位角图只有一个峰,说明可以采用含有一个时间常数的电路模型进行描述。图3为采用ZSimpWin软件对电化学阻抗谱拟合的等效电路图,其中,Rs表示溶液电阻,CPEdl表示膜层/基体界面的电容,Rct表示电荷转移电阻。由于腐蚀过程中Rs相对于Rct小很多,且其值变化并不大,所以Rct的大小体现了缓蚀剂缓蚀性能的好坏。

图3 对EIS拟合的等效电路图Fig.3 Equivalent circuit diagram fitted to EIS
表3为拟合等效电路的各参数值,由结果可知,复配缓蚀剂的Rct均远大于单一缓蚀剂,并且在复配比为1∶1时达到最大,为22 100 Ω·cm2,说明复配缓蚀剂对于碳钢在循环水体系中的缓蚀效果比单一缓蚀剂好得多。

表3 等效电路图的参数Table 3 Parameters of the equivalent circuit diagram
2.4 表面形貌
试片在单一缓蚀剂和复配缓蚀剂中腐蚀72 h后的光学显微镜照片如图4所示。由图中可以明显看出,空白组的腐蚀最严重,单独SG和单独DMAPMA均出现不同程度的腐蚀现象,其中SG的缓蚀效果较好;复合缓蚀剂的试样表面较光亮,无明显腐蚀痕迹,说明其缓蚀效果最好。

图4 在单一缓蚀剂和复配缓蚀剂中浸泡72 h后试片的光学显微镜照片Fig.4 Optical microscope photos of the test pieces immersed in the single and compound corrosion inhibitors for 72 h
试片在复配缓蚀剂(50 mg/L SG+50 mg/L DMAPMA)中腐蚀72 h后的FESEM照片如图5所示。从图中可以看出,空白组的表面腐蚀坑很多,而添加复配缓蚀剂后钢片的表面基本没有缺陷,表面成膜较好,砂纸打磨过的痕迹清晰可见,说明该复配缓蚀剂的缓蚀性能良好。

图5 在复配缓蚀剂中浸泡72 h后试片的FESEM照片Fig.5 FESEM photos of the test pieces immersed in the compound corrosion inhibitor for 72 h
2.5 XPS结果


图6 试片在复配缓蚀剂中浸泡12 h后的XPS图谱Fig.6 XPS spectra of the test pieces immersed in the compound corrosion inhibitor for 12 h
2.6 分子动力学模拟结果
图7为通过分子动力学模拟得到的缓蚀剂分子在铁表面上的吸附模型。从图中可以看出,两种缓蚀剂分子都吸附在铁表面,其上的O原子与Fe原子存在吸附作用,使得缓蚀剂分子靠近Fe表面,从而吸附在金属表面,起到抑制腐蚀的作用。通过模拟计算得到SG、DMAPMA、复配缓蚀剂的吸附能分别为324.339、235.363、378.267 kJ/mol,表明复配缓蚀剂的吸附能大于单一缓蚀剂,理论上性能更优于单一缓蚀剂。

图7 通过分子动力学模拟得到的缓蚀剂分子在铁表面上的吸附模型Fig.7 Adsorption model of the corrosion inhibitor molecules on the iron surface as obtained by molecular dynamics simulation
2.7 缓蚀剂之间的协同参数
通常通过协同参数S来说明缓蚀剂组分之间协同程度的大小。对于复配使用的SG和DMAPMA,协同参数S的计算公式如下[16]。
(5)
式中,ηa和ηb分别为SG和DMAPMA单独存在时的缓蚀率(失重法),ηab为二者复配时的缓蚀率(失重法)。若S>1,表示复配体系具有明显的协同效应;若S≤1,表示复配体系的协同效果不明显或者存在拮抗效应;S值越大,复配缓蚀剂的协同作用越强。
通过计算得到3种复配体系(复配比1∶4、1∶1、4∶1)的协同系数分别为37.30、32.58、33.95,均远大于1,说明它们之间存在较强的协同效应。
2.8 缓蚀剂之间的协同机理
本文的研究结果表明,SG和DMAPMA在循环水体系中具有良好的协同缓蚀效果。失重法结果表明,50 mg/L SG+50 mg/L DMAPMA复配后将单一缓蚀剂的缓蚀率(100 mg/L SG,64.02%;100 mg/L DMAPMA,59.75%)提升至98.01%。结合以上研究结果,本文提出SG和DMAPMA的协同缓蚀机理,示意图如图8所示。

图8 SG和DMAPMA的协同缓蚀机理示意图Fig.8 Schematic diagram of synergistic corrosion inhibition mechanism of SG and DMAPMA
分子动力学模拟结果表明,SG在碳钢表面的吸附能力要强于DMAPMA,所以在循环水体系中SG优先吸附于碳钢表面,形成具有一定缺陷的吸附膜层。基于补强理论,引入DMAPMA能够使SG进一步吸附在碳钢表面,填充原有SG吸附膜的缺陷,使得吸附膜层更加致密。同时,SG分子中具有—COO-,能够和DMAPMA分子中的酰胺基相互作用,形成双层吸附膜,实现对碳钢的双重保护。因此,SG和DMAPMA复配之后极大地提升了碳钢在循环水体系中的缓蚀效果,实现了对碳钢的有效保护。
3 结论
(1)由失重法和电化学测试结果可知,当复配缓蚀剂的总质量浓度为100 mg/L时,SG和DMAPMA复配具有良好的协同作用,对20#钢的缓蚀效果良好,缓蚀率达到95%以上。当复配缓蚀剂含有50 mg/L SG和50 mg/L DMAPMA时,其缓蚀效果最好,成膜较好,性能较优。
(2)分子动力学模拟和XPS结果表明,SG和DMAPMA可以吸附在Fe表面,并且相互补强,促进其在Fe表面形成较致密的吸附膜,从而对碳钢起到较好的保护作用,可作为一种有效的缓蚀剂使用。

