葵花杆的热解特性及热解产物分析
纪东骅, 李红岩, 雷振东, 缪高健, 赵 明, 王志和
(南京林业大学 材料科学与工程学院,江苏 南京 210037)
随着各国工业的迅速发展,温室气体的排放导致全球气候异常,发展低碳清洁的能源成为人类应对气候变化的有效途径[1]。生物质能源作为一种清洁的可再生能源[2],它的可再生性和环保性得到了各国能源机构以及国际能源机构(IEA)的一致认可。通过光合作用目前全球每年能产生1 730亿吨的生物有机质,其所蕴含的能量相当于全球能源消耗量的10~20倍[3]。我国“十三五规划”指出,我国正处于能源转型升级的重要时期,开发和利用生物质能对支持我国在能源供给侧结构性改革,减少对化石能源的依赖和建设良好的生态环境都有着重要的战略意义。然而,我国生物质能源产业市场化程度低,社会对生物质能源缺乏正确的认识,露天焚烧和就地填埋仍是生物质资源主要的处理手段。
生物质热解技术是通过热化学的方法实现生物质能的利用[4]。张艳等[5]将玉米秸秆和芦苇秸秆按一定质量比混合后进行共热解实验,探究了混合物共热解的热解规律以及热重(TG)和微分热重(DTG)。童晟轩等[6]采用热重-质谱联用技术,对比并分析了3种生物质原料在热裂解中气体产物(CO、H2、CH4、CO)随温度变化的释放规律。严云等[7]以4种生物质(野生狸藻、荞麦壳、玉米秸秆、柳树枝)为研究对象,利用差热-热重分析仪进行热重分析,考虑不同升温速率对热解反应的影响,通过分析TG-DTG曲线探讨生物质的热解特性,运用Coats-Redfern积分法进行动力学计算,得到4种生物质的热解活化能。葵花杆在我国的储量巨大,但是综合利用效率却很低,本研究利用同步热分析仪对葵花杆进行热解,分析不同升温速率对热解特性的影响,并对葵花杆热解产物进行分析,以期为深入研究葵花杆的热解机理以及热解产物的有效利用提供理论基础。
1 材料与方法
1.1 材料及仪器
葵花杆,来源于甘肃省庆阳市,在自然条件下风干,经高速智能粉碎机粉碎后,选取≤0.2 mm的样品,利用烘箱将样品烘干并进行热解实验。原料的工业分析、组分分析及元素分析结果如表1所示。

表1 葵花杆工业分析、组分分析及元素分析结果
Vario ELⅢ全自动元素分析仪;STA409PC型同步热分析仪,德国Netzsch公司;Agilen GC7890A-MSD5975C型气相色谱-质谱联用仪,美国安捷伦公司。
1.2 实验方法
1.2.1TG分析 称取质量为10 mg的试样放入氧化铝坩埚中,放入同步热分仪中进行分析。升温速率选取10、 20和30 ℃/min,热解温度从室温升温至800 ℃,保护气为25 mL/min的氮气。
1.2.2Py-GC/MS分析 称取质量为0.5 mg的试样放入热裂解仪的石英管中,采用石英棉固定管的两端,将该管放到快速加热铂金灯丝中间的位置。热裂解仪附件温度保持在250 ℃,探针初温为 20 ℃,升温至800 ℃,等样品热解完全后,进行GC/MS分析。GC/MS工作条件:HP-5MS毛细管柱(30 m×250 μm×0.25 μm);分流比50 ∶1;进样口温度250 ℃;氦气流速1 mL/min;程序升温为50 ℃保持2 min,再以10 ℃/min的升温速率升至160 ℃,然后以20 ℃/min的升温速率升至 280 ℃并保持2 min,总运行时间为21 min。接口温度280 ℃;电子轰击离子源温度230 ℃;四极杆温度150 ℃;电离能70 eV;质量扫描范围97~350 u。利用NIST08谱库对GC/MS检测结果进行定性分析,单个化合物的相对含量用GC/MS数据分析软件直接计算得出。
2 结果与分析
2.1 热解特性参数分析
葵花杆在不同升温速率下的TG/DTG曲线如图1所示。由图可知,葵花杆热解过程主要分为预热干燥(室温~125 ℃)、主要热解(125~400 ℃)和炭化(400~800 ℃)3个阶段。葵花杆的热解特征参数见表2和表3。
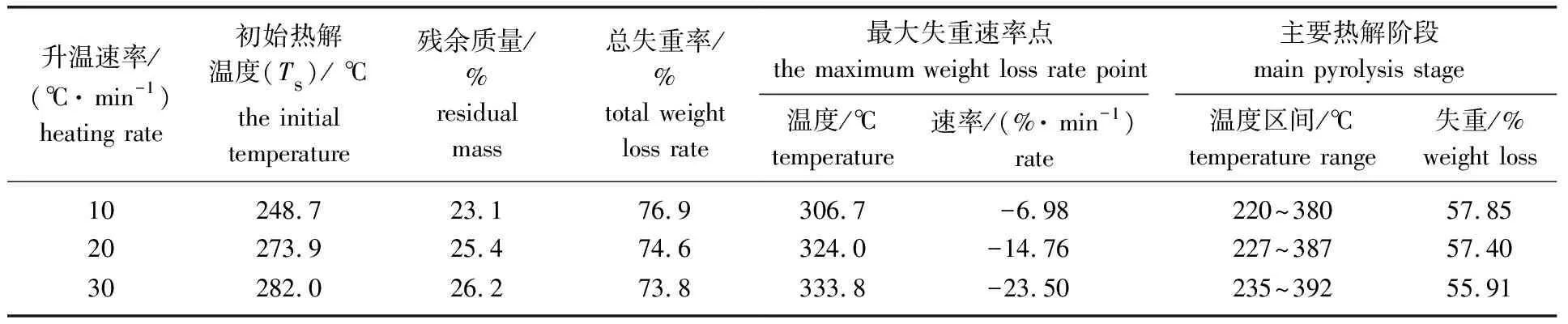
表2 不同升温速率下葵花杆热解参数
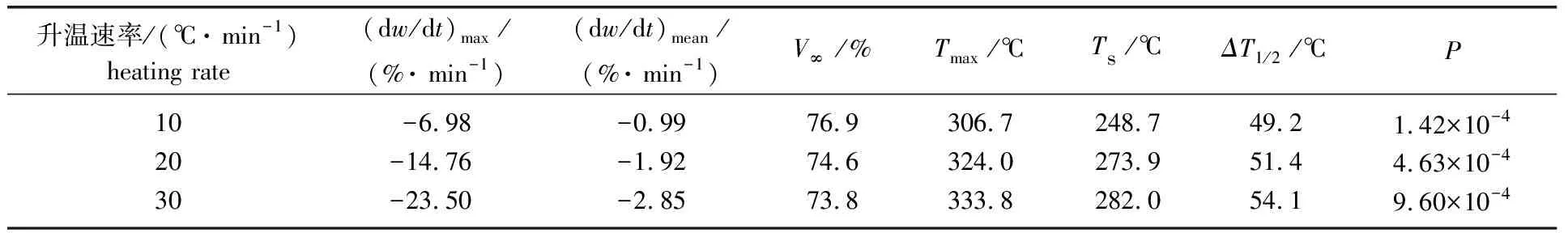
表3 不同升温速率下葵花杆热解特性指数
为综合评价葵花杆的热解特性,定义热解特性指数(P)[8]为:
P=(dw/dt)max(dw/dt)meanV∞/(TmaxTsΔT1/2)
(1)
式中:P—热解特性指数,生物质热解特性的判断指标,P值越大,挥发分的析出特性越好,热解效果越强; (dw/dt)max—挥发分最大失重速率,DTG曲线中峰值,%/min; (dw/dt)mean—挥发分平均失重速率,热解的失重率与时间的比值,%/min;V∞—热解最大失重率,%;Tmax—对应(dw/dt)max的峰值温度, ℃;Ts—初始热解温度, ℃; ΔT1/2—半峰宽,指(dw/dt)/(dw/dt)mean=1/2时对应的温度区间。
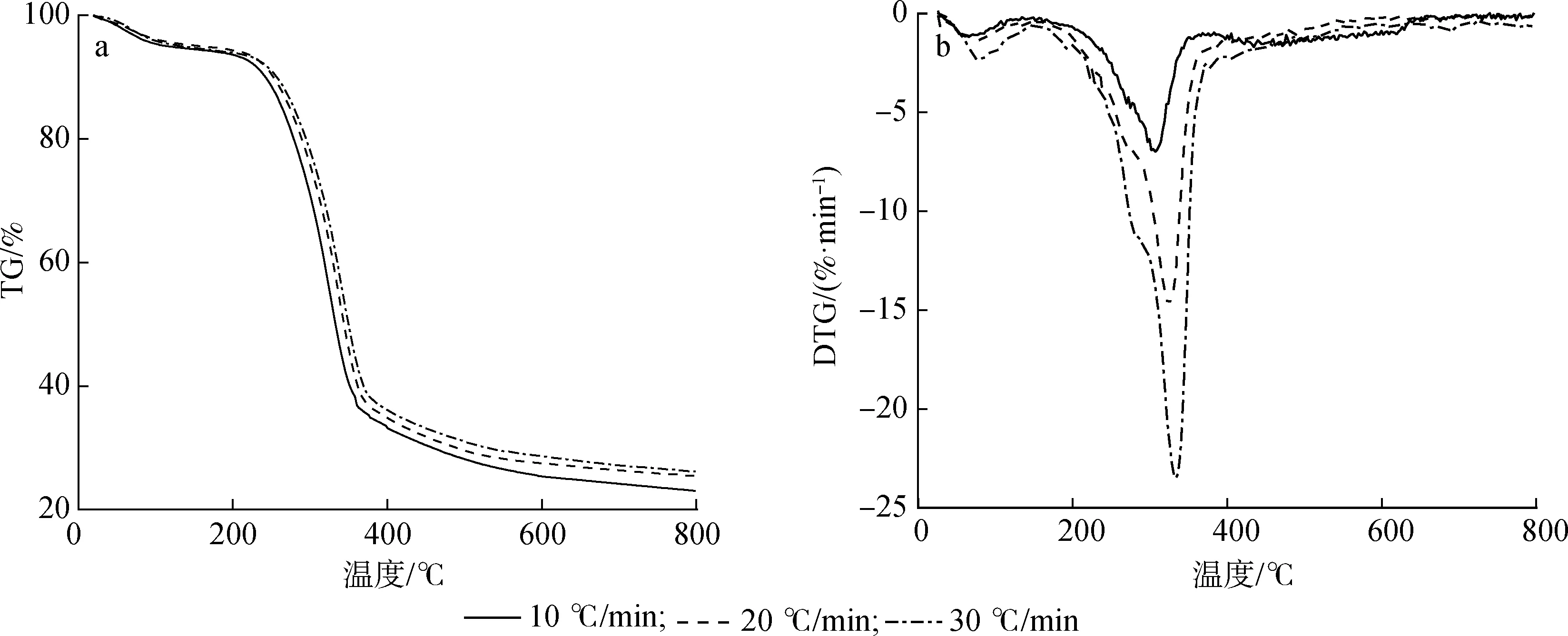
a.TG; b.DTG图1 不同升温速率对葵花杆热解过程的影响Fig.1 TG/DTG curves of sunflower stem at different heating rate in pyrolysis process
由表可知,随着升温速率的增大,葵花杆热解的初始温度增大,峰值温度、速率增大,主要热解温度区间向高温区移动,从传热学角度分析,主要是因为升温速率不同导致热滞后而引起的[9]。升温速率越大,葵花杆热解特性指数P越大,即热解反应越容易,挥发分释放越剧烈,但挥发分释放量减少;升温速率越低,挥发分释放高峰越早,总体热解反应就越集中。
由图1还可以看出,葵花杆在第一阶段TG曲线呈较小幅度下降的趋势,而DTG在此区间内有一个峰值,此过程试样中的自由水干燥脱离;葵花杆热解的第二阶段又可分为两部分,其中125~220 ℃区间内TG曲线只有微量波动,此过程中释放出小分子化合物[10-11];在220~400 ℃内葵花杆的TG曲线呈现急剧下降的形式,DTG曲线出现了峰值,此过程葵花杆热解为小分子气体及大分子可冷凝性挥发成分,该阶段失重约为总失重的85%[12-13];葵花杆在第三阶段,TG及DTG曲线都趋于平缓,在此阶段内主要以木质素热解为主,热解的主要产物为炭及灰分。在葵花杆热解主要阶段,需要先进行半纤维素缓慢热解,再进行纤维素快速热解,在DTG曲线上则表现出,升温速率为30 ℃/min时葵花杆热解出现肩峰,而在升温速率为10 ℃/min时肩峰不明显,主要是由半纤维素和纤维素相对含量相差不大导致,这与三大素含量测试结果相符[14-15]。
2.2 热解动力学参数分析
生物质热解的动力学方程可表示为:
dα/dt=k(T)f(α)
(2)
式中:t—反应时间,s;T—反应温度,K;α—反应转化率,可由TG曲线求得,α=(mo-mt)/(mo-mf),mo为初始原料质量,mt为原料在反应某时刻时的质量,mf为反应结束时残余物质量;f(α)=(1-α)n,n为反应级数;k(T)—阿伦尼乌斯速率常数,k(T)=Ae-E/RT,A为指前因子,min-1,E为活化能,kJ/mol,R为气体常数,8.314 J/(mol·K)。
将升温速率常数β=dT/dt代入式(2),动力学方程可写成:
(3)
本研究采用CR法计算葵花杆热解动力学参数,对式(3)进行分离变量积分并取近似值,最终得到式(4)和式(5):
当n=1时
(4)
当n≠1时
(5)
当n=1时,ln[-ln(1-α)/T2]对1/T作图;当n≠1时,ln[(1-(1-α)1-n)/(T2(1-n))]对1/T作图,如果选定的n值正确,回归拟合结果为一条直线,根据直线斜率(-E/R)和截距(lnAR/Eβ)求热解动力学参数得到活化能(E)和指前因子(A)。
表4为葵花杆在升温速率为10、 20、 30 ℃/min时的热解动力学拟合结果(n=1)。
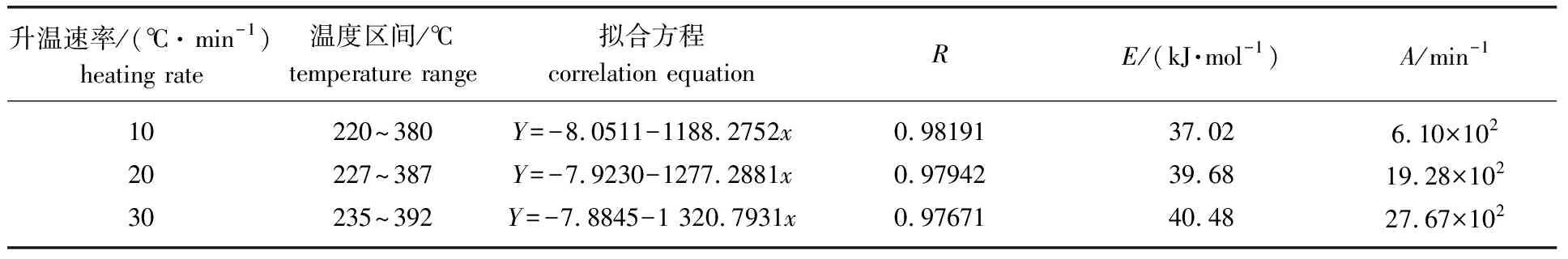
表4 葵花杆热解动力学拟合结果
经计算得出,级数n取1时,葵花杆热解过程的曲线拟合效果较好,线性相关系数均大于0.97,具有较高的线性拟合相似度。不同升温速率下的A为6.10×102~27.67×102min-1,随着升温速率的提高,葵花杆活化能的变化不大,但仍呈上升趋势,主要是因为热解反应过程中由于升温速率的提高使热量短时间内无法均匀传递造成滞后现象,使得该反应需要更多的能量。葵花杆的活化能最大值只有40.48 kJ/mol,低于家禽粪便(60 kJ/mol)[16]和白松(43.78 kJ/mol)[17],这说明葵花杆的热解反应更容易发生。从表4还可以看出,指前因子与活化能之间存在一定动力学规律,随着活化能的增大,指前因子也增大,二者可能存在某种补偿效应[18-19]。
2.3 热解产物分析
使用热裂解-气相色谱/质谱联用(Py-GC/MS)技术对葵花杆热解产物进行分析,得到葵花杆的总离子流色谱图如图2所示,热解产物保留时间为1.5~20 min,有224个特征峰。利用NIST08谱库检索相似度高于80%以上的热解产物,一共测出106个特征峰86种特征物质,包括17种酚类化合物(6.07%)、 9种芳香烃化合物(1.82%)、 11种烷烃(10.74%)、 13种烯烃(7.9%)、 5种醛类化合物(1.87%)、 8种酮类化合物(4.47%)、 7种羧酸类化合物(39.27%)、 4种醇类化合物(1.922%)、 4种酯类化合物(18.94%)、 3种醚类化合物(0.35%)和5种含氮有机化合物(1.48%)。
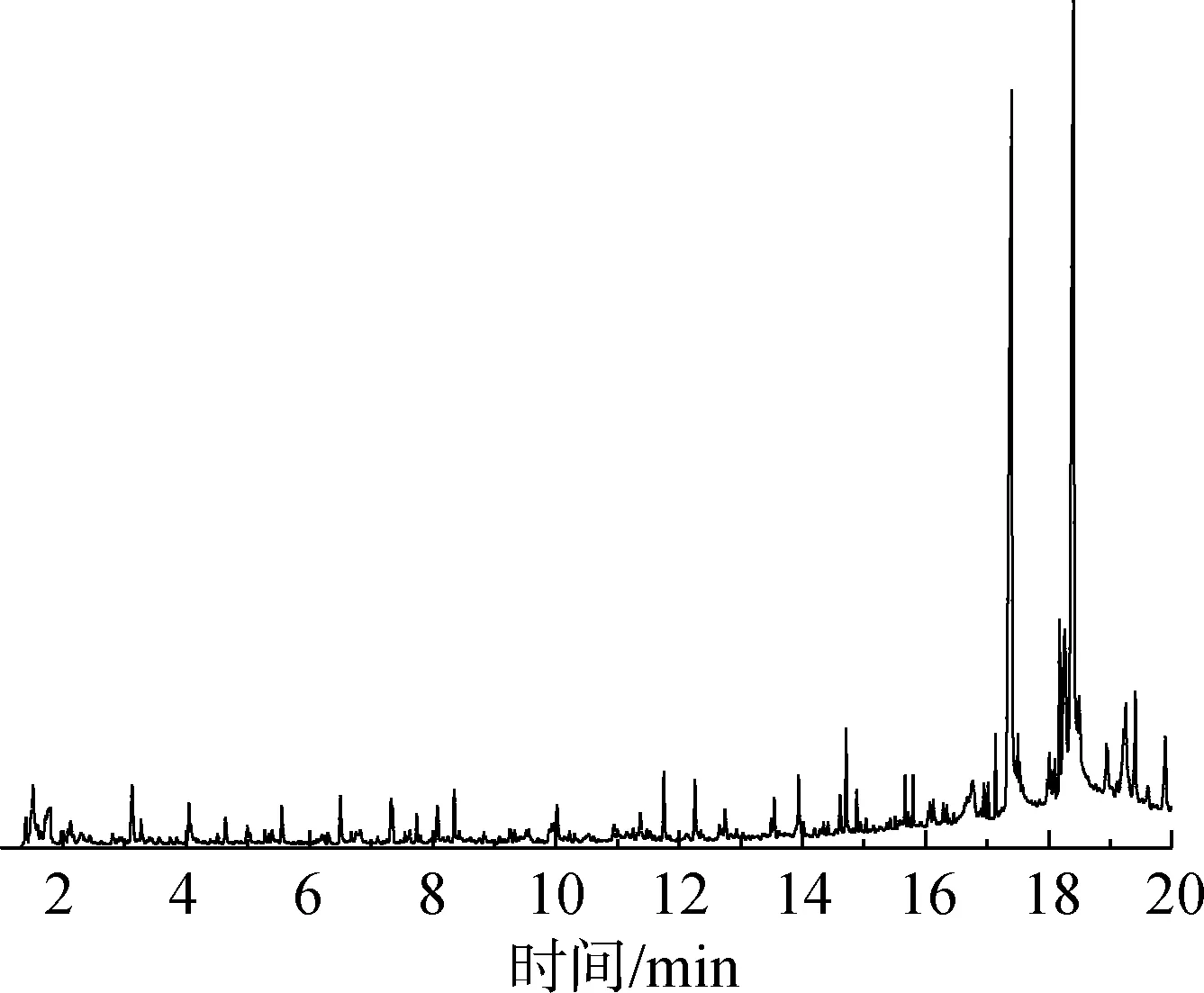
图2 葵花杆Py-GC/MS总离子流色谱图Fig.2 Sunflower stem Py-GC/MS total ion chromatogram
取葵花杆热解产物中相对含量较高的25种有机物进行分析,结果如表5所示。由表可知,葵花杆热解以后的主要产物为酸类、烃类和脂类化合物,这3种产物的相对峰面积占检测出挥发性物质的55.44%,其中酸类化合物最多。硬脂酸在葵花杆热解产物中最多,高达29.991%,硬脂酸在工业上可以作为添加剂,用来提高聚氯乙烯(PVC)的热稳定性。在橡胶的合成和加工过程中硬脂酸都有着不可替代的作用[20]。而酸类中的棕榈酸含量仅次于硬脂酸,高达27.642%,它是一种饱和高级脂肪酸,以棕榈酸为基材可以制备复合变相材料[21]。在烷烃化合物中含量最高的是正十八烷,为7.185%,以原位聚合法可以制备以正十八烷为囊芯的微胶囊,制备的微胶囊具有很好的相转变热性能,可以广泛应用于能量储存和温度控制方面[22]。对葵花杆热解产物的定性定量分析能够为其进一步高效利用提供依据。
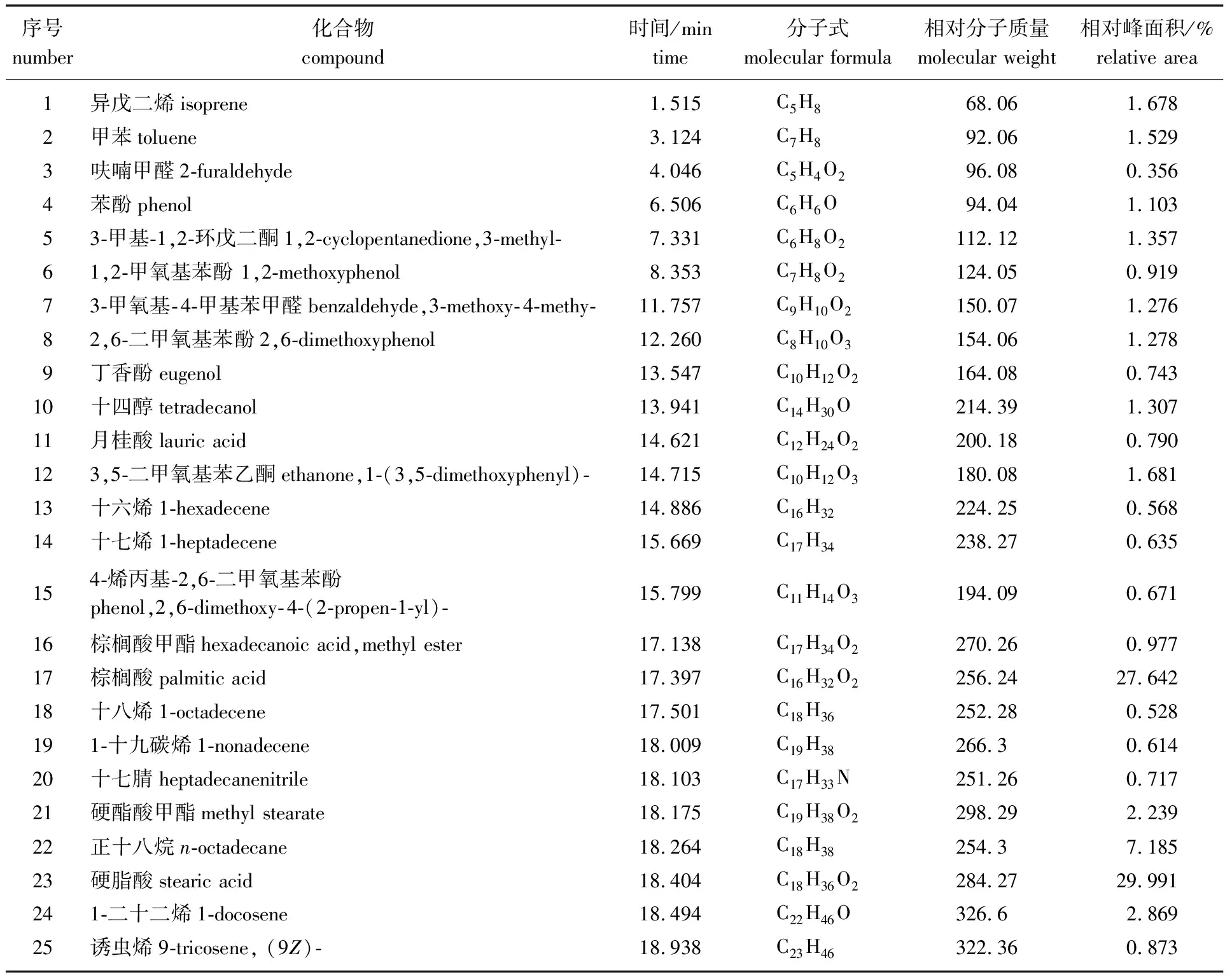
表5 葵花杆的热解产物分析
3 结 论
3.1葵花杆的热解过程可分为预热干燥、主要热解及炭化3个阶段;在主要热解阶段,升温速率较小时肩峰不明显,这主要与葵花杆中纤维素、半纤维素相对含量相差较小有关,该结论与三大素测量结果相一致。根据CR法求得葵花杆热解动力学参数可知,随着升温速率的增大,活化能(E)与指前因子(A)都呈现增大趋势,二者可能存在某种补偿效应。在主热解阶段(125~400 ℃),葵花杆的失重率约为总失重的85%,活化能(E)为37.02~40.48(kJ/mol),指前因子(A)6.10×102~27.67×102min-1,线性拟合相关系数均大于0.97。
3.2根据热裂解-气相色谱/质谱联用(Py-GC/MS)仪对葵花杆热解产物检测结果可知,葵花杆热解产物主要有11类不同化学物质,其中酸类、烃类和脂类化合物的相对含量较高,约占检测出挥发性物质的55.44%。葵花杆热解产物中,相对含量较高的分别是硬脂酸(29.991%),棕榈酸(27.642%)和正十八烷(7.185%)。

