强力枇杷露质量控制方法的研究进展
黎强 樊文研 陈宇 庞小莲 卢森华

摘要 强力枇杷露是2020年版《中国药典》新增品种,由枇杷叶、罂粟壳和百部等药组成,具有养阴敛肺和镇咳祛痰的功效,适用于久咳劳嗽和支气管炎等病症。药典规定对其处方中枇杷叶、罂粟壳、薄荷脑进行定性鉴别,并对罂粟壳中的吗啡含量进行测定。为进一步完善其质量控制体系,对强力枇杷露质量控制方法的研究进展进行综述,包括定性鉴别、有效成分含量测定、微生物限度检查等,并分析各方法的优势和不足,以期为建立该品种更为完善的质量控制体系提供参考。
关键词 强力枇杷露;质量控制;临床应用
中图分类号 R286.0 文献标识码 A 文章编号 0517-6611(2021)13-0012-05
doi:10.3969/j.issn.0517-6611.2021.13.004
开放科学(资源服务)标识码(OSID):
Research Progress on Quality Control of Qiangli Pipa Syrup
LI Qiang,FAN Wen yan,CHEN Yu et al
(Yulin Center for Food and Drug Control,Yulin, Guangxi 537000)
Abstract Qiangli Pipa Syrup is a new variety of Chinese Pharmacopoeia (2020 Edition), which is composed of loquat leaf, poppy shell and Baibu. It has the effect of nourishing yin and astringent lung and relieving cough and expectoration. It is suitable for chronic cough, cough and bronchitis. According to the Pharmacopoeia, loquat leaf, poppy shell and menthol in the prescription were identified qualitatively, and the content of morphine in poppy shell was determined. In order to further improve its quality control system, the research progress of quality control methods for Qiangli Pipa Syrup was reviewed, including qualitative identification, determination of effective components content, microbial limit test, etc., and the advantages and disadvantages of each method were analyzed, so as to provide reference for establishing a more perfect quality control system of this variety.
Key words Qiangli Pipa Syrup;Quality control;Clinical application
強力枇杷露是2020年版《中国药典》新增品种和《中华人民共和国卫生部标准·中药成方制剂》(第二册)收载品种,处方中包含枇杷叶、罂粟壳、百部、桔梗、桑白皮和薄荷脑等,其功效是养阴敛肺和镇咳祛痰,适用于久咳劳嗽合支气管炎等病症[1-2]。强力枇杷露是在传统止咳枇杷露的基础上加入罂粟壳而制成。因其止咳功能比一般的枇杷露大大加强,故称为强力枇杷露。众多的医药工作者采用现代科技手段,对强力枇杷露的内在质量作用机理及临床应用等进行了深入研究,为其生产和临床使用提供了科学依据,在此,笔者主要针对强力枇杷露质量控制方法方面的研究情况进行总结,分析各方法的优势与不足,为进一步提高和改进其质量控制方法、建立该品种更为完善的质量控制体系提供参考。
1 定性鉴别
按照有关中药复方制剂的鉴别选择原则,需对制剂中1/3以上药材进行鉴别说明。因此,2020年版《中国药典》中强力枇杷露建立了药材枇杷叶、罂粟壳、薄荷脑的定性鉴别方法,原标准仅有生物碱及黄酮的化学反应鉴别,专属性差,可控性不强,新标准大大提升了强力枇杷露定性鉴别水平[2]。目前,强力枇杷露制剂的定性鉴别方法包括化学鉴别、薄层鉴别等技术,还有一些新技术也逐渐得到应用。
1.1 化学鉴别
化学鉴别是根据药物与化学试剂在一定条件下发生的化学反应所产生的颜色、沉淀、气体、荧光等现象,鉴别药物真伪的方法,多采用典型的官能团反应。盛平钦[3]研究发现按该品种《中华人民共和国卫生部标准·中药成方制剂》标准项下的鉴别(2)操作,显色不明显,结果难判断,为此,在以桑白皮药材作为对照鉴别的基础上,改用加大取样量、置平底瓷蒸发皿内、水浴加热的方法操作,结果理想。王方升[4]对强力枇杷露鉴别项操作要点提出多项提示,如加正丁醇振摇提取时,应轻轻摇动,使正丁醇与供检品能充分混合接触即可。若剧烈振摇,则会使供检品与正丁醇发生乳化作用,静置后很难分层,无法分取提取液,从而使操作难以继续进行。加镁粉要足量,加盐酸要迅速,使黄酮类成分有充分的机会被盐酸-镁粉产生的足量原子态氢还原,生成花色甙元及其二聚物而显色。若加镁粉量不足,滴加盐酸速度过慢,则使反应不能充分进行,从而使颜色变化不明显或无变化。
1.2 薄层鉴别
薄层色谱法是对中药成分组分体系分析的重要手段,具有分离和鉴别双重功效,且快速、经济、使用范围广[5]。强力枇杷露中枇杷叶、罂粟壳、百部、桔梗和薄荷脑等均建立了薄层色谱鉴别方法。2020年版《中国药典》中建立了枇杷葉、罂粟壳、薄荷脑的薄层鉴别方法。
1.2.1 枇杷叶。张国跃等[6]采用薄层色谱法鉴别强力枇杷露中枇杷叶,枇杷叶的鉴别供试样用正丁醇萃取,蒸干,残渣加甲醇0.5 mL作为供试品溶液,在硅胶 G 薄层板上,以环己烷-乙酸乙酯-冰醋酸(12∶2∶0.2)为展开剂展开,取出,晾干,喷以10%硫酸乙醇溶液,110 ℃加热至斑点清晰,置紫外光灯(365 nm)下检视,结果供试品色谱中,在与对照品色谱相应的位置上,显相同颜色的荧光斑点。吴洋等[7]优化和提高强力枇杷露的质量标准,应用薄层色谱法对处方中的枇杷叶进行鉴别,枇杷叶的鉴别供试样先加氢氧化钠试液调节pH,再用乙酸乙酯振摇提取,以甲环己烷-乙酸乙酯-冰醋酸(8∶4∶0.1)为展开剂,喷上10%的硫酸乙醇溶液,放置到烘箱中在105 ℃加热至斑点显色清晰。2020年版《中国药典》规定供试品溶液制备方法:取本品30 mL,加水饱和的正丁醇30 mL振摇提取,分取正丁醇液,用氨试液30 mL洗涤,弃去氨洗液,正丁醇液回收溶剂至干,残渣加甲醇1 mL使溶解,即得。展开剂为环己烷-乙酸乙酯-冰醋酸(8∶4∶0.1);显色喷以10%硫酸乙醇溶液,在105 ℃加热至斑点显色清晰,分别在日光和紫外光(365 nm)下检视[2]。
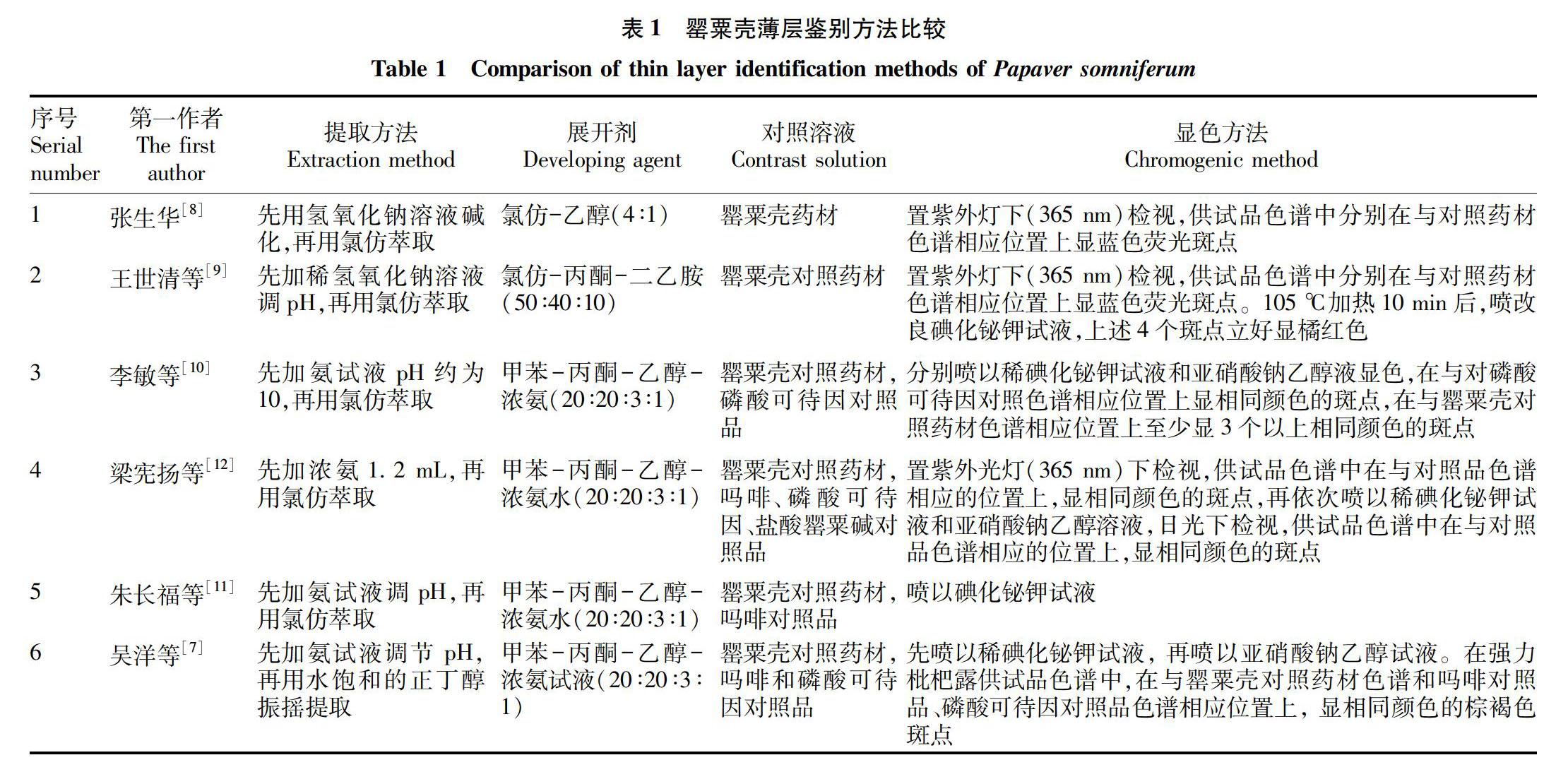
1.2.2 罂粟壳。张生华[8]和王世清等[9]应用薄层色谱法最先建立了强力枇杷露中罂粟壳鉴别方法,李敏等[10]以磷酸可待因对照品为参照,朱长福等[11]以吗啡对照品为参照,梁宪扬等[12]以吗啡、磷酸可待因、盐酸罂粟碱混合对照品溶液作参照,吴洋等[7]以吗啡和磷酸可待因对照品作参照,对强力枇杷露中罂粟壳鉴别方法进行改进,优化和提高强力枇杷露中罂粟壳的鉴别水平。罂粟壳鉴别方法比较见表1。2020年版《中国药典》规定供试品溶液制备方法:取本品20 mL,用浓氨试液调节pH至11~13,用水饱和的正丁醇振摇提取2次,每次20 mL,合并正丁醇液,回收溶剂至干,残渣加甲醇1 mL使溶解,即得。展开剂为甲苯-丙酮-乙醇-浓氨试液(20∶20∶3∶1);显色依次喷以稀碘化铋钾试液和亚硝酸钠乙醇试液,在日光下检视[2]。
1.2.3 百部。朱长福等[11]对强力枇杷露中百部采用薄层色谱法鉴别,百部的鉴别供试样用加正丁醇萃取,蒸干,残渣加甲醇1 mL作为供试品溶液,展开剂为甲苯-丙酮-乙醇-浓氨水(20∶20∶3∶1),喷以改良碘化铋钾试液,以此鉴别百部。
1.2.4 桔梗。吴洋等[7]优化和提高强力枇杷露的质量标准,应用薄层色谱法对处方中的桔梗进行鉴别,桔梗的鉴别:供试样先加5%硫酸乙醇溶液和水加热回流,再用二氯甲烷振摇提取,蒸干,残渣加甲醇1mL作为供试品溶液,在硅胶 G 薄层板上,展开剂为二氯甲烷-乙醚(1∶1),喷以10%硫酸乙醇溶液,放置到烘箱中在110 ℃加热至斑点显色清晰,以此鉴别桔梗。
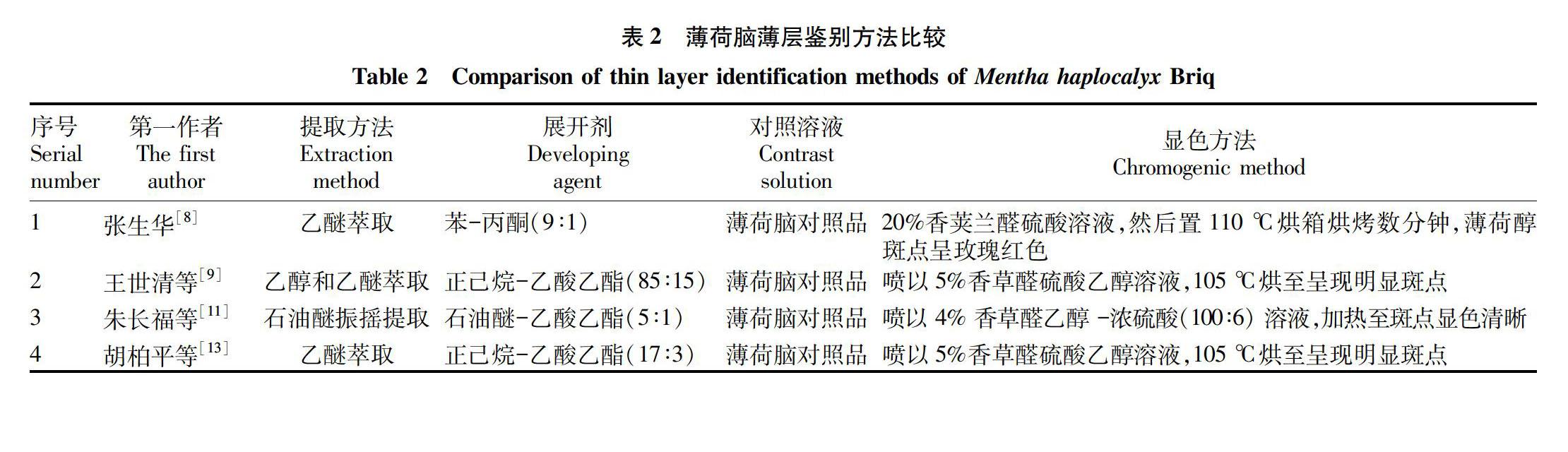
1.2.5 薄荷脑。张生华[8]、王世清等[9]、朱长福等[11]和胡柏平等[13]均采用薄层色谱法对制剂中的薄荷脑进行定性鉴别。薄荷脑的鉴别供试样提取方法,展开剂和显色方式各有不同,鉴别方法比较见表2。2020年版《中国药典》规定供试品溶液制备方法:取本品40 mL,用石油醚(30~60 ℃)40 mL振摇提取,分取石油醚液,挥干,残渣加乙醇1 mL使溶解,即得。展开剂为石油醚(30~60 ℃)-乙酸乙酯(5∶1),喷以香草醛硫酸试液-乙醇(1∶4)的混合溶液,在100 ℃加热至斑点显色清晰,日光下检视[2]。
2 有效成分含量测定
按照中成药君臣佐使的配伍原则,采用现代化的检测技术测定强力枇杷露中某味药材中所含有效成分的含量,从而评价该制剂的含量,并为临床用药提供参考[5]。强力枇杷露的含量测定方法包括紫外-可见分光光度法、气相色谱法、高效液相色谱法、原子吸收分光光度法、液相色谱-串联质谱法等。2020年版《中国药典》中仅建立了罂粟壳中吗啡的高效液相色谱定量方法。
2.1 紫外分光光度法
紫外分光光度法是根据物质对不同波长的紫外线吸收程度不同而对物质组成进行分析的方法,具有灵敏度高、操作简便、快速、适用范围广、设备便宜等优点,是中药分析中应用最广泛的分析方法之一[14]。尹萌等[15]采用酸性染料比色法测定强力枇杷露中盐酸罂粟碱的含量,样品加氨试液调pH 10,用苯提取出其中的盐酸罂粟碱,加溴甲酚紫形成有色化合物,在波长410 nm测定,结果盐酸罂粟碱含量在0.066~0.33 mg线性关系良好,平均加样回收率为97.12%。
2.2 气相色谱法
气相色谱法具有高效快速、高选择性、高灵敏度、样品用量少、方法稳定性好等特点,适用于挥发性成分的研究[14]。关晓娟等[16]和柴鑫莉等[17]采用顶空气相色谱法测定强力枇杷露中薄荷脑的含量,加样回收率分别为95.4%~99.8%、94.3%~99.6%。汪剑飞[18]和陈晓颙等[19]采用内标定量建立气相色谱法测定强力枇杷露中薄荷脑的含量的方法,平均加样回收率为96.90%。符映均等[20]则建立气相色谱法同时测定强力枇杷露中薄荷脑、磷酸可待因、吗啡、盐酸罂粟碱4种成分含量的方法,各成分在各自测定范围内有良好的线性关系,平均加样回收率在96.76%~11334%。气相色谱法测定强力枇杷露中有效成分含量的测定方法比较见表3。
2.3 高效液相色谱法
高效液相色谱法定量检测具有分离效率高、分析速度快、精密度高、稳定性好等特点,且不受样品挥发性和热稳定性的限制,是中成药进行含量测定的主要方法之一[14]。朱长福等[11]、王述蓉等[21]、周建衡等[22]、张国跃等[6]、李彬[23]采用高效液相色谱法测定强力枇杷露中吗啡的含量,平均加样回收率依次为103.4%、98.87%、9994%、100.73、97.95%。秦文杰等[24] 建立了测定强力枇杷露中罂粟碱的含量,平均回收率99.1%。章红等[25]、金阳[26]、巩晓宇等[27] 建立了测定强力枇杷露中磷酸可待因(可待因)的方法,平均加样回收率依次为99.9%、98.4%和982%。魏春芬[28]采用高效液相色谱法对强力枇杷露中的吗啡与可待因含量进行同时测定,吗啡的平均加样回收率为100.35%,可待因的平均加样回收率为106.78%。庞晓星等[29]采用高效液相色谱法同时测定吗啡、可待因、罂粟碱3种成分的含量并制定含量限度要求,平均回收率依次为992%、93.7%、89.7%。胡卫南[30] 建立了测定强力枇杷露中苯甲酸钠含量的方法,加样回收率为98.6%~101.70%。袁海英等[31]建立了强力枇杷露中齐墩果酸和熊果酸含量测定方法,齐墩果酸的平均加样回收率为93.7%,熊果酸的平均加样回收率为98.6%。高效液相色谱法测定强力枇杷露中有效成分含量的测定方法比较见表4。2020年版《中国药典》中供试品溶液制备方法:精密量取本品25 mL,用氨试液调节pH至10~11,用水饱和的正丁醇振摇提取3次,每次25 mL,合并正丁醇液,回收溶剂至干,残渣加甲醇适量使溶解,转移至25 mL棕色量瓶中,加甲醇至刻度,摇匀,即得。流动相为乙腈-0.1%磷酸溶液(3∶97);检测波长为210 nm;规定本品1 mL含罂粟壳以吗啡计,应为0.02~0.15 mg[2]。
2.4 液相色谱-串联质谱法
液相色谱-串联质谱法是以液相色谱作为分离系统,质谱仪为检测手段集高分离能力和高灵敏度、高选择性于一体,弥补了传统液相检测器的不足,尤其適用于在紫外区域无特征吸收,或含量较低的化合物的分析测定[14]。卢森华等[32]采用超高液相色谱-串联质谱法建立了强力枇杷露中罂粟碱、那可丁、蒂巴因、吗啡和可待因5种罂粟壳生物碱的多指标成分含量测定方法,流动相为含01%甲酸的乙腈溶液-含0.1%甲酸的10 mmol/L甲酸铵水溶液,梯度洗脱;采用ESI+源,MRM模式,罂粟碱、那可丁、蒂巴因、吗啡和可待因平均回收率依次为103.5%、101.4%、996%、98.9%、101.3%。,在5 min内即可同时准确测定强力枇杷露中罂粟碱、那可丁、蒂巴因、吗啡、可待因5种生物碱的含量,为强力枇杷露的质量控制提供了一种快速、灵敏、稳定、可靠的方法。
2.5 原子吸收分光光度法
原子吸收法是利用被测元素基态原子蒸汽对其共振辐射线的吸收特性进行元素定量分析的方法,具有灵敏度高、精密度好、应用范围广、干扰少、快速简便、易于自动化等特点[14]。郑民等[33]采用原子吸收光谱法测定7个不同厂家所生产的强力枇杷露中镁和镉元素含量,加样回收率在95.5%~104.2%。重金属超标是中药不良反应中最突出的问题之一,有害元素镉不仅影响中药和中药制剂的质量,还直接危及患者的用药安全性和疗效。因此研究强力枇杷露中镉元素的含量,对于强力枇杷露的安全性、疗效有极其重要的意义[33]。
2.6 电感耦合等离子体质谱法
卢森华等[34]采用电感耦合等离子体质谱建立强力枇杷露中20种无机元素的ICP-MS分析方法并对其进行质量评价。20种无机元素线性关系良好(R2>0.998),平均回收率为86.2%~104.9%,相应的RSD为0.55%~9.21%,检出限为0.01~5.94 ng/mL。19批强力枇杷露中Sr、Mn、Ba、Rb、Zn的平均含量最高,因子分析提取到6个主成分,且有16对元素呈显著正相关。
3 微生物限度检查
微生物检查作为药品安全性的重要指标,是中药制剂质量标准检查项目内容之一,是保障药品使用安全的重要工作。其标准的制定也随着科技的发展,生产工艺水平的提高,国际贸易的日益增多及与国际标准接轨的需求而逐步修订提高[35]。欧阳琴华等[36]采用培养基稀释法检验强力枇杷露,人工加入5种菌液,稀释剂对照组的回收率均高于70%,试验组回收率均高于70%,细菌数测定采用培养基稀释法检验。霉菌数测定及控制菌均可采用常规法检验。汪正宇[37]建立强力枇杷露微生物限度检查的方法验证,按2015年版《中国药典》,用大肠埃希菌枯草芽孢杆菌、金黄色葡萄球菌、黑曲霉菌和白色念珠菌对强力枇杷露微生物限度检查法进行方法学试验验证。强力枇杷露对大肠埃希菌无抑菌作用或抑菌作用较弱。汪学军等[38]采用平板涂布法从出现涨瓶现象的强力枇杷露样品中分离纯化有害菌,通过形态学、生理生化和分子生物学方法对其种属鉴定,且对该菌株的防治方法进行了初步研究。结果表明,从出现涨瓶现象的样品中筛选到一株有害菌,种属鉴定结果表明,菌株与拜耳接合酵母特征最为接近,初步将其鉴定为拜耳接合酵母。防治方法研究结果表明,在110 ℃加热处理20 min时,可达到彻底杀灭要求。
4 结语与展望
中药制剂的有效性与安全性是中医药现代化的基础。找到影响强力枇杷露标准的关键点和不足点,制定科学、合理的强力枇杷露质量标准,对中医药传承与发展有重要意义。强力枇杷露作为2020年版《中国药典》新增品种,对其处方、制法、性状、鉴别、检查、含量测定、功能与主治、用法与用量等均进行了规定。但量效关系、量毒关系、谱效关系、谱毒关系尚需进一步研究,制剂工艺对化学成分的含量、释放、吸收和药理作用之间的关系亦需深入研究。由于强力枇杷露的其中一种成分罂粟壳,含有吗啡、可待因、蒂巴因、那可汀、罂粟碱、罂粟壳碱等生物碱[32]。由于吗啡、可待因具有强烈的镇咳作用,能抑制咳嗽中枢,阻断咳嗽反射,降低咳嗽中枢的兴奋性,抑制了咳嗽反射,产生镇咳作用。其含量过低无法达到镇咳效果,而含量过高则较易引发成瘾性,故应有效控制其含量,使其在发挥药效的同时减少毒副作用[32]。鉴于市售的强力枇杷露产品质量参差不齐,建议在强力枇杷露质量检验过程中引入一测多评、多维检测、中药质量标志物等现代新技术、新方法,实现指标成分的精准定性分析与定量测定,建立强力枇杷露整体质量控制标准的精准评价[39]。继续加强强力枇杷露的药理学和质量控制研究,将能够进一步阐明其安全性和有效性,为临床使用提供科学依据,亦能为产品的二次开发奠定基础[39]。
参考文献
[1] 中华人民共和国卫生部药典委员会.中华人民共和国卫生部药品标准 中药成方制剂:第2册[M].中华人民共和国卫生部药典委员会,1990:272.
[2] 国家药典委员会.中华人民共和国药典:2020年版 一部[S].北京:中国医药科技出版社,2020.
[3] 盛平钦.强力枇杷露鉴别方法的改进实验[J].江西中医学院学报,1995(S1):10-11.
[4] 王方升.强力枇杷露鉴别项操作要点提示[J].基层中药杂志,1999,13(2):40.
[5] 李文龙,吴思俊,秦文杰,等.复方苦参注射液质量控制方法研究进展[J].中国民族民间医药,2019,28(11):48-51.
[6] 张国跃,乔蓉霞.强力枇杷露质量标准研究[J].医药导报,2009,28(12):1627-1628.
[7] 吴洋,尹晓东,巩伟,等.强力枇杷露质量标准的提高和优化[J].中国药师,2018,21(6):1119-1123.
[8] 张生华.强力枇杷露内控标准的探讨[J].中成药,1991,13(8):44.
[9] 王世清,彭英.强力枇杷露的TLC鉴别[J].中国药业,1999,8(11):34.
[10] 李敏,张宝华,孟灵华.强力枇杷露鉴别方法的改进[J].黑龙江医药,2002,15(2):117,119.
[11] 朱长福,同利琪,由会玲,等.强力枇杷露的质量标准研究[J].中草药,2003,34(11):1003-1005.
[12] 梁宪扬,尹萌.强力枇杷露中罂粟壳的薄层色谱鉴别法[J].江苏药学与临床研究,2001,9(1):28-29.
[13] 胡柏平,毛慧芳,洪卸英.强力枇杷露质量鉴别改进[J].中国现代应用药学,2003,20(S1):70-71.
[14] 郝云芳,倪艳,李先荣.中药配方颗粒的质量控制方法研究进展[J].药物评价研究,2013,36(4):307-310.
[15] 尹萌,梁宪扬.酸性染料比色法测定强力枇杷露中盐酸罂粟碱的含量[ J].华西药学杂志,2001,16(6):460-461.
[16] 关晓娟,吴查青.顶空气相色谱法测定强力枇杷露中薄荷脑的含量[J].中国药房,2016,27(12):1708-1710.
[17] 柴鑫莉,祝春仙,姜玲丽,等.顶空气相色谱法测定市售56批次强力枇杷露中薄荷脑的含量[J].中国药房,2015,26(30):4288-4290.
[18] 汪剑飞.GC色谱法测定强力枇杷露中薄荷脑的含量[J].北方药学,2012,9(12):1-2.
[19] 陈晓颙,杨 萍,辜 明,等.强力枇杷露质量状况分析[J].世界最新医学信息文摘,2016,16(55):190-191.
[20] 符映均,张莉,胡浩彬,等.气相色谱法测定强力枇杷露中薄荷脑、磷酸可待因、吗啡、盐酸罂粟碱的含量[J].药学与临床研究,2014,22(5):416-418.
[21] 王述蓉,叶利明,陈聪,等.HPLC测定强力枇杷露中吗啡的含量[J].华西药学杂志,2005,20(6):557-558.
[22] 周建衡,曾建伟.HPLC法测定强力枇杷露(煎膏剂)中吗啡的含量[J].中医药导报,2008,14(9):71-72.
[23] 李彬.高效液相色谱法测定强力枇杷露中吗啡的含量[J].现代中药研究与实践,2009,23(2):41-43.
[24] 秦文杰,马开,高寒,等.HPLC测定强力枇杷露中罂粟碱的含量[J].中国中药杂志,2006,31(16):1330-1332.
[25] 章红,周国平,熊蔚,等.HPLC法测定强力枇杷露中可待因的含量[J].中国实验方剂学杂志,2003,9(1):13-14.
[26] 金阳.RP-HPLC法测定强力枇杷露中磷酸可待因的含量[J].现代中药研究与实践,2007,21(4):40-42.
[27] 巩晓宇,陆燕萍,邱凤邹.SPE-HPLC 法测定强力枇杷露中盐酸可待因[J].药物评价研究,2017,40(5):672-674.
[28] 魏春芬.HPLC法同时测定强力枇杷露中吗啡与可待因含量[J].药学研究,2016,35(8):466-468.
[29] 庞晓星,麻风华,王清华,等.UPLC法测定强力枇杷露中吗啡、可待因和罂粟碱的含量[J].中医药信息,2011,28(1):35-38.
[30] 胡衛南.HPLC法测定强力枇杷露中苯甲酸钠的含量[J].中国药房,2016,27(9):1257-1259.
[31] 袁海英,叶利明.强力枇杷露中齐墩果酸和熊果酸含量测定研究[J].中国测试,2018,44(5):63-66.
[32] 卢森华,黎强,梁爽,等.超高效液相色谱-串联质谱法同时测定强力枇杷露中5种罂粟壳生物碱含量[J].中国中医药信息杂志,2019,26(12):62-66.
[33] 郑民,徐素琴,朱霞石,等.原子吸收光谱法测定强力枇杷露中微量镁和镉[J].光谱实验室,2010,27(2):496-500.
[34] 卢森华,高源,丘一仙,等.强力枇杷露中20种无机元素的 ICP-MS 分析与评价[J].现代中药研究与实践,2020,34(4):53-58.
[35] 陶红.中药制剂微生物限度检查方法研究进展[J].中国药房,2010,21(19):1813-1815.
[36] 欧阳琴华,肖文莉.强力枇杷露微生物限度检查方法验证结果[J].现代食品与药品杂志,2007,17(6):48-50.
[37] 汪正宇.强力枇杷露微生物限度检查方法的验证试验[J].中国民族民间医药,2015,24(16):11-12.
[38] 汪学军,闵长莉,韩彭垒,等.涨瓶强力枇杷露中有害微生物的筛选鉴定及其防治初步研究[J].天然产物研究与开发,2017,29(4):635-640.
[39] 王雪芙.腰痛宁胶囊的药理作用和质量控制研究进展[J].中草药,2019,50(9):2224-2228.

