基于传质数学模型研究丹参-枳实复方中成分存在状态与纳滤分离机制
李存玉,蒋佳丽,邹雨岑,许启龙,支兴蕾,彭国平*
1.南京中医药大学药学院,江苏 南京 210023
2.江苏康缘药业股份有限公司,江苏 连云港 222001
3.中药制药过程新技术国家重点实验室,江苏 连云港 222001
中药制药过程中成分存在状态与其传递规律息息相关,包括提取、分离、制剂成型等关键环节。中药复方是分子、离子、缔合物、复合物等多状态共存的溶液体系,不同存在状态间的作用力差异,导致在制药关键环节,如醇沉、树脂吸附、澄清化过滤等,难以取得一致的成分传递规律,影响制剂中间体及产品质量均一性[1-2]。
目前,中药成分存在状态解析多通过红外光谱、核磁共振技术综合分析[3-4],但是成分脱离原溶液环境,引起存在状态比例或官能团结合位点变化,难以进行准确评价,且仅能对存在状态进行定性分析,无法解读复杂溶液体系中成分存在状态比例。纳滤作为常温化分离的技术手段,截留相对分子质量为100~1000,适用于荷电中药成分精制[5-6]。前期研究发现[7-8],溶质存在状态决定纳滤分离行为,且分离过程中传质系数与溶质浓度呈幂值相关,沟通“存在状态-传质系数-溶质浓度”的内在联系,提出传质系数是溶质多种存在状态分离综合的假说,以期为中药复杂溶液体系中成分状态拟合分析提供理论基础。
本实验以酸碱共存溶液体系丹参-枳实复方为研究对象,选择丹参酚酸及枳实生物碱为指标,计算膜通量、成分截留率,拟合传质数学模型,以单体成分为参照,计算丹参-枳实复方药液中原儿茶醛、迷迭香酸、丹酚酸B、辛弗林的存在状态比例,阐明多状态共存的复方溶液纳滤分离机制,为中药复方成分分离精制提供技术支撑。
1 仪器与材料
Fog-machine 中压纳滤泵、TNZ-1 型纳滤分离组件,南京拓鉒医药科技有限公司;Waters e2695高效液相色谱仪、PDA 检测器,美国Waters 公司;PB-10 型pH 计,德国Sartorius 公司;MS105DU 型十万分之一电子天平,瑞士Mettler Toledo 集团;KH-250B 型超声波清洗器,昆山禾创超声仪器有限公司;CS-60 型电热型蒸煮炉,山东启信厨业有限公司。
1812 型卷式膜,纳滤膜截留相对分子质量800、微滤膜孔径0.45 μm,有效过滤面积0.30 m2,星达(泰州)膜科技有限公司;丹参、枳实饮片购于安徽普仁中药饮片有限公司,经南京中医药大学中药鉴定教研室严辉副教授鉴定,分别为唇形科植物丹参Salvia miltiorrhizaBge.的干燥根及根茎、芸香科植物酸橙Citrus aurantiumL.的干燥幼果,符合《中国药典》2020年版相关项下要求;对照品丹酚酸B(批号111562-201716,质量分数94.1%)、原儿茶醛(批号110810-201608,质量分数99.3%)、迷迭香酸(批号111871-201706,质量分数90.5%)、辛弗林(批号110727-201809,质量分数99.5%),中国食品药品检定研究院;提取物丹酚酸B(批号jbz0501,质量分数98.0%)、原儿茶醛(批号jbz1001,质量分数98.0%)、迷迭香酸(批号jbz0810,质量分数98.0%)、辛弗林(批号jbz0101,质量分数99.0%),南京金益柏生物科技有限公司;乙腈、甲醇、甲酸为色谱纯,水为纯化水。
2 方法与结果
2.1 溶液制备
2.1.1 丹参-枳壳复方溶液 称取丹参饮片3.0 kg、枳壳饮片2.0 kg 置于电热型蒸煮炉中常压煎煮,加入10 倍纯化水常压煎煮2 次,每次为1.0 h,滤液采用0.45 μm 卷式微滤膜滤过,制得复方溶液。
2.1.2 单体成分溶液 根据复方溶液中原儿茶醛、迷迭香酸、丹酚酸B、辛弗林质量浓度,分别称取原儿茶醛、迷迭香酸、丹酚酸B、辛弗林提取物,采用纯化水分别配制质量浓度为85.20 μg/mL 的原儿茶醛单体溶液、42.50 μg/mL 迷迭香酸单体溶液、6.43 mg/mL 丹酚酸B 单体溶液、103.5 μg/mL 辛弗林单体溶液,根据复方溶液pH 值,分别调节单体成分溶液pH 值为5.40,超声10 min,即得4 种单体成分溶液。
2.1.3 混合对照品溶液 分别精密称取干燥至恒定质量的丹酚酸B、迷迭香酸、原儿茶醛对照品6.50、1.82、2.55 mg,置于25 mL 棕色量瓶中,加入甲醇稀释至刻度,得含3 种成分质量浓度分别为260.0、84.0、102.0 μg/mL 的混合对照品溶液。
2.1.4 辛弗林对照品溶液 精密称取干燥至恒定质量的辛弗林对照品10.2 mg,置于10 mL 量瓶中,50%甲醇水溶液稀释至刻度,得质量浓度为1.02 mg/mL 辛弗林对照品溶液。
2.2 纳滤分离
根据图1 所示,组装纳滤分离设备,采用管路依次连接储液罐、中压泵、压力表、纳滤膜、截留阀,以及进液、截留液、纳滤液。供试品溶液置于储液罐中,分离过程中通过中压泵转速以及截留阀调节分离压力,进行纳滤分离,待储液罐中溶质质量浓度趋于平稳后,取样平衡液,检测纳滤膜通量(Jv,m/s),进而收集纳滤液,高效液相检测平衡液、纳滤液中溶质质量浓度,计算截留率(R)。
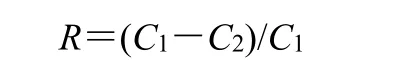
C1、C2分别为溶质在平衡液、纳滤液中的质量浓度
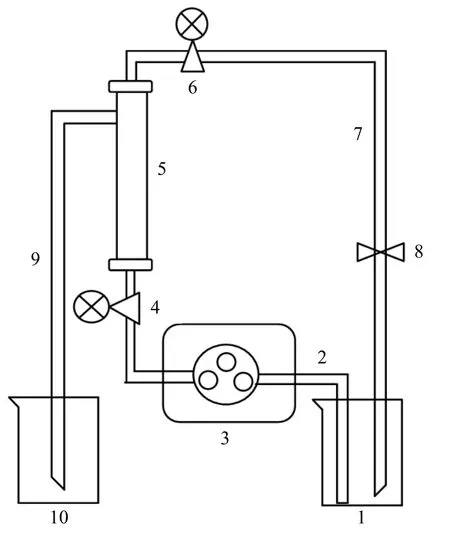
图1 纳滤分离设备Fig.1 Nanofiltration separation equipment
2.3 纳滤传质数学模型
前期研究发现[9-10],中药成分的纳滤传质系数(k)与成分质量浓度呈幂值相关,调节溶液环境以保障单体成分溶液中分子态与离子态比例与复杂溶液的一致性。基于“传质系数可以表征成分通过纳滤膜孔的难易程度,且是多种存在状态的综合分离的表现”理论,拟合单体目标成分传质系数,计算复杂溶液中目标成分在达到相同传质系数时对应的成分浓度,二者的浓差值,即为除了分子态、离子态的其他存在状态。
取单体成分供试品溶液,采用纯化水稀释,分别稀释1.25、2.5、5.0 倍,调节溶液pH 值为5.40,将供试品溶液置于纳滤储液罐中,调节纳滤分离压力分别为0.2、0.4、0.6、0.8、1.0、1.2 MPa,收集系列质量浓度单体溶液不同操作压力下的Jv、R。
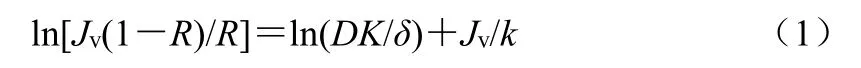
根据式(1)拟合ln[Jv(1-R)/R]与Jv的线性方程,斜率为1/k,截距为ln(DK/δ);δ为膜厚度(cm);DK/δ用于表征膜传质性能(cm/s)。根据线性方程斜率计算k,通过式(2)计算k与溶质初始质量浓度C0的相关性,其中a为相关系数,n为幂值。

根据单体成分传质数学模型中k与C0的相关性,进行丹参-枳实复方溶液纳滤分离,采用纯化水稀释分别稀释1.25、2.5、5.0 倍,调节溶液pH 值为5.40,将复方溶液供试品溶液置于纳滤储液罐中收集系列浓度相应条件下的Jv、R,根据式(1)计算k,根据式(2)拟合k与C0的相关性,方程回归系数大于0.98,说明二者相关性强,传质数学模型成立。基于成分存在状态决定纳滤传质行为的纳滤分离理论,通过复方溶液中溶质k值,计算单体溶液中C0,进而对比相同溶质在复方溶液和单体溶液中质量浓度差异,计算溶质发生复合反应的比例。
2.4 样品检测
2.4.1 辛弗林 参考文献中色谱条件[11],分别精密吸取辛弗林对照品溶液0.1、0.5、1.0、2.0、5.0 mL置于10 mL 量瓶中,50%甲醇水溶液稀释至刻度,高效液相色谱仪检测,以峰面积为纵坐标(Y1),对照品质量浓度为横坐标(X1),绘制标准曲线,进行线性回归,得回归方程为Y1=1 340.2X1+26 711,R2=0.999 3,结果表明辛弗林在10.2~510.0 μg/mL线性关系良好。
2.4.2 丹参酚酸 参考文献中色谱条件[7],分别精密吸取混合对照品溶液0.1、0.2、0.4、0.6、1.0 mL置于1 mL 棕色量瓶中,甲醇稀释至刻度,高效液相色谱仪检测,以峰面积为纵坐标(Y),对照品质量浓度为横坐标(X),绘制标准曲线,进行线性回归,得回归方程:原儿茶醛Y=1 068.8X+641.53,R2=0.999 1;迷迭香酸Y=6 248.2X-8 873.7,R2=0.999 4;丹酚酸BY=3 363.1X-9 776.9,R2= 0.999 3;结果表明原儿茶醛在10.2~102.0 μg/mL、迷迭香酸在7.28~72.8 μg/mL、丹酚酸B 在26.0~260.0 μg/mL 线性关系良好。
精密度RSD 为原儿茶醛0.76%、迷迭香酸0.85%、丹酚酸B 1.13%;重复性RSD 为原儿茶醛1.12%、迷迭香酸1.40%、丹酚酸B 1.78%;加样回收率分别为原儿茶醛100.75%、迷迭香酸97.40%、丹酚酸B 102.20%,RSD 分别为1.82%、2.11%、2.32%;该方法精密度、重复性和加样回收率均符合要求,供试品溶液在24 h 内稳定性良好。
2.5 操作压力与膜通量的相关性
不同成分在系列操作压力下的膜通量如图2 所示,随着纳滤压力增加,驱动力增加,膜通量呈现出升高趋势,其中原儿茶醛、迷迭香酸、丹酚酸B、辛弗林水溶液的相关性散点图分布相对集中,计算压力(P)和膜通量的相关性,结果如表1 所示,二者线性关系良好,4 种成分的线性方程回归系数R2均大于0.96。丹参-枳实复方溶液出现通量增加进而平缓的趋势,压力和膜通量的相关性方程回归系数为0.940 6,提示在复方溶液纳滤分离时,随着压力升高,纳滤膜表面因出现浓差极化,膜通量趋于稳定。
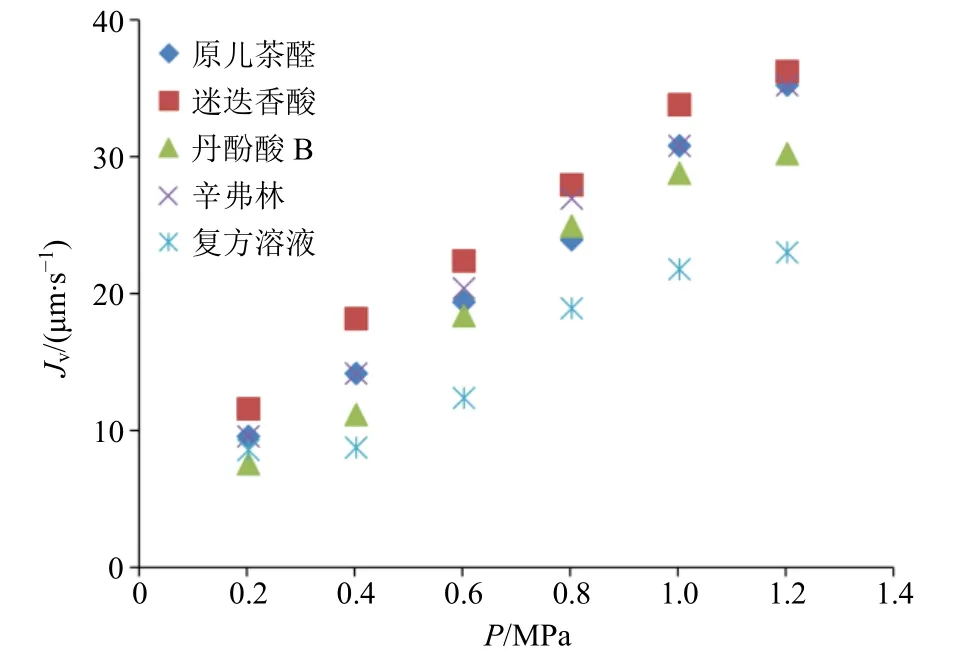
图2 压力对纳滤膜通量的影响Fig.2 Effect of pressure on nanofiltration flux

表1 压力与纳滤膜通量的线性方程Table 1 Linear equation of pressure and nanofiltration flux
2.6 压力对成分截留率的影响
2.6.1 单体成分 分析图3-a 中操作压力对成分分离行为的影响,其中随着压力升高,成分均呈现出截留率轻微下降的趋势,且压力越高,此趋势越明 显,说明高压力环境下的纳滤分离过程,出现浓差极化[12],致使膜表面成分浓度高于溶液环境,在道南效应和溶解-扩散效应的协同下[13-14],成分透过纳滤膜。此外,原儿茶醛、迷迭香酸、丹酚酸B 分离符合孔径筛分模型,而辛弗林在pH 值为5.4 时,多以离子态形式存在,虽相对分子质量与原儿茶醛相近,在道南效应作用下,截留率稍高于原儿茶醛。
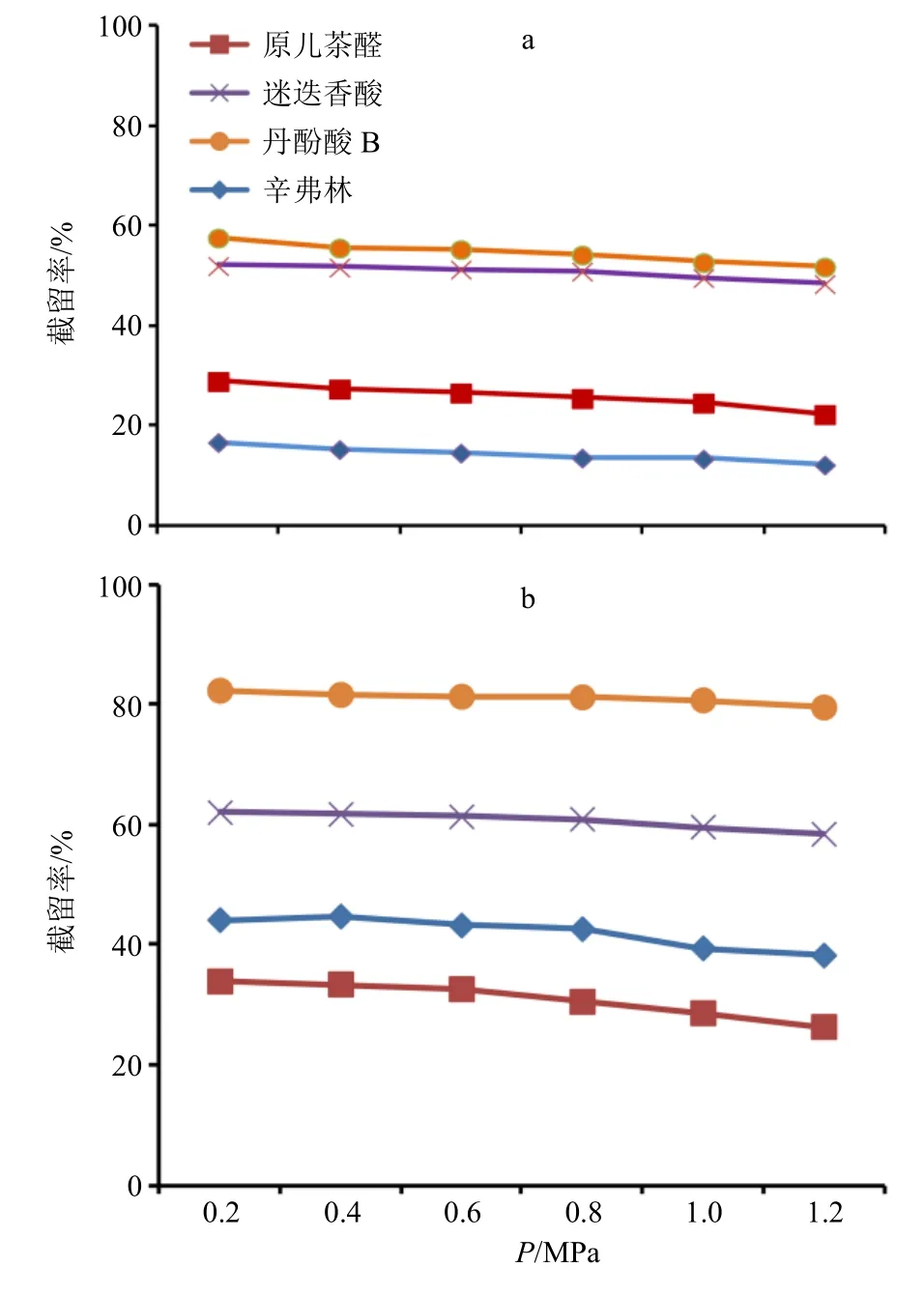
图3 压力对成分截留率的影响Fig.3 Effect of pressure on component rejection
2.6.2 丹参-枳实复方溶液 对比图3-a 和图3-b,相较于单体溶液,复方溶液中4 种指标性成分截留率均明显升高,结合成分的物化性质,推测丹参、枳实提取时,发生酸碱复合反应[15],成分空间尺寸增加,基于纳滤孔道位阻效应,复合态形式存在的成分难以通过纳滤膜,出现截留率升高的现象。根据截留率变化可以初步判断成分存在状态变化规律,但是对于阐明存在状态比例存在局限性。
2.7 成分存在状态拟合
2.7.1 原儿茶醛 对不同质量浓度、溶液条件下的原儿茶醛的ln[Jv(1-Ro)/Ro]和Jv进行相关性拟合,结果见图4,根据相关性散点分布图,可以看出, ln[Jv(1-Ro)/Ro]和Jv呈现线性相关性,对比原儿茶醛单体溶液和复方溶液,散点分布存在差异,说明不同溶液环境影响原儿茶醛的纳滤传质行为。进而对传质系数k与原儿茶醛质量浓度C进行幂相关拟合,结果见图5,二者呈现较高的幂值相关,回归系数均大于0.99,纳滤传质数学模型成立。
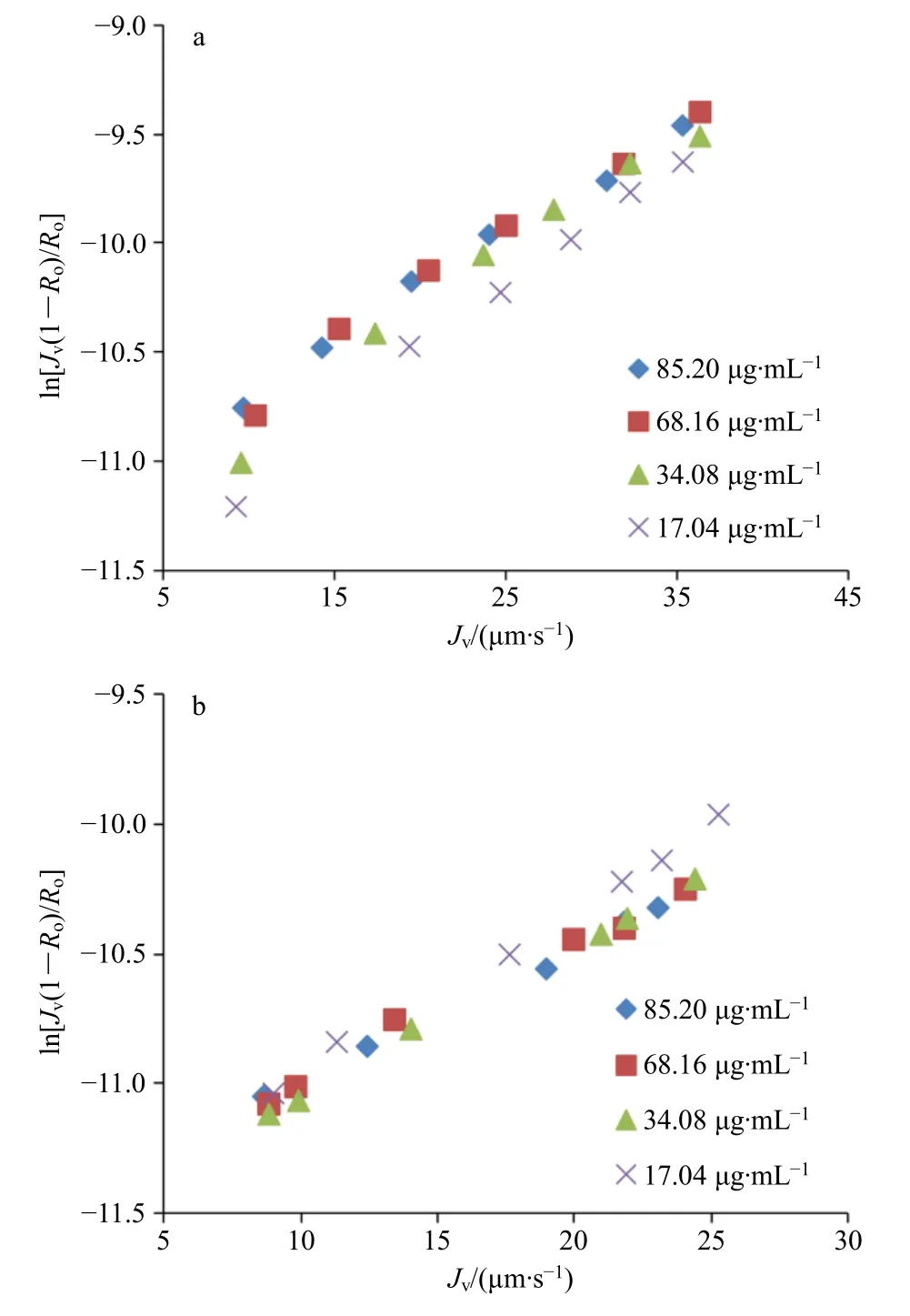
图4 原儿茶醛ln[Jv(1-Ro)/Ro]对JV 的相关性Fig.4 Correlation between ln[Jv(1-Ro)/Ro] and Jv of protocatechuic aldehyde
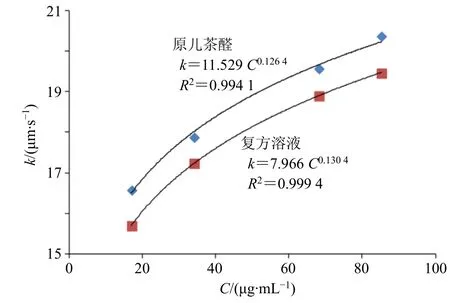
图5 原儿茶醛纳滤传质系数与质量浓度的相关性曲线Fig.5 Correlation curve between k and C of protocatechuic aldehyde
纳滤分离时溶质存在状态决定了纳滤传质行为,pH 值为5.4 时,原儿茶醛主要以分子态形式存在,以原儿茶醛单体溶液为参照,根据传质系数与浓度的相关性方程,计算复方提取液中以复合态形式存在的原儿茶醛质量浓度,结果见表2,随着复方提取液的逐步稀释,溶液中以原儿茶醛存在状态相对稳定,大部分以分子态形式存在,丹参、枳实提取液原液中以复合态形式存在的比例为26.17%。
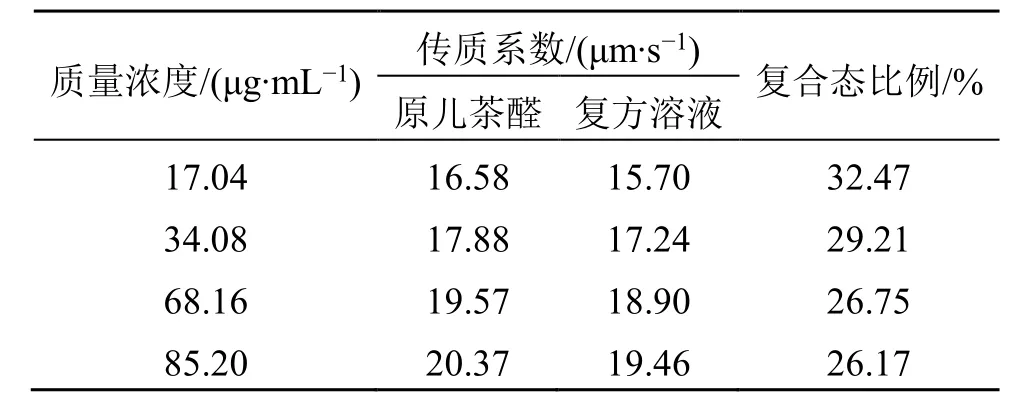
表2 复方溶液中原儿茶醛复合态比例Table 2 Composite state proportion of protocatechuic aldehyde in complex solution
2.7.2 迷迭香酸 拟合迷迭香酸ln[Jv(1-Ro)/Ro]和Jv的相关性,结果见图6,ln[Jv(1-Ro)/Ro]与Jv呈现线性相关性,回归系数均大于0.98。根据线性方程斜率计算传质系数,进而与质量浓度进行幂相关拟合,结果见图7,二者呈现良好的幂值相关,回归系数均大于0.99,纳滤传质数学模型成立。
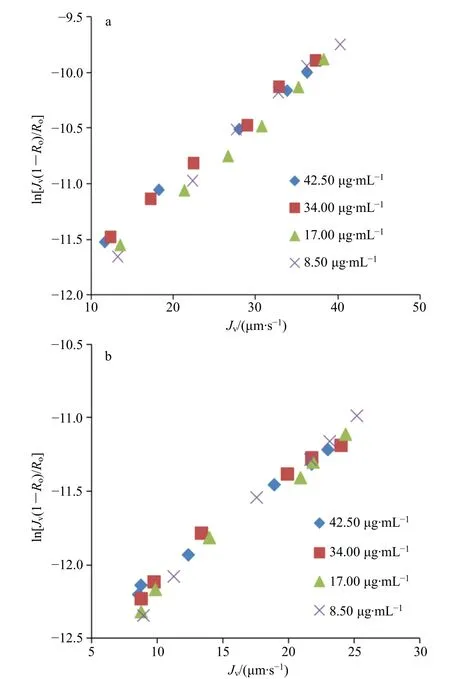
图6 迷迭香酸ln[Jv(1-Ro)/Ro]对Jv 的相关性Fig.6 Correlation between ln[Jv(1-Ro)/Ro] and Jv of rosmarinic acid
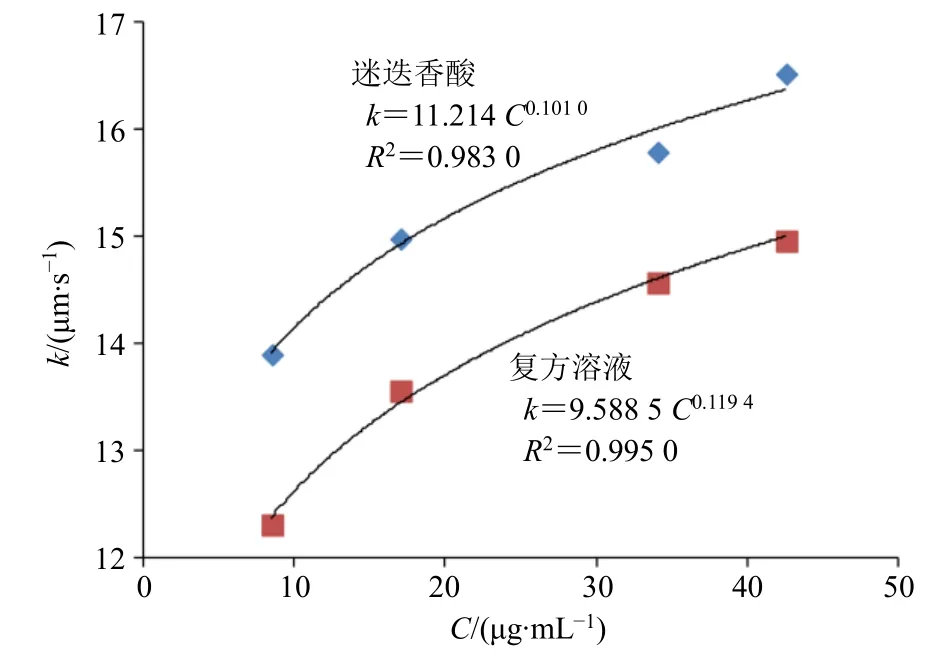
图7 迷迭香酸纳滤传质系数与质量浓度的相关性曲线Fig.7 Correlation curve between k and C0 of rosmarinic acid
迷迭香酸解离常数为4.10,在pH 值为5.4 时,主要以单分子形式的离子态存在,根据迷迭香酸单体成分传质系数与质量浓度的相关性方程,计算复方溶液中相应传质系数下的对应质量浓度,进而计算复方提取液中迷迭香酸复合态存在的比例,结果见表3,其中复方提取液中占比为79.87%。同时,在相同溶质质量浓度环境下,复方提取液中传质系数同比下降,说明迷迭香酸因酸碱复合引起的成分存在状态变化。同时,随着复方提取液的稀释,迷迭香酸存在状态相对稳定。
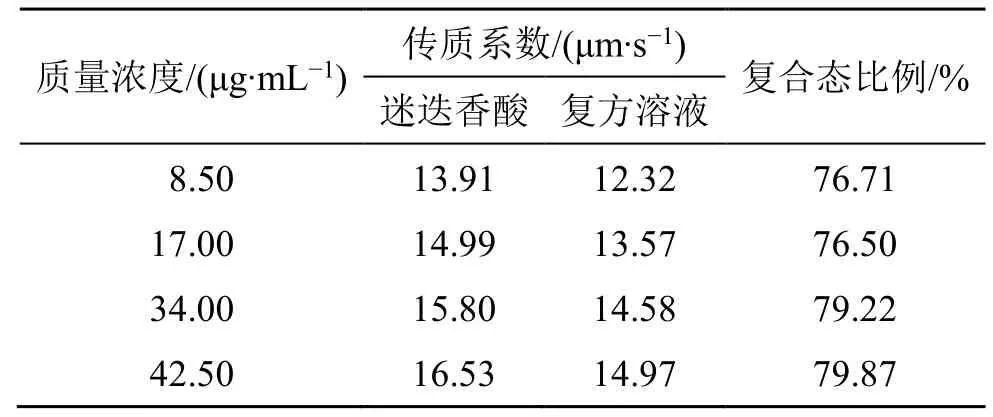
表3 复方溶液中迷迭香酸复合态比例Table 3 Composite state proportion of rosmarinic acid in complex solution
2.7.3 丹酚酸B 拟合丹酚酸B ln[Jv(1-Ro)/Ro]和Jv的相关性,结果见图8,ln[Jv(1-Ro)/Ro]与Jv呈现线性相关性,回归系数均大于0.98。进而拟合传质系数与质量浓度的相关性,结果见图9,二者呈现良好的幂值相关,回归系数均大于0.99,纳滤传质数学模型成立。
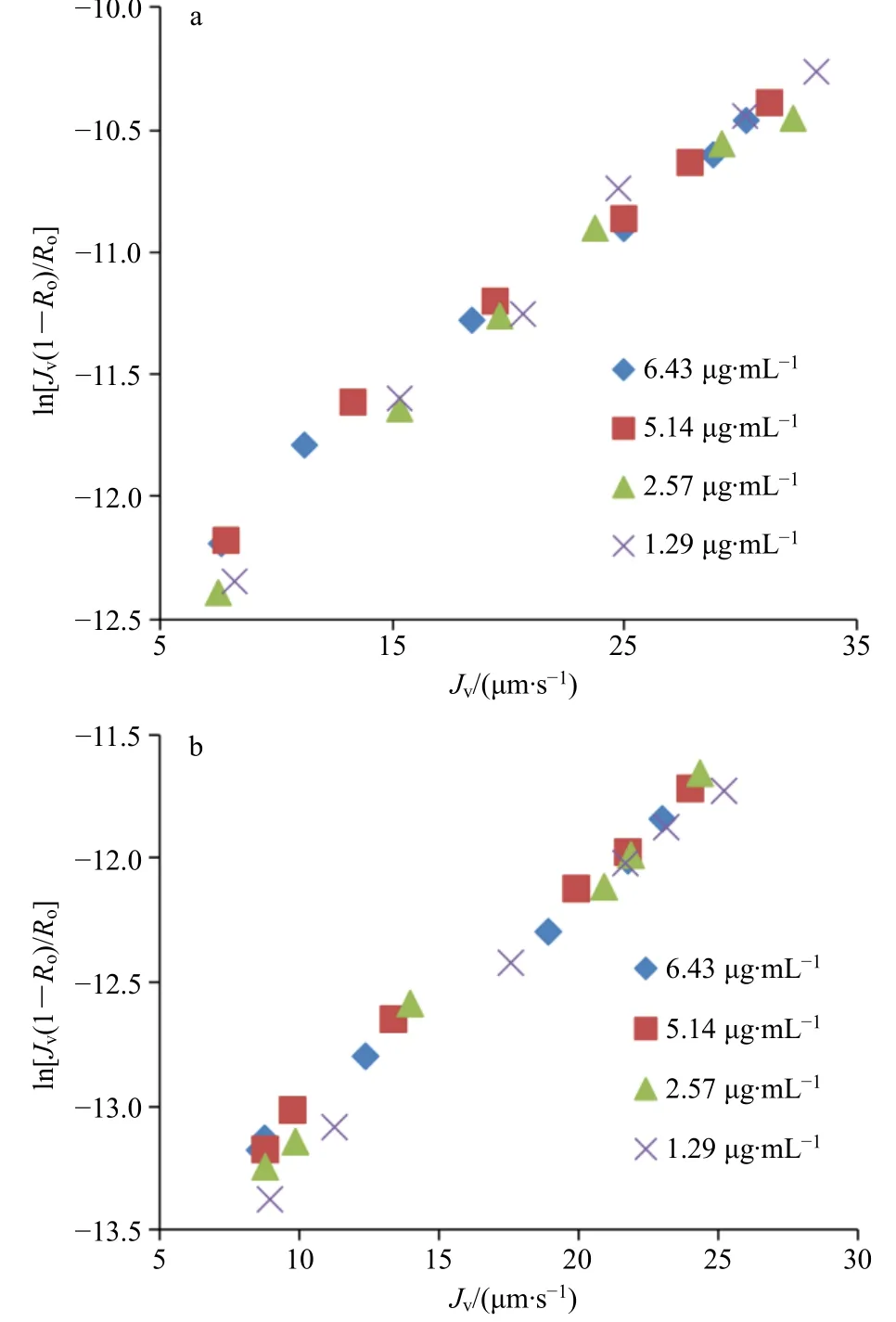
图8 丹酚酸B ln[Jv(1-Ro)/Ro]对Jv 的相关性Fig.8 Correlation between ln[Jv(1-Ro)/Ro] and Jv of salvianolic acid B
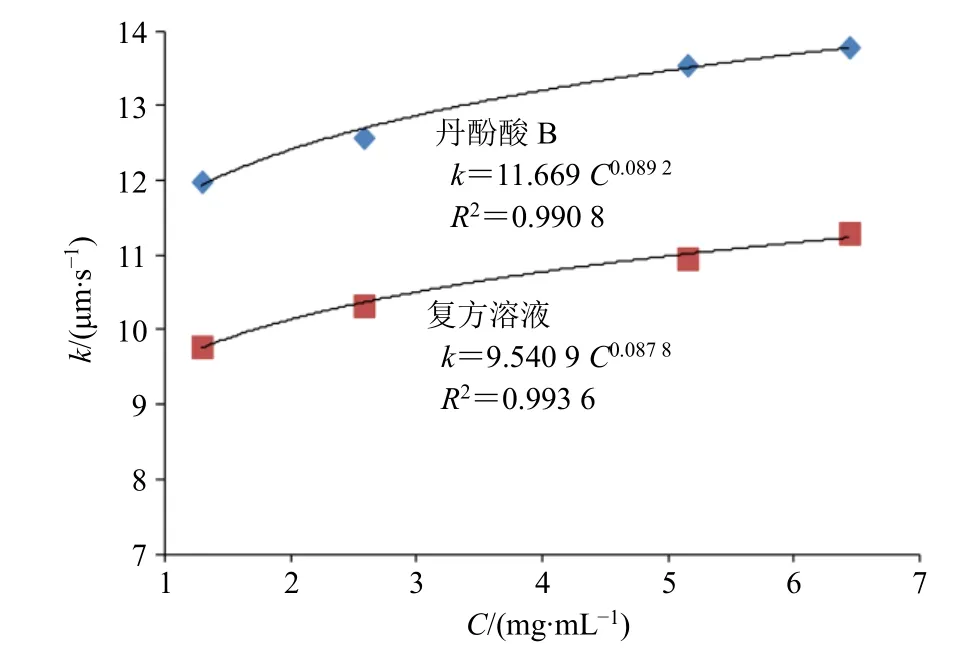
图9 丹酚酸B 纳滤传质系数与质量浓度的相关性曲线Fig.9 Correlation curve between k and C of salvianolic acid B
丹酚酸B 解离常数为2.77,在pH 5.4 时,主要以离子态形式存在,其中复方溶液中丹酚酸B 截留率高于单体溶液,提示复方提取液中存在复合反应引起成分存在状态变化,根据丹酚酸B 单体成分传 质系数与浓度的相关性方程,计算复方溶液中相应传质系数下的发生复合反应的丹酚酸B 质量浓度,结果见表4,复方提取液中占比为89.15%。结合表2、3 中数据,丹参、枳实复方提取过程中,酚酸和 生物碱之间存在复合反应,其中反应发生的程度为丹酚酸B>迷迭香酸>原儿茶醛,其中丹酚酸B 和迷迭香酸主要以复合态形式存在与复方提取液中,而原儿茶醛主要以分子态形式存在。
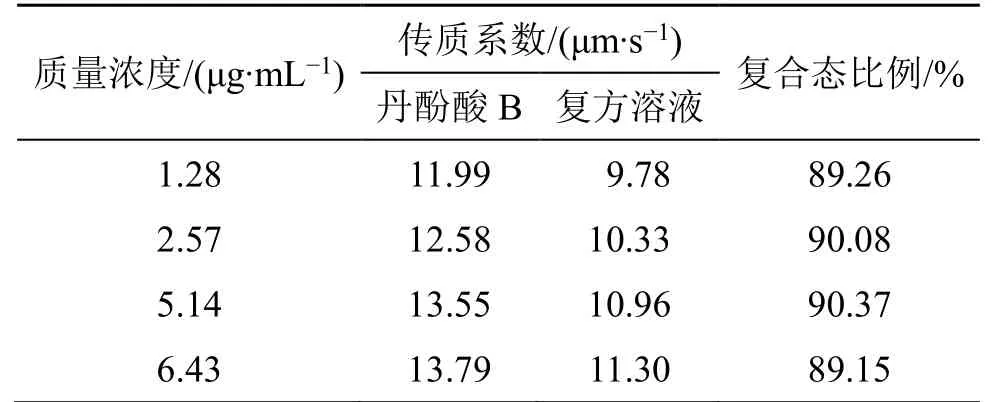
表4 复方溶液中丹酚酸B 复合态比例Table 4 Composite state proportion of salvianolic acid B in complex solution
2.7.4 辛弗林 从图10 可知,ln[Jv(1-Ro)/Ro]与Jv呈现线性正相关,拟合传质系数与辛弗林浓度的相关性,结果见图11,在单体溶液和提取液中均呈幂值相关,且回归系数大于0.98,纳滤传质模型成立。辛弗林解离常数在8.57 左右,在pH 值为5.4 溶液 环境下,主要以离子态形式存在,经过拟合计算辛弗林存在状态(表5),复方提取液中辛弗林以复合态形式存在,其传质系数较单体溶液明显下降。
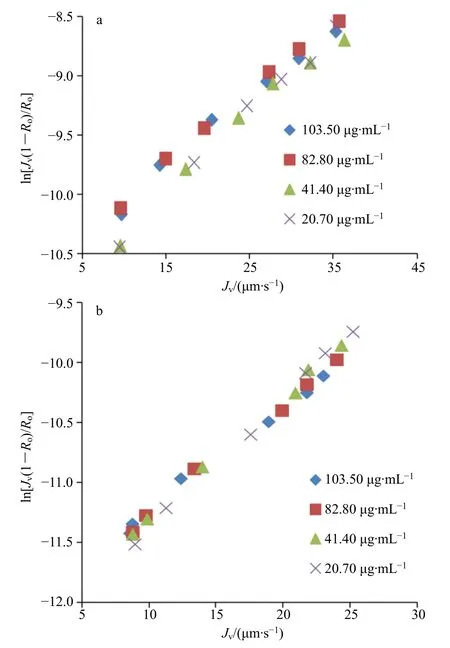
图10 辛弗林ln[Jv(1-Ro)/Ro]对Jv 的相关性Fig.10 Correlation between ln[Jv(1-Ro)/Ro] and Jv of synephrine
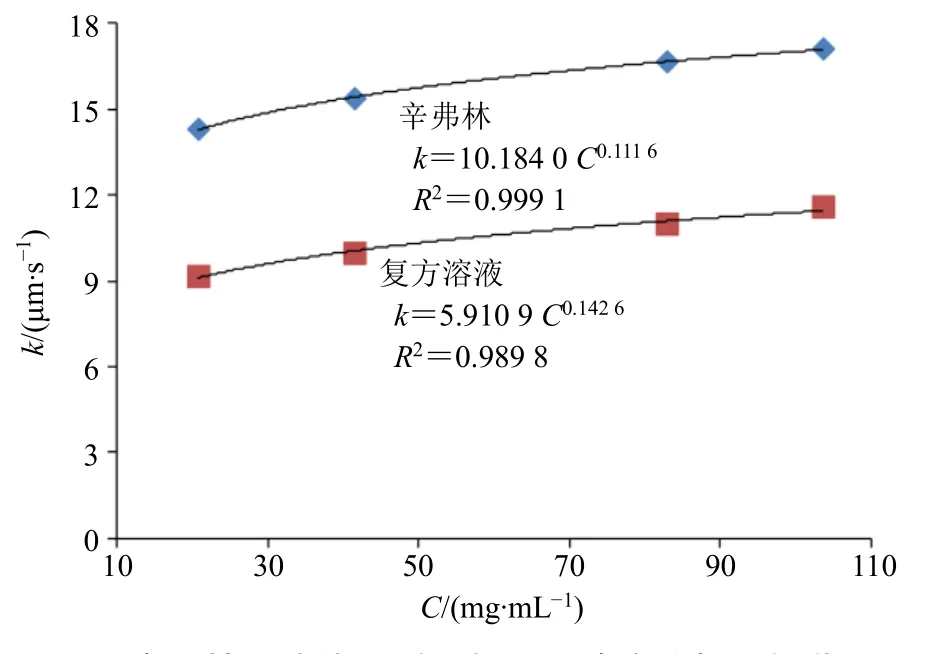
图11 辛弗林纳滤传质系数与质量浓度的相关性曲线Fig.11 Correlation curve between k and C of synephrine
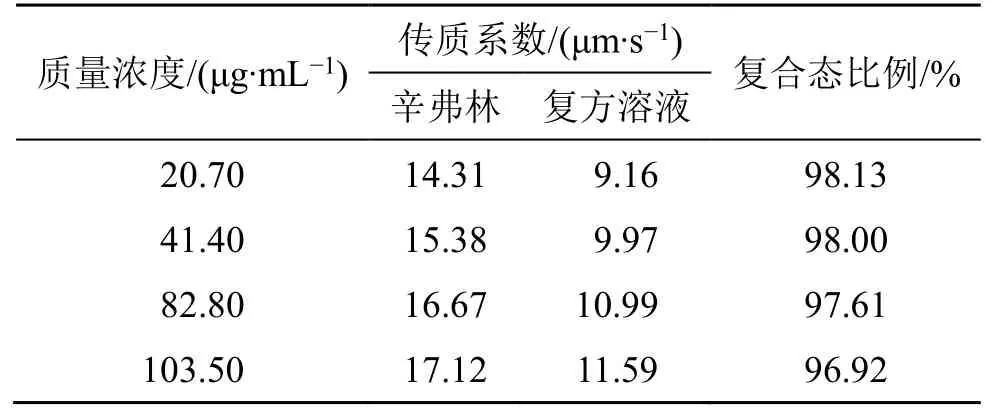
表5 复方溶液中辛弗林复合态比例Table 5 Composite state proportion of synephrine in complex solution
综合对比表2~5,经过丹参、枳实配伍提取,结合成分存在状态与传质系数的相关性,复方提取液中生物碱主要与迷迭香酸、丹酚酸B 发生复合反应。相较于单体成分,复方提取液中原儿茶醛截留率升高5%左右,但仍有26.17%的原儿茶醛与枳实中生物碱发生复合反应,改变其纳滤传质行为。
3 讨论
成分存在状态决定了物化性质,影响中药制药过程中的成分传递规律和制剂质量均一性。中药复杂溶液体系,成分间作用行为复杂,难以借助检测手段予以表征,目前采用核磁共振、红外扫描、X衍射技术需要改变成分所在溶液环境,或采取固体状态进行分析,仅能对可能存在的分子间作用行为进行定性评估,难以定量评价。本实验研究丹参-枳实复方,是基于丹参中水溶性酚酸类成分呈现出分子量、解离常数呈现梯度差异,在考察酸碱复合反应对纳滤分离的影响时,枳实中代表性生物碱辛弗林与丹参酚酸类成分发生酸碱复合反应,引起成分存在状态改变和分离行为变化,但分离机制不清 晰,因此探索复杂溶液体系中成分存在状态定量计算方法。
基于纳滤传质数学模型中成分状态与传质行为的相关性,在相同质量浓度、pH 值质量条件下,选择单体成分为参照,拟合浓度与传质系数的幂值方程,构建复方溶液中成分状态解析模式。丹参-枳实复方溶液中以复合态形式存在的比例为原儿茶醛26.17%,迷迭香酸79.87%,丹酚酸B 89.15%,辛弗林96.92%,成分的纳滤分离效果是多种存在状态协同的体现,其中迷迭香酸、丹酚酸B、辛弗林主要以复合态形式分离,而原儿茶醛主要以分子态形式分离。中药复方配伍衍生出多成分、多状态共存的复杂溶液环境,如枳实理中汤加丹参饮,方中除了丹参、枳实外还包括干姜、炙甘草、砂仁等中药,存在酸碱复合反应、皂苷-挥发油缔合反应等,通过微滤预处理降低不溶性微粒引起的膜组件污染,保障膜通量,理论上适用于复杂溶液中成分存在状态解析。
中药成分结构多样,分子量分布广泛,而所构建的复方溶液中成分状态解析模式是基于水溶液环境,同时纳滤膜截留相对分子质量在100~1000,针对有机溶液环境,以及相对分子质量超出纳滤分离范围的中药成分存在状态解析应用中存在局限性。因此,围绕有机溶液环境下的纳滤分离机制,超滤传质行为与溶质浓度的相关性研究拓展成分状态解析模式应用范围的关键[16-18]。基于传质数学模型研究中药复方中成分存在状态,进而阐明纳滤分离机制,对于指导制药过程中的成分精制分离、提升纳滤技术的适用性提供了技术支撑。
利益冲突所有作者均声明不存在利益冲突

