难溶性中药成分在过饱和体系下晶体成核和生长行为研究
欧阳料淇,蒋且英,陈绪龙,赵国巍,丁海波,刘 欢,廖正根*
1.江西中医药大学,现代中药制剂教育部重点实验室,江西 南昌 330004
2.江西中医药大学实验动物科技中心,江西 南昌 330004
许多中药中的有效成分是难溶性成分,难溶会导致口服生物利用度低,提高难溶性药物的溶解度/溶出性能一直是药剂学研究的热点。在众多的增溶技术中,无定形化是提高溶解度/溶出性能的重要手段[1-3],然而,无定形药物在制备、贮存和溶出的过程中容易发生重结晶而导致溶出性能发生改变[4]。为了提高无定形药物的物理稳定性,通常需要加入辅料以制备成固体分散体。固体分散体的物理稳定性既受分子与载体的相互作用的影响,也与药物本身的晶体成核和生长等结晶趋势有关。研究药物的晶体成核和生长性能从而了解药物的结晶趋势对无定形固体分散体的处方设计具有重要意义[5]。
穿心莲内酯、延胡索乙素、水飞蓟宾、丹皮酚、姜黄素与银杏内酯B 6 种化合物均是具有重要药理活作用的中药活性成分,除姜黄素外均有制剂上市,这些化合物为难溶性化合物,制成口服固体制剂时需要改善溶解度/溶出度,而研究这些药物的晶体成核和生长等结晶行为对其无定形制剂的处方设计有良好的指导作用,但其晶体成核和生长性能尚未见报道,故本实验开展难溶性中药成分在过饱和体系下晶体成核和生长行为的研究。
1 仪器与材料
1.1 仪器
Agilent 1260 型高效液相色谱仪,美国Agilent公司;BAS124S 电子天平,赛多利斯科学仪器北京有限公司;85-2A 双数显恒温磁力搅拌器,金坛市城东新瑞仪器厂;Oxford-diffraction X 射线单晶衍射仪,日本Rigaku 公司;UV-2550 紫外分光光度计,岛津-GL 消耗品销售有限公司;Diamond DSC 型差示扫描量热分析仪,美国Perkin Elmer 公司;明美Mshot MS60 偏振光显微镜,广州市明美光电技术有限公司。
1.2 材料
穿心莲内酯(批号CXLNZ20181230,质量分数>98%)、延胡索乙素(批号YHS20191209,质量分数>98%)、延胡索乙素对照品(批号110726- 200610,质量分数>98%)、水飞蓟宾(批号HXSFJB 20190305,质量分数>98%)、丹皮酚(批号DPF 20200326,质量分数>98%)、丹皮酚对照品(批号HX200908132,质量分数>98%)、姜黄素(批号JHS20180328,质量分数>98%),西安昊轩生物科技有限公司;穿心莲内酯对照品(批号5508-58-7,质量分数>98%)、水飞蓟宾对照品(批号S-0240181008,质量分数>98%)、姜黄素对照品(批号AF7111708,质量分数>98%)、银杏内酯B 对照品(批号AF9061206,质量分数>98%),成都埃法生物科技有限公司;二甲基亚砜(DMSO),批号2007282,西陇科学股份有限公司;水为超纯水,其余试剂均为分析纯。
2 方法与结果
2.1 含量测定
穿心莲内酯[6]、延胡索乙素[7]、水飞蓟宾[8]、丹皮酚[9]、姜黄素[10]、银杏内酯B[11]6 种成分的含量测定分别按照文献方法进行,6 种成分的回归方程分别为Y=42.311X-13.190,R2=0.999 9,线性范围9.99~199.80 μg/mL;Y=4 935.2X-2.084 1,R2=0.999 9,线性范围4.99~99.80 μg/mL;Y=26 815X-30.476,R2=0.999 8,线性范围4.80~240.06 μg/mL;Y=24 553X-4.173 7,R2=0.999 8,线性范围 2.01~101.00 μg/mL;Y=77.739X-24.702,R2=0.999 9,线性范围1.14~45.52 μg/mL;Y=506.72X-3 409.5,R2=0.999 8,线性范围10.01~1 000.00 μg/mL。
2.2 平衡溶解度测定
将过量的原料药加入2% DMSO 中,37 ℃恒温摇床平衡24 h[12],滤过,续滤液用甲醇稀释适宜倍数后,HPLC 法测定平衡溶解度,结果见表1。
表1 药物在2% DMSO 中的平衡溶解度 ( ± s, n = 3)Table 1 Equilibrium solubility of drugs in 2% DMSO ( ± s, n = 3)
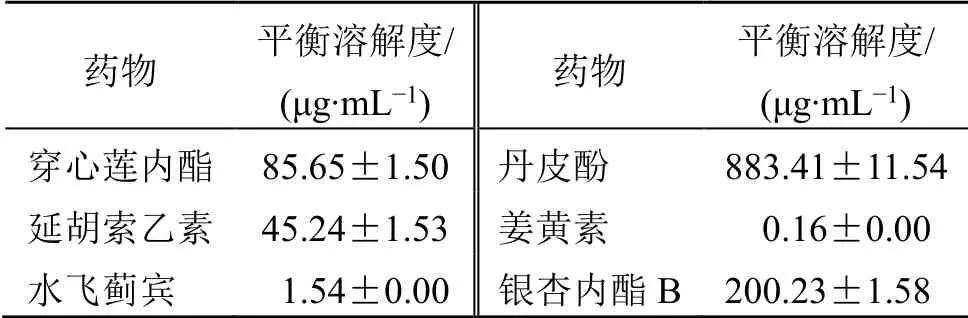
表1 药物在2% DMSO 中的平衡溶解度 ( ± s, n = 3)Table 1 Equilibrium solubility of drugs in 2% DMSO ( ± s, n = 3)
药物 平衡溶解度/ (μg·mL−1) 药物 平衡溶解度/ (μg·mL−1) 穿心莲内酯 85.65±1.50 丹皮酚 883.41±11.54 延胡索乙素 45.24±1.53 姜黄素 0.16±0.00 水飞蓟宾 1.54±0.00 银杏内酯B 200.23±1.58
2.3 过饱和度(S)的确定
根据基于溶液状态下的成核和晶体生长行为建立的结晶分类方法[13],采用S分别为5、20 的过饱和体系,研究6 种成分的结晶行为[14]。S按下式计算[15-16]。
S=C/C*
C*为药物在含2% DMSO 的水中测定的平衡质量浓度,C为根据所需的过饱和水平配制的药物DMSO 溶液加入水中后计算的理论质量浓度
2.4 成核时间的测定
根据“2.3”项下方法,取一定量的穿心莲内酯、延胡索乙素、水飞蓟宾、丹皮酚、姜黄素、银杏内酯B 溶于DMSO 中,再将其转移到水中,分别配制成S为5、20 的溶液,使用紫外/可见分光光度计测量溶液在非吸收波长(λ=500 nm)的光散射随时间的变化,每隔20 s 测量1 次吸光度(A)值,持续1 h。绘制吸光度-时间曲线,A值随时间变化的曲线由2 个不同的线性区域组成(图1),2 个区域绘制的回归线的交点称为成核时间(tind)(另外2个成分丹皮酚和银杏内酯B 一加入到水中立刻产生沉淀,成核诱导时间为0,因此没有相应的图)。
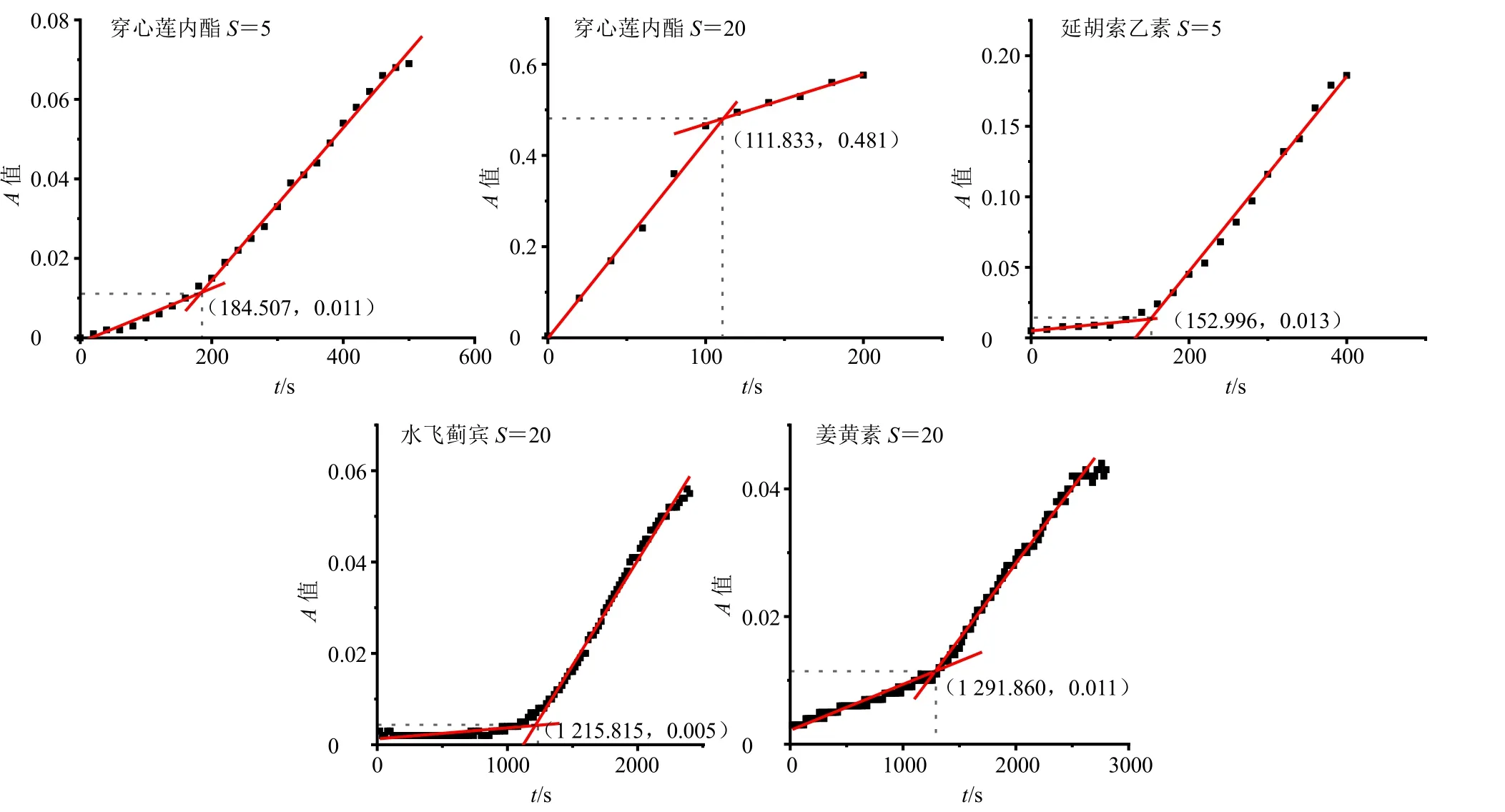
图1 穿心莲内酯、延胡索乙素、水飞蓟宾、姜黄素成核诱导时间的测定Fig.1 Determination of nucleation induction time of andrographolide, tetrahydropalmatine, silybin, and curcumin
使用Origin Pro 对A值-时间曲线分段回归分析确定的tind见表2,结果显示,S=20 时,6 种成分在1 h 内均观察到沉淀产生,且延胡索乙素、丹皮酚和银杏内酯B 的DMSO 溶液一转移到水中立刻成核;而S=5 时,仅穿心莲内酯、延胡索乙素、丹皮酚、银杏内酯B 在1 h 内观察到沉淀产生,且丹皮酚和银杏内酯B 在S=5 时也立刻成核。
表2 在不同过饱和度条件下药物的tind ( ± s, n = 3)Table 2 tind of drugs under different supersaturation conditions ( ± s, n = 3)
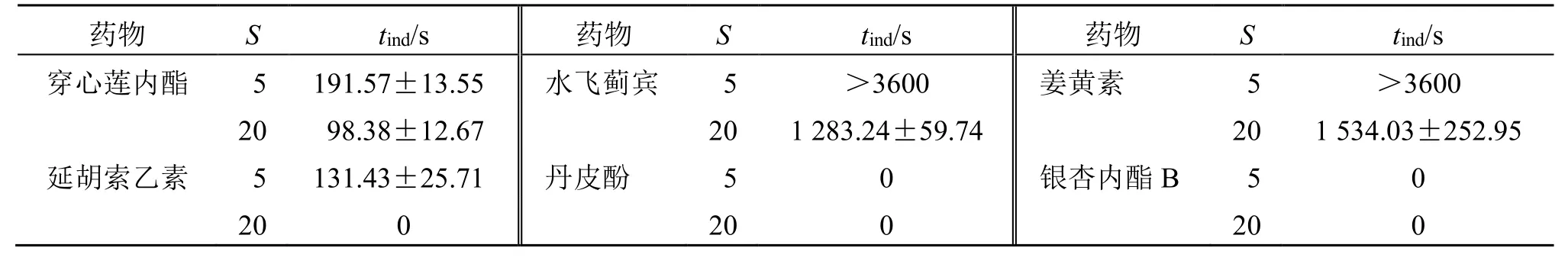
表2 在不同过饱和度条件下药物的tind ( ± s, n = 3)Table 2 tind of drugs under different supersaturation conditions ( ± s, n = 3)
药物 S tind/s 药物 S tind/s 药物 S tind/s 穿心莲内酯 5 191.57±13.55 水飞蓟宾 5 >3600 姜黄素 5 >3600 20 98.38±12.67 20 1 283.24±59.74 20 1 534.03±252.95 延胡索乙素 5 131.43±25.71 丹皮酚 5 0 银杏内酯B 5 0 20 0 20 0 20 0
2.5 晶体生长速率的测定
药物有机溶液和盛有一定量水的锥形瓶预先放在(37.0±0.1)℃、100 r/min 的振荡水浴中预热,按S分别为5、20 分别将“2.4”项中的药物有机溶液加入到锥形瓶中,混合30 s 后,加入5%药物量过60 目筛的原料药作为晶种,分别在0、10、20、30、45、60、90、120 min 取1 mL 样品,0.22 μm微孔滤膜滤过除去结晶沉淀,适当稀释后,立即使用紫外可见分光光度计在λmax处对样品进行分析。以实验开始30 min 的A值-时间曲线的斜率作为晶体生长速率[17],结果见表3、4,结果显示穿心莲内 酯和延胡索乙素在2 种过饱和度下的斜率为负值,表明发生了快速晶体生长,而其余4 种物质斜率为正值,表示晶体生长缓慢。
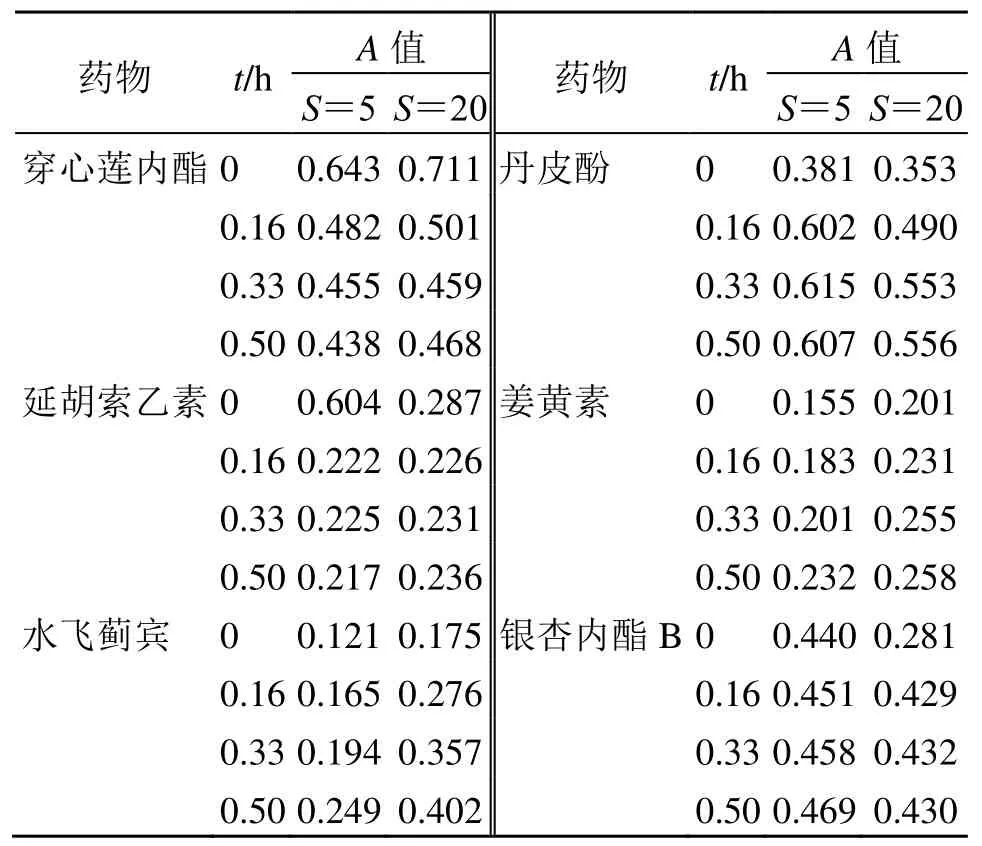
表3 晶体生长速率的测定Table 3 Determination of crystal growth rate
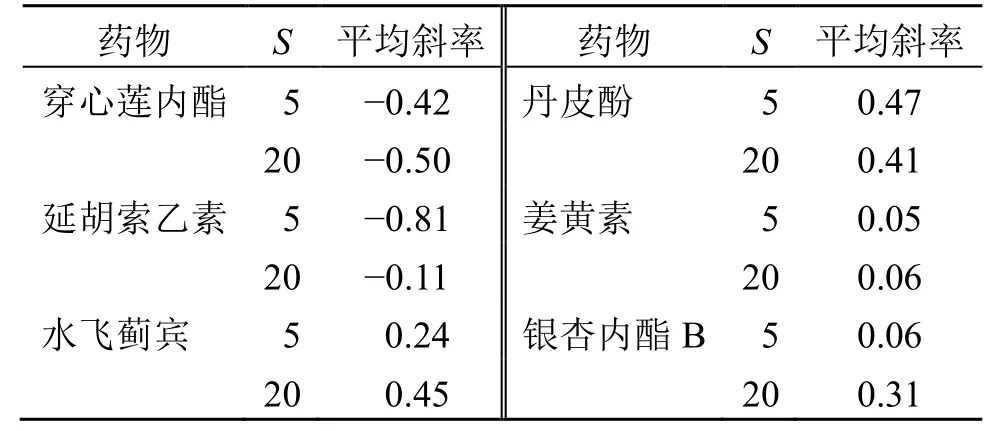
表4 在不同过饱和度下药物的晶体生长速率 (n = 3)Table 4 Crystal growth rate of drugs under different supersaturation (n = 3)
2.6 偏光下沉淀形态观察
取“2.4”项下过饱和度为20、实验1 h 后的混悬液20 μL,滴于载玻片上,盖上盖玻片,置于偏振光显微镜下观察,结果见图2,沉淀在偏光下具有明显双折射现象,表明产生结晶沉淀,这个结果与成核实验结果相一致,且每个药物沉淀所表现出来的形状和大小因药物而异。
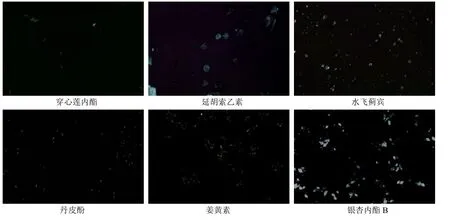
图2 药物在2% DMSO 溶液 (S = 20) 中的结晶偏光图Fig.2 Polarization diagram of drug in 2% DMSO solution (S = 20)
2.7 沉淀表征
2.7.1 沉淀处理方法 将晶体生长研究结束时收集的沉淀物置于离心管中,13 000 r/min 离心10 min,倾去上清液后至真空干燥箱,25 ℃,干燥,得沉淀粉末。
2.7.2 差示扫描量热法(differential scanning calorimeter,DSC) 分别取各原料药与沉淀粉末适量,置入铝皿中后放入DSC 样品炉中,进行DSC测定。升温速率10 ℃/min,记录各个样品差示扫描量热曲线,结果见图3。穿心莲内酯、延胡索乙素、水飞蓟宾、姜黄素沉淀粉末与原料药相比,晶体吸热峰位置未见明显变化。银杏内酯B 原料药在330.08 ℃有尖锐熔融峰存在,而银杏内酯B 沉淀粉末在348.51 ℃处有明显的吸热峰,与银杏内酯B 原料药相比,沉淀粉末吸热峰位置发现明显位移,表明银杏内酯B 沉淀晶体结构已发生了明显变化。丹皮酚原料药在50.74 ℃有尖锐熔融峰存在;丹皮酚沉淀粉末在45.92 ℃处有明显的吸热峰,吸热峰位置发现明显位移,说明丹皮酚沉淀晶体结构发生了改变。DSC 图谱中,各沉淀粉末没有出现脱水峰,说明药物在晶体生长研究中没有形成水合物。
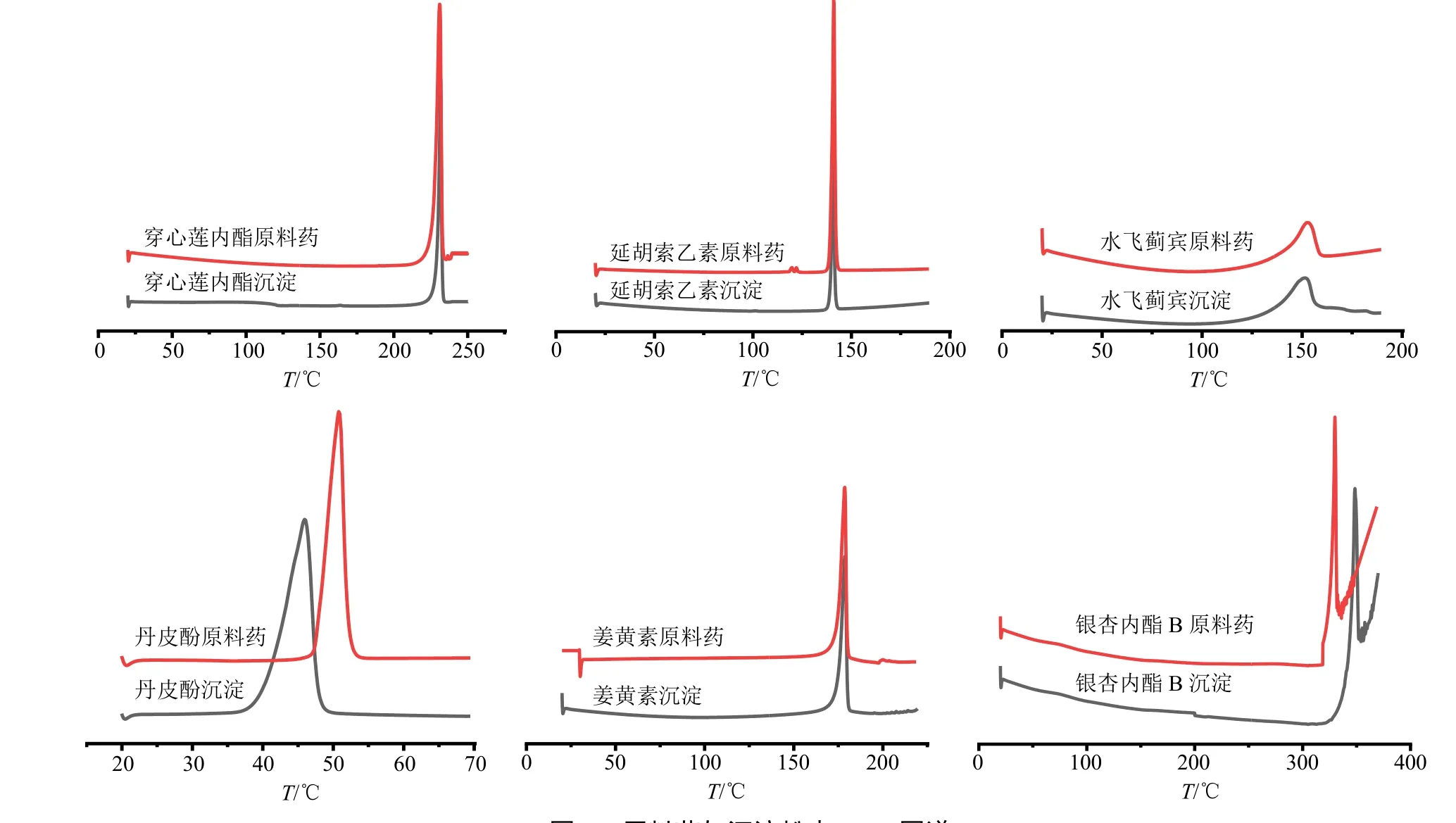
图3 原料药与沉淀粉末DSC 图谱Fig.3 DSC spectrum of API and precipitated powder
2.7.3 X 射线粉末衍射(XRD) 分别取各原料药, 沉淀粉末适量,置于样品槽中,压平,进行X 射线衍射分析。测定条件:Cu-Kα 靶,工作电压为50 kV,电流为1.0 mA,曝光时间80 s 扫描2θ角度0°~60°,记录样品X 射线衍射曲线,结果见图4。穿心莲内酯、延胡索乙素、水飞蓟宾、姜黄素沉淀粉末与原料药相比,衍射峰未见明显变化,表明其晶型未发生改变;而丹皮酚沉淀粉末与原料药相比,26.29°的衍射峰偏移至25.13°且在16.11°出现新的衍射峰,银杏内酯B 沉淀粉末与原料药相比,8.33°的衍射峰偏移至7.61°且在13.30°,15.29°处出现新的衍射峰,说明丹皮酚、银杏内酯B 沉淀晶型发生了改变,与DSC 图谱结果一致。
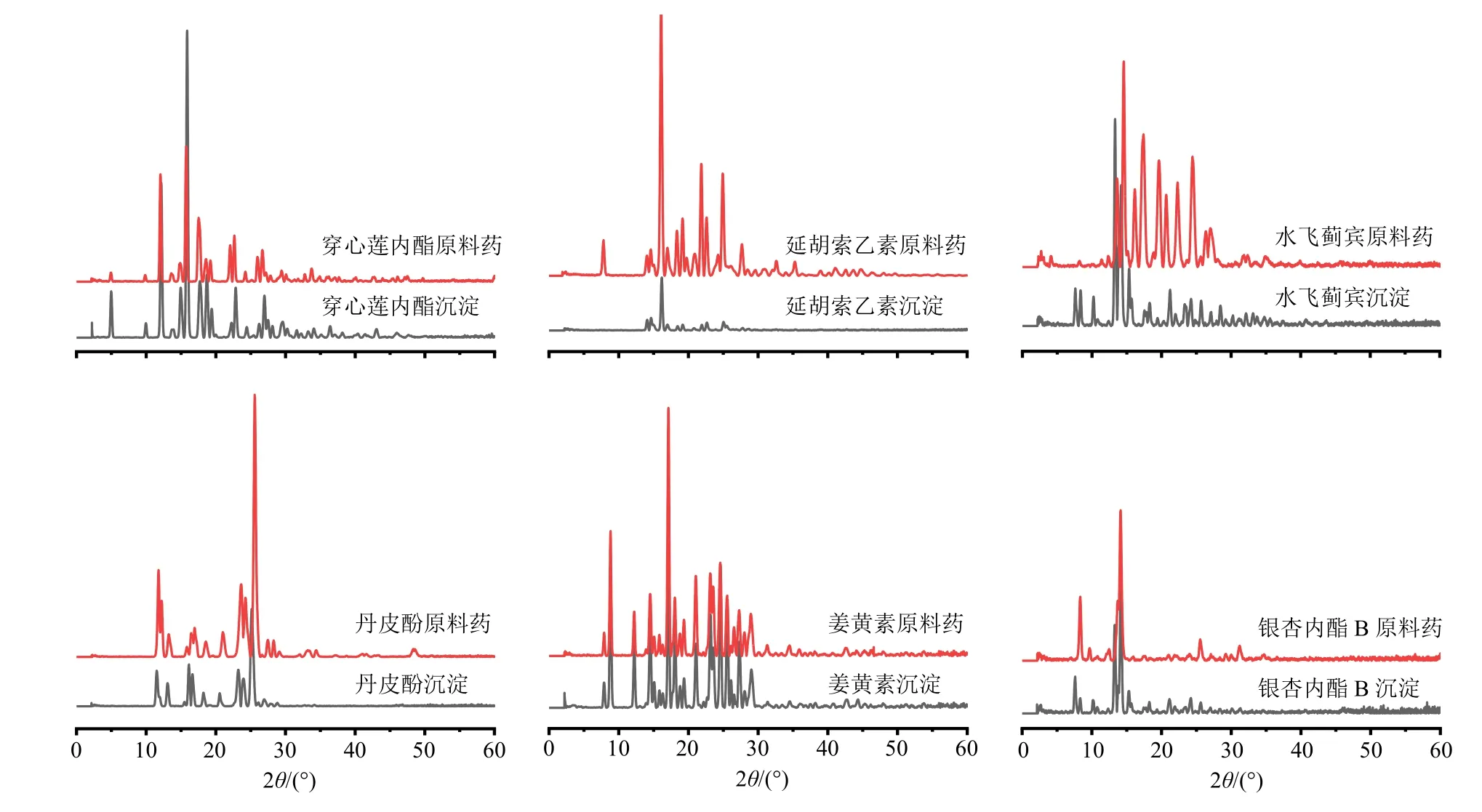
图4 原料药与沉淀粉末XRD 图谱Fig.4 XRD spectrum of API and precipitated powder
3 讨论
由于药物自身的结晶趋势是影响无定形固体分散体制备和储存稳定性的重要因素,并与无定形固体分散体的处方设计密切相关[5],近年来有多篇文献运用模拟药剂学中产生结晶过程的方法研究了药物的结晶行为并建立了药物结晶趋势分类体系,包括模拟构建固体分散体的熔融冷却法[18-19]、溶剂蒸发法[20]以及模拟体内分散行为的反溶剂法[13,21]。考虑到无论哪种过饱和体系最终都可能在体内分散时产生结晶,故本实验采用反溶剂法研究难溶性中药活性成分的结晶行为。
根据Rathi 等[13]的分类标准,成核时间小于1 h的药物为快速成核药物,大于1 h 则为缓慢成核药物;晶体生长过程中表现出负斜率的药物归为快速晶体生长药物,表现出正斜率或者为常数的药物归为缓慢晶体生长药物。所研究的6 种药物中,无论是高过饱和度(S=20)还是低过饱和度(S=5),穿心莲内酯、延胡索乙素的成核时间均少于1 h,晶体生长速率的斜率为负值,故属于快速成核-快速晶体生长类药物(I 类);丹皮酚、银杏内酯B 的成核时间均小于1 h,晶体生长速率的斜率为正值,故属于快速成核-缓慢晶体生长类药物(II 类)。水飞蓟宾、姜黄素在高过饱和度(S=20)时成核时间小于1 h、低过饱和度(S=5)时的成核时间大于1 h,但晶体生长速率的斜率均为正值,故在高过饱和度(S=20)属于快速成核-缓慢晶体生长(II 类)、低过饱和度(S=5)时属于缓慢成核-缓慢晶体生长类药物(IV 类),这可能是由于这类药物具有较大的亚稳态宽度[22]。
对于结晶趋势较大的药物,一般需要大量的辅料且需要辅料与药物达到分子水平的均匀混合才能维持药物的无定形状态;对于结晶趋势较低的药物,即使药物的量超过了固体溶解度极限,药物仍会保持无定形状态,因此,可以减少辅料用量,以提高 载药量[5]。穿心莲内酯、延胡索乙素、丹皮酚、银杏内酯B、高过饱和度下的水飞蓟宾、姜黄素属于I 或II 类等结晶趋势较强的药物,制备成无定形固体分散体时,可能需要加入较多的辅料,并需要辅料与药物达到分子水平的混合;而将结晶趋势较低的低过饱和度的水飞蓟宾、姜黄素制备成无定形固体分散体则可能较易实现。
本实验采用去过饱和法测定晶体生长,即测定除去沉淀后溶液中各物质的最大吸收波长处的吸光度以反映生长。一般如果成核迅速,许多晶体同时形成,导致立即去过饱和而显示快生长[13]。本研究中成核时间测定的结果表明丹皮酚和银杏内酯B 为快速成核化合物,但却显示为慢生长,可能是因为成核过快,大量成核后消耗了大量药物分子使其浓度下降导致生长速度减慢。由于该2 种物质成核速度过快,可能来不及形成稳定晶型的晶核,触发以自身形成的亚稳定晶核为基准的晶体生长,从而发生转晶,为了验证这种推测,故进一步采用DSC 和XRD 对其晶型结构进行表征,结果显示该2 种物质发生了转晶,从而证实了推论,也进一步证实了该2 种物质为快成核化合物。
药物结晶趋势与药物分子结构密切相关,分子量小、苯环数较大及双键较多等刚性结构分子、分支较少和高对称性的分子易结晶[23]。本研究中6 种分子均含有相对较多的苯环数(延胡索乙素、水飞蓟宾、丹皮酚),或含有较多的苯环数和双键(姜黄素),或以环形结构为主(穿心莲内酯、银杏内酯B),均表现为刚性结构,这可能是它们容易结晶的原因。
根据现有文献报道,选用2% DMSO 作为溶剂体系不影响药物的结晶行为[21],在过饱和溶液中加入原料药晶体作为晶种,可以避开成核步骤,从而能够仅测量晶体生长速率[24-25]。由于吸光度和浓度之间有直接的相关性,因此,本研究从众多的测量成核和晶体生长速率的方法中选择紫外-分光光度计[26-29],通过监测透射率吸收-时间曲线,观察透射率的急剧变化,可以快速、方便地确定分子的结晶倾向。本研究基于过饱和体系下药物的结晶过程,对晶体成核和生长行为进行分类,是一种有效的评价方法,可为无定形固体分散体制剂开发提供基础。
利益冲突所有作者均声明不存在利益冲突

