昆明市2019年HIV非职业暴露后的预防效果
田 波,刘 俊,李重熙,何 蓉,古善群,王维波
(昆明市第三人民医院感染一科,云南 昆明 650041)
艾滋病病毒(human immunodeficiency virus,HIV)的暴露后预防(post exposure prophy-laxis,PEP),是指在暴露于HIV后尽快服用抗逆转录病毒药物,以降低HIV感染风险的措施[1]。作为新型生物学预防措施,暴露后预防正在成为预防艾滋病传播的有效手段。面对全球严峻的艾滋病防治形势,云南省在2015年制定了《云南省艾滋病病毒非职业暴露后预防性服药指导意见(试行)》[2],以便更有效地预防艾滋病的传播。非职业暴露是指:性暴露和注射吸毒暴露;职业暴露是指:工作环境中发生的暴露[3]。有证据表明PEP的有效性和安全性,同时对于减少HIV感染效果显著[4],但实际实施过程中,要达到理想效果还与很多因素有关。本文对昆明市HIV非职业暴露后预防的开展情况及效果进行分析,以期对暴露后预防的广泛开展提供指导依据。
1 对象与方法
1.1 研究对象
昆明市第三人民医院暴露后预防门诊2019年1月至12月期间服用暴露后预防药物的就诊者。纳入标准:(1)年龄大于18周岁;(2)发生过未正确使用安全套的性行为(包括同性和异性);(3)暴露于HIV患者的血液(包括共用针具吸毒)、精液、阴道分泌物等带菌体液。排除标准:(1)职业暴露者;(2)筛查HIV阳性者;(3)暴露前预防服药者;(4)咨询但未服用药物者。
1.2 观察指标和方法
从门诊医生工作站系统提取2019年患者信息、门诊病历、处方及检验结果,同时进行电话随访,进而了解昆明市HIV非职业暴露后预防的人群特征、高危行为到就诊的时间间隔、完成28 d疗程的比例、治疗方案的构成以及暴露后预防效果,同时分析完成28 d疗程的影响因素。定义暴露后预防必须连续服药满28 d,而不是服用几天或者间断给药[5-6]。
1.3 统计学处理
用EXCEL收集HIV非职业暴露后预防用药者的数据及电话随访信息,整理后用SPSS 20.0软件统计分析,偏态分布的计量资料用中位数及四分位数间距M(P25,P75)描述,计数资料用n(%)描述,Logistic回归分析完成28 d疗程的影响因素。检验水准α=0.05,P<0.05为差异有统计学意义。
2 结果
2.1 研究对象基本情况
2019年1月1日至12月31日共有HIV非职业暴露后预防者836人,其中男性703(84.09%)人,年龄中位数32(26,36)岁,最小16岁,最大68岁。未婚344(41.15%)人,已婚478(57.18%)人,离异或丧偶14人(1.67%)。明确暴露源是HIV阳性的有52(6.22%)人。治疗方案为恩曲他滨替诺福韦+多替拉韦或拉替拉韦的比例为77.99%。24 h内就诊的比例为65.90%,见表1。
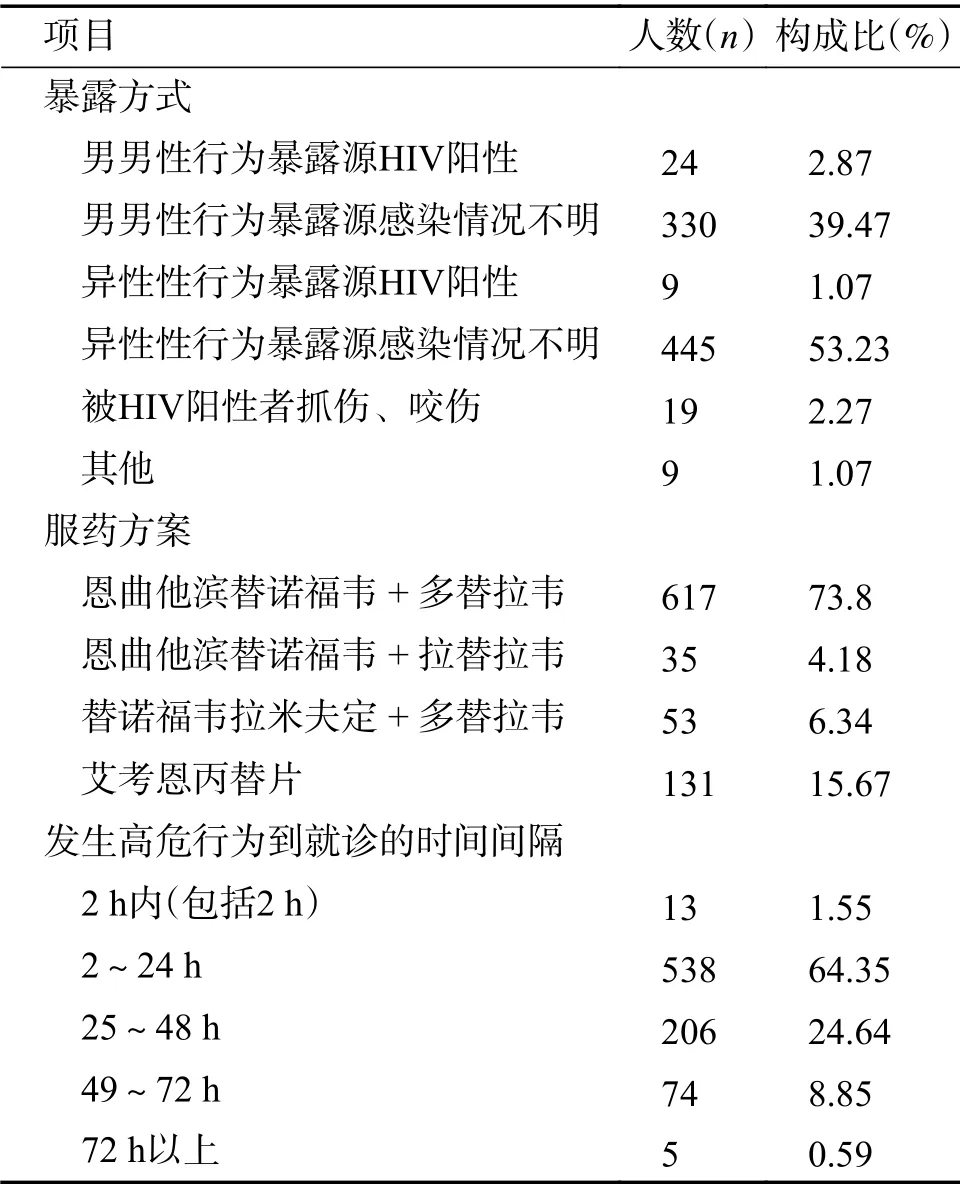
表1 暴露后预防人群基本情况Tab.1 Basic characteristics of post-exposure prophylaxis
2.2 完成28 d疗程的就诊者情况
从门诊医生工作站查询就诊者以往处方记录,有654人完成28 d服药疗程,占78.23%。182人未完成28 d的服药疗程,其中137人服用疗程小于8 d,45人服用疗程为14 d。
2.3 是否完成28 d疗程的影响因素分析
分析可能影响就诊者完成28 d疗程的因素,因变量为是否完成28 d疗程;自变量为年龄、性别、职业、MSM、高危行为到就诊的时间、是否明确暴露源HIV阳性。最终进入模型的自变量为职业和性别,变量赋值见表2。

表2 暴露后预防是否完成28 d疗程影响因素变量赋值Tab.2 Completion of 28-day treatment variable assignment of post-exposure prophylaxis
Logistic回归分析结果:职业的回归系数为正值,OR>1,是危险因素,无职业的就诊者更不容易完成28 d疗程。性别的回归系数为负值,OR<1,是保护因素,男性就诊者更容易完成28 d疗程,见表3。

表3 暴露后预防完成28 d疗程影响因素分析Tab.3 Analysis of influencing factors of 28-day treatment of post-exposure prophylaxis
2.4 完成随访检测的情况
门诊医生工作站查询到216人在治疗3个月后进行了HIV抗体检测,占25.84%。其余620人进行了电话随访,有303人电话告知外院检测结果为阴性;有30人未进行复查;有141人不接电话,有121人电话为关机、停机、空号、无法接通状态;有25人接通电话后拒绝随访。
有检测结果或者电话告知检测结果的519人中有1人检测HIV为阳性。对这位阳性患者随访了解到当时是发生了无保护的异性性行为,高危行为到服药的时间间隔是21 h,治疗方案是指南[4]推荐的恩曲他滨替诺福韦+多替拉韦方案,完成了28 d的服药疗程。服药依从性好,每天定时服药,未出现漏服、延迟服药的情况。患者确诊后在本机构接受ART,进行耐药检测发现整合酶和非核苷类耐药,可能是阻断失败的主要原因。由于患者对暴露源的身份信息不清楚,不明确对方是否为HIV阳性,后续也无法联系上,故暴露源是否整合酶耐药不清楚。
2.5 药物不良反应的观察
随访到的549人中490人未出现药物不良反应,有59人(10.74%)出现过不良反应。胃肠道反应22人,中枢神经系统症状16人,乏力15人,其他(皮疹、掉头发、关节疼痛)6人。发生不良反应的患者症状较轻,只有一位皮疹的患者自行口服药物处理,其余没有特殊处理后自行好转。
3 讨论
截止2019年底,全球现存活的HIV/AIDS约有3 800万例,2019年新报告的151 250例HIV/AIDS中,经性传播者97.1%[7]。暴露后预防措施的积极开展,将有利于减少HIV的传播。一项针对昆明市MSM人群的调查显示暴露后预防知晓率为69.2%,愿意服用暴露后预防药物的比例为69.5%[8]。本研究结果显示暴露后预防的就诊者以男性为主,暴露方式以性行为为主。明确暴露源是HIV阳性的比例仅为6.22%,多数就诊者在发生高危行为后无法明确对方的HIV感染状况。MSM人群中明确暴露源为HIV阳性的比例为6.78%,低于王春梅等[9]在MSM人群中的研究结果(22.8%),但略高于其他人群,这可能与MSM对PEP有较高的需求[10]以及文化程度较高有关。2018版中国艾滋病诊疗指南[11]推荐的职业暴露后预防首选方案为TDF/FTC+RAL或DTG,且发生暴露后尽可能在2 h内服药。本研究中治疗方案为恩曲他滨替诺福韦+多替拉韦或拉替拉韦的比例为77.99%,符合指南推荐。研究显示发生高危行为后2 h内采取暴露后预防措施,可降低80%的HIV感染风险[12]。而本研究中2 h内就诊的比例仅为1.55%,对于非职业暴露的就诊者,就诊的及时性与自己的就诊意识、时间可及性和位置可及性有关,应加强宣传教育,提高自我保护意识,提高就诊的及时性,以保证更好的阻断效果。
完成28 d服药疗程者占78.23%。比利时一项针对全人群的暴露后预防前瞻性研究发现,仅有66.4%的就诊者能够完成28 d的疗程[13]。如同HIV的ART需要良好的服药依从性一样,暴露后预防也需要良好的服药依从性保证阻断的成功率,完成28 d疗程是阻断的基础。分析完成28 d疗程的影响因素发现没有职业的就诊者更不容易完成28 d疗程,可能原因为该人群为无收入或低收入人群,没有经济能力购买28 d的阻断药物。男性就诊者更容易完成28 d疗程,可能与男性的经济能力、社会地位等因素有关。比利时针对全人群的暴露后预防前瞻性研究发现,本地人、MSM、年龄较大、曾被性侵、曾接受过暴露后预防、有保险、白天咨询是提高暴露后预防用药完成率的因素[13]。本研究未发现MSM和年龄是影响因素,可能与人种和地域有关系。
本研究中药物不良反应发生率较低,主要的不良反应为胃肠道反应、中枢神经系统症状及乏力,与Nadia Valin 等[14]的研究结果相似。有Meta分析显示,积极采取暴露后预防措施可以降低89%HIV感染风险[15]。一些观察研究和病例研究以及专家意见都显示,暴露后预防对高危人群有用,并已得到广泛接受[16]。应在全人群中加强宣传教育,提高自我防护意识,发生高危行为后能及时有效的接受预防阻断。同时加强后续的随访检测,以便了解预防阻断效果。
本研究为回顾性研究,有些观察指标缺失,还有些患者失访未能追踪到结果,望能有更完善的前瞻性研究。
综上所述,接受HIV暴露后预防药物者以男性为主,多数就诊者不能明确暴露源是否为HIV阳性。降低暴露后预防药物的费用有利于提高28 d服药完成率。2 h内阻断的比例较低,应多渠道加强宣传教育提高就诊的及时有效性,同时提高28 d服药完成率,以期更好的阻断效果。

