基于组方药味古今炮制工艺的经典名方桃红四物汤质量差异性研究
王升菊 ,郑 雨,段 赟,江华娟 ,王 琳,李固良,何 瑶,章津铭*,裴 瑾 *
1.西南特色中药资源国家重点实验室,四川 成都 611137
2.成都中医药大学药学院,四川 成都 611137
桃红四物汤(Taohong Siwu Decoction,TSD)出自清代柴得华所著《妇科冰鉴》[1],是国家中医药管理局发布的《古代经典名方目录(第一批)》[2]的经典名方品种之一(编号97)。古籍记载处方用量及制法为:“生地三钱(酒洗),当归四钱(酒洗),白芍钱五分(酒炒),川芎一钱,桃仁十四粒(去皮尖研泥),红花一钱(酒洗)。水煎温服。”TSD具有养血、活血、逐瘀的功效,主治血虚血瘀证,症见妇女月经不调、血多有块、色紫质黏、腹痛腹胀等。被历代医家推崇为治疗妇科疾病的首选良方。临床多用于治疗痛经、月经不调、乳腺癌等诸多瘀血类妇科疾病[3-4]。
地黄以酒为辅料进行炮制首见于梁代《本草经集注》[5]:“地黄…得清酒良”。宋代《洪氏急验方》[6]始载生地黄“酒洗”。金元时期《世医得救方》[7]记载地黄“酒炒”;此外还沿用了“酒蒸”“酒煮”“酒浸”等。考证发现地黄酒洗本意为用酒将药材润,润透后进行干燥的方法;《雷公炮炙论》[8]首载当归以酒为辅料炮制当归,原文记载“凡使(当归)…酒浸一宿”,所用辅料为酒,与现代使用辅料一致。唐宋时期除沿用酒浸及炒法外,还新增酒洗。明代《药性会元》[9]详细记载当归酒洗之法:“夏酒洗,切,焙干用”,方法与今酒炙法类似。元代《汤液本草》[10]记载当归“微炒黄”,其炒制程度与现代一致,并首次提到酒炙法理论。说明酒炒和酒洗是历代当归主流的炮制方法;红花以酒为辅料的炮制方法始见于宋《开宝本草》[11],原文记载“并酒煮服”。明代也有“红花酒洗”的记载,另有“慢火微炒”“酒炒”,即现代“酒炙”法。可见历代红花以酒处理后进行干燥为主流;综上,地黄、当归、红花的“酒洗”之意即为用酒将药材润透后烘干;“酒炙”之意即为用酒将药材润透后炒干。
“酒洗”一词始见于汉代张仲景《伤寒论》[12]中,原文记载大黄“去皮,清酒洗”,并用于调味承气汤中。《古代经典名方目录(第一批)》目录中有7首方剂与“酒洗”相关,涉及的药材有大黄(汉)、当归(金、明、清)、肉苁蓉(明)、生地黄(清)、红花(清),而古籍中并未明确“酒洗”的具体操作。TSD复方中生地、当归、红花均为“酒洗”,因此可作为代表方进行酒洗研究。
课题组前期通过参考《上海市炮制规范》2018年版[13]中当归、大黄“酒洗”标准,研究确定了3个药味的最佳“酒洗”工艺。2020年11月国家中医药管理局公布的《古代经典名方关键信息表(7首方剂)》[14]中公布了TSD中6味药的炮制规格为酒地黄,酒当归,酒白芍,生品川芎,燀桃仁(研泥),酒红花。不再强调酒洗,但并未明确如何酒制。其中还提到TSD“鉴于古代酒洗炮制方法演变到现代,与酒炙法内涵基本一致,且有国家标准,建议采用酒炙法”[14]。但组方药物尊古“酒洗”与现代“酒炙”对经典名方制剂质量是否存在差异,仍不清楚。因此,本研究按照TSD制备方法制备了生品煎液、药典“酒炙”煎液以及尊古“酒洗”煎液。借助超高效液相色谱系统(UPLC)建立了TSD指纹图谱,并通过多元统计分析和化学成分分析,评价组方药物生品、药典“酒炙”、尊古“酒洗”的TSD之间的质量差异,筛选出对煎液整体质量贡献较大的成分,并检测其含量。为TSD的质量属性控制以及经典名方复方制剂炮制研究提供参考。
1 仪器与试药
UltiMate3000超高效液相色谱仪,美国Thermo Fisher公司;色谱柱Eclipse Plus C18(150 mm×3.0 mm,1.8 μm),美国Agilent公司;XP26型百万分之一电子天平,瑞士梅特勒-托利多有限公司;KQ-600DE型数控超声波清洗器,昆山市超声仪器有限公司;FTS-10A全自动煎药壶,潮州市一壶百饮电器实业有限公司。DGH-9000电热鼓风干燥箱,上海一恒科学仪器有限公司。对照品羟基红花黄色素A(批号wkq18010407)、5-羟甲基糠醛(批号wkq19010805)、苦杏仁苷(批号wkq19012401)、芍药苷(批号wkq20041008)、苯甲酸(批号wkq18031305)、阿魏酸(批号wkq20010902)、绿原酸(批号wkq20010902)、芍药内酯苷(批号wkq18052205)、没食子酸(批号wkq20010902),质量分数均大于99.0%,均购自四川省维克奇生物科技有限公司。炮制用黄酒,产品标准号:GB/T13662,浙江塔牌绍兴酒有限公司;甲醇、乙腈为色谱醇,赛默飞世尔科技有限公司;磷酸为色谱级,成都市科隆化学品有限公司;水为超纯水。
TSD组方药味地黄、当归、白芍、川芎、桃仁、红花原药材产地信息见表1,6味药均收集5个批次,于2020年7月课题组统一购进。经成都中医药大学药学院裴瑾教授鉴定品种,鉴定结果依次为红花为菊科红花属植物红花Carthamus tinctoriusL.的干燥花,桃仁为蔷薇科樱桃属植物桃Prunus persica(L.) Batsch的干燥成熟种子,川芎为伞形科藁本属植物川芎Ligusticum chuanxiongHort.的干燥根茎,当归为伞形科当归属植物当归Angelica sinensis(Oliv.) Diels的干燥根,白芍为毛茛科芍药属植物芍药Paeonia lactifloraPall.的干燥根,地黄为玄参科地黄属植物地黄Rehmannia glutinosaLibosch.的干燥块根。且课题组按照《中国药典》2020年版一部项下规定的质量检查方法,对6个药味进行显微鉴别、薄层色谱鉴别和指标性成分含量测定,均符合《中国药典》2020年版一部各药材项下规定。

表1 TSD中各药味产地信息Table 1 Origin information of decoction pieces in TSD
2 方法与结果
2.1 饮片炮制
2.1.1 生品炮制方法 参照《中国药典》2020年版第四部[7]“炮制通则”“净制”项下规定,制定地黄、当归、白芍、川芎的切制方法。
2.1.2 药典“酒炙”法 参照《中国药典》2020年版四部“炮制通则”项下“酒炙”法的规定,制定酒炙地黄、酒炙当归、酒炙白芍、酒炙红花的炮制方法。
2.1.3 尊古“酒洗”法 参照《上海市中药饮片炮制规范》2018年版[13]当归项下“酒洗”法的规定,制定酒洗地黄、酒洗当归、酒洗红花的炮制方法。
每个药味的具体炮制方法见表2。

表2 各味药材炮制方法Table 2 Processing method of medicinal materials
2.2 TSD供试样品的制备
《妇科冰鉴》[1]中记载TSD的用法和用量为“生地三钱(酒洗),当归四钱(酒洗),白芍一钱五分(酒炒),川芎一钱,桃仁十四粒(去皮尖研泥),红花一钱(酒洗)”。《古代经典名方关键信息表(7首方剂)》[14]公布其折合现代剂量为生地黄11.19 g,当归14.92 g,白芍5.60 g,川芎3.73 g,桃仁3.78 g,红花3.73 g。取处方的3倍剂量,共128.85 g,第1次加10倍量水,浸泡30 min,煎煮1 h,纱布滤过,第2次加8倍量水,煎煮30 min,合并2次煎液,定容至约2 L,静置,取上清液,0.22 μm微孔滤膜滤过,制得TSD煎液。不同批次的组方按照对应的方法组合为复方(如S1样品:DHYC-1、DGYC-1、BSYC-1、CXYC-1、TRYC-1、HHYC-1,S2~S5以此类推),3种炮制方法按照5个批次各制备5份煎液,共得15批TSD样品,生品组5份煎液按批次依次编号S1~S5,药典“酒炙”组5份煎液按批次依次编号S6~S10,尊古“酒洗”组5份煎液按批次依次编号S11~S15,用于后续实验。
2.3 TSD阴性样品的制备
按3倍处方量分别称取缺地黄、当归、川芎、白芍、桃仁、红花其他5味药,缺当归川芎其它4味药的饮片,按“2.2”项下制备方法制得缺地黄、缺当归、缺川芎、缺当归川芎、缺白芍、缺桃仁、缺红花7个阴性煎液。
2.4 TSD煎液特征图谱研究
2.4.1 对照品溶液的制备 取羟基红花黄色素A、芍药内酯苷、没食子酸、5-羟甲基糠醛、芍药苷、苯甲酸、阿魏酸、绿原酸对照品,精密称定,加50%甲醇制成分别含羟基红花黄素色A 504 μg/mL、芍药内酯苷436 μg/mL、没食子酸406 μg/mL、5-羟甲基糠醛444 μg/mL、芍药苷216 μg/mL、苯甲酸160 μg/mL、阿魏酸265 μg/mL、绿原酸233 μg/mL的对照品溶液,分别吸取1 mL上述对照品溶液,制得混合对照品溶液。
2.4.2 色谱条件 色谱仪为UltiMate3000超高效液相色谱仪;色谱柱为SunFireC18柱(150 mm×3.0 mm,3.5 μm);流动相为乙腈-0.1%磷酸水溶液,梯度洗脱:0~3 min,5%乙腈;3~10 min,5%~15%乙腈;10~25 min,15%~25%乙腈;25~35 min,25%~85%乙腈;35~37 min,85%乙腈;37~40 min,85%~5%乙腈;40~45 min,5%乙腈;检测波长为230 nm;柱温30 ℃;体积流量0.3 mL/min;进样体积10 μL。
2.4.3 精密度试验 取同一供试品溶液(S1),按“2.4.2”项下色谱条件测定,连续进样6次,计算5-羟甲基糠醛、没食子酸、绿原酸、羟基红花黄色素A、芍药内酯苷、芍药苷、阿魏酸、苯甲酸峰面积的RSD分别为3.17%、8.09%、2.74%、4.2%、3.26%、1.74%、1.7%、0.92%;以《中药色谱指纹图谱相似度评价系统软件》(2012.130723版)评价,6次进样相似度为1,表明该仪器精密度良好。
2.4.4 重复性试验 取同一批次样品(S1),按照“2.2”项下样品制备方法平行制备6份,按照“2.4.2”项下色谱条件测定,计算5-羟甲基糠醛、没食子酸、绿原酸、羟基红花黄色素A、芍药内酯苷、芍药苷、阿魏酸、苯甲酸质量分数的RSD依次为0.76%、4.59%、0.94%、0.75%、3.42%、3.83%、4.28%、1.34%;以《中药色谱指纹图谱相似度评价系统软件》(2012.130723版)评价,6次进样相似度为1,表明该方法重复性良好。
2.4.5 稳定性试验 取同一供试品溶液(S6),分别于制备后0、2、4、8、12、24 h按照“2.4.2”项下色谱条件进样测定,结果5-羟甲基糠醛、没食子酸、绿原酸、羟基红花黄色素A、芍药内酯苷、芍药苷、阿魏酸、苯甲酸峰面积的RSD分别为1.26%、1.59%、0.77%、0.85%、4.33%、4.13%、3.15%、4.84%;以《中药色谱指纹图谱相似度评价系统软件》(2012.130723版)评价,6次进样相似度为1,表明供试品溶液在24 h内稳定。
2.4.6 特征图谱相似度评价 将生品、药典“酒炙”和尊古“酒洗”煎液特征图谱的cdf格式导入国家药典委员会《中药色谱指纹图谱相似度评价系统软件》(2012.130723版)进行分析。以S1号样品的UPLC特征图谱作为参照图谱进行指纹匹配,利用平均数法,设置时间窗口为0.1 min,共确定了20个共有峰、15批TSD的特征图谱叠加图(图1),并进行相似度计算(表1),结果发现S1~S5、S6~S10、S11~S15组内的相似度均≥0.996,说明同一炮制方法制备样品差异较小。但3个炮制组间的相似度均≤0.980,表明生品、药典“酒炙”和尊古“酒洗”煎液间存在差异。
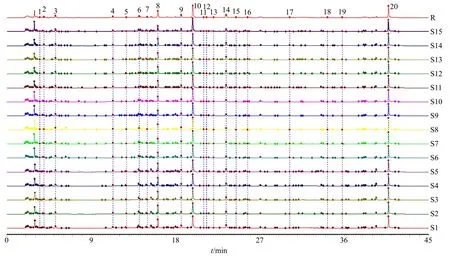
图1 15批TSD的UPLC特征图谱与对照特征图谱 (R)Fig.1 UPLC characteristic map and control characteristic map (R) of 15 batches of TSD
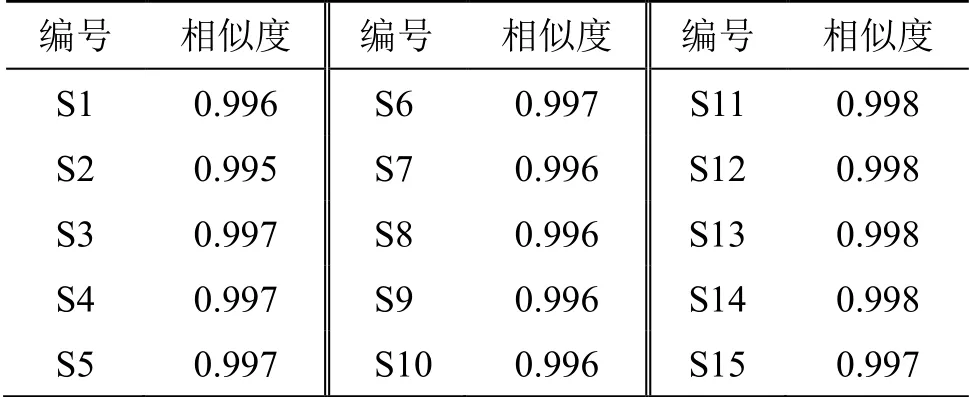
表3 15批TSD的相似度结果Table 3 Similarity results of 15 batches of TSD
2.4.7 色谱峰化学成分指认及归属 通过与对照品比对(图2),共指认了8个色谱峰,色谱峰依次为5-羟甲基糠醛(3号峰)、没食子酸(4号峰)、绿原酸(7号峰)、羟基红花黄色素A(8号峰)、芍药内酯苷(9号峰)、芍药苷(10号峰)、阿魏酸(14号峰)、苯甲酸(17号峰);根据阴性物质基准色谱图(图3),确定羟基红花黄色素A为红花的专属性成分;5-羟甲基糠醛归属于地黄;芍药苷、芍药内酯苷、没食子酸为白芍的专属性成分;阿魏酸归属于当归和川芎。

图2 TSD中各单味药主要成分指认Fig.2 Identification of characteristic components of each single medicine in TSD
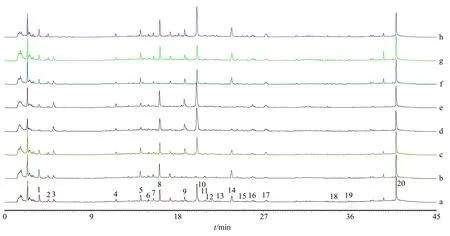
图3 TSD中各成分归属Fig.3 Attribution of components in TSD
2.4.8 层次聚类分析(hierarchical clustering analysis,HCA) 运用SPSS 21软件对S1~S15批次样品进行HCA,以20个共有峰作为分类依据,选择系统聚类分析,采用组间连接法,欧式距离为度量标准,聚类结果如图4所示,生品聚为一类,药典“酒炙”聚为一类,尊古“酒洗”聚为一类,且药典“酒炙”和尊古“酒洗”聚为一个大类。
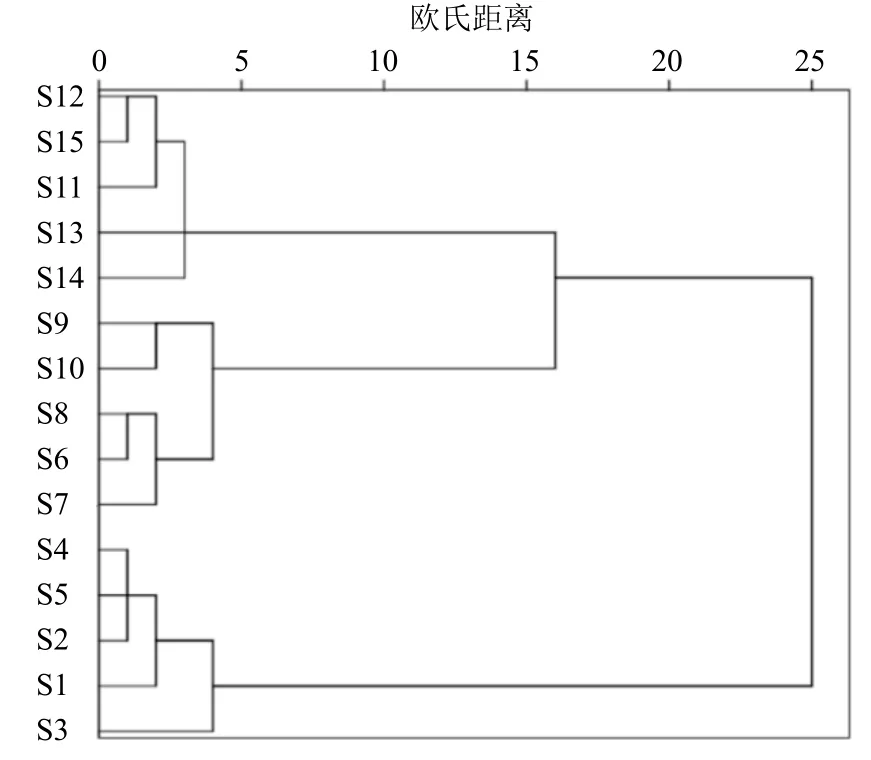
图4 生品 (S1~S5)、药典“酒炙”法 (S6~S10)、尊古“酒洗”法 (S11~S15) 样品的HCAFig.4 HCA result of original medicinal materials (S1—S5),Pharmacopoeia “stir-fried wine” (S6—S10), and ancient“wine washing” (S11—S15)
2.4.9 主成分分析(principal component analysis,PCA) 以15批次生品煎液、药典“酒炙”和尊古“酒洗”为研究对象,将20个共有峰的数据导入SPSS 21统计软件进行无监督的PCA,通过降维处理后提取主成分特征值、累积贡献率和主成分因子载荷值。前4个主成分的累积方差贡献率值为92.898%,说明该模型预测能力较好,其中PC1方差贡献率为55.264%,说明成分1所含信息量较大。主成分因子的特征值和方差贡献率见表4。主成分载荷值可代表各色谱峰对主成分的贡献率,载荷的绝对值越大,对主成分的贡献越大,从表5可知,第1主成分的信息主要来自于色谱峰20、8(羟基红黄色素A)、14(阿魏酸)、2、3(5-羟甲基糠醛)、18。第2主成分的信息主要来自于色谱峰16、12、10、9(绿原酸)、5。第3主成分信息主要来自于色谱峰6。第4主成分的信息主要来自于色谱峰1。主成分3D图见图5。

图5 主成分3D图Fig.5 3D diagram of principal components

表4 主成分因子的特征值和方差贡献率Table 4 Eigenvalue and variance contribution rate of principal component factor

表5 主成分载荷Table 5 Principal component load
2.4.10 偏最小二乘-判别分析(partial least square-discriminant analysis,PLS-DA) 本研究进一步采用有监督的PLS-DA对15批次样品进行分析,通过《中药色谱指纹图谱相似度评价系统》软件得到15×20阶矩阵,将数据导入SIMCA 14.1软件,选取20个色谱峰的相对峰面积值作为变量,PLS-DA结果见图6。结果显示,在置信区间(95%)内,生品汤剂、现代汤剂和尊古汤剂能明显分开,根据分布将S1~S5分为一类,S6~S10分为一类,S11~S15分为一类,即同种炮制方法所得煎液样品差异较小,不同炮制方法所得煎液样品差异较大。

图6 生品 (S1~S5)、药典“酒炙”(S6~S10)、尊古“酒洗”(S11~S15) 的PLS-DA得分图Fig.6 PLS-DA score plot of original medicinal materials(S1—S5), Pharmacopoeia “stir-fried wine” (S6—S10) and ancient “wine washing” (S11—S15)
为进一步搜寻出对上述样品分类贡献值较大的成分,采用变量重要性投影(variable importance in project,VIP)进行分析(VIP值越大,表明对样品分类贡献越大),其中有10个成分VIP值>1,按照VIP值由大到小分别对应峰号为12、5、16、9(绿原酸)、13、3(5-羟甲基糠醛)、7、14(阿魏酸)、4、8(羟基红黄色素A),以上10个成分可能是不同炮制方法的重要差异性成分,也是酒炙与酒洗的差异质量标志性成分。见图7。
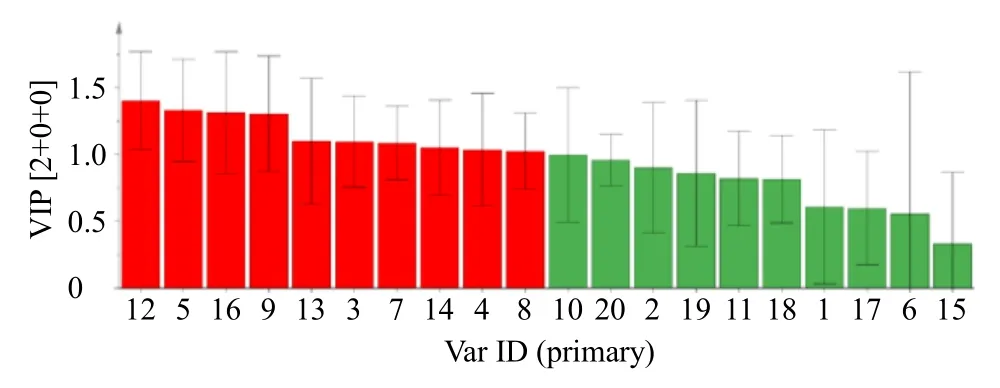
图7 TSD煎液中20个共有成分的VIP值Fig.7 VIP values of 20 common components in material reference of TSD
2.5 羟基红花黄色素A、阿魏酸、5-羟甲基糠醛的含量测定
2.5.1 线性关系考察 精密称取羟基红花黄色素A 4.35 mg、阿魏酸4.36 mg、5-羟甲基糠醛8.08 mg,加50%甲醇稀释通过二倍稀释法制得6个不同质量浓度的对照品溶液,以峰面积为纵坐标(Y),质量浓度为横坐标(X),进行线性回归,得到回归方程分别为羟基红花黄色素AY=0.102X+3.021 7,r=0.999 1,线性范围13.594~435 μg/mL;阿魏酸Y=0.270 8X+2.667 3,r=0.999 3,线性范围13.593 8~436 μg/mL;5-羟甲基糠醛Y=0.234 6X+1.778 2,r=0.999 2,线性范围12.625~404 μg/mL;结果表明,各个对照品的线性关系良好,r均大于0.999。
2.5.2 加样回收率考察 取S1批次样品约0.2 g,分别精密添加已知各成分质量浓度的对照品溶液适量,按照“2.2”项下方法平行制备6份供试品溶液,按照按照“2.4.2”项色谱条件进样,测定峰面积,计算羟基红花黄色素A、阿魏酸、5-羟甲基糠醛的加样回收率。结果显示,3个成分的平均加样回收率依次为99.62%、100.46%、99.47%,RSD分别为1.26%、1.66%、0.89%。结果表明含量测定方法准确可靠。
2.5.3 含量测定结果 取S1~S5生品、S6~S10药典“酒炙”和S11~S15尊古“酒洗”供试品,按照“2.4.2”色谱条件检测,含量测定结果见表7,结果显示羟基红花黄色素A和阿魏酸在炮制后含量下降,而5-羟甲基糠醛在炮制后升高。相对于药典“酒炙”,尊古“酒洗”中羟基红花黄色素A含量增加3.84%;阿魏酸含量增加2.47%,而5-羟甲基糠醛含量降低9.07%。

表7 羟基红花黄色素A、阿魏酸、5-羟甲基糠醛含量测定结果Table 7 Determination of hydroxysafflor yellow A, ferulic acid and 5-hydroxymethylfurfural
3 讨论
本实验在流动相洗脱系统考察时,对比了乙腈-水、乙腈-0.1%甲酸水溶液、乙腈-0.1%磷酸水溶液、乙腈-0.5%磷酸水溶液等不同体积分数、不同洗脱梯度,结果发现,乙腈-0.1%磷酸水溶液作为流动相梯度洗脱时,峰形较佳,各峰分离度较好。实验采用UPLC-DAD法对供试品进行全波长扫描,分析3D图谱,发现230 nm波长下出峰较多,基线平稳且各色谱峰响应值较高。实验还比较了25、30、35 ℃下色谱峰的分离效果,结果显示以30 ℃分离效果最佳。最终确定色谱条件以乙腈-0.1%磷酸水溶液作为流动相,体积流量为0.3 mL/min,柱温为30 ℃,进样量为10 μL。
《古代经典名方关键信息考证原则》[15]指出“信息考证在尊古的基础上充分考虑当前临床和生产实际,传承不泥古,用历史和发展的角度去认识经典名方中药物炮制等关键共性问题”。本次研究对生品煎液、药典“酒炙”、尊古“酒洗”进行了相似度评价、聚类分析、PLS-DA分析以及PCA,结果发现,3种汤剂批次内相似度大于0.996,说明物质基准制备的均一性与稳定性。而组间相似度均小于0.980,且多元统计分析结果显示,3个组能有效聚为3类,说明炮制组间存在差异。对20个共有峰进行主成分分析,前4个主成分的累积方差贡献率值为92.898%。其中第1主成分载荷值较大的成分有羟基红黄色素A、阿魏酸、5-羟甲基糠醛等已被识别的化合物。第2主成分载荷值较大的有被指认的绿原酸等。采用PLS-DA分析对分类贡献值较大的成分,发现已被指认的绿原酸、5-羟甲基糠醛、阿魏酸、羟基红黄色素A等成分的VIP值大于1,2种统计分析方法结论趋于一致,其统计结果说明以上4种成分可能是影响不同炮制组别质量的标志性差异物质。本次研究对质量标志性物质羟基红花黄色素A、阿魏酸、5-羟甲基糠醛进行含量测定。羟基红花黄色素A属于查耳酮类化合物,是《中国药典》2020年版规定的红花指标性成分,也是红花发挥活血化瘀药效的主要成分[16]。研究表明[17-18],羟基红花黄色素A是热不稳定性成分,遇热易分解。结果显示红花酒制后煎液中羟基红花黄色素A含量降低,且酒炙后下降更为明显,说明酒洗低温干燥更利于红花的质量。阿魏酸来源于于当归,具有抗炎活性[19]。研究表明[20],阿魏酸会随着温度的升高,含量降低。5-羟甲基糠醛归属于地黄,有研究认为,5-羟甲基糠醛受高温和加热影响,在高温条件下,药材中的葡萄糖、果糖等单糖化合物发生美拉德反应,脱水生成5-羟甲基糠醛[21]。所以地黄“酒炙”后5-羟甲基糠醛含量会明显升高。绿原酸因专属性不强,所以剔除。综上,提示羟基红黄色素A、阿魏酸、5-羟甲基糠醛化合物可作为质量标志性差异物质对TSD进行质量控制。
本次研究综合评价了TSD组方药味生品煎液,“酒炙”煎液以及“酒洗”煎液间的质量差异。结果显示相对于生品,药典“酒炙”与尊古“酒洗”2种不同炮制工艺均导致TSD样品质量的差异,且“酒炙”和“酒洗”炮制品二者间也存在质量差异。因此现代“酒炙”与尊古“酒洗”之间的差异性值得深入探讨,后续课题组将综合药效学研究综合评价炮制工艺的合理性。本次研究结果为TSD的质量属性控制提供基础,以及为经典名方复方制剂炮制研究提供实验依据。
利益冲突所有作者均声明不存在利益冲突